周邊型
頻率:最常見的典型類型。
眼底表現:在眼底周邊形成橙紅色圓形腫塊,伴有明顯擴張、迂曲的流入動脈和流出靜脈。
進展:按階段進展:毛細血管瘤→腫瘤明確化→滲出性變化→滲出性視網膜剝離→纖維增殖。

視網膜微血管瘤是發生在年輕人視網膜或視神經乳頭的橙色良性腫瘤。由於與腦血管母細胞瘤病理學上具有同源性,近年來也被稱為視網膜血管母細胞瘤。可為單發/多發、單眼/雙眼、散發/症候性。
僅發生散發性視網膜血管母細胞瘤時稱為von Hippel病。伴有全身性腫瘤症候群時診斷為VHL病(von Hippel-Lindau病)。日本眼科學會術語集依據VHL診療指引(2024年版)記載為「視網膜血管瘤」,但本文使用通用名稱「視網膜微血管瘤」。
VHL病是由抑癌基因VHL基因(3p25-26)突變引起的體染色體顯性遺傳性腫瘤症候群。發生率為3萬6千分之1。VHL病除視網膜血管瘤外,還合併小腦、延髓、橋腦、脊髓的血管母細胞瘤,腎細胞癌,嗜鉻細胞瘤,以及腹部臟器(胰臟、腎臟、腎上腺)囊腫等多器官病變。生命預後也取決於全身病變的管理,因此多科別協作至關重要。
根據VHL診療指引(2024年版)的診斷標準,有家族史時,存在血管母細胞瘤或視網膜血管瘤等1個以上病變即可診斷1)。無家族史時,存在2個以上病變(包括血管母細胞瘤或視網膜血管瘤),或確認VHL基因突變加1個病變即可診斷。年輕人的散發性視網膜血管瘤,尤其是10歲以下,常後來被診斷為VHL病,因此應積極考慮全身檢查和基因檢測。
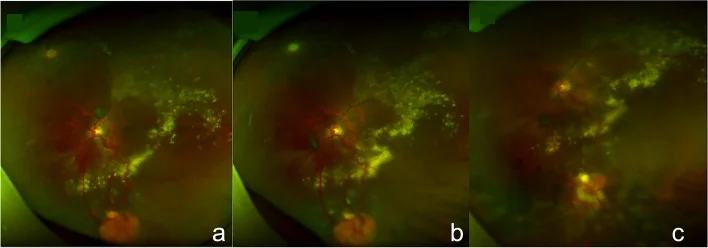
視網膜血管母細胞瘤根據發生方式和部位分類如下。
周邊型
頻率:最常見的典型類型。
眼底表現:在眼底周邊形成橙紅色圓形腫塊,伴有明顯擴張、迂曲的流入動脈和流出靜脈。
進展:按階段進展:毛細血管瘤→腫瘤明確化→滲出性變化→滲出性視網膜剝離→纖維增殖。
視神經乳頭型
頻率:約佔全部病例的15%。
眼底表現:發生在視神經乳頭附近。常難以識別流入和流出血管。
預後:超過50%的病例視力降至0.1以下,預後不良。治療方法尚未確立。
早期常無症狀。隨著病變進展,出現以下症狀。
出血罕見,但在進展病例中,也可能發生玻璃體出血。
眼底所見以孤立或多發的圓形視網膜腫瘤為特徵。周邊部病變伴有擴張、迂曲的流入和流出血管,病變通常在30歲前出現。約半數病例為雙眼性,也可在眼底不同部位多發。
腫瘤本身是由毛細血管和泡沫樣間質細胞構成的血管母細胞瘤,產生大量VEGF(血管內皮生長因子)。VEGF導致滲出性視網膜剝離,引起視力下降。
螢光眼底造影可見特徵性的三期變化。
進展後可轉為以下嚴重病態:
廣角眼底攝影和OCT血管造影(OCTA)有助於評估病變和追蹤觀察1)。OCT可評估腫瘤形態、有無視網膜下液以及黃斑部水腫。
VHL病的發生率為1/36,000。日本VHL患者數估計為600~1,000例。VHL患者中視網膜血管瘤的發生率為40%~70%,平均發病年齡為25歲1)。
VHL基因遵循體染色體顯性遺傳模式。VHL基因的一個對偶基因存在生殖細胞系突變(第一次打擊),體細胞發生第二次打擊導致腫瘤抑制功能喪失(二次打擊假說)。
作為遺傳風險因素,帶有VHL基因致病性突變的家族所有成員都需要進行監測,對於40歲以下視網膜血管瘤病例應考慮進行VHL基因檢測1)。
基於VHL診療指引(2024年版)的診斷標準如下1)。
| 情況 | 診斷標準 |
|---|---|
| 有家族史 | 血管母細胞瘤、視網膜血管瘤等1個以上病變 |
| 無家族史 | 兩個或以上病變(包括血管母細胞瘤/視網膜血管瘤)或VHL基因突變加一個病變 |
眼底檢查中,周邊部橙紅色腫瘤與擴張、迂曲的流入和流出血管的組合是特徵性的。結合以下檢查進行評估。
在VHL家系中,從出生後(0歲)立即開始眼底檢查,並至少每年進行一次定期檢查1)。結合免散瞳眼底相機和廣角眼底攝影,可防止遺漏周邊部病變。
VHL病除視網膜外,其他器官也可能出現多個病變,因此多學科團隊定期進行全身篩查是必要的1)。
VHL基因檢測適用於40歲以下散發性視網膜血管母細胞瘤病例,以及疑似VHL病的患者及其家屬1)。建議與遺傳諮詢同時進行。
需要與以下疾病進行鑑別。
周邊型多發生於眼底周邊部,因此需要在散瞳下進行詳細的眼底檢查。早期小腫瘤可呈毛細血管瘤樣外觀,利用廣角眼底攝影可防止漏診。視神經乳頭型表現為乳頭周圍的腫塊,常難以確定輸入/輸出血管。
根據血管瘤的位置、大小和滲出性變化的程度選擇治療方法。血管瘤增大後會變得難治,因此早期發現和早期治療很重要。在病變較小時開始治療可改善視功能預後。
雷射光凝固
適應症:周邊型的第一線治療。對於≤1個視乳頭直徑的病變,可望根治。
方法:重複直接凝固血管瘤直到獲得足夠效果。對於小於1個視乳頭直徑的小病變,也建議早期光凝固1)。
限制:超過1個視乳頭直徑的大型病變需要多次治療。
冷凍凝固
適應症:大型病變或雷射光凝固難以到達的病例。
方法:根據血管瘤的大小和突出程度選擇冷凍凝固。
合併滲出性變化時:合併視網膜下液引流、透熱療法等等,但難以治療。
牽引性視網膜剝離:如果纖維增生進展導致牽引性視網膜剝離,則進行玻璃體手術。
PDT/抗VEGF療法:近年來,光動力療法(PDT)和抗VEGF藥物(貝伐珠單抗、雷珠單抗等)單獨或合併治療的病例報告不斷累積3)。用於輔助抑制滲出性變化,但不在保險給付範圍內,需要根據個案判斷。
視神經乳頭型的治療方法尚未確立1)。雷射光凝固對視神經和黃斑損傷的風險很高,需要特別謹慎判斷適應症。以下治療方法在病例報告層級有報告,但均未確立為標準治療。
需要謹慎判斷介入時機,建議在專業機構進行多學科討論。
治療後仍容易出現復發和新病變,因此需要終身追蹤。每次治療後應在3至6個月內進行眼底檢查以確認療效並檢查有無新病變。VHL病中多個病變會先後出現,因此不應忽視全周眼底檢查。
對於VHL病的生命預後,腎細胞癌和中樞神經系統血管母細胞瘤的管理至關重要。需與神經外科、泌尿科、內分泌科等多科室協作,對各器官病變進行適當的監測和介入。
VHL基因是位於染色體3p25-26的抑癌基因,編碼pVHL蛋白,該蛋白是E3泛素連接酶複合體的組成部分。pVHL蛋白的主要功能是使缺氧誘導因子(HIF)α亞基泛素化並降解。
在正常條件下,HIFα被pVHL識別、泛素化並迅速降解。當VHL基因失活時,pVHL功能喪失,HIFα積累。
在VHL病中,除了生殖細胞突變(第一次打擊)外,體細胞中的第二次打擊(如雜合性缺失,LOH)導致VHL基因功能完全喪失,從而形成腫瘤。
當HIFα在細胞核中積累時,VEGF、PDGF、EPO等許多血管生成和細胞增殖相關基因的轉錄被持續激活。在VHL病中,HIF-2α(EPAS1)作為主要驅動因子發揮作用1)。
視網膜血管母細胞瘤由兩種細胞構成。
這些間質細胞是腫瘤的主體,VEGF的持續產生直接導致腫瘤血管增生和滲出性視網膜剝離。
VHL基因突變類型與臨床表現型之間的部分關聯(如第1型:非嗜鉻細胞瘤型,第2型:嗜鉻細胞瘤合併型)已知,但詳細分類及眼部病變頻率差異有待進一步分析。
Belzutifan是一種選擇性抑制HIF-2α的小分子化合物,2021年FDA(美國食品藥物管理局)核准用於患有轉移性腎細胞癌、中樞神經系統血管母細胞瘤和視網膜血管母細胞瘤的VHL病患者7)。
第2期試驗(LITESPARK-004)中視網膜血管瘤的結果如下1)。
主要不良事件包括貧血(約90%)和疲勞(約66%)。日本也計劃進行臨床試驗,作為未來的標準治療候選藥物備受關注1)。
Jonasch等人(2021)報告的第二期試驗中,VHL病患者每日口服belzutifan 120 mg一次,視網膜血管母細胞瘤的縮小效果達到100%7)。
di Nicola等人(2022)報告了PDT對視網膜血管母細胞瘤的療效,特別顯示了其對近乳頭型的適用性4)。 Schmidt-Erfurth等人評估了PDT對視盤型的適用性和併發症風險6)。
Hussain等人報告了質子束治療對近乳頭型視網膜毛細血管瘤的效果5)。作為難治性視盤型的一種選擇,病例累積正在推進。
雖然直接縮小腫瘤的效果有限,但作為滲出性變化的輔助控制手段,病例報告正在增加1)。治療方案尚未確立,需要根據具體病例進行判斷。
截至2026年4月,belzutifan尚未在日本獲批常規使用。FDA於2021年批准,但在日本仍處於臨床試驗準備階段1)。對於診斷為VHL病且標準治療困難的患者,可考慮與主治醫師或專科機構商討參加臨床試驗的可能性。
如果血管瘤增大,會變得難治,視力預後顯著惡化。如果滲出性視網膜剝離累及黃斑,視力下降可能不可逆,若進展為牽拉性視網膜剝離或新生血管性青光眼,最終可能導致失明。VHL病會終身出現新病變,因此在治療的同時必須進行持續的眼底檢查。