周边型
频率:最常见的典型类型。
眼底表现:在眼底周边形成橙红色圆形肿块,伴有明显扩张、迂曲的流入动脉和流出静脉。
进展:按阶段进展:毛细血管瘤→肿瘤明确化→渗出性改变→渗出性视网膜脱离→纤维增殖。

视网膜毛细血管瘤是发生在年轻人视网膜或视乳头的橙色良性肿瘤。由于与脑血管母细胞瘤病理学上具有同源性,近年来也被称为视网膜血管母细胞瘤。可为单发/多发、单眼/双眼、散发/综合征性。
仅发生散发性视网膜血管母细胞瘤时称为von Hippel病。伴有全身性肿瘤综合征时诊断为VHL病(von Hippel-Lindau病)。日本眼科学会术语集依据VHL诊疗指南(2024年版)记载为“视网膜血管瘤”,但本文使用通用名称“视网膜毛细血管瘤”。
VHL病是由抑癌基因VHL基因(3p25-26)突变引起的常染色体显性遗传性肿瘤综合征。发病率为1/36000。VHL病除视网膜血管瘤外,还合并小脑、延髓、脑桥、脊髓的血管母细胞瘤,肾细胞癌,嗜铬细胞瘤,以及腹部脏器(胰腺、肾脏、肾上腺)囊肿等多器官病变。生命预后也取决于全身病变的管理,因此多学科协作至关重要。
根据VHL诊疗指南(2024年版)的诊断标准,有家族史时,存在血管母细胞瘤或视网膜血管瘤等1个以上病变即可诊断1)。无家族史时,存在2个以上病变(包括血管母细胞瘤或视网膜血管瘤),或确认VHL基因突变加1个病变即可诊断。年轻人的散发性视网膜血管瘤,尤其是10岁以下,常后来被诊断为VHL病,因此应积极考虑全身检查和基因检测。
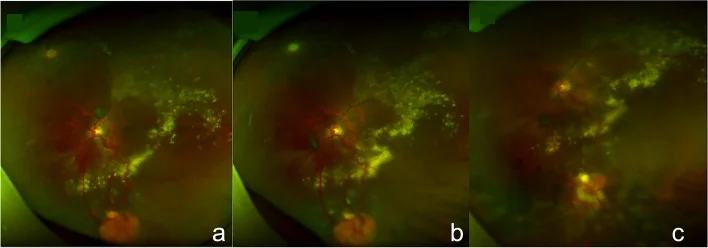
视网膜血管母细胞瘤根据发生方式和部位分类如下。
周边型
频率:最常见的典型类型。
眼底表现:在眼底周边形成橙红色圆形肿块,伴有明显扩张、迂曲的流入动脉和流出静脉。
进展:按阶段进展:毛细血管瘤→肿瘤明确化→渗出性改变→渗出性视网膜脱离→纤维增殖。
视乳头型
频率:约占全部病例的15%。
眼底表现:发生在视乳头附近。常难以识别流入和流出血管。
预后:超过50%的病例视力降至0.1以下,预后不良。治疗方法尚未确立。
早期常无症状。随着病变进展,出现以下症状。
出血少见,但在进展期病例中,也可能发生玻璃体积血。
眼底表现为孤立或多发的圆形视网膜肿瘤,具有特征性。周边部病变伴有扩张、迂曲的流入和流出血管,病变通常在30岁前出现。约半数病例为双眼性,也可在眼底不同部位多发。
肿瘤本身是由毛细血管和泡沫样间质细胞构成的血管母细胞瘤,产生大量VEGF(血管内皮生长因子)。VEGF导致渗出性视网膜脱离,引起视力下降。
荧光眼底造影可见特征性的三期变化。
进展后可转为以下严重病态:
广角眼底摄影和OCT血管成像(OCTA)有助于评估病变和随访观察1)。OCT可以评估肿瘤形态、是否存在视网膜下液以及黄斑水肿。
VHL病的发病率为1/36,000。日本VHL患者数估计为600~1,000例。VHL患者中视网膜血管瘤的发生率为40%~70%,平均发病年龄为25岁1)。
VHL基因遵循常染色体显性遗传模式。VHL基因的一个等位基因存在生殖细胞系突变(第一次打击),体细胞发生第二次打击导致肿瘤抑制功能丧失(二次打击假说)。
作为遗传风险因素,携带VHL基因致病性突变的家族所有成员都需要进行监测,对于40岁以下视网膜血管瘤病例应考虑进行VHL基因检测1)。
基于VHL诊疗指南(2024年版)的诊断标准如下1)。
| 情况 | 诊断标准 |
|---|---|
| 有家族史 | 血管母细胞瘤、视网膜血管瘤等1个以上病变 |
| 无家族史 | 两个或以上病变(包括血管母细胞瘤/视网膜血管瘤)或VHL基因突变加一个病变 |
眼底检查中,周边部橙红色肿物与扩张、迂曲的流入和流出血管的组合是特征性的。结合以下检查进行评估。
在VHL家系中,从出生后(0岁)立即开始眼底检查,并至少每年进行一次定期检查1)。结合免散瞳眼底相机和广角眼底照相,可防止遗漏周边部病变。
VHL病除视网膜外,其他器官也可能出现多个病变,因此多学科团队定期进行全身筛查是必要的1)。
VHL基因检测适用于40岁以下散发性视网膜血管母细胞瘤病例,以及疑似VHL病的患者及其家属1)。建议与遗传咨询同时进行。
需要与以下疾病进行鉴别。
周边型多发生于眼底周边部,因此需要在散瞳下进行详细的眼底检查。早期小肿瘤可呈毛细血管瘤样外观,利用广角眼底摄影可防止漏诊。视乳头型表现为视乳头周围的肿块,常难以确定输入/输出血管。
根据血管瘤的位置、大小和渗出性变化的程度选择治疗方法。血管瘤增大后会变得难治,因此早期发现和早期治疗很重要。在病变较小时开始治疗可改善视功能预后。
激光光凝
适应症:周边型的首选治疗。对于≤1个视盘直径的病变,有望根治。
方法:重复直接凝固血管瘤直至获得足够效果。对于小于1个视盘直径的小病变,也推荐早期光凝1)。
局限性:超过1个视盘直径的大病变需要多次治疗。
冷冻凝固
适应症:大病变或激光光凝难以到达的病例。
方法:根据血管瘤的大小和突出程度选择冷冻凝固。
合并渗出性改变时:联合视网膜下液引流、透热疗法等,但难以治愈。
牵拉性视网膜脱离:如果纤维增生进展导致牵拉性视网膜脱离,则进行玻璃体手术。
PDT/抗VEGF治疗:近年来,光动力疗法(PDT)和抗VEGF药物(贝伐珠单抗、雷珠单抗等)单独或联合治疗的病例报告不断积累3)。用于辅助抑制渗出性改变,但不在医保范围内,需要根据具体病例判断。
视乳头型的治疗方法尚未确立1)。激光光凝对视神经和黄斑损伤的风险很高,需要特别谨慎地判断适应症。以下治疗方法在病例报告层面有报道,但均未确立为标准治疗。
需要谨慎判断干预时机,建议在专业机构进行多学科讨论。
治疗后仍易出现复发和新病变,因此需要终身随访。每次治疗后应在3至6个月内进行眼底检查以确认疗效并检查有无新病变。VHL病中多个病变会先后出现,因此不应忽视全周眼底检查。
对于VHL病的生命预后,肾细胞癌和中枢神经系统血管母细胞瘤的管理至关重要。需与神经外科、泌尿科、内分泌科等多科室协作,对各器官病变进行适当的监测和干预。
VHL基因是位于染色体3p25-26的抑癌基因,编码pVHL蛋白,该蛋白是E3泛素连接酶复合体的组成部分。pVHL蛋白的主要功能是使缺氧诱导因子(HIF)α亚基泛素化并降解。
在正常条件下,HIFα被pVHL识别、泛素化并迅速降解。当VHL基因失活时,pVHL功能丧失,HIFα积累。
在VHL病中,除了生殖细胞突变(第一次打击)外,体细胞中的第二次打击(如杂合性缺失,LOH)导致VHL基因功能完全丧失,从而形成肿瘤。
当HIFα在细胞核中积累时,VEGF、PDGF、EPO等许多血管生成和细胞增殖相关基因的转录被持续激活。在VHL病中,HIF-2α(EPAS1)作为主要驱动因子发挥作用1)。
视网膜血管母细胞瘤由两种细胞构成。
这些间质细胞是肿瘤的主体,VEGF的持续产生直接导致肿瘤血管增生和渗出性视网膜脱离。
VHL基因突变类型与临床表型之间的部分关联(如1型:非嗜铬细胞瘤型,2型:嗜铬细胞瘤合并型)已知,但详细的分类及眼部病变频率差异有待进一步分析。
Belzutifan是一种选择性抑制HIF-2α的小分子化合物,2021年FDA(美国食品药品监督管理局)批准用于患有转移性肾细胞癌、中枢神经系统血管母细胞瘤和视网膜血管母细胞瘤的VHL病患者7)。
第2期试验(LITESPARK-004)中视网膜血管瘤的结果如下1)。
主要不良事件包括贫血(约90%)和疲劳(约66%)。日本也计划进行临床试验,作为未来的标准治疗候选药物备受关注1)。
Jonasch等人(2021)报告的2期试验中,VHL病患者每日口服belzutifan 120 mg一次,视网膜血管母细胞瘤的缩小效果达到100%7)。
di Nicola等人(2022)报告了PDT对视网膜血管母细胞瘤的疗效,特别显示了其对近乳头型的适用性4)。 Schmidt-Erfurth等人评估了PDT对视盘型的适用性和并发症风险6)。
Hussain等人报告了质子束治疗对近乳头型视网膜毛细血管瘤的效果5)。作为难治性视盘型的一种选择,病例积累正在推进。
虽然直接缩小肿瘤的效果有限,但作为渗出性变化的辅助控制手段,病例报告正在增加1)。治疗方案尚未确立,需要根据具体病例进行判断。
截至2026年4月,belzutifan尚未在日本获批常规使用。FDA于2021年批准,但在日本仍处于临床试验准备阶段1)。对于诊断为VHL病且标准治疗困难的患者,可考虑与主治医生或专科机构商讨参加临床试验的可能性。