VMT表现
中心凹凹陷消失/变形:正常的中心凹凹陷形状变平或扭曲。
假性囊肿/囊样改变:黄斑内液体聚集,伴有代表Müller细胞的组织柱。见于81%的VMT眼。囊样改变可累及整个黄斑,与VMT特有的前后方向牵拉有关,不同于ERM的切线方向牵拉8)。
中心凹从RPE抬高:后玻璃体皮质向前牵拉的直接证据。
后玻璃体皮质增厚/高反射:表现为视网膜前方的高反射带。

玻璃体黄斑牵拉综合征(VMT)是一种基于不完全性后玻璃体脱离(PVD)发生的玻璃体视网膜界面疾病。随着年龄增长,黄斑前的玻璃体液化形成玻璃体袋,但黄斑前存在的玻璃体皮质因后玻璃体脱离的进展而起到前后方向的牵拉作用。后玻璃体皮质异常牢固地附着在黄斑部残留,液化的玻璃体对黄斑附着部进行前后牵拉,导致形态和功能改变。当后玻璃体脱离的进展在黄斑附近停止时,后玻璃体皮质前袋的后壁对黄斑部进行前后牵拉而发病。
指牵拉导致视网膜发生形态变化的情况;视网膜完全没有变化、仅玻璃体附着于黄斑的情况称为玻璃体黄斑粘连(VMA),不纳入VMT范畴。
VMT包括因玻璃体年龄变化引起的狭义(特发性)和继发于葡萄膜炎、增殖性糖尿病视网膜病变、视网膜分支静脉阻塞等视网膜血管病变的广义(继发性)。
1953年Irvine首次以“玻璃体条索综合征”报告相关病变,1967年Jaffe提出“玻璃体视网膜牵拉综合征”作为独立疾病。随后Reese等人的组织病理学研究确立了疾病概念。
据报道,孤立性VMT的患病率为每10万人22.5例1)。合并糖尿病视网膜病变、糖尿病黄斑水肿、年龄相关性黄斑变性等疾病的VMT患病率远高于此。VMT可发生于所有年龄和种族,但年龄增长是最大的风险因素,估计63岁及以上的美国成年人患病率为0.4%至2.0%2)。女性发病率略高。
约80%的病例伴有囊样黄斑水肿,大多数病例伴有视网膜前膜。视网膜前膜的存在进一步加强了玻璃体与黄斑的粘连,导致长期持续的牵拉。
随着OCT的普及,国际玻璃体黄斑牵拉研究组(IVTS)提出了基于OCT的定义和分类。
**玻璃体黄斑粘连(VMA)**是指中心凹附近存在部分玻璃体附着,但未引起视网膜形态改变的状态。通常无症状,仅VMA不作为治疗对象。
**玻璃体黄斑牵拉(VMT)**是指在VMA的基础上,出现中心凹形态改变(如中心凹表面扭曲、假性囊肿形成、中心凹从RPE隆起等)的状态。无全层裂孔是VMT的必要条件。
IVTS分类将附着直径≤1500 µm的病例归为局灶型,>1500 µm的归为广泛型。附着宽度是连续的,从极小的点状附着到超过1500 µm的广泛附着,多种多样8)。
按附着宽度分类:
| 分类 | 附着宽度 | 主要特征 |
|---|---|---|
| 局灶型 | ≤ 1500 µm | 易伴有囊样改变。较易自然消退。 |
| 广泛型 | > 1500 µm | 易引起黄斑隆起和牵拉性视网膜脱离。 |
VMA是指玻璃体附着于黄斑但视网膜形态正常的状态,通常无症状且无需治疗。VMT是在VMA基础上出现视网膜形态改变(扭曲、假性囊肿、隆起)的状态,可能导致视功能障碍。两者通过OCT检查区分。只有牵拉导致视网膜形态改变的情况才诊断为VMT,仅玻璃体附着于黄斑的情况则区分为VMA。
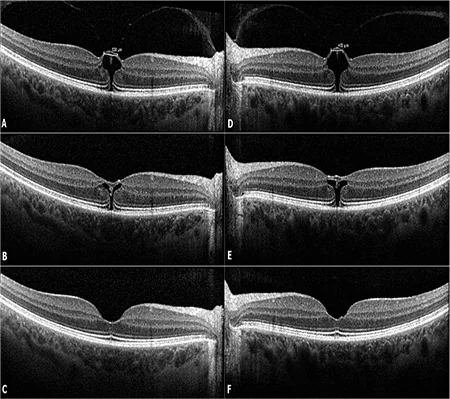
VMT的自觉症状缓慢出现并进展,短期内通常不会出现视力的剧烈变化8)。
如果严重牵拉导致中心凹脱离,可能出现急剧视力下降或暗点。仅VMA阶段无症状。
裂隙灯生物显微镜检查可见玻璃体与黄斑部粘连,周围有后玻璃体脱离。有时可观察到附着于中心凹的紧绷的半透明膜。眼底检查可能发现黄斑前膜,或表现为中心性浆液性脉络膜视网膜病变样黄斑脱离或水肿、黄斑裂孔样改变。眼底镜下可见黄斑部视网膜表面有透明膜组织,视网膜血管因牵拉而迂曲。
OCT确认的主要表现如下所示。
VMT表现
中心凹凹陷消失/变形:正常的中心凹凹陷形状变平或扭曲。
假性囊肿/囊样改变:黄斑内液体聚集,伴有代表Müller细胞的组织柱。见于81%的VMT眼。囊样改变可累及整个黄斑,与VMT特有的前后方向牵拉有关,不同于ERM的切线方向牵拉8)。
中心凹从RPE抬高:后玻璃体皮质向前牵拉的直接证据。
后玻璃体皮质增厚/高反射:表现为视网膜前方的高反射带。
合并表现
荧光素眼底血管造影可见黄斑部强荧光、囊样黄斑水肿和视盘荧光渗漏。如果视盘处有后玻璃体脱离,则不会出现视盘渗漏。FA上,晚期可见毛细血管渗漏,囊腔内染料积存8)。
Yamada和Kishi报道了VMT的两种玻璃体牵拉类型。V型(中心凹颞侧和鼻侧均脱离,仅中心凹处附着)术后效果良好,而J型或弓形(中心凹鼻侧也有残留附着)术后易进展为黄斑裂孔或萎缩,效果较差。
VMT/ERM眼可能伴有玻璃体视盘牵拉(VPT),即视盘周围玻璃体仍附着。VPT通过OCT诊断,可能被误认为视盘水肿,双眼病例可能被误认为视乳头水肿。有研究表明VPT可能与视力下降和缺血性视神经病变有关8)。
随着年龄增长,玻璃体凝胶发生液化(synchysis)和浓缩(syneresis),后玻璃体脱离(PVD)进展。在正常PVD中,玻璃体从视网膜均匀脱离,但在异常PVD中,脱离和粘连解除不同步,导致VMT。
玻璃体在内界膜(ILM)最薄的部位与视网膜附着最牢固。在后部,视盘周围、黄斑部(中心凹及中心凹周围直径1500 µm的区域)以及主要视网膜血管沿线附着较强。这是VMT中中心凹附着持续的解剖学基础。
该检查在VMT的诊断和评估中起核心作用。OCT被认为是ERM和VMT诊断、分型和随访的金标准8)。它能无创地显示玻璃体黄斑界面,详细观察牵拉的宽度和视网膜的变化。OCT诊断VMT需要以下表现:
除上述OCT表现外,还需评估以下信息:
评估附着宽度是否≤1500 µm(局灶型)或>1500 µm(广泛型)对制定治疗方案很重要。SD-OCT还能评估视网膜外层(外界膜、光感受器椭圆体带)的状态,有助于预后预测。
“棉球征”(中心凹中心内节外节连接处与光感受器终末部之间的圆形或弥漫性高反射区)可能是中心凹向前牵拉的指标。
使用眼底接触镜或高倍间接检眼镜评估黄斑部的皱褶、水肿和牵拉性改变。裂隙灯显微镜眼底检查可确认与黄斑粘连的玻璃体及其周围的后玻璃体脱离。
VMT可能表现出与以下疾病相似的症状和体征:
临床诊断可通过裂隙灯眼底检查和荧光素眼底血管造影进行,但VMT的确诊标准是OCT。OCT可以详细评估牵拉宽度、视网膜形态变化和合并表现,对制定治疗方案至关重要。特别是附着宽度(局灶型或广泛型)的准确评估只能通过OCT完成。
对于症状轻微且判断VMT解除的风险大于获益的病例,观察随访是首选。荟萃分析显示,自然消退在11%至40%的病例中有报道3)。局灶型VMT(≤1500 µm)在1至2年内自然消退率为23%至47%8)。局灶型且不合并视网膜前膜时,更容易自然消退3)。
对于视网膜变化轻微的病例,可能多年不变;而粘连点小的病例可能自然分离。因此需要密切观察其类型和病程。不伴有视网膜前膜的病例,可能自然发生后玻璃体脱离,从而解除牵引。自觉症状不明显的病例可以暂时观察。需注意进展为黄斑孔,定期进行OCT随访。
另一方面,基线存在囊样改变的患眼需注意预后。一项53只眼的研究显示,有囊样改变的眼在60个月时81%出现2行或以上的视力下降8)。
这是治疗VMT最可靠的方法。进行单纯玻璃体切除和黄斑部膜剥离。黄斑部粘连较强,需在观察视网膜附着情况的同时缓慢剥离。大多数病例为解除玻璃体对黄斑的牵引,有玻璃体切除术的适应证。
一旦明确诊断,建议尽早手术,以免发生黄斑孔或不可逆改变。特别是视网膜与玻璃体粘连面积大的病例,由于视网膜玻璃体粘连较强,需注意。观察期间若发生黄斑孔,或手术延迟,术后囊样黄斑水肿可能发展为黄斑孔。
手术适应证判断标准:
据报道,最佳治疗结果为VMT解除率100%,黄斑孔闭合率95%2)。系统评价和荟萃分析显示,玻璃体手术在VMT解除率(RR=0.48, 95% CI 0.38–0.62)和黄斑孔闭合率(RR=0.49, 95% CI 0.30–0.81)方面显著优于奥克纤溶酶(酶促玻璃体溶解)2)。术后视力改善也大于奥克纤溶酶(SMD=0.38, 95% CI 0.03–0.73)2)。
PPV术后视力在荟萃分析(259眼)中从术前logMAR 0.67改善至术后0.42,33%的患者改善2行或以上,而21%保持不变或恶化8)。平均约80%的患者获得2行或以上的视力改善8)。
合并视网膜前膜或黄斑裂孔时,标准做法是增加内界膜(ILM)剥离。用亮蓝染料或其他辅助染料染色ILM后进行剥离。合并黄斑裂孔的病例中,ILM剥离后使用C3F8气体填塞的黄斑裂孔闭合率超过95%4)。一项系统评价(13项研究)显示,ILM剥离与否在视力结果上无显著差异,但ILM剥离降低了ERM复发率8)。近期一项RCT(213眼)显示,主动ILM剥离组的复发率为0%,而非剥离组为19.6%8)。
一例83岁男性VMT合并黄斑裂孔(1b级)的报告中,玻璃体手术后部玻璃体皮质剥离后出现全层黄斑裂孔(422 µm),但第二次玻璃体手术+ILM剥离(使用亮蓝染料)+14% C3F8气体填塞后,6周时视力改善至20/120,中心凹形态恢复4)。
术前解剖形态影响手术效果。局灶型VMT(V型牵引轮廓)比广泛型或弓状(J型)有更好的术后视力改善趋势4)。
这是一种微创治疗,将C3F8(全氟丙烷)或SF6(六氟化硫)等膨胀性气体注射到玻璃体内,通过气体的浮力和机械力解除VMT。C3F8使用0.3 mL。
“饮水鸟手法”:术后反复前后倾斜头部的操作,促进气泡和玻璃体液的混合,提高VMT解除率。
荟萃分析显示,PV的VMT解除率显著高于奥克纤溶酶(RR=0.49, 95% CI 0.35–0.70),与PPV相比视力改善无显著差异2)。VMT解除率报告为46%(奥克纤溶酶)、68%(PV)和100%(玻璃体手术)2)。
在DRCR网络的RCT中,C3F8气体注射组78%的患者黄斑部VMT解除,而假手术组为9%。但气体注射组视网膜脱离和裂孔的发生率高于预期,因安全性担忧而提前终止8)。该治疗的安全性仍需注意。
奥克纤溶酶(ocriplasmin)是一种重组蛋白酶,对玻璃体视网膜界面的成分纤连蛋白和层粘连蛋白具有活性。单次玻璃体内注射125 µg可促进VMA解除。其疗效不太理想,约20%的患者有效。
在MIVI-TRUST和OASIS临床试验中,VMA解除率显著优于安慰剂(RR=3.61, 95% CI 1.99–6.53)3),但与玻璃体切除术相比,VMT解除率较差。III期(MIVI-TRUST)中,ocriplasmin组27% vs 安慰剂组10%实现了VMA解除(P<0.001)7)。奥克纤溶酶的使用存在争议,未在临床广泛普及7)。该药于2020年退出市场5),不同地区和机构的可及性不同。
与年龄相关的玻璃体变化按以下顺序进展。
当PVD正常进展时,玻璃体与视网膜均匀分离。但在牵引力与脱离不同步的“异常PVD”中,中心凹处的附着持续到最后,导致VMT。
附着直径越小,单位面积的牵引应力越高,中心凹变形越大5)。
当PVD不完全时,残留的后玻璃体的弹性特性对中心凹施加静态的前方牵引。此外,眼球运动产生的动态牵引也参与其中,在VMT中动态牵引被认为比静态牵引更重要。严重病例可能伴有视网膜劈裂或视网膜脱离。
视网膜前膜存在于40–65%的VMT眼中,通过两种机制加重VMT5)。
组织病理学上,ERM含有玻璃体胶原,ERM与ILM的牢固附着在将残留玻璃体附着固定于黄斑方面发挥作用8)。
关于ERM的形成机制,除了传统理论认为RPE细胞和胶质细胞通过ILM微小断裂迁移到视网膜表面外,还提出了一个新假说:后部玻璃体皮质的残留细胞被激活为肌成纤维细胞,导致膜形成和收缩,而无需ILM断裂8)。
组织学上,即使在检眼镜下未见视网膜前膜的病例中,内界膜的玻璃体侧也附着有以肌成纤维细胞为中心的细胞。在有膜样组织的病例中,据报道组织内含有肌成纤维细胞和纤维性星形胶质细胞,与特发性视网膜前膜相似。
VMT标本的组织病理学显示,由纤维性星形胶质细胞、肌成纤维细胞、纤维细胞和RPE细胞组成的纤维细胞增殖,形成连接后部玻璃体界面和视网膜界面的“双膜”。透射电子显微镜可识别两种类型的视网膜前膜。玻璃体劈裂的存在与否被认为是决定这两种类型的因素。
奥克纤溶酶(Jetrea;125 µg单次玻璃体内注射)是一种重组蛋白酶,由人纤溶酶的催化结构域组成,通过溶解玻璃体视网膜界面的蛋白质成分促进VMA解除。
Chen等人的荟萃分析(55项研究,4,159例)显示,与安慰剂相比,奥克纤溶酶治疗在28天VMA解除率(RR=3.61,95% CI 1.99–6.53)、黄斑裂孔闭合率(RR=3.84,95% CI 1.62–9.08)和6个月≥3行BCVA改善(RR=1.97,95% CI 1.08–3.57)方面显著更优3)。队列研究的合并分析显示,VMA解除率为50%(95% CI 47–53%),黄斑裂孔闭合率为36%(95% CI 32–39%)3)。
治疗效果预测因素(奥克纤溶酶):
Cochrane综述显示,治疗组中多达20%的患者在6个月内需要额外的PPV7)。奥克纤溶酶的使用存在争议,未能在临床上广泛普及7)。自2020年退出市场后,其可获得性有限5)。
Quiroz-Reyes等人的系统评价和荟萃分析(2023年)显示,比较PPV和气体注射(PV)的随机试验中,PPV在VMT解除率和黄斑裂孔闭合率方面更优,但术后BCVA改善无显著差异(SMD=-0.15, 95% CI -0.47~0.16)2)。有C3F8 PV的RCT因安全性问题(视网膜脱离、视网膜裂孔)而提前终止的案例2, 8),该治疗方法的安全性仍需持续评估。
比较同时进行晶状体玻璃体联合手术与分期手术的荟萃分析显示,并发症、视力和屈光结果无显著差异8)。有晶状体眼PPV后核性白内障常快速进展,因此建议术前与患者讨论同时手术的适应症。
Ashby等人报告了一例66岁女性在飞行模拟器体验后VMT解除的病例(2025年)5)。假设模拟器的三维加速产生的多方向力有助于VMA界面的分离。长期随访中视力从20/60改善至20/25。然而,VMT解除后短暂出现紧迫性黄斑裂孔征象,表明全层黄斑裂孔形成是潜在风险5)。不能排除与自发性VMT消退的时间关联,这不是一种确定的治疗方法。
Rios Gonzalez等人报告了一例69岁男性患者,在开始使用1%毛果芸香碱滴眼液(用于青光眼治疗)6周后出现双侧VMT,停药8周后VMT解除但VMA持续存在(2023年)1)。随着用于老视治疗的新型毛果芸香碱制剂(1.25%等)的普及,人们担心其诱发或加重VMT的风险,建议在PVD未完成的病例中,在开始治疗前进行后段检查和OCT1)。
一项关于玻璃体黄斑界面疾病(VMID)患者报告结局指标(PROMs)的系统综述从86项研究中识别出17种VMID特异性PROMs,但当前的PROMs存在以下问题6):
PROMs与定性研究中识别的QOL问题之间的重叠仅限于9个项目(阅读、驾驶、夜间驾驶、对手术的恐惧、视物变形、复视、对与医疗人员沟通的担忧、体位保持的不便、以及体位保持导致的睡眠障碍)6)。患者报告的VMID的QOL问题包括视觉问题如视物变形、中心视力障碍和阅读困难,以及情感健康(乐观、沮丧、焦虑、压力、希望)、社会健康(获得社会支持、维持与朋友和家人的互动)和应对策略(忽视、分散注意力、信任医生、祈祷/冥想、接受、实用工具、社会支持、症状监测)。当前的PROMs未能充分涵盖这些方面6)。未来需要通过患者参与的内容开发和包括Rasch分析在内的严格心理测量学验证,开发VMID特异性PROMs。
Rios Gonzalez R, Villegas VM, Blasini M. Bilateral vitreomacular traction syndrome associated with topical pilocarpine 1% ophthalmic solution. Am J Ophthalmol Case Rep. 2023;30:101834.
QuirozReyes MA, QuirozGonzalez EA, QuirozGonzalez MA, LimaGomez V. Pneumatic vitreolysis versus vitrectomy for the treatment of vitreomacular traction syndrome and macular holes: complication analysis and systematic review with meta-analysis of functional outcomes. Int J Retina Vitreous. 2023;9:33.
Chen X, Li M, You R, Wang W, Wang Y. Efficacy and Safety of Ocriplasmin Use for Vitreomacular Adhesion and Its Predictive Factors: A Systematic Review and Meta-Analysis. Front Med. 2022;8:759311.
Tayyab M, Iqbal K, Abid MA, Rahman FU, Tayyab HA. Surgical Outcome of Vitreomacular Traction Associated With Macular Hole. Cureus. 2022;14(12):e32620.
Ashby N, Kaftan T, Ohlhausen M, Kim S, McGill E, Yeh S. Resolution of Vitreomacular Traction Following a Commercial Flight Simulator Experience. J VitreoRetinal Dis. 2025.
Woudstra-de Jong JE, Busschbach JJ, Manning-Charalampidou SS, Vingerling JR, Pesudovs K. Assessment of patient-reported outcomes in vitreomacular interface disorders: A systematic literature review. Surv Ophthalmol. 2024. doi:10.1016/j.survophthal.2024.08.004.
Flaxel CJ, Adelman RA, Bailey ST, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2020;127(2):P145-P183.
Bailey ST, Vemulakonda GA, Kim SJ, et al. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2024.