结节型(56%)
黄色调结节性肿块:由于肿瘤细胞内的脂质,呈特征性黄色外观。好发于上眼睑缘,表面不规则,伴有易出血的肿瘤血管。
通过眼睑翻转观察:翻转眼睑检查结膜侧也很重要。

眼睑皮脂腺癌(SGC)是一种起源于眼睑皮脂腺——睑板腺、Zeis腺和泪阜皮脂腺——的高度恶性肿瘤。它被认为是眼睑最重要的恶性肿瘤之一。起源部位的分布为:睑板腺占92%,Zeis腺占6%,泪阜占2%2)。由于上眼睑约有50个睑板腺,下眼睑约有25个,因此好发于上眼睑。主要发生在50岁以后,女性略多,10%~20%的病例发生转移或复发。这是一种预后不良的疾病,有时可能致命。
该疾病在欧美和东亚地区的定位有很大不同。在欧美,基底细胞癌占眼睑恶性肿瘤的80%~95%,而脂腺癌仅占1%~3% 1)。相比之下,亚洲人群中脂腺癌的比例显著较高。
| 地区/人群 | 脂腺癌的比例 |
|---|---|
| 欧美 | 1%~3% 1) |
| 印度(536例) | 53% 1) |
| 中国(1086例) | 32% 1) |
| 日本(38例) | 29% 1) |
亚洲人患有眼睑恶性肿瘤时,其为脂腺癌的概率是非亚洲人的6.21倍(范围3.8~10.1)1)。但脂腺癌本身的发病率在白人中(2.03/百万)高于亚洲/太平洋岛民(1.07/百万)。由于亚洲人基底细胞癌相对较少,因此脂腺癌在所有恶性肿瘤中的比例显得较高。
发病平均年龄在印度人群中为58岁,总体报告为57~72岁 1)。除眼睑外,25%的病例可能发生在头颈部、其他皮肤或生殖器区域。
Muir–Torre综合征是一种常染色体显性遗传病,表现为脂腺肿瘤与内脏恶性肿瘤(胃肠道、子宫内膜、泌尿系统)并存。其背景是DNA错配修复基因(MLH1、MSH2、MSH6)的突变,24%的Muir–Torre综合征患者会发生脂腺癌。诊断脂腺癌时,建议同时询问家族史和消化道症状。
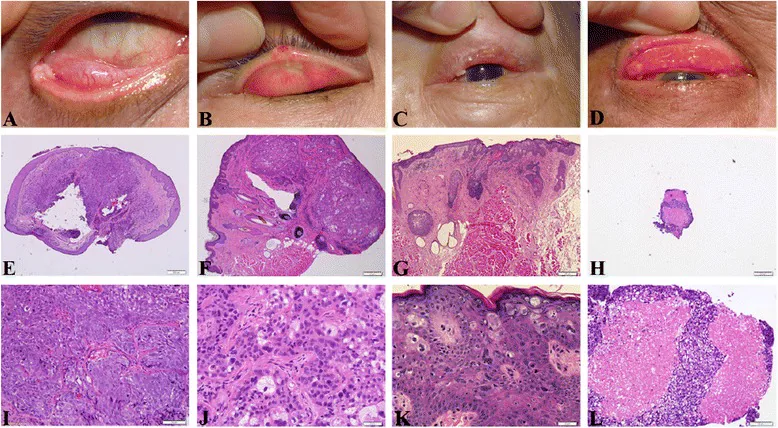
结节型(56%)
黄色调结节性肿块:由于肿瘤细胞内的脂质,呈特征性黄色外观。好发于上眼睑缘,表面不规则,伴有易出血的肿瘤血管。
通过眼睑翻转观察:翻转眼睑检查结膜侧也很重要。
弥漫型(7%)
不形成肿块的上皮内浸润:从睑板腺开口向睑缘皮肤和睑结膜薄层扩散的类型。诊断最易延迟。
睫毛脱落(睫毛秃):弥漫型的一个特征性表现。必须作为恶性肿瘤或严重炎症的体征进行检查。
肿瘤发生部位:上眼睑59%,下眼睑29%,内眦3%,外眦2%1)。
睫毛脱落的重要性:当眼睑缘存在皮脂腺癌等恶性肿瘤或严重炎症时,睫毛会脱落。发现睫毛脱落时,应仔细观察周围是否有致病病变,对怀疑恶性的病变考虑活检或咨询肿瘤专科医生。
佩吉特样播散:肿瘤细胞从主病灶向远离的睑球结膜上皮内呈片状增殖扩散的特征性模式。表现为覆盖整个睑结膜的烟花状肿瘤血管和肿瘤细胞增生,可形成跳跃性病变。
伟大伪装者(great masquerader):类似霰粒肿、慢性睑缘炎、基底细胞癌、鳞状细胞癌、上方角膜缘角结膜炎、眼瘢痕性类天疱疮。结节性病变易被误认为霰粒肿,切开后反复复发增大。有时可通过抗生素眼膏治疗是否改善来鉴别佩吉特样播散和睑缘炎。
亚洲人患有眼睑恶性肿瘤时,患睑板腺癌的概率是非亚洲人的6.21倍1)。但这是相对比例的问题,睑板腺癌的发病率(每人口)实际上是白人(2.03/百万)高于亚洲/太平洋岛民(1.07/百万)。由于亚洲人基底细胞癌较少,因此睑板腺癌的比例相对显得较高。
保持高度怀疑(high index of suspicion)最为重要。以下情况应积极怀疑睑板腺癌:
即使认为是霰粒肿,刮除物也必须送病理检查。 使用抗生素眼膏后是否改善,有时可帮助鉴别佩吉特样扩散与睑缘炎。
如果怀疑皮脂腺癌,应进行以下影像学检查以评估转移和浸润。
根据肿瘤大小和眼睑/眼眶浸润情况,分为T1至T42)。
| T分类 | 定义 |
|---|---|
| T1 | 肿瘤最大径 ≤10 mm |
| T2 | 肿瘤最大径 >10~20 mm |
| T3 | 肿瘤最大径 >20 mm |
| T4 | 浸润眼眶、鼻窦等 |
第8版与第7版相比,T1的定义扩大(从≤5 mm改为≤10 mm),并且显示会发生降期2)。
组织学上,嗜碱性肿瘤细胞呈巢状增殖,异型性和多形性明显,胞质内脂滴(HE染色中呈空泡状)是其特征。分化差时脂滴不明显,可能被诊断为鳞状细胞癌。如果肿瘤起源于睑板内,即使只有少数胞质内脂滴,也应诊断为皮脂腺癌。
目前标准的免疫组织化学标志物如下所示。
| 标志物 | 特征 |
|---|---|
| 脂滴包被蛋白 | 细胞内脂滴相关蛋白。对皮脂腺分化敏感性高且实用3) |
| 雄激素受体 | 眼睑皮脂腺癌通常阳性 |
| 上皮膜抗原(EMA) | 阳性 |
Muir-Torre综合征筛查:通过免疫组织化学染色检查MLH1、MSH2、MSH6的表达是否缺失。
手术切除是治疗的主要手段。
对于眼睑局限病例,切除时安全边界应**≥3 mm**。最好进行冰冻切片术中切缘评估。
根据睑板缺损范围的重建策略:
欧美的莫氏显微手术或完全周边及深部切缘评估法(CCPDMA)是在评估所有切缘的同时切除的方法,有望降低切缘阳性率。
如果佩吉特样播散局限于上皮内,抗肿瘤滴眼液可能保留眼球。如果病变侵犯超过基底膜,滴眼液治疗无效。
丝裂霉素C(MMC)滴眼液:
5-氟尿嘧啶(5-FU)滴眼液:
适用于眼眶浸润、巨大且深部浸润的病变、广泛球结膜波及的病例。据报道,按AJCC分期的手术实施率分别为T1 3%、T2 3%、T3 8%、T4 63%2)。
对于T2c期及以上的眼眶周围肿瘤可考虑。
皮脂腺癌对放射线敏感,用于根治性切除困难或术后辅助治疗。
标准做法是切除时保证3 mm以上的安全切缘。通过冰冻切片进行术中切缘评估,如果切缘阳性则追加切除。如果睑板缺损不超过1/3,可通过单纯缝合或局部皮瓣重建;如果超过,则分别重建前层和后层。对于T4肿瘤或眼眶浸润病例,考虑眼眶内容物剜除术。
皮脂腺癌是起源于皮脂腺腺上皮的恶性肿瘤。原发部位分布据报道为:睑板腺来源92%,蔡氏腺6%,泪阜2%2)。
组织学上,皮脂腺细胞(胞质空泡化、富含脂质的细胞)与未分化基底样细胞混合存在,分化程度从高分化到低分化不等。肿瘤细胞内的脂质使其肉眼呈黄色。分化低时,组织学上与鳞状细胞癌的鉴别可能困难,但如果肿瘤发生在睑板内,即使发现少量胞质内脂滴也应诊断为皮脂腺癌。
佩吉特样扩散的机制:恶性细胞从主肿瘤部位单独迁移并增殖到远离主肿瘤的上皮——睑结膜、球结膜和皮肤。这形成跳跃性病变,肉眼看似正常的区域也可能存在肿瘤细胞。因此,通过结膜地图活检了解扩散范围对治疗至关重要。
Muir-Torre综合征的分子机制:由DNA错配修复基因(MLH1、MSH2、MSH6、PMS2)突变引起的常染色体显性遗传病。突变导致DNA复制错误修复功能丧失,肿瘤抑制基因突变积累,从而产生皮脂腺肿瘤。
预后相关因素:肿瘤尺寸超过15 mm时区域淋巴结转移风险增加。佩吉特样扩散或眼眶浸润病例预后不良倾向,可能发生转移相关死亡。
Morawala(2023)对119例皮脂腺癌进行了AJCC第8版T分类的评估,表明T分类对预后预测有用2)。T4肿瘤的淋巴结转移风险比为2.38,远处转移风险比为4.30,转移相关死亡风险比为6.62。此外,第8版将T1的定义从第7版的5毫米以下改为10毫米以下,确认了降期的发生。
Li & Finger(2021)对T2bN0M0眼眶皮脂腺癌进行了切除、冷冻凝固和超厚羊膜移植,随后进行了高剂量率近距离治疗(2000 cGy/5次)和电子束外照射放疗(36 Gy/20次),总剂量56 Gy5)。1年后视力20/20,无放射性视网膜病变或视神经病变。但发生了颈部淋巴结转移。
Adachi(2022)对一名97岁无法手术的耳前皮脂腺癌患者进行了60 Gy/30次的电子束治疗联合过氧化氢浸渍纱布4)。8个月后达到肉眼完全缓解。不良事件仅为2级放射性皮炎。提示过氧化氢有放射增敏作用,但仅为少数病例报告,需要进一步验证。
Kaliki S, Bothra N, Bejjanki KM, et al. Malignant eyelid tumors in India: a study of 536 Asian Indian patients. Ocul Oncol Pathol. 2019;5(3):210-219.
Morawala A, Mohamed A, Krishnamurthy A, Jajapuram SD, Kaliki S. Sebaceous gland carcinoma: analysis based on the 8th edition of American Joint Committee on Cancer classification. Eye (Lond). 2023;37(4):714-719.
Ramachandran V, Tumyan G, Loya A, Treat K, Vrcek I. Sebaceous carcinoma masquerading as orbital cellulitis. Cureus. 2022;14(2):e22288.
Adachi A, Oike T, Tamura M, Ota N, Ohno T. Radiotherapy with hydrogen peroxide-soaked gauze for preauricular sebaceous carcinoma. Cureus. 2022;14(7):e27464.
Li F, Stewart RD, Finger PT. Interstitial brachytherapy for orbital sebaceous carcinoma. Ophthalmic Plast Reconstr Surg. 2021;37(6):e215-e217.