前驱病变
光化性角化病:40岁以上肤色白皙者常见的过度角化病变。圆形至椭圆形,伴有红斑性基底。被视为鳞状细胞原位癌。
鲍温病(原位癌):表现为持续性褐色至红色斑块。易被误诊为银屑病或湿疹。与HPV16型密切相关。若不治疗,可进展为浸润性鳞状细胞癌。
皮角:丘疹至结节状基底上带有角质帽。基底可能伴有原位癌或浸润性鳞状细胞癌,需始终切除。
角化棘皮瘤:中央有角质凹陷的杯状结节。有时被归类为鳞状细胞癌的亚型。

眼睑鳞状细胞癌是一种起源于皮肤表皮棘层的浸润性恶性肿瘤。它是眼睑恶性肿瘤中仅次于基底细胞癌的第二常见类型。
眼睑鳞状细胞癌有两种发生模式。
结膜面(睑结膜)发生型在日本多见。在睑结膜面形成扁平红色肿瘤,可见烟花状肿瘤血管。角化明显时呈白色。肿瘤增生隆起时呈结节性病变。初发病变需与良性结膜乳头状瘤鉴别。乳头状瘤通过细血管蒂从结膜面生长,而鳞状细胞癌呈广基性生长。
皮肤/睫毛部发生型发生在眼睑附近皮肤或睫毛部(罕见)。部分被认为是日光性角化病(下一节)的恶变。根据角化程度呈白色、黄白色或红色,表面粗糙。具有角化倾向的嗜酸性多角形肿瘤细胞呈铺路石样增殖,有时形成癌珠。
注意:如果组织学上看似鳞状细胞癌但似乎起源于眼睑内部,需考虑低分化脂腺癌的可能性。
从睑结膜面发生的鳞状细胞癌与眼表面鳞状上皮肿瘤(OSSN)的概念重叠。OSSN是以角膜缘、球结膜和角膜为中心的上皮内至浸润性病变的总称。眼睑皮肤发生型属于AJCC眼睑分类,而睑结膜发生型属于OSSN(AJCC结膜分类)4)。
发病率报告为每10万人0.09至2.42例2)。在美国和加拿大,年龄调整后的发病率在过去几十年中增加了50-200%。在西方国家,它仅占眼睑恶性肿瘤的5-10%,但在印度一项536例的研究中占18%(仅次于脂腺癌53%和基底细胞癌24%),日本一项研究报告约占48%,表明亚洲比例较高1)。
在印度536例的回顾性研究(Kaliki 2019)中,诊断时平均年龄55岁(范围8-90岁),男女比例为1:1.1,女性略多,好发部位为上眼睑40%、下眼睑41%1)。转移率报告为1-21%,生物学行为比基底细胞癌更具侵袭性。
估计每10万人0.09至2.42例。在西方国家,它占眼睑恶性肿瘤的5-10%,但在亚洲比例较高,日本有报告称约占眼睑恶性肿瘤的一半。
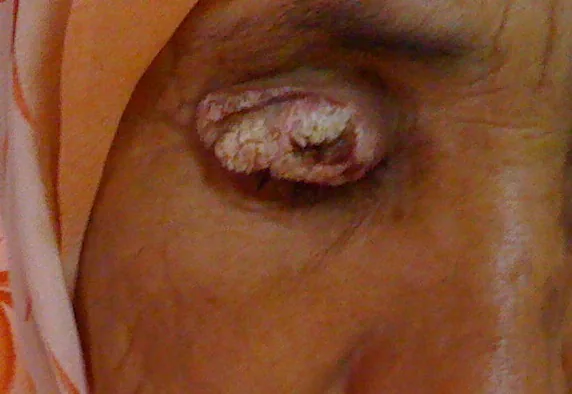
前驱病变和浸润性鳞状细胞癌的临床表现差异很大。
前驱病变
光化性角化病:40岁以上肤色白皙者常见的过度角化病变。圆形至椭圆形,伴有红斑性基底。被视为鳞状细胞原位癌。
鲍温病(原位癌):表现为持续性褐色至红色斑块。易被误诊为银屑病或湿疹。与HPV16型密切相关。若不治疗,可进展为浸润性鳞状细胞癌。
皮角:丘疹至结节状基底上带有角质帽。基底可能伴有原位癌或浸润性鳞状细胞癌,需始终切除。
角化棘皮瘤:中央有角质凹陷的杯状结节。有时被归类为鳞状细胞癌的亚型。
浸润性鳞状细胞癌
结膜型:平坦的红色肿瘤,伴有烟花状肿瘤血管。角化明显时呈白色。增生隆起后形成结节性病变。
皮肤型:白色、黄白色或红色,表面粗糙。表现为结节型(52%)或溃疡型(40%)。
注意肿瘤浸润方向:如果肿瘤越过睑缘并浸润至睑板前方,则需要像睑板腺癌一样进行眼睑全层切除和重建手术。
眼睑表现:睫毛脱落、毛细血管扩张、眼睑结构扭曲、眼睑位置异常。
鳞状细胞癌的发生是由多种风险因素共同促进的。
会显著增加。皮肤鳞状细胞癌是实体器官移植后最常见的恶性肿瘤之一,5年内发病率在肺移植中达30%,心脏移植中高达26%。移植后定期进行皮肤和眼科检查非常重要。
鳞状细胞癌的临床诊断与病理诊断符合率仅为46%(基底细胞癌为86%,脂腺癌为91%),因此必须通过病理组织检查(切除活检)进行确诊1)。
术前进行头颈部CT或MRI以检查有无转移。
对于结膜病变,以下无创诊断辅助工具非常有用4)。
当临床难以区分基底细胞癌或低分化皮脂腺癌时,免疫组织化学染色可作为辅助诊断工具。
| 标志物 | 鳞状细胞癌 | 基底细胞癌 |
|---|---|---|
| Ber-EP4 | 阴性 | 几乎总是阳性 |
| 上皮膜抗原(EMA) | 高阳性率 | 低阳性率 |
组织学确认肿瘤切缘阴性的完全手术切除是证据最强的标准治疗。
对于早期病灶(局限于睑结膜面),行包括部分睑板的全切除。确认切缘阴性后,在切除面追加2~3次冷冻凝固(冻融)。
如果肿瘤越过睑缘并浸润至睑板前方,需参照皮脂腺癌行眼睑全层切除和重建术。
与皮脂腺癌一样,术前需确认有无转移(头颈部CT/MRI)。
主要手术方式如下:
在Kaliki 2019中,76%的鳞状细胞癌病例接受了广泛切除活检1)。
使用液氮破坏组织。仅适用于光化性角化病和鳞状细胞原位癌(不适用于浸润癌)。此外,对于早期病灶,可作为术中切除面的附加冷冻融解使用。
用于手术风险过高的患者的单独治疗,或作为神经/淋巴结扩展或边界不清的癌的术后辅助治疗。每周照射3-5次,持续约1-2个月。鳞状细胞癌对放射线敏感,是根治性切除困难时的选择。
适用于伴有远处转移的进展期鳞状细胞癌。
印度99例鳞状细胞癌患者的治疗结果如下所示1)。
| 指标 | 比例 |
|---|---|
| 肿瘤复发 | 8% |
| 局部淋巴结转移 | 8% |
| 远处转移 | 4% |
| 疾病相关死亡 | 4% |
| 眼球保留 | 79% |
在5年Kaplan-Meier估计中,局部淋巴结转移为22%,远处转移为11%,转移相关死亡为11%1)。
在Kaliki 2019的研究中,术后肿瘤复发率为8%。5年Kaplan-Meier估计显示局部淋巴结转移达到22%,表明术后定期随访很重要。
紫外线直接(碱基转换)或间接(通过活性氧引起的氧化损伤)损伤DNA2)。晒伤诱导的细胞凋亡作为防御机制,但当DNA修复跟不上时,突变会积累。
增生/角化过度 → 轻至中度异型增生 → 重度异型增生/原位癌(光化性角化病/Bowen病)→ 浸润性鳞状细胞癌 → 转移性鳞状细胞癌
Marjolin溃疡:慢性难愈性创面或长期烧伤疤痕组织中发生鳞状细胞癌的病变。
眼睑皮肤型(皮肤型)是棘层细胞的逐步恶性转化,按AJCC眼睑TNM分类管理。睑结膜型是OSSN的一种形式,从结膜上皮异型增生(CIN:结膜上皮内瘤变)进展为浸润性SCC,适用AJCC结膜分类 4)。
0期至IB期
0期(Tis N0 M0):原位癌。未突破基底膜。
IA期(T1 N0 M0):肿瘤直径≤5mm,无睑板浸润。
IB期(T2a N0 M0):肿瘤直径>5mm至≤10mm,或睑板浸润。
IC期至IV期
IC期(T2b N0 M0):肿瘤直径>10mm至≤20mm,或眼睑全层受累。
II期(T3a N0 M0):肿瘤直径>20mm,或侵犯邻近眼部结构。
IIIB期(任何T N1 M0):区域淋巴结转移。
IV期(任何T任何N M1):远处转移。
Kaliki 2019的分期分布为T1: 26%、T2: 37%、T3: 7%、T4: 29%1)。组织学分级从G1(高分化)到G4(未分化),分级越低预后越好。
Ye等人(NEJM 2025)报告了一例34岁女性,因ZAP70种系突变导致T细胞受体信号障碍,发生伴有β-HPV19基因组整合的难治性浸润性皮肤鳞状细胞癌3)。该病例未检测到典型的鳞状细胞癌驱动突变(TP53、NOTCH1/2、CDKN2A),紫外线突变特征也较低,为26%(通常皮肤鳞状细胞癌平均77%)。通过异基因造血干细胞移植修复T细胞受体信号后,HPV特异性T细胞应答恢复,在35个月的随访中,包括鳞状细胞癌在内的所有HPV相关疾病均稳定消退。
该报告提示适应性免疫T细胞应答参与控制鳞状细胞癌的发生和进展3)。
西米普利单抗(抗PD-1抗体)已获FDA批准用于不可切除或转移性皮肤鳞状细胞癌,预计未来将扩展至眼眶和淋巴结受累的病例。免疫监视机制的参与逐渐明确,免疫抑制状态(如器官移植后、血液肿瘤等)下鳞状细胞癌风险增加也与T细胞应答调控异常有关2)3)。
抗PD-1抗体西米普利单抗已获FDA批准用于不可切除或转移性皮肤鳞状细胞癌。在HPV驱动的鳞状细胞癌中,也有通过造血干细胞移植进行免疫重建后肿瘤消退的病例报告。但后者属于研究阶段发现,并非标准治疗。
早期发现和完全切除后预后良好。然而,其生物学行为比基底细胞癌更具侵袭性,存在向眼眶、淋巴结和远处器官转移的风险。恶性眼眶浸润病例需与肿瘤内科、放射肿瘤科等多学科协作管理。
随访要点如下。
5年Kaplan-Meier估计显示区域淋巴结转移22%、远处转移11%、转移相关死亡11% 1),需要长期监测。