มะเร็งเซลล์สความัสของเปลือกตาเป็นเนื้องอกร้ายที่ลุกลามซึ่งเกิดจากชั้นสไปนอซัมของผิวหนังชั้นนอก เป็นเนื้องอกร้ายของเปลือกตาที่พบบ่อยเป็นอันดับสองรองจากมะเร็งเซลล์เบซอล
มะเร็งเซลล์สความัสของเปลือกตามีรูปแบบการเกิด 2 แบบ
แบบที่เกิดจากผิวเยื่อบุตา (เยื่อบุเปลือกตา) พบได้บ่อยในญี่ปุ่น ก่อตัวเป็นเนื้องอกแบนสีแดงซึ่งมองเห็นเส้นเลือดของเนื้องอกคล้ายดอกไม้ไฟบนผิวเยื่อบุเปลือกตา หากมีการสร้างเคราตินมาก เนื้องอกจะมีสีขาว เมื่อเนื้องอกโตและนูนขึ้น จะมีลักษณะเป็นก้อนกลม รอยโรคเริ่มต้นต้องแยกจากติ่งเนื้อเยื่อบุตา ชนิดไม่ร้ายแรง ในขณะที่ติ่งเนื้อจะเติบโตจากผิวเยื่อบุตา ผ่านก้านเส้นเลือดบางๆ แต่มะเร็งเซลล์สความัส จะเติบโตแบบฐานกว้าง
แบบที่เกิดจากผิวหนังหรือแนวขนตา เกิดขึ้นที่ผิวหนังใกล้เปลือกตาหรือแนวขนตา (พบน้อย) บางกรณีคิดว่าเป็นการกลายเป็นมะเร็งของภาวะเคราตินจากแสงแดด (หัวข้อถัดไป) ขึ้นอยู่กับระดับการสร้างเคราติน เนื้องอกมีสีขาว ขาวเหลือง หรือแดง ผิวขรุขระ เซลล์เนื้องอกรูปหลายเหลี่ยมที่ชอบสีอีโอซินและมีแนวโน้มสร้างเคราตินจะเพิ่มจำนวนแบบแผ่นหิน และบางครั้งก่อตัวเป็นไข่มุกมะเร็ง
หมายเหตุ: แม้ว่าลักษณะเนื้อเยื่อจะดูเหมือนมะเร็งเซลล์สความัส แต่หากดูเหมือนเกิดจากภายในเปลือกตา ควรพิจารณาความเป็นไปได้ของมะเร็งต่อมไขมัน ชนิดแยกตัวไม่ดี
มะเร็งเซลล์สความัส ที่เกิดจากเยื่อบุเปลือกตาทับซ้อนกับแนวคิดของเนื้องอกผิวเยื่อบุผิวสความัสของผิวตา (OSSN ) OSSN เป็นคำรวมสำหรับรอยโรคตั้งแต่ในเยื่อบุผิวจนถึงรุกรานซึ่งมีศูนย์กลางที่ลิมบัส เยื่อบุลูกตา และกระจกตา แบบที่เกิดจากผิวหนังเปลือกตาจัดอยู่ในประเภท AJCC ของเปลือกตา ในขณะที่แบบที่เกิดจากเยื่อบุเปลือกตาจัดอยู่ใน OSSN (ประเภท AJCC ของเยื่อบุตา )4)
อุบัติการณ์รายงานอยู่ระหว่าง 0.09 ถึง 2.42 ต่อ 100,000 คนต่อปี2) ในสหรัฐอเมริกาและแคนาดา อุบัติการณ์ที่ปรับตามอายุเพิ่มขึ้น 50-200% ในช่วงหลายทศวรรษที่ผ่านมา ในยุโรปและอเมริกา พบเพียง 5-10% ของเนื้องอกร้ายของเปลือกตา แต่ในการศึกษาของอินเดีย 536 ราย พบ 18% (อันดับสามรองจากมะเร็งต่อมไขมัน 53% และมะเร็งเซลล์เบซอล 24%) และการศึกษาของญี่ปุ่นรายงานประมาณ 48% ซึ่งบ่งชี้สัดส่วนที่สูงกว่าในเอเชีย1)
ในการศึกษาย้อนหลัง 536 รายในอินเดีย (Kaliki 2019) อายุเฉลี่ยเมื่อวินิจฉัยคือ 55 ปี (ช่วง 8-90 ปี) อัตราส่วนเพศชาย:หญิง 1:1.1 โดยผู้หญิงมากกว่าเล็กน้อย และตำแหน่งที่พบบ่อยคือเปลือกตาบน 40% และเปลือกตาล่าง 41%1) อัตราการแพร่กระจายอยู่ระหว่าง 1% ถึง 21% ซึ่งบ่งชี้พฤติกรรมทางชีวภาพที่รุกรานมากกว่ามะเร็งเซลล์เบซอล
Q
มะเร็งเซลล์สความัสของเปลือกตาเกิดขึ้นบ่อยแค่ไหน?
A
อุบัติการณ์ประมาณ 0.09 ถึง 2.42 ต่อ 100,000 คน ในยุโรปและอเมริกา พบ 5-10% ของเนื้องอกร้ายของเปลือกตา แต่สัดส่วนสูงกว่าในเอเชีย และรายงานบางฉบับระบุว่าพบประมาณครึ่งหนึ่งของเนื้องอกร้ายของเปลือกตาในญี่ปุ่น
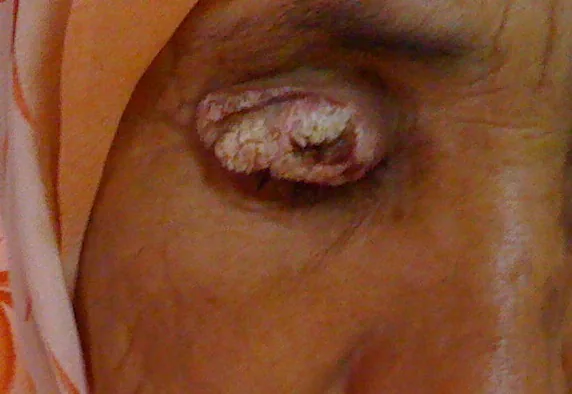
ภาพทางคลินิกของมะเร็งเซลล์สความัสที่เยื่อบุหนังตา: ก้อนสีขาวนูนร่วมกับภาวะเคราตินเกินและการเกิดสะเก็ด Lkhoyaali S, et al. Carcinome épidermoïde de la paupière supérieure droite. Pan Afr Med J. 2014;18:93. Figure 1. PM
CI D: PMC4231312. License: CC BY.
ก้อนสีขาวมีเคราติน เจริญออกนอก ครอบครองหนังตาบนขวาทั้งหมด ร่วมกับการเกิดสะเก็ดและการทำลายขอบหนังตา เป็นภาพทางคลินิกทั่วไปของมะเร็งเซลล์สความัส สอดคล้องกับลักษณะเป็นก้อน-แผลของ SCC ชนิดผิวหนังที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ตาแดง และรู้สึกมีสิ่งแปลกปลอมเยื่อบุตา อาจเริ่มด้วยอาการคล้ายเยื่อบุตาอักเสบ เลือดออกและสะเก็ด : เลือดออกหรือเกิดสะเก็ดจากรอยโรคที่มีการเจริญ proliferativeรู้สึกมีก้อน : สังเกตเป็นก้อน proliferative ที่หนังตาแผล : แผลจากเนื้อตายของเนื้องอกปวด : เกิดขึ้นเมื่อการลุกลามมากขึ้นชา : ความรู้สึกลดลงจากการลุกลามรอบเส้นประสาท
ภาพทางคลินิกแตกต่างกันอย่างมากระหว่างรอยโรคก่อนมะเร็งและมะเร็งเซลล์สความัส ชนิดลุกลาม
รอยโรคก่อนมะเร็ง
แอคทินิกเคอราโทซิส : รอยโรคเคราตินเกิน พบมากในคนผิวขาวอายุ 40 ปีขึ้นไป รูปกลมถึงรี มีฐานแดง จัดเป็นมะเร็งเซลล์สความัส ชนิดในที่
โรคโบเวน (มะเร็งในที่) : ปรากฏเป็นปื้นสีน้ำตาลถึงแดงเรื้อรัง มักถูกวินิจฉัยผิดเป็นโรคสะเก็ดเงินหรือกลาก สัมพันธ์อย่างมากกับ HPV ชนิด 16 หากปล่อยไว้จะกลายเป็นมะเร็งเซลล์สความัส ชนิดลุกลาม
เขาหนัง : มีตุ่มหรือก้อนมีปลอกเคราตินที่ฐาน ฐานอาจมีมะเร็งในที่หรือมะเร็งเซลล์สความัส ชนิดลุกลามร่วมด้วย จึงต้องตัดออกเสมอ
Keratoacanthoma : ก้อนรูปถ้วยที่มีหลุมเคราตินตรงกลาง บางครั้งจัดเป็นชนิดย่อยของมะเร็งเซลล์สความัส
มะเร็งเซลล์สความัสชนิดลุกลาม
ชนิดเยื่อบุตา : เนื้องอกสีแดงแบนที่มีหลอดเลือดคล้ายดอกไม้ไฟ ถ้ามีเคราตินมากจะออกสีขาว เมื่อโตและนูนขึ้นจะกลายเป็นรอยโรคแบบก้อน
ชนิดผิวหนัง : สีขาว ขาวเหลือง หรือแดง ผิวขรุขระ แสดงเป็นชนิดก้อน (52%) หรือชนิดแผล (40%)
ระวังทิศทางการลุกลามของเนื้องอก : ถ้าเนื้องอกเลยขอบเปลือกตาและลุกลามไปด้านหน้าของแผ่นเยื่อตาตุ่ม (tarsus) จำเป็นต้องตัดเปลือกตาทั้งชั้นและสร้างใหม่ เช่นเดียวกับมะเร็งต่อมไขมัน
อาการทางเปลือกตา : ขนตาร่วง, หลอดเลือดฝอยขยาย, โครงสร้างเปลือกตาผิดรูป, ตำแหน่งเปลือกตาผิดปกติ
การเกิดมะเร็งเซลล์สความัส ถูกกระตุ้นโดยปัจจัยเสี่ยงหลายอย่างที่ซ้อนทับกัน
การได้รับรังสีอัลตราไวโอเลต : ปัจจัยเสี่ยงที่สำคัญที่สุดที่สามารถย้อนกลับได้ การได้รับรังสี UVA และ UVB สะสมทำลาย DNA โดยตรง (base transition) หรือโดยอ้อม (reactive oxygen species) ส่งเสริมการเกิดมะเร็งผ่านการกลายพันธุ์ของ p532) อายุที่มากขึ้น : ความเสี่ยงเพิ่มขึ้นตามอายุผิวขาว (Fitzpatrick skin type ต่ำ) : ความเสี่ยงเพิ่มขึ้นในคนผิวขาว2) รอยโรคก่อนมะเร็ง : การดำเนินไปเป็นขั้นตอนจาก actinic keratosis → มะเร็งเซลล์สความัส ชนิดในที่ → มะเร็งเซลล์สความัส ชนิดลุกลาม → มะเร็งเซลล์สความัส ชนิดแพร่กระจายการติดเชื้อ human papilloma virus (HPV) : ในโรค Bowen มีความสัมพันธ์อย่างมากกับ HPV ชนิด 16 มีรายงานการเกี่ยวข้องของ HPV ชนิด 6/11, 16 และ 184) ภาวะภูมิคุ้มกันบกพร่อง : หลังการปลูกถ่ายอวัยวะ การใช้ยากดภูมิคุ้มกัน การติดเชื้อ HIV/AIDS เพิ่มความเสี่ยง2) โรคซีโรเดอร์มา พิกเมนโตซัม : การกลายพันธุ์แบบ autosomal recessive ในยีนซ่อมแซม DNA (XPA ถึง XPF) ทำให้มีความเสี่ยงมะเร็งผิวหนังชนิด non-melanoma สูงกว่าประชากรทั่วไป 10,000 เท่า2) อื่นๆ : การสัมผัสกับอนุพันธ์ของปิโตรเลียมและสารหนู การสูบบุหรี่ ภาวะผิวเผือก แผลเป็นจากไฟไหม้เก่า (แผล Marjolin) แผลเรื้อรัง
การใช้ครีมกันแดดทุกวันและพฤติกรรมที่หลีกเลี่ยงการสัมผัสแสงแดด (เช่น สวมหมวกและแว่นกันแดด หลีกเลี่ยงกิจกรรมกลางแจ้งในช่วงเวลาที่มีแสงแดดจัด) ช่วยลดการสัมผัสรังสียูวีซึ่งเป็นปัจจัยเสี่ยงหลัก หากมีแผลหรือรอยโรคที่มีการเจริญเติบโตผิดปกติที่ไม่หายเป็นเวลานานบนเปลือกตา ควรปรึกษาจักษุแพทย์หรือศัลยแพทย์ตกแต่งโดยเร็ว
Q
ความเสี่ยงของมะเร็งเซลล์สความัสที่เปลือกตาเพิ่มขึ้นหลังการปลูกถ่ายอวัยวะหรือไม่?
A
ใช่ เพิ่มขึ้นอย่างมีนัยสำคัญ มะเร็งเซลล์สความัส ที่ผิวหนังเป็นหนึ่งในเนื้องอกร้ายที่พบบ่อยที่สุดหลังการปลูกถ่ายอวัยวะแข็ง โดยอุบัติการณ์ภายใน 5 ปีสูงถึง 30% หลังปลูกถ่ายปอด และ 26% หลังปลูกถ่ายหัวใจ การตรวจผิวหนังและตาอย่างสม่ำเสมอหลังการปลูกถ่ายเป็นสิ่งสำคัญ
อัตราความสอดคล้องระหว่างการวินิจฉัยทางคลินิกและการวินิจฉัยทางพยาธิวิทยาสำหรับมะเร็งเซลล์สความัส ต่ำเพียง 46% (เทียบกับ 86% สำหรับมะเร็งเซลล์ฐาน และ 91% สำหรับมะเร็งต่อมไขมัน ) ดังนั้นการตรวจทางจุลพยาธิวิทยา (การตัดชิ้นเนื้อเพื่อการวินิจฉัย) จึงจำเป็นสำหรับการวินิจฉัยที่แน่นอน1)
บันทึกลักษณะทั่วไปของรอยโรค ขนาด การเป็นแผล การสูญเสียขนตา และการขยายตัวของเส้นเลือดฝอย
การตรวจตาอย่างสมบูรณ์รวมถึงการเคลื่อนไหวของลูกตาและภาวะตายื่น
การประเมินใบหน้าทั้งหมดและบริเวณที่สัมผัสแสงแดด และการตรวจสอบความรู้สึกบนใบหน้า
การคลำต่อมน้ำเหลืองในบริเวณ (ก่อนหู, ใต้ลิ้น, ใต้ขากรรไกร, คอ)
การสังเกตภาพการเปิดและปิดเปลือกตาทั้งหมด และพื้นผิวเยื่อบุตา ของเปลือกตาบนและล่าง
สำหรับเนื้องอกขนาดใหญ่ ให้ทำ CT หรือ MRI ของเบ้าตา เพื่อประเมินโครงสร้างภายในและการลุกลามเข้าไปในเบ้าตา
ก่อนการผ่าตัด จะทำ CT หรือ MRI ของศีรษะและคอเพื่อตรวจสอบการมีอยู่ของการแพร่กระจาย
การตัดชิ้นเนื้อแบบตัดออกทั้งหมด (มาตรฐานทองคำ) : วิธีการวินิจฉัยที่แน่นอนเพื่อกำหนดความลึกและขอบเขตของการลุกลามการเจาะดูดด้วยเข็มเล็ก : ทำเพื่อยืนยันการแพร่กระจายหากมีการเปลี่ยนแปลงในต่อมน้ำเหลืองในภูมิภาค
สำหรับรอยโรคที่เยื่อบุตา เครื่องมือช่วยวินิจฉัยแบบไม่รุกรานต่อไปนี้มีประโยชน์4)
OCT ความละเอียดสูง (HR-OCT )เซลล์วิทยาแบบประทับ : เก็บเซลล์จากผิวกระจกตา และเยื่อบุตา เพื่อตรวจเซลล์วิทยากล้องจุลทรรศน์คอนโฟคอล ในร่างกาย
ชนิดเจริญดี : เซลล์รูปหลายเหลี่ยม ไซโทพลาซึมติดสี eosin มาก นิวเคลียสติดสีเข้ม เซลล์เคราตินผิดปกติ สะพานเชื่อมระหว่างเซลล์ เม็ดเคราติน (cancer pearl)ชนิดเจริญไม่ดี : เซลล์ dysplasia แบบ pleomorphic ภาพการแบ่งเซลล์ผิดปกติ ไม่มีหลักฐานของเคราตินไนเซชัน สูญเสียสะพานเชื่อมระหว่างเซลล์ชนิดย่อย : ชนิดเซลล์รูปกระสวย ชนิดต่อม (adenoid)
เมื่อแยกทางคลินิกระหว่างมะเร็งเซลล์ฐาน หรือมะเร็งต่อมไขมัน ชนิดเจริญไม่ดีได้ยาก การย้อมอิมมูโนฮิสโตเคมีมีประโยชน์ในการวินิจฉัยเสริม
เครื่องหมาย มะเร็งเซลล์สความัส มะเร็งเซลล์ฐาน Ber-EP4 ลบ เกือบเป็นบวกเสมอ แอนติเจนเยื่อหุ้มเซลล์เยื่อบุผิว (EMA) อัตราการเป็นบวกสูง อัตราการเป็นบวกต่ำ
โรคไม่ร้ายแรง : ติ่งเนื้อเยื่อบุตา (มีก้าน, ก้านหลอดเลือดเล็ก), ไขมันในหนังศีรษะ, ไขมันจากแสงแดด, เนื้องอกเคอราติน, กุ้งยิง ใน, ถุงน้ำโรคร้ายแรง : มะเร็งเซลล์ฐาน , มะเร็งต่อมไขมัน (ชนิดแยกตัวไม่ดี—คล้ายกันทางเนื้อเยื่อ→ต้องย้อมอิมมูโน), มะเร็งผิวหนังชนิดเมลาโนมา, มะเร็งต่อมน้ำเหลือง, เนื้องอกเซลล์เมอร์เคิล, เนื้องอกแพร่กระจายรอยโรคก่อนมะเร็ง/ในเยื่อบุผิว : เนื้องอกในเยื่อบุเยื่อบุตา (CIN , พบบ่อยที่ลิมบัส กระจกตา ถึงเยื่อบุตา ส่วนลูกตา)
การตัดออกทางศัลยกรรมทั้งหมดโดยยืนยันทางเนื้อเยื่อว่าขอบเขตปลอดเนื้องอกเป็นการรักษามาตรฐานที่มีหลักฐานแข็งแกร่งที่สุด
รอยโรคระยะเริ่มต้น (จำกัดเฉพาะเยื่อบุตา ส่วนเปลือกตา) : ทำการตัดออกทั้งหมดรวมถึงส่วนหนึ่งของแผ่นเปลือกตา หลังจากยืนยันขอบตัดเป็นลบ ให้ทำการจี้เย็น (แช่แข็งและละลาย) บนพื้นผิวที่ตัด 2-3 รอบ
หากเนื้องอกเลยขอบเปลือกตาและลุกลามไปด้านหน้าของแผ่นเปลือกตา : จำเป็นต้องตัดเปลือกตาทั้งชั้นและสร้างใหม่ตามแนวทางสำหรับมะเร็งต่อมไขมัน
เช่นเดียวกับมะเร็งต่อมไขมัน ก่อนผ่าตัดต้องยืนยันว่ามีหรือไม่มีการแพร่กระจาย (CT/MRI ศีรษะและคอ)
วิธีการผ่าตัดหลักมีดังนี้:
การผ่าตัด Mohs แบบจุลทรรศน์ : เทคนิคการตัดออกพร้อมประเมินขอบตัดทางพยาธิวิทยาแบบเรียลไทม์ ช่วยให้ตัดออกได้แม่นยำในขณะที่รักษาเนื้อเยื่อปกติให้มากที่สุดการตัดออกพร้อมตรวจทางพยาธิวิทยาเร็วระหว่างผ่าตัด : ยืนยันขอบตัดระหว่างผ่าตัดเมื่อตัดหนังตาทั้งชั้นออกทั้งหมด : การสร้างใหม่ด้วยแผ่นปิดหมุนหรือวิธี Cutler-Beardการตัดชิ้นเนื้อต่อมน้ำเหลืองเซนติเนล : พิจารณาในรอยโรคกว้าง การลุกลามรอบเส้นประสาท หรือรอยโรคกลับเป็นซ้ำการตัดเบ้าตา ออก : ทำเมื่อมีการลุกลามเข้าเบ้าตา โดยพยากรณ์การมองเห็น ไม่ดีและยังไม่ถึงโพรงเลือดดำคาเวอร์นัส กระทำใน 19% ของมะเร็งเซลล์สความัส 1)
ใน Kaliki 2019 การตัดออกกว้างพร้อมตัดชิ้นเนื้อกระทำใน 76% ของมะเร็งเซลล์สความัส 1)
การทำลายเนื้อเยื่อด้วยไนโตรเจนเหลว บ่งชี้เฉพาะสำหรับเคอราตินจากแสงแดดและมะเร็งเซลล์สความัส ชนิดในที่ (ไม่เหมาะสำหรับมะเร็งชนิดลุกลาม) และใช้เป็นการแช่แข็ง-ละลายเพิ่มเติมบนผิวตัดระหว่างผ่าตัดสำหรับรอยโรคระยะแรก
ใช้เป็นการรักษาเดี่ยวในผู้ป่วยที่มีความเสี่ยงสูงเกินไปต่อการผ่าตัด หรือเป็นการรักษาเสริมหลังผ่าตัดสำหรับมะเร็งที่มีการแพร่กระจายทางเส้นประสาท/ต่อมน้ำเหลืองหรือขอบเขตไม่ชัดเจน ฉายรังสี 3-5 ครั้งต่อสัปดาห์ประมาณ 1-2 เดือน มะเร็งเซลล์สความัส ไวต่อรังสี จึงเป็นทางเลือกเมื่อการตัดออกแบบรุนแรงทำได้ยาก
ครีม Imiquimod : ยาปรับภูมิคุ้มกัน บ่งชี้สำหรับเคอราตินจากแสงแดดและโรคโบเวน (รอยโรคก่อนมะเร็ง) ทา 3 ครั้งต่อสัปดาห์นาน 4-6 สัปดาห์ยาหยอดตา Mitomycin C (0.04%) : บ่งชี้สำหรับรอยโรคเยื่อบุตา เช่นการแพร่กระจายแบบพาเจ็ท อยด์ที่จำกัดเฉพาะเยื่อบุ หยอด 4 ครั้งต่อวันนาน 1 สัปดาห์ พัก 1 สัปดาห์ ทำซ้ำ 2-3 รอบ4) ยาหยอดตา 5-ฟลูออโรยูราซิล (1%) : ใช้สำหรับรอยโรคที่จำกัดอยู่เฉพาะในเยื่อบุผิวเช่นกัน หยอดวันละ 4 ครั้ง หยอด 4 วัน หยุด 30 วัน ทำซ้ำสูงสุด 6 รอบ4) ยาหยอดตา IFNα-2b : ผลข้างเคียงน้อยและมีการใช้ในผู้ป่วยนอกเพิ่มขึ้น มีประโยชน์สำหรับ OSSN ที่จำกัดอยู่ที่เยื่อบุตา 4)
ยาหยอดตาไมโตมัยซินซีและยาหยอดตา 5-ฟลูออโรยูราซิลเป็นการใช้นอกเหนือข้อบ่งชี้ที่ได้รับอนุมัติ (off-label) และต้องได้รับการอนุมัติจากคณะกรรมการจริยธรรม นอกจากนี้ยังไม่ได้ผลกับรอยโรคที่ลุกลามผ่านเยื่อฐาน ดังนั้นจึงใช้ได้เฉพาะรอยโรคที่จำกัดอยู่ภายในเยื่อบุผิวเท่านั้น
ใช้สำหรับมะเร็งเซลล์สความัส ชนิดลุกลามที่มีการแพร่กระจายไปไกล
เซมิพลิแมบ : แอนติบอดีต่อต้าน PD-1 ได้รับการอนุมัติจาก FDA สำหรับมะเร็งเซลล์สความัส ผิวหนังชนิดกว้างขวาง ผ่าตัดไม่ได้ หรือแพร่กระจายซีทูซิแมบ : แอนติบอดีต่อต้าน EGFR มีประสิทธิภาพในผู้ป่วยบางราย
ด้านล่างนี้คือผลการรักษาในผู้ป่วยมะเร็งเซลล์สความัส 99 รายในอินเดีย1)
ตัวชี้วัด สัดส่วน การกลับเป็นซ้ำของเนื้องอก 8% การแพร่กระจายไปยังต่อมน้ำเหลืองเฉพาะที่ 8% การแพร่กระจายระยะไกล 4% การเสียชีวิตจากโรค 4% การรักษาลูกตาไว้ 79%
ในการประมาณค่า Kaplan-Meier ที่ 5 ปี การแพร่กระจายไปยังต่อมน้ำเหลืองเฉพาะที่ 22% การแพร่กระจายระยะไกล 11% และการเสียชีวิตที่เกี่ยวข้องกับการแพร่กระจาย 11%1)
Q
โอกาสที่มะเร็งเซลล์สความัสของเปลือกตาจะกลับมาเป็นซ้ำหลังการผ่าตัดมีเท่าใด?
A
ในการศึกษาของ Kaliki 2019 พบการกลับมาเป็นซ้ำของเนื้องอกหลังผ่าตัดใน 8% ของกรณี การประมาณค่า Kaplan-Meier ที่ 5 ปีแสดงให้เห็นว่าการแพร่กระจายไปยังต่อมน้ำเหลืองเฉพาะที่สูงถึง 22% ดังนั้นการติดตามผลอย่างสม่ำเสมอหลังการผ่าตัดจึงมีความสำคัญ
รังสีอัลตราไวโอเลตทำลายดีเอ็นเอโดยตรง (การเปลี่ยนเบส) หรือโดยอ้อม (ความเสียหายจากออกซิเดชันผ่านอนุมูลอิสระ)2) การเหนี่ยวนำให้เกิดอะพอพโทซิส จากการถูกแดดเผาทำหน้าที่เป็นกลไกป้องกัน แต่ถ้าการซ่อมแซมดีเอ็นเอไม่ทัน การกลายพันธุ์จะสะสม
การยับยั้ง p53 : ยีนต้านเนื้องอก p53 ถูกทำลายโดยตรงจากรังสีอัลตราไวโอเลตและถูกยับยั้ง การทำงานในการยับยั้งวัฏจักรเซลล์และการควบคุมอะพอพโทซิส หายไป ทำให้เซลล์กลายพันธุ์เพิ่มจำนวน2) ความไม่เสถียรของจีโนม : ความไม่เสถียรของจีโนมในเคราติโนไซต์น่าจะเกิดจากการยับยั้ง p53การกลายพันธุ์แบบไดรเวอร์โซมาติกทั่วไป : TP53, NOTCH1/2, CDKN2A และอื่นๆ3) ภาระการกลายพันธุ์ของเนื้องอกโดยเฉลี่ย : ในมะเร็งเซลล์สความัส ของผิวหนัง ประมาณ 50 การกลายพันธุ์/เมกะเบส ซึ่งสูง3)
การเพิ่มจำนวนและภาวะเคราตินมากเกิน → ภาวะ dysplasia เล็กน้อยถึงปานกลาง → ภาวะ dysplasia รุนแรงและมะเร็งระยะเริ่มต้น (actinic keratosis/โรค Bowen) → มะเร็งเซลล์สความัส ชนิดลุกลาม → มะเร็งเซลล์สความัส ชนิดแพร่กระจาย
แผล Marjolin : ภาวะที่มะเร็งเซลล์สความัส เกิดขึ้นจากเนื้อเยื่อแผลเป็นของบาดแผลเรื้อรังที่ไม่หายหรือรอยแผลเป็นจากการไหม้ระยะยาว
ชนิดผิวหนังเปลือกตา (ชนิดผิวหนัง) คือการเปลี่ยนแปลงเป็นมะเร็งแบบค่อยเป็นค่อยไปของเซลล์ชั้น spinous ซึ่งจัดการโดยการจำแนก TNM ของ AJCC สำหรับเปลือกตา ชนิดเยื่อบุเปลือกตาเป็นรูปแบบหนึ่งของ OSSN ที่พัฒนาจาก dysplasia ของเยื่อบุตา (CIN ) ไปเป็น SCC ชนิดลุกลาม และใช้การจำแนกของ AJCC สำหรับเยื่อบุตา 4)
ระยะ 0 ถึง IB
ระยะ 0 (Tis N0 M0) : มะเร็งระยะเริ่มต้น (carcinoma in situ) ไม่ลุกลามผ่านเยื่อฐาน
ระยะ IA (T1 N0 M0) : เส้นผ่านศูนย์กลางเนื้องอก ≤5 มม. ไม่มีการบุกรุกเข้าไปในแผ่นเปลือกตา (tarsus)
ระยะ IB (T2a N0 M0) : เส้นผ่านศูนย์กลางเนื้องอก >5 มม. ถึง ≤10 มม. หรือมีการบุกรุกเข้าไปในแผ่นเปลือกตา
ระยะ IC ถึง IV
ระยะ IC (T2b N0 M0) : เส้นผ่านศูนย์กลางเนื้องอก >10 มม. ถึง ≤20 มม. หรือมีการลุกลามตลอดความหนาของเปลือกตา
ระยะ II (T3a N0 M0) : เส้นผ่านศูนย์กลางเนื้องอก >20 มม. หรือมีการลุกลามไปยังโครงสร้างใกล้เคียงตา
ระยะ IIIB (ใดๆ T N1 M0) : มีการแพร่กระจายไปยังต่อมน้ำเหลืองในภูมิภาค
ระยะที่ IV (ใดๆ T ใดๆ N M1) : การแพร่กระจายระยะไกล
การกระจายระยะตาม Kaliki 2019 คือ T1: 26%, T2: 37%, T3: 7%, T4: 29%1) ระดับเนื้อเยื่อวิทยาตั้งแต่ G1 (มีความแตกต่างดี) ถึง G4 (ไม่มีความแตกต่าง) ยิ่งระดับต่ำยิ่งพยากรณ์โรคดี
เนื้อหาต่อไปนี้อยู่ในระยะวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
Ye และคณะ (NEJM 2025) รายงานกรณีหญิงอายุ 34 ปีที่มีความบกพร่องในการส่งสัญญาณของรีเซพเตอร์ทีเซลล์เนื่องจากการกลายพันธุ์ของยีน ZAP70 ในเซลล์สืบพันธุ์ ซึ่งเกิดมะเร็งเซลล์สความัส ผิวหนังชนิดลุกลามดื้อต่อการรักษาร่วมกับการรวมตัวของจีโนม β-HPV193) ในกรณีนี้ ไม่พบการกลายพันธุ์ขับเคลื่อนทั่วไปของมะเร็งเซลล์สความัส (TP53, NOTCH1/2, CDKN2A) และลายเซ็นการกลายพันธุ์จากรังสียูวีต่ำที่ 26% (เทียบกับค่าเฉลี่ย 77% ในมะเร็งเซลล์สความัส ผิวหนังทั่วไป) หลังจากซ่อมแซมการส่งสัญญาณของรีเซพเตอร์ทีเซลล์โดยการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดแบบ allogeneic การตอบสนองของทีเซลล์จำเพาะต่อ HPV ฟื้นตัว และโรคที่เกี่ยวข้องกับ HPV ทั้งหมดรวมถึงมะเร็งเซลล์สความัส มีการถดถอยอย่างคงที่ในระหว่างการติดตามผล 35 เดือน
รายงานนี้ชี้ให้เห็นว่าการตอบสนองของทีเซลล์ภูมิคุ้มกันแบบปรับตัวมีส่วนเกี่ยวข้องในการควบคุมการเริ่มต้นและการดำเนินของมะเร็งเซลล์สความัส 3)
Cemiplimab (แอนติบอดีต่อต้าน PD-1) ได้รับการอนุมัติจาก FDA สำหรับมะเร็งเซลล์สความัส ผิวหนังชนิดไม่สามารถผ่าตัดได้หรือแพร่กระจาย และคาดว่าจะมีการขยายข้อบ่งชี้ในอนาคตสำหรับกรณีที่มีการลุกลามไปยังเบ้าตา หรือต่อมน้ำเหลือง บทบาทของการเฝ้าระวังภูมิคุ้มกันเริ่มชัดเจนขึ้น และความเสี่ยงที่เพิ่มขึ้นของมะเร็งเซลล์สความัส ในภาวะกดภูมิคุ้มกัน (หลังการปลูกถ่ายอวัยวะ เนื้องอกในเลือด ฯลฯ) เชื่อว่าเกี่ยวข้องกับความผิดปกติในการควบคุมการตอบสนองของทีเซลล์2) 3)
Q
การบำบัดด้วยภูมิคุ้มกันมีประสิทธิภาพสำหรับมะเร็งเซลล์สความัสที่เปลือกตาหรือไม่?
A
Cemiplimab (แอนติบอดีต่อต้าน PD-1) ได้รับการอนุมัติจาก FDA สำหรับมะเร็งเซลล์สความัส ผิวหนังชนิดไม่สามารถผ่าตัดได้หรือแพร่กระจาย นอกจากนี้ยังมีรายงานกรณีการถดถอยของเนื้องอกในมะเร็งเซลล์สความัส ที่ขับเคลื่อนโดย HPV หลังการฟื้นฟูภูมิคุ้มกันโดยการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือด อย่างไรก็ตาม กรณีหลังเป็นความรู้ในระยะวิจัย ไม่ใช่การรักษามาตรฐานทั่วไป
ด้วยการตรวจพบตั้งแต่เนิ่นๆ และการตัดออกอย่างสมบูรณ์ การพยากรณ์โรคดี อย่างไรก็ตาม มีพฤติกรรมทางชีววิทยาที่รุกรานมากกว่ามะเร็งเซลล์ฐาน โดยมีความเสี่ยงต่อการแพร่กระจายไปยังเบ้าตา ต่อมน้ำเหลือง และอวัยวะระยะไกล กรณีที่มีการลุกลามเข้าสู่เบ้าตา ชนิดร้ายจะจัดการด้วยความร่วมมือแบบสหสาขาวิชาชีพกับอายุรศาสตร์มะเร็งวิทยา รังสีรักษา ฯลฯ
ประเด็นสำคัญของการติดตามผลมีดังนี้:
การตรวจตาเป็นระยะหลังผ่าตัดและการคลำต่อมน้ำเหลืองในบริเวณ
การสังเกตผิวหนังเป็นระยะรวมถึงบริเวณใบหน้าที่โดนแสงแดด
การใช้ครีมกันแดดและคำแนะนำในการใช้ชีวิตเพื่อลดการสัมผัสแสงแดด
การติดตามผลบ่อยขึ้นในผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง
การประมาณค่า Kaplan-Meier ที่ 5 ปีแสดงการแพร่กระจายไปยังต่อมน้ำเหลืองเฉพาะที่ 22% การแพร่กระจายระยะไกล 11% และการเสียชีวิตที่เกี่ยวข้องกับการแพร่กระจาย 11% 1) จึงจำเป็นต้องมีการเฝ้าระวังในระยะยาว
Kaliki S, Bothra N, Bejjanki KM, et al. Malignant Eyelid Tumors in India: A Study of 536 Asian Indian Patients. Ocul Oncol Pathol. 2019;5(3):210-219.
Scholl AR, Flanagan MB, Thompson AD. Educational Case: Squamous cell carcinoma. Acad Pathol. 2025;12(3):100206.
Ye P, Bergerson JRE, Brownell I, et al. Resolution of Squamous-Cell Carcinoma by Restoring T-Cell Receptor Signaling. N Engl J Med. 2025;393(5):469-478.
Tsatsos M, Delimitrou C, Tsinopoulos I, et al. Update in the Diagnosis and Management of Ocular Surface Squamous Neoplasia (OSSN ).