前驅病變
光化性角化病:40歲以上膚色白皙者常見的過度角化病變。圓形至橢圓形,伴有紅斑性基底。被視為鱗狀細胞原位癌。
鮑溫病(原位癌):表現為持續性褐色至紅色斑塊。易被誤診為乾癬或濕疹。與HPV16型密切相關。若不治療,可進展為浸潤性鱗狀細胞癌。
皮角:丘疹至結節狀基底上帶有角質帽。基底可能伴有原位癌或浸潤性鱗狀細胞癌,需始終切除。
角化棘皮瘤:中央有角質凹陷的杯狀結節。有時被歸類為鱗狀細胞癌的亞型。

眼瞼鱗狀細胞癌是一種起源於皮膚表皮棘層的浸潤性惡性腫瘤。它是眼瞼惡性腫瘤中僅次於基底細胞癌的第二常見類型。
眼瞼鱗狀細胞癌有兩種發生模式。
結膜面(瞼結膜)發生型在日本多見。在瞼結膜面形成扁平紅色腫瘤,可見煙火狀腫瘤血管。角化明顯時呈白色。腫瘤增生隆起時呈結節性病變。初發病變需與良性結膜乳頭狀瘤鑑別。乳頭狀瘤透過細血管蒂從結膜面生長,而鱗狀細胞癌呈廣基性生長。
皮膚/睫毛部發生型發生在眼瞼附近皮膚或睫毛部(罕見)。部分被認為是日光性角化病(下一節)的惡變。根據角化程度呈白色、黃白色或紅色,表面粗糙。具有角化傾向的嗜酸性多角形腫瘤細胞呈鋪路石樣增殖,有時形成癌珠。
注意:如果組織學上看似鱗狀細胞癌但似乎起源於眼瞼內部,需考慮低分化脂腺癌的可能性。
從瞼結膜面發生的鱗狀細胞癌與眼表面鱗狀上皮腫瘤(OSSN)的概念重疊。OSSN是以角膜緣、球結膜和角膜為中心的上皮內至浸潤性病變的總稱。眼瞼皮膚發生型屬於AJCC眼瞼分類,而瞼結膜發生型屬於OSSN(AJCC結膜分類)4)。
發生率報告為每10萬人0.09至2.42例2)。在美國和加拿大,年齡調整後的發生率在過去幾十年中增加了50-200%。在西方國家,它僅佔眼瞼惡性腫瘤的5-10%,但在印度一項536例的研究中佔18%(僅次於脂腺癌53%和基底細胞癌24%),日本一項研究報告約佔48%,表明亞洲比例較高1)。
在印度536例的回顧性研究(Kaliki 2019)中,診斷時平均年齡55歲(範圍8-90歲),男女比例為1:1.1,女性略多,好發部位為上眼瞼40%、下眼瞼41%1)。轉移率報告為1-21%,生物學行為比基底細胞癌更具侵襲性。
估計每10萬人0.09至2.42例。在西方國家,它佔眼瞼惡性腫瘤的5-10%,但在亞洲比例較高,日本有報告稱約佔眼瞼惡性腫瘤的一半。
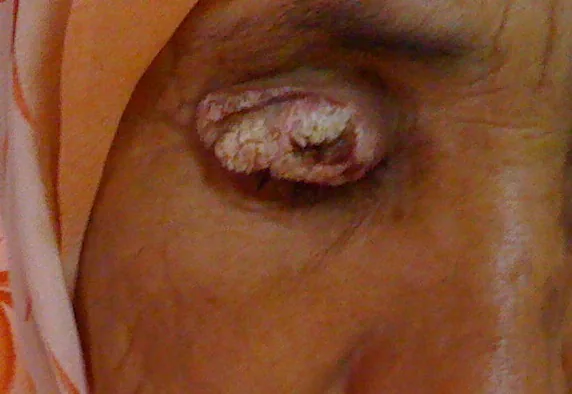
前驅病變和浸潤性鱗狀細胞癌的臨床表現差異很大。
前驅病變
光化性角化病:40歲以上膚色白皙者常見的過度角化病變。圓形至橢圓形,伴有紅斑性基底。被視為鱗狀細胞原位癌。
鮑溫病(原位癌):表現為持續性褐色至紅色斑塊。易被誤診為乾癬或濕疹。與HPV16型密切相關。若不治療,可進展為浸潤性鱗狀細胞癌。
皮角:丘疹至結節狀基底上帶有角質帽。基底可能伴有原位癌或浸潤性鱗狀細胞癌,需始終切除。
角化棘皮瘤:中央有角質凹陷的杯狀結節。有時被歸類為鱗狀細胞癌的亞型。
浸潤性鱗狀細胞癌
結膜型:平坦的紅色腫瘤,帶有煙火狀腫瘤血管。角化明顯時呈白色。增生隆起後形成結節性病變。
皮膚型:白色、黃白色或紅色,表面粗糙。表現為結節型(52%)或潰瘍型(40%)。
注意腫瘤浸潤方向:如果腫瘤越過瞼緣並浸潤至瞼板前方,則需要像瞼板腺癌一樣進行眼瞼全層切除和重建手術。
眼瞼表現:睫毛脫落、毛細血管擴張、眼瞼結構扭曲、眼瞼位置異常。
鱗狀細胞癌的發生是由多種風險因素共同促進的。
會顯著增加。皮膚鱗狀細胞癌是實體器官移植後最常見的惡性腫瘤之一,5年內發生率在肺移植中達30%,心臟移植中高達26%。移植後定期進行皮膚和眼科檢查非常重要。
鱗狀細胞癌的臨床診斷與病理診斷符合率僅為46%(基底細胞癌為86%,脂腺癌為91%),因此必須透過病理組織檢查(切除切片)進行確診1)。
術前進行頭頸部CT或MRI以檢查有無轉移。
對於結膜病變,以下非侵入性診斷輔助工具很有用4)。
當臨床上難以區分基底細胞癌或低分化皮脂腺癌時,免疫組織化學染色可作為輔助診斷工具。
| 標記 | 鱗狀細胞癌 | 基底細胞癌 |
|---|---|---|
| Ber-EP4 | 陰性 | 幾乎總是陽性 |
| 上皮膜抗原(EMA) | 高陽性率 | 低陽性率 |
組織學確認腫瘤切除邊緣陰性的完全手術切除是證據最強的標準治療。
對於早期病灶(侷限於瞼結膜面),行包含部分瞼板的全切除。確認切緣陰性後,在切除面追加2~3次冷凍凝固(凍融)。
如果腫瘤越過瞼緣並浸潤至瞼板前方,需參照皮脂腺癌行眼瞼全層切除和重建術。
與皮脂腺癌相同,術前需確認有無轉移(頭頸部CT/MRI)。
主要手術方式如下:
在Kaliki 2019中,76%的鱗狀細胞癌病例接受了廣泛切除活檢1)。
使用液氮破壞組織。僅適用於光化性角化病和鱗狀細胞原位癌(不適用於浸潤癌)。此外,對於早期病灶,可作為術中切除面的附加冷凍融解使用。
用於手術風險過高的患者的單獨治療,或作為神經/淋巴結擴展或邊界不清的癌的術後輔助治療。每週照射3-5次,持續約1-2個月。鱗狀細胞癌對放射線敏感,是根治性切除困難時的選擇。
適用於伴有遠端轉移的進展性鱗狀細胞癌。
印度99例鱗狀細胞癌患者的治療結果如下所示1)。
| 指標 | 比例 |
|---|---|
| 腫瘤復發 | 8% |
| 局部淋巴結轉移 | 8% |
| 遠端轉移 | 4% |
| 疾病相關死亡 | 4% |
| 眼球保留 | 79% |
在5年Kaplan-Meier估計中,局部淋巴結轉移為22%,遠端轉移為11%,轉移相關死亡為11%1)。
在Kaliki 2019的研究中,術後腫瘤復發率為8%。5年Kaplan-Meier估計顯示局部淋巴結轉移達到22%,表明術後定期追蹤很重要。
紫外線直接(鹼基轉換)或間接(通過活性氧引起的氧化損傷)損傷DNA2)。曬傷誘導的細胞凋亡作為防禦機制,但當DNA修復跟不上時,突變會累積。
增生/角化過度 → 輕至中度異型增生 → 重度異型增生/原位癌(光化性角化病/Bowen病)→ 浸潤性鱗狀細胞癌 → 轉移性鱗狀細胞癌
Marjolin潰瘍:慢性難癒合傷口或長期燒傷疤痕組織中發生鱗狀細胞癌的病變。
眼瞼皮膚型(皮膚型)是棘層細胞的逐步惡性轉化,按AJCC眼瞼TNM分類管理。瞼結膜型是OSSN的一種形式,從結膜上皮異型增生(CIN:結膜上皮內瘤變)進展為浸潤性SCC,適用AJCC結膜分類 4)。
0期至IB期
0期(Tis N0 M0):原位癌。未突破基底膜。
IA期(T1 N0 M0):腫瘤直徑≤5mm,無瞼板浸潤。
IB期(T2a N0 M0):腫瘤直徑>5mm至≤10mm,或瞼板浸潤。
IC期至IV期
IC期(T2b N0 M0):腫瘤直徑>10mm至≤20mm,或眼瞼全層侵犯。
II期(T3a N0 M0):腫瘤直徑>20mm,或侵犯鄰近眼部結構。
IIIB期(任何T N1 M0):區域淋巴結轉移。
第IV期(任何T任何N M1):遠端轉移。
Kaliki 2019的期別分布為T1: 26%、T2: 37%、T3: 7%、T4: 29%1)。組織學分級從G1(高分化)到G4(未分化),分級越低預後越好。
Ye等人(NEJM 2025)報告了一例34歲女性,因ZAP70生殖細胞系突變導致T細胞受體訊號障礙,發生帶有β-HPV19基因組整合的難治性浸潤性皮膚鱗狀細胞癌3)。該病例未檢測到典型的鱗狀細胞癌驅動突變(TP53、NOTCH1/2、CDKN2A),紫外線突變特徵也較低,為26%(通常皮膚鱗狀細胞癌平均77%)。透過異基因造血幹細胞移植修復T細胞受體訊號後,HPV特異性T細胞反應恢復,在35個月的追蹤中,包括鱗狀細胞癌在內的所有HPV相關疾病均穩定消退。
該報告提示適應性免疫T細胞反應參與控制鱗狀細胞癌的發生和進展3)。
西米普利單抗(抗PD-1抗體)已獲FDA核准用於不可切除或轉移性皮膚鱗狀細胞癌,預計未來將擴展至眼眶和淋巴結受累的病例。免疫監視機制的參與逐漸明確,免疫抑制狀態(如器官移植後、血液腫瘤等)下鱗狀細胞癌風險增加也與T細胞反應調控異常有關2)3)。
抗PD-1抗體西米普利單抗已獲FDA核准用於不可切除或轉移性皮膚鱗狀細胞癌。在HPV驅動的鱗狀細胞癌中,也有透過造血幹細胞移植進行免疫重建後腫瘤消退的病例報告。但後者屬於研究階段發現,並非標準治療。
早期發現和完全切除後預後良好。然而,其生物學行為比基底細胞癌更具侵襲性,存在向眼眶、淋巴結和遠端器官轉移的風險。惡性眼眶浸潤病例需與腫瘤內科、放射腫瘤科等多學科協作管理。
追蹤要點如下。
5年Kaplan-Meier估計顯示區域淋巴結轉移22%、遠端轉移11%、轉移相關死亡11% 1),需要長期監測。