結節型(56%)
黃色調結節性腫塊:由於腫瘤細胞內的脂質,呈特徵性黃色外觀。好發於上眼瞼緣,表面不規則,伴有易出血的腫瘤血管。
透過眼瞼翻轉觀察:翻轉眼瞼檢查結膜側也很重要。

眼瞼皮脂腺癌(SGC)是一種起源於眼瞼皮脂腺——瞼板腺、Zeis腺和淚阜皮脂腺——的高度惡性腫瘤。它被認為是眼瞼最重要的惡性腫瘤之一。起源部位的分佈為:瞼板腺佔92%,Zeis腺佔6%,淚阜佔2%2)。由於上眼瞼約有50個瞼板腺,下眼瞼約有25個,因此好發於上眼瞼。主要發生在50歲以後,女性略多,10%~20%的病例發生轉移或復發。這是一種預後不良的疾病,有時可能致命。
該疾病在歐美和東亞地區的定位有很大不同。在歐美,基底細胞癌占眼瞼惡性腫瘤的80%~95%,而脂腺癌僅占1%~3% 1)。相比之下,亞洲人群中脂腺癌的比例顯著較高。
| 地區/族群 | 脂腺癌的比例 |
|---|---|
| 歐美 | 1%~3% 1) |
| 印度(536例) | 53% 1) |
| 中國(1086例) | 32% 1) |
| 日本(38例) | 29% 1) |
亞洲人患有眼瞼惡性腫瘤時,其為脂腺癌的機率是非亞洲人的6.21倍(範圍3.8~10.1)1)。但脂腺癌本身的發生率在白人中(2.03/百萬)高於亞洲/太平洋島民(1.07/百萬)。由於亞洲人基底細胞癌相對較少,因此脂腺癌在所有惡性腫瘤中的比例顯得較高。
發病平均年齡在印度族群中為58歲,整體報告為57~72歲 1)。除眼瞼外,25%的病例可能發生在頭頸部、其他皮膚或生殖器區域。
Muir–Torre症候群是一種體染色體顯性遺傳疾病,表現為脂腺腫瘤與內臟惡性腫瘤(胃腸道、子宮內膜、泌尿系統)並存。其背景是DNA錯配修復基因(MLH1、MSH2、MSH6)的突變,24%的Muir–Torre症候群患者會發生脂腺癌。診斷脂腺癌時,建議同時詢問家族史和消化道症狀。
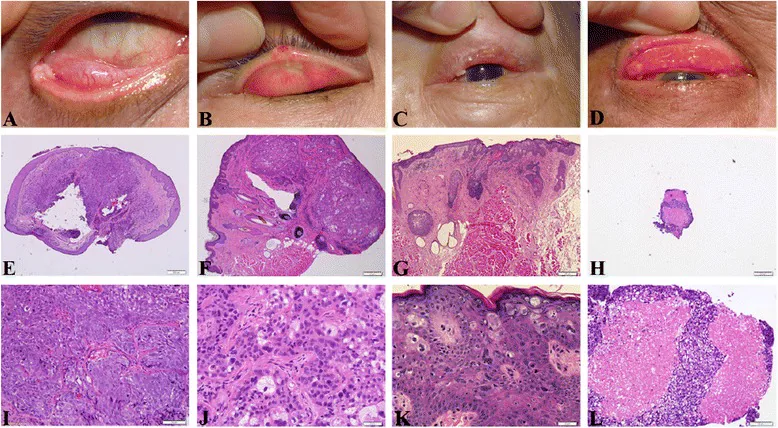
結節型(56%)
黃色調結節性腫塊:由於腫瘤細胞內的脂質,呈特徵性黃色外觀。好發於上眼瞼緣,表面不規則,伴有易出血的腫瘤血管。
透過眼瞼翻轉觀察:翻轉眼瞼檢查結膜側也很重要。
瀰漫型(7%)
不形成腫塊的上皮內浸潤:從瞼板腺開口向瞼緣皮膚和瞼結膜薄層擴散的類型。診斷最易延遲。
睫毛脫落(睫毛禿):瀰漫型的一個特徵性表現。必須作為惡性腫瘤或嚴重發炎的徵象進行檢查。
腫瘤發生部位:上眼瞼59%,下眼瞼29%,內眥3%,外眥2%1)。
睫毛脫落的重要性:當眼瞼緣存在皮脂腺癌等惡性腫瘤或嚴重發炎時,睫毛會脫落。發現睫毛脫落時,應仔細觀察周圍是否有致病病變,對懷疑惡性的病變考慮切片或諮詢腫瘤專科醫師。
佩吉特樣擴展:腫瘤細胞從主病灶向遠離的瞼球結膜上皮內呈片狀增殖擴散的特徵性模式。表現為覆蓋整個瞼結膜的煙火狀腫瘤血管和腫瘤細胞增生,可形成跳躍性病變。
偉大偽裝者(great masquerader):類似霰粒腫、慢性瞼緣炎、基底細胞癌、鱗狀細胞癌、上方角膜緣角結膜炎、眼瘢痕性類天皰瘡。結節性病變易被誤認為霰粒腫,切開後反覆復發增大。有時可透過抗生素眼膏治療是否改善來鑑別佩吉特樣擴展和瞼緣炎。
亞洲人患有眼瞼惡性腫瘤時,脂腺癌的機率是非亞洲人的6.21倍1)。但這是相對比例的問題,脂腺癌的發生率(每人口)實際上是白人(2.03/百萬)高於亞洲/太平洋島民(1.07/百萬)。由於亞洲人基底細胞癌較少,因此脂腺癌的比例相對顯得較高。
保持高度懷疑(high index of suspicion)最為重要。以下情況應積極懷疑脂腺癌:
即使認為是霰粒腫,刮除物也必須送病理檢查。 使用抗生素眼藥膏後是否改善,有時可幫助鑑別佩吉特樣擴散與眼瞼緣炎。
如果懷疑皮脂腺癌,應進行以下影像學檢查以評估轉移和浸潤。
根據腫瘤大小和眼瞼/眼眶浸潤情況,分為T1至T42)。
| T分類 | 定義 |
|---|---|
| T1 | 腫瘤最大徑 ≤10 mm |
| T2 | 腫瘤最大徑 >10~20 mm |
| T3 | 腫瘤最大徑 >20 mm |
| T4 | 浸潤眼眶、鼻竇等 |
第8版與第7版相比,T1的定義擴大(從≤5 mm改為≤10 mm),並且顯示會發生降期2)。
組織學上,嗜鹼性腫瘤細胞呈巢狀增殖,異型性和多形性明顯,細胞質內脂滴(HE染色中呈現空泡狀)是特徵。分化差時脂滴不明顯,可能被診斷為鱗狀細胞癌。如果腫瘤起源於瞼板內,即使只有少數細胞質內脂滴,也應診斷為皮脂腺癌。
目前標準的免疫組織化學標誌物如下所示。
| 標誌物 | 特徵 |
|---|---|
| 脂滴包被蛋白 | 細胞內脂滴相關蛋白。對皮脂腺分化敏感性高且實用3) |
| 雄激素受體 | 眼瞼皮脂腺癌通常陽性 |
| 上皮膜抗原(EMA) | 陽性 |
Muir-Torre症候群篩查:通過免疫組織化學染色檢查MLH1、MSH2、MSH6的表達是否缺失。
手術切除是治療的主要方式。
對於眼瞼侷限病例,切除時安全邊界應**≥3 mm**。最好進行冰凍切片術中邊緣評估。
根據瞼板缺損範圍的重建策略:
歐美的莫氏顯微手術或完全周邊及深部邊緣評估法(CCPDMA)是在評估所有邊緣的同時切除的方法,有望降低邊緣陽性率。
如果佩吉特樣擴散侷限於上皮內,抗腫瘤眼藥水可能保留眼球。如果病變侵犯超過基底膜,眼藥水治療無效。
絲裂黴素C(MMC)眼藥水:
5-氟尿嘧啶(5-FU)眼藥水:
適用於眼窩浸潤、巨大且深部浸潤的病變、廣泛球結膜波及的病例。根據報告,按AJCC分期的手術施行率分別為T1 3%、T2 3%、T3 8%、T4 63%2)。
對於T2c期以上的眼窩周圍腫瘤可考慮。
皮脂腺癌對放射線敏感,用於根除性切除困難或術後輔助治療。
標準做法是切除時保證3 mm以上的安全邊緣。通過冰凍切片進行術中邊緣評估,如果邊緣陽性則追加切除。如果瞼板缺損不超過1/3,可通過單純縫合或局部皮瓣重建;如果超過,則分別重建前層和後層。對於T4腫瘤或眼眶浸潤病例,考慮眼眶內容物剜除術。
皮脂腺癌是起源於皮脂腺腺上皮的惡性腫瘤。原發部位分佈據報導為:瞼板腺來源92%,蔡氏腺6%,淚阜2%2)。
組織學上,皮脂腺細胞(胞質空泡化、富含脂質的細胞)與未分化基底樣細胞混合存在,分化程度從高分化到低分化不等。腫瘤細胞內的脂質使其肉眼呈黃色。分化低時,組織學上與鱗狀細胞癌的鑑別可能困難,但如果腫瘤發生在瞼板內,即使發現少量胞質內脂滴也應診斷為皮脂腺癌。
佩吉特樣擴展的機制:惡性細胞從主腫瘤部位單獨遷移並增殖到遠離主腫瘤的上皮——瞼結膜、球結膜和皮膚。這形成跳躍性病變,肉眼看似正常的區域也可能存在腫瘤細胞。因此,通過結膜地圖切片了解擴展範圍對治療至關重要。
Muir-Torre症候群的分子機制:由DNA錯配修復基因(MLH1、MSH2、MSH6、PMS2)突變引起的體染色體顯性遺傳病。突變導致DNA複製錯誤修復功能喪失,腫瘤抑制基因突變積累,從而產生皮脂腺腫瘤。
預後相關因素:腫瘤尺寸超過15 mm時區域淋巴結轉移風險增加。佩吉特樣擴展或眼眶浸潤病例預後不良傾向,可能發生轉移相關死亡。
Morawala(2023)對119例皮脂腺癌進行了AJCC第8版T分類的評估,顯示T分類對預後預測有用2)。T4腫瘤的淋巴結轉移風險比為2.38,遠端轉移風險比為4.30,轉移相關死亡風險比為6.62。此外,第8版將T1的定義從第7版的5毫米以下改為10毫米以下,確認了降期的發生。
Li & Finger(2021)對T2bN0M0眼眶皮脂腺癌進行了切除、冷凍凝固和超厚羊膜移植,隨後進行了高劑量率近接治療(2000 cGy/5次)和電子束外部放射治療(36 Gy/20次),總劑量56 Gy5)。1年後視力20/20,無放射性視網膜病變或視神經病變。但發生了頸部淋巴結轉移。
Adachi(2022)對一名97歲無法手術的耳前皮脂腺癌患者進行了60 Gy/30次的電子束治療合併過氧化氫浸潤紗布4)。8個月後達到肉眼完全緩解。不良事件僅為2級放射性皮膚炎。提示過氧化氫有放射增敏作用,但僅為少數病例報告,需要進一步驗證。
Kaliki S, Bothra N, Bejjanki KM, et al. Malignant eyelid tumors in India: a study of 536 Asian Indian patients. Ocul Oncol Pathol. 2019;5(3):210-219.
Morawala A, Mohamed A, Krishnamurthy A, Jajapuram SD, Kaliki S. Sebaceous gland carcinoma: analysis based on the 8th edition of American Joint Committee on Cancer classification. Eye (Lond). 2023;37(4):714-719.
Ramachandran V, Tumyan G, Loya A, Treat K, Vrcek I. Sebaceous carcinoma masquerading as orbital cellulitis. Cureus. 2022;14(2):e22288.
Adachi A, Oike T, Tamura M, Ota N, Ohno T. Radiotherapy with hydrogen peroxide-soaked gauze for preauricular sebaceous carcinoma. Cureus. 2022;14(7):e27464.
Li F, Stewart RD, Finger PT. Interstitial brachytherapy for orbital sebaceous carcinoma. Ophthalmic Plast Reconstr Surg. 2021;37(6):e215-e217.