결절형 (56%)
황색조의 결절성 종괴: 종양 세포 내 지질로 인한 노란색 외관이 특징입니다. 위눈꺼풀 가장자리에 호발하며, 표면이 불규칙하고 출혈하기 쉬운 종양 혈관을 동반합니다.
눈꺼풀 뒤집기를 통한 관찰: 눈꺼풀을 뒤집어 결막 쪽도 확인하는 것이 중요합니다.

눈꺼풀 피지선암(SGC)은 눈꺼풀의 피지선——마이봄샘, 차이스샘, 눈물언덕 피지선——에서 발생하는 악성도가 높은 종양입니다. 눈꺼풀에서 가장 중요한 악성 종양 중 하나로 간주됩니다. 발생 부위의 분포는 마이봄샘 기원 92%, 차이스샘 6%, 눈물언덕 2%입니다2). 위눈꺼풀에는 마이봄샘이 약 50개, 아래눈꺼풀에는 약 25개 있으므로 위눈꺼풀에 호발합니다. 주로 50대 이후에 발생하며, 여성에 약간 더 많고, 10~20%에서 전이 또는 재발합니다. 때로는 치명적일 수 있는 예후가 좋지 않은 질환입니다.
이 질환은 서양과 동아시아에서 질환의 위치가 크게 다릅니다. 서양에서는 눈꺼풀 악성 종양 중 기저세포암이 8095%를 차지하는 반면, 피지선암은 13%에 불과합니다 1). 반면, 아시아인에서는 피지선암의 비율이 현저히 높습니다.
| 지역/인구 | 피지선암의 비율 |
|---|---|
| 서양 | 1~3% 1) |
| 인도 (536예) | 53% 1) |
| 중국 (1,086예) | 32% 1) |
| 일본 (38예) | 29% 1) |
아시아인에서 눈꺼풀 악성 종양이 있을 경우, 그것이 피지선암일 확률은 비아시아인의 6.21배(범위 3.8~10.1)에 달합니다 1). 그러나 피지선암 자체의 발생률은 백인(2.03/100만)이 아시아/태평양계(1.07/100만)보다 높습니다. 아시아인에서 기저세포암이 상대적으로 적기 때문에 악성 종양 전체에서 피지선암이 차지하는 비율이 높게 보입니다.
발병 평균 연령은 인도계에서 58세, 전체적으로는 57~72세로 보고됩니다 1). 눈꺼풀 외에도 25%의 증례에서 두경부, 다른 피부, 생식기에 발생할 수 있습니다.
뮤어-토레 증후군은 피지선 종양과 내장 악성 종양(위장관, 자궁내막, 비뇨기계)을 동반하는 상염색체 우성 유전 질환입니다. DNA 불일치 복구 유전자(MLH1, MSH2, MSH6)의 돌연변이가 배경에 있으며, 뮤어-토레 증후군 환자의 24%에서 피지선암이 발생합니다. 피지선암을 진단할 때는 가족력이나 소화기 증상도 청취하는 것이 바람직합니다.
결절형 (56%)
황색조의 결절성 종괴: 종양 세포 내 지질로 인한 노란색 외관이 특징입니다. 위눈꺼풀 가장자리에 호발하며, 표면이 불규칙하고 출혈하기 쉬운 종양 혈관을 동반합니다.
눈꺼풀 뒤집기를 통한 관찰: 눈꺼풀을 뒤집어 결막 쪽도 확인하는 것이 중요합니다.
미만형 (7%)
종괴를 형성하지 않는 상피내 침윤: 마이봄샘 개구부에서 눈꺼풀 가장자리 피부와 눈꺼풀 결막으로 얇게 퍼지는 유형입니다. 진단이 가장 지연되기 쉽습니다.
속눈썹 탈락(속눈썹 빠짐) : 미만형의 특징적인 소견 중 하나. 악성 종양이나 심한 염증의 징후로 반드시 확인한다.
종양 발생 부위는 위눈꺼풀 59%, 아래눈꺼풀 29%, 안쪽 눈구석 3%, 바깥쪽 눈구석 2%이다1).
속눈썹 탈락의 중요성 : 눈꺼풀 가장자리에 피지선암 등의 악성 종양이나 심한 염증이 있으면 속눈썹이 빠진다. 속눈썹 탈락이 관찰되면 주변에 원인이 되는 병변이 없는지 자세히 관찰하고, 악성 종양이 의심되는 병변에는 생검 또는 종양 전문의 상담을 고려한다.
파제트양 진행 : 주 병변에서 떨어진 눈꺼풀·안구 결막 상피 내로 종양 세포가 시트 모양으로 증식 확산하는 특징적인 패턴. 눈꺼풀 결막 전체를 덮는 불꽃 모양의 종양 혈관과 종양 세포 증식을 보이며, 건너뛰기 병변을 형성할 수 있다.
위대한 가장(great masquerader) : 콩다래끼, 만성 눈꺼풀염, 기저세포암, 편평세포암, 위윤부 각결막염, 눈 흉터성 유천포창과 유사하다. 결절성 병변은 콩다래끼로 오인되기 쉬우며, 절개 후 재발과 증대를 반복한다. 항생제 안연고 투여로 호전 여부에 따라 파제트양 진행과 눈꺼풀가장자리염을 감별할 수 있는 경우가 있다.
콩다래끼, 눈꺼풀염, 기저세포암 등 여러 질환과 유사하여 임상 진단이 현저히 어렵기 때문이다. 결절성 병변은 콩다래끼로 오인되기 쉽고, 미만형은 파제트양 진행이 눈꺼풀가장자리염과 유사하다. 절개를 반복하는 재발성 콩다래끼에서는 피지선암을 항상 염두에 두어야 하며, 소파 내용물은 반드시 병리 검사에 제출한다.
아시아인에서 눈꺼풀 악성 종양이 있을 때 피지선암일 확률은 비아시아인의 6.21배입니다1). 그러나 이는 상대적 비율에 관한 이야기이며, 피지선암의 발생률(인구당) 자체는 백인(2.03/100만)이 아시아/태평양계(1.07/100만)보다 높습니다. 아시아인에서 기저세포암이 적기 때문에 상대적으로 피지선암의 비율이 높게 보입니다.
높은 의심 지수(high index of suspicion)를 갖는 것이 가장 중요합니다. 다음의 경우에 피지선암을 적극적으로 의심합니다.
콩다래끼로 생각되더라도 소파술 내용물은 반드시 병리 검사에 제출합니다. 항생제 안연고 투여 후 호전 여부로 파제트양 진행과 안검연염을 감별할 수 있는 경우가 있습니다.
피지선암이 의심되는 경우, 다음 영상 검사를 통해 전이 및 침윤을 평가합니다.
종양 크기와 눈꺼풀/안와 침윤에 따라 T1~T4로 분류됩니다2).
| T 분류 | 정의 |
|---|---|
| T1 | 종양 최대 직경 ≤10 mm |
| T2 | 종양 최대 직경 >10~20 mm |
| T3 | 종양 최대 직경 >20 mm |
| T4 | 안와, 부비동 등으로의 침윤 |
제8판에서는 제7판과 비교하여 T1의 정의가 확대(5 mm 이하 → 10 mm 이하)되었으며, 다운스테이징이 발생하는 것으로 나타났습니다2).
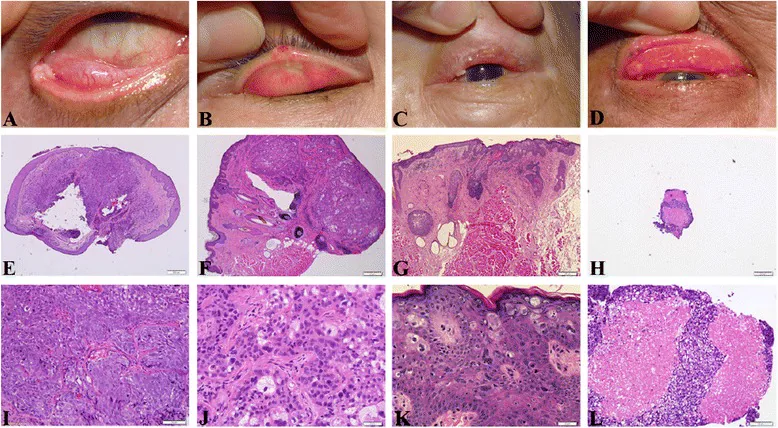
조직학적으로 호염기성 종양 세포가 덩어리로 증식하고, 이형성 및 다형성이 현저하며, 세포질 내 지방적(HE 염색에서 흰색으로 비어 보임)이 특징입니다. 분화도가 낮으면 지방적이 눈에 띄지 않아 편평상피암의 병리 진단명이 붙을 수 있습니다. 검판 내에서 발생하는 경우, 소수라도 세포질 내에 지방적이 확인되면 피지선암으로 진단해야 합니다.
현재 표준적인 면역조직화학 마커는 아래와 같습니다.
| 마커 | 특징 |
|---|---|
| 아디포필린 | 세포 내 지질적 관련 단백질. 피지 분화에 대한 민감도가 높고 실용적입니다3) |
| 안드로겐 수용체 | 눈꺼풀의 피지선암에서 일반적으로 양성 |
| 상피막 항원(EMA) | 양성 |
뮤어-토레 증후군 선별검사: MLH1, MSH2, MSH6의 면역조직화학 염색으로 발현 소실 여부를 확인합니다.
외과적 절제가 치료의 주된 방법이다.
눈꺼풀에 국한된 경우 안전 여유를 3 mm 이상 두고 절제한다. 동결 절편을 이용한 수술 중 절제연 평가를 시행하는 것이 바람직하다.
검판 결손 범위에 따른 재건 방침:
서양에서의 모스 현미경 수술 또는 완전 주변·심부 절제연 평가법(CCPDMA)은 조직을 모든 절제연에서 평가하면서 절제하는 방법으로, 절제연 양성률 감소가 기대된다.
파제트양 진행이 상피 내에 국한된 경우, 항종양 점안약으로 안구를 보존할 수 있는 경우가 있다. 병변이 기저막을 넘어 침윤하면 점안 치료는 효과가 없다.
마이토마이신 C (MMC) 점안액:
5-플루오로우라실 (5-FU) 점안액:
안와 침윤, 크고 깊게 침윤된 병변, 광범위한 구결막 파급 증례에서 시행됩니다. AJCC 병기별 시행률은 T1 3%, T2 3%, T3 8%, T4 63%로 보고되었습니다2).
T2c기 이상의 안와 주위 종양에서 고려됩니다.
피지선암은 방사선에 민감하며, 근치적 절제가 어려운 경우나 수술 후 보조 요법으로 사용됩니다.
안전 여유를 3mm 이상 두고 절제하는 것이 표준입니다. 동결 절편을 이용한 수술 중 절제연 평가를 시행하고, 절제연 양성인 경우 추가 절제를 시행합니다. 안검판 결손이 1/3 이하이면 단순 봉합이나 국소 피판으로 재건 가능하지만, 그 이상이면 전엽과 후엽을 각각 재건합니다. T4 종양이나 안와 침윤의 경우 안와 내용 제거술이 고려됩니다.
피지선암은 피지선의 선상피에서 발생하는 악성 종양입니다. 발생 부위의 구성은 마이봄샘 유래 92%, 차이스샘 6%, 눈물언덕 2%로 보고되었습니다2).
조직학적으로 피지세포(공포화된 세포질을 가진 지질이 풍부한 세포)와 미분화 기저양 세포가 혼재하며, 분화도는 고분화에서 저분화까지 다양합니다. 종양 세포 내 지질이 황색조의 육안적 외관을 초래합니다. 분화가 낮은 경우 조직학적으로 편평세포암과의 감별이 어려울 수 있지만, 안검판 내 발생이라면 소수라도 세포질 내 지방적을 인정한 시점에서 피지선암으로 판단해야 합니다.
파제트양 진행의 메커니즘: 주 종양에서 떨어진 부위의 상피——안검 결막, 구 결막, 피부——로 악성 세포가 개별적으로 이동하여 증식하는 패턴입니다. 스킵 병변을 형성하여 육안적으로 병변이 없는 것처럼 보이는 부위에도 종양 세포가 존재할 수 있습니다. 따라서 결막 매핑 생검을 통한 범위 파악이 치료에 필수적입니다.
뮤어-토레 증후군의 분자 기전: DNA 불일치 복구 유전자(MLH1, MSH2, MSH6, PMS2)의 돌연변이에 의한 상염색체 우성 유전 질환입니다. 돌연변이로 인해 DNA 복제 오류의 복구 기능이 상실되어 종양 억제 유전자에 돌연변이가 축적됨으로써 피지선 종양이 발생합니다.
예후 관련 인자: 종양 크기 15mm 초과 시 국소 림프절 전이 위험이 증가합니다. 파제트양 진행 예나 안와 침윤 예는 예후 불량 경향이 있으며, 전이 관련 사망도 있을 수 있습니다.
Morawala(2023)는 119예의 피지선암을 대상으로 AJCC 제8판 T 분류를 검토하여 T 분류가 예후 예측에 유용함을 보여주었습니다2). T4 종양의 림프절 전이 위험비 2.38, 원격 전이 위험비 4.30, 전이 관련 사망 위험비 6.62였습니다. 또한 제8판에서는 T1의 정의가 제7판의 5 mm 이하에서 10 mm 이하로 변경되어 다운스테이징이 발생함이 확인되었습니다.
Li & Finger(2021)는 T2bN0M0 안와 피지선암에 대해 절제, 냉동 응고, 초두께 양막 이식 후 고선량률 근접 치료(2,000 cGy/5회) 및 전자선 외부 방사선 치료(36 Gy/20회)를 합하여 총 56 Gy를 조사했습니다5). 1년 후 시력 20/20, 방사선 망막병증 및 시신경병증 없음. 그러나 경부 림프절 전이가 발생했습니다.
Adachi(2022)는 97세의 수술 불가능한 이개 전방 피지선암에 대해 60 Gy/30회의 전자선 치료와 과산화수소 함침 거즈를 시행했습니다4). 8개월 후 육안적 완전 관해. 유해 사례는 Grade 2 방사선 피부염뿐이었습니다. 과산화수소의 방사선 증감 효과가 시사되지만 소수 예의 보고이며 향후 검증이 필요합니다.
Kaliki S, Bothra N, Bejjanki KM, et al. Malignant eyelid tumors in India: a study of 536 Asian Indian patients. Ocul Oncol Pathol. 2019;5(3):210-219.
Morawala A, Mohamed A, Krishnamurthy A, Jajapuram SD, Kaliki S. Sebaceous gland carcinoma: analysis based on the 8th edition of American Joint Committee on Cancer classification. Eye (Lond). 2023;37(4):714-719.
Ramachandran V, Tumyan G, Loya A, Treat K, Vrcek I. Sebaceous carcinoma masquerading as orbital cellulitis. Cureus. 2022;14(2):e22288.
Adachi A, Oike T, Tamura M, Ota N, Ohno T. Radiotherapy with hydrogen peroxide-soaked gauze for preauricular sebaceous carcinoma. Cureus. 2022;14(7):e27464.
Li F, Stewart RD, Finger PT. Interstitial brachytherapy for orbital sebaceous carcinoma. Ophthalmic Plast Reconstr Surg. 2021;37(6):e215-e217.