胶冻状
半透明隆起性肿块:最常见的形态。结膜血管呈发夹样走行。
滋养血管:异常扩张迂曲的滋养动脉提示恶性增生 1)。

该术语由Lee等人于1995年提出,涵盖起源于角膜、结膜和角膜缘的非复合型鳞状上皮肿瘤1)。它是眼表最常见的非色素性肿瘤;在一项单中心研究中,OSSN占771例非黑色素细胞性结膜肿瘤的23%(179例)1)。
OSSN包括以下病变:
发病率的地理差异很大。在高纬度地区为0.02/10万,而在赤道附近的低纬度地区则达到3.5/10万1)。全球年龄标准化发病率为0.26/10万/年,且呈上升趋势1)。非洲发病率最高(3.4/10万/年),HIV和HPV感染的高频率是原因之一1)。
在西半球,好发于60岁以上的白人男性,但在非洲和亚洲部分地区,HIV感染者中的年轻人也会发病,且病程更具侵袭性1)。
AJCC第8版根据原发肿瘤(T)、区域淋巴结(N)和远处转移(M)对OSSN进行分类1)。
| 分类 | 定义 |
|---|---|
| Tis | 原位癌(局限于上皮内) |
| T1 | 局限于结膜,未侵犯邻近结构 |
| T2 | 侵犯邻近眼部结构(角膜、穹窿、泪阜、巩膜、眼球) |
| T3 | 侵犯眼眶、鼻窦或眼睑 |
| T4 | 侵犯中枢神经系统或远处部位 |
未经治疗的SCC可导致眼眶侵犯(约10%)、区域淋巴结转移,罕见远处转移,死亡率报告为8%至24% 1)。
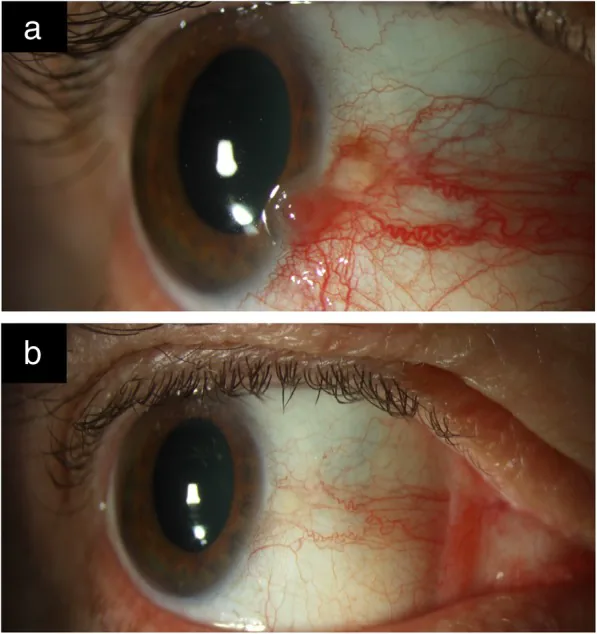
OSSN病变通常无症状,偶然发现。有症状时,主要表现为充血、异物感和眼刺激症状 2)。也可能伴有疼痛。视力下降见于肿瘤波及角膜或眼内浸润的病例。
单侧血管性肿块最为常见,好发于睑裂间(鼻侧或颞侧)的角膜缘附近 1)。多累及角膜和球结膜,眼睑结膜发病罕见 1)。白种人呈黄粉色,有色人种可伴有色素沉着 1)3)。
胶冻状
半透明隆起性肿块:最常见的形态。结膜血管呈发夹样走行。
滋养血管:异常扩张迂曲的滋养动脉提示恶性增生 1)。
白斑状
表面白色化、增厚:因过度角化导致的肿瘤表面角化。
干燥外观:呈不透明的白色调,与胶冻状相反。
乳头状
乳头状增生:已知与HPV相关的形态4)。
结节状表面:可能呈疣状外观。
结节溃疡型
罕见但具侵袭性:强烈提示浸润性肿瘤的形态1)。
溃疡形成:预后较其他类型差。
角膜受累时呈半透明、灰色磨玻璃样外观,并呈流苏状或伪足样扩展。
眼内浸润罕见,但可表现为前房白色肿块、前房炎症或继发性青光眼2)。
OSSN的病因是多因素的。主要危险因素如下1)。
因为HIV感染导致的免疫抑制削弱了肿瘤免疫监视机制。HIV阳性者OSSN风险增加10~13倍3),且可在年轻时发病。在非洲,HIV与HPV的合并感染被认为是疾病增加的原因之一1)。
OSSN的确诊依靠切除活检或切开活检的组织学检查(金标准)1)。小于4小时的小肿瘤适用切除活检,大于等于4小时的大肿瘤适用切开活检。
诊断辅助中可使用玫瑰红、丽丝胺绿、亚甲蓝、甲苯胺蓝等特殊染色1)。玫瑰红可将凋亡或代谢不活跃的上皮细胞染成鲜明的粉红色,使肿瘤轮廓更清晰1)。
主要诊断方式总结如下。
| 检查方法 | 特点 |
|---|---|
| 活检(组织检查) | 金标准。可评估浸润深度。 |
| HR-OCT | 无创。特征为上皮增厚和高反射。 |
| IVCM | 细胞水平评估。操作复杂。 |
| 印迹细胞学 | 无创,但仅评估表面组织。 |
OSSN与翼状胬肉和睑裂斑的鉴别尤为重要1)。两者可能并存,导致诊断困难。其他鉴别诊断包括角膜血管翳、光化性角化病、化脓性肉芽肿、结膜痣和恶性黑色素瘤。
仅凭临床所见有时难以鉴别。HR-OCT上的上皮增厚和高反射表现,以及玫瑰红或亚甲蓝的特殊染色可为鉴别提供线索1)。确诊需要活检。
OSSN的治疗根据肿瘤大小、浸润深度和患者因素个体化1)。据报道,手术切除和局部化疗疗效相当1)。
无接触技术+冷冻疗法是金标准1)。
如果切除边缘阳性,建议术后辅助化疗1)2)。在没有冷冻疗法和术后化疗的情况下,眼内浸润的风险增加2)。
Pike等人(2023)报告了一例OSSN病例,切除后未进行冷冻疗法或化疗,通过全层角膜缘缺损发生眼内播散(前房肿块形成),最终导致眼球摘除2)。这强调了无接触技术、冷冻疗法和术后化疗的重要性。
局部化疗既可作为单一疗法,也可作为术后辅助治疗使用1)。
丝裂霉素C
5-FU
5-氟尿嘧啶:一种嘧啶类似物,抑制S期DNA和RNA合成1)。
有效率:高。复发率最高达20%。比丝裂霉素C和IFN便宜。
给药方法:使用1%滴眼液,每周给药、停药3周的周期。
IFNα-2b
干扰素α-2b:具有抗增殖、抗病毒和免疫调节作用1)。
有效率:80%~100%。通过结膜下注射(100万IU/mL)或滴眼给药。
特点:副作用少,但价格昂贵且需要冷藏保存。
其他药物治疗包括抗VEGF药物(贝伐珠单抗、雷珠单抗),对结膜病变显示出有希望的结果,但对角膜病变的效果不明确,需要大规模试验1)。HPV相关患者可能使用西多福韦1)。
基于AJCC第8版的治疗方法如下所示1)。
以下因素与复发相关1)。
据报道,单独化疗(MMC、5-FU、IFNα-2b)的疗效与手术相当1)。根据肿瘤大小、浸润深度、患者全身状况和依从性选择。对于大于4个钟点的病变、多发性或复发性病例,局部化疗可能更有优势。
OSSN被认为起源于角膜缘干细胞1)。大多数原发性结膜恶性肿瘤出现在睑裂间角膜缘附近,该区域干细胞分裂活跃1)。
组织学上,浸润性SCC中恶性鳞状上皮细胞穿透基底膜并在间质内增殖1)。CIN I至III根据上皮内异型增生的范围分类。全层上皮异型增生(CIN III)与原位癌同义1)。
眼内浸润罕见,但可通过以下途径发生2):
Pike等人(2023)的病例中,切除活检后形成全层角膜缘缺损,肿瘤细胞通过该路径播散至前房,并扩散至角膜后面、房角、虹膜、睫状体和晶状体2)。病理学表现类似于恶性上皮向下生长。
在黏液表皮样癌中,黏液染色显示异型增生的鳞状上皮细胞和恶性杯状细胞。当黏液成分占优势时,临床侵袭性被认为相对较低。
放射治疗正在被考虑作为OSSN和SCC的治疗选择1)。
这是一种结合维替泊芬和激光的治疗方法1)。在一项初步研究中,结膜SCC的肿瘤消失率达到100%,且在观察期间无复发1)。然而,高成本、设施有限以及需要专业培训是普及的障碍。
Zein等人(2024)对一名两次切除后复发的乳头状OSSN(HPV阳性、p16阳性)患者,每6周肌肉注射一次9价HPV疫苗(Gardasil-9),共4次4)。第三次注射后观察到肿瘤显著缩小,HR-OCT证实上皮增厚和高反射性改善。但未达到根治,随后进行了额外的5-FU和丝裂霉素C滴眼治疗。
这是全球首次报道将HPV疫苗用于OSSN治疗4),作为未来的治疗选择正在研究中。治疗机制推测为抑制HPV特异性E6/E7癌蛋白4)。