Gelatinoso
Masa elevada translúcida: La forma más común. Los vasos conjuntivales muestran un trayecto en forma de horquilla.
Vasos nutricios: Arterias nutricias anormalmente dilatadas y tortuosas sugieren crecimiento maligno 1).

El término fue propuesto por Lee et al. en 1995 y abarca los tumores escamosos no complejos que surgen de la córnea, la conjuntiva y el limbo 1). Es el tumor no pigmentado más común de la superficie ocular; en un estudio de un solo centro, la OSSN representó el 23% (179 casos) de 771 tumores conjuntivales no melanocíticos 1).
La OSSN incluye las siguientes lesiones:
La incidencia varía mucho según la región geográfica. En latitudes altas es de 0.02/100,000, mientras que en latitudes bajas cerca del ecuador alcanza 3.5/100,0001). La tasa de incidencia estandarizada por edad a nivel mundial es de 0.26/100,000/año y está en aumento1). África tiene la tasa más alta (3.4/100,000/año), contribuyendo la alta frecuencia de infección por VIH y VPH1).
En el hemisferio occidental, es frecuente en hombres blancos mayores de 60 años, pero en partes de África y Asia también afecta a jóvenes con infección por VIH y sigue un curso más agresivo1).
La 8.ª edición del AJCC clasifica el OSSN según el tumor primario (T), los ganglios linfáticos regionales (N) y la metástasis a distancia (M)1).
| Clasificación | Definición |
|---|---|
| Tis | Carcinoma in situ (confinado al epitelio) |
| T1 | Confinado a la conjuntiva, sin invasión de estructuras adyacentes |
| T2 | Invasión de estructuras oculares adyacentes (córnea, fondo de saco, carúncula, esclerótica, globo ocular) |
| T3 | Invasión de órbita, senos paranasales o párpado |
| T4 | Invasión del sistema nervioso central o sitios distantes |
El SCC no tratado puede provocar invasión orbitaria (aproximadamente 10%), metástasis en ganglios linfáticos regionales y, raramente, metástasis a distancia, con tasas de mortalidad reportadas del 8 al 24% 1).
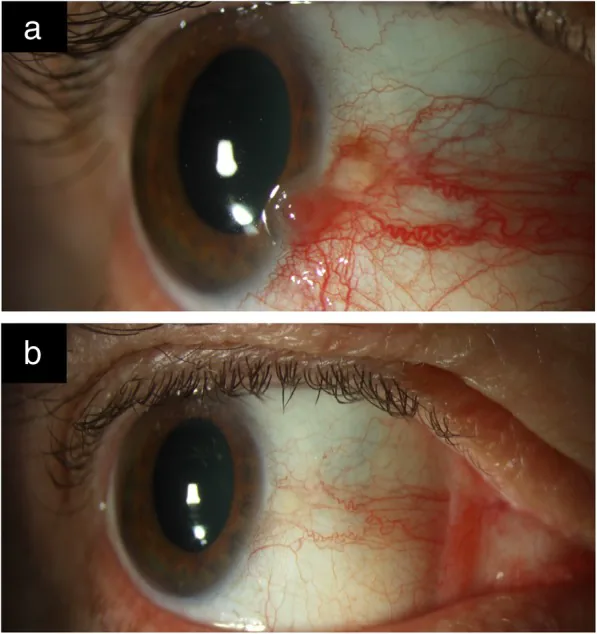
Las lesiones de OSSN a menudo son asintomáticas y se descubren incidentalmente. Cuando hay síntomas, predominan el enrojecimiento, la sensación de cuerpo extraño y la irritación ocular 2). También puede haber dolor. La disminución de la agudeza visual se observa cuando el tumor afecta la córnea o en casos de invasión intraocular.
Una masa vascularizada unilateral es lo más común, y ocurre típicamente cerca del limbo en la hendidura palpebral (lado nasal o temporal) 1). Afecta con frecuencia la córnea y la conjuntiva bulbar, mientras que la afectación de la conjuntiva palpebral es rara 1). En caucásicos, la lesión es de color amarillo-rosado; en razas pigmentadas, puede presentar pigmentación 1)3).
Gelatinoso
Masa elevada translúcida: La forma más común. Los vasos conjuntivales muestran un trayecto en forma de horquilla.
Vasos nutricios: Arterias nutricias anormalmente dilatadas y tortuosas sugieren crecimiento maligno 1).
Leucoplásico
Superficie blanquecina y engrosada: Queratinización de la superficie tumoral debido a hiperqueratosis.
Aspecto seco: Presenta un color blanco opaco, en contraste con el gelatinoso.
Papilomatoso
Crecimiento papilomatoso: Conocido como una morfología asociada al VPH 4).
Superficie nodular: Puede tener una apariencia verrugosa.
Noduloulcerativo
Raro pero invasivo: Morfología que sugiere fuertemente una neoplasia invasiva 1).
Ulceración: Peor pronóstico que otras formas.
La afectación corneal presenta una apariencia translúcida, grisácea, de vidrio esmerilado, con extensión fimbriada o en seudópodos.
La invasión intraocular es rara, pero puede presentarse como una masa blanca en la cámara anterior, inflamación de la cámara anterior o glaucoma secundario 2).
La etiología de la OSSN es multifactorial. Los principales factores de riesgo se enumeran a continuación 1).
Porque la inmunosupresión causada por la infección por VIH deteriora el mecanismo de vigilancia inmunitaria tumoral. En personas VIH positivas, el riesgo de OSSN aumenta de 10 a 13 veces 3) y puede ocurrir a una edad temprana. En África, la coinfección con VIH y VPH se considera un factor contribuyente al aumento de la enfermedad 1).
El diagnóstico definitivo de la OSSN es el examen histológico mediante biopsia escisional o incisional (estándar de oro) 1). Para tumores pequeños de menos de 4 horas, está indicada la biopsia escisional; para tumores grandes de 4 horas o más, está indicada la biopsia incisional.
Para ayudar al diagnóstico se utilizan tinciones especiales como rosa de Bengala, verde de lissamina, azul de metileno y azul de toluidina 1). El rosa de Bengala tiñe las células epiteliales apoptóticas o metabólicamente inactivas de un color rosa brillante, aclarando los márgenes del tumor 1).
Las principales modalidades diagnósticas se resumen a continuación.
| Prueba | Características |
|---|---|
| Biopsia (histopatología) | Estándar de oro. Puede evaluar la profundidad de invasión. |
| HR-OCT | No invasivo. Se caracteriza por engrosamiento epitelial e hiperreflectividad. |
| IVCM | Evaluación a nivel celular. Técnicamente exigente. |
| Citología por impresión | No invasivo pero solo evalúa tejido superficial. |
El OSSN debe diferenciarse especialmente del pterigión y la pingüécula 1). Pueden coexistir, dificultando el diagnóstico. Otros diagnósticos diferenciales incluyen pannus corneal, queratosis actínica, granuloma piógeno, nevus conjuntival y melanoma maligno.
Cuando solo los hallazgos clínicos dificultan el diagnóstico diferencial, el engrosamiento epitelial y la hiperreflectividad en la HR-OCT, así como la tinción especial con rosa de Bengala o azul de metileno, pueden proporcionar pistas para el diagnóstico diferencial 1). Se requiere biopsia para el diagnóstico definitivo.
El tratamiento de la OSSN se individualiza según el tamaño del tumor, la profundidad de invasión y los factores del paciente 1). Se ha informado que la escisión quirúrgica y la quimioterapia tópica tienen una eficacia equivalente 1).
Técnica de no contacto más crioterapia es el estándar de oro 1).
Si los márgenes de escisión son positivos, se recomienda quimioterapia adyuvante postoperatoria 1)2). Sin crioterapia ni quimioterapia postoperatoria, aumenta el riesgo de invasión intraocular 2).
Pike et al. (2023) informaron un caso de OSSN en el que, sin crioterapia ni quimioterapia después de la escisión, se produjo diseminación intraocular (formación de masa en la cámara anterior) a través de un defecto limbal de espesor total, lo que llevó a la enucleación 2). Esto destaca la importancia de la técnica de no contacto, la crioterapia y la quimioterapia postoperatoria.
La quimioterapia tópica se utiliza tanto como monoterapia como terapia adyuvante postoperatoria 1).
Mitomicina C
Mitomicina C: gotas oftálmicas al 0.02–0.04%. Mata las células tumorales mediante entrecruzamiento del ADN.
Tasa de eficacia: 80–100%. El tiempo hasta la resolución tiende a ser más corto que con IFN1).
Efectos secundarios: Dolor ocular, deficiencia de células madre limbares, riesgo de estenosis del punto lagrimal.
5-FU
5-Fluorouracilo: Análogo de pirimidina que inhibe la síntesis de ADN y ARN en la fase S1).
Tasa de eficacia: Alta. Tasa de recurrencia de hasta el 20%. Más barato que la mitomicina C y el IFN.
Administración: Se usa en ciclos de gotas oftálmicas al 1% durante 1 semana seguidas de 3 semanas de descanso.
IFNα-2b
Interferón α-2b: Tiene efectos antiproliferativos, antivirales e inmunomoduladores1).
Tasa de eficacia: 80–100%. Se administra mediante inyección subconjuntival (1 millón de UI/mL) o gotas oftálmicas.
Características: Pocos efectos secundarios pero caro y requiere refrigeración.
Otras terapias farmacológicas incluyen agentes anti-VEGF (bevacizumab, ranibizumab), que muestran resultados prometedores en lesiones conjuntivales pero efectos poco claros en lesiones corneales; se necesitan ensayos a gran escala1). El cidofovir puede usarse en pacientes relacionados con VPH1).
El enfoque de tratamiento basado en la 8.ª edición del AJCC se muestra a continuación1).
Los siguientes factores están asociados con la recurrencia1).
Se ha informado que la quimioterapia sola (MMC, 5-FU, IFNα-2b) es tan efectiva como la cirugía1). La elección depende del tamaño del tumor, la profundidad de la invasión, el estado general del paciente y la adherencia. Para lesiones mayores de 4 horas, múltiples o recurrentes, la quimioterapia tópica puede ser ventajosa.
Se cree que el OSSN se origina a partir de las células madre del limbo 1). La mayoría de los tumores malignos conjuntivales primarios aparecen cerca del limbo en la hendidura palpebral, donde la división de las células madre es activa 1).
Histológicamente, en el SCC invasivo, las células epiteliales escamosas malignas atraviesan la membrana basal y proliferan en el estroma 1). La NIC I a III se clasifica según la extensión de la displasia dentro del epitelio. La displasia de espesor completo (NIC III) es sinónimo de carcinoma in situ 1).
La invasión intraocular es rara pero ocurre a través de las siguientes vías 2):
En el caso de Pike et al. (2023), se formó un defecto limbal de espesor completo después de la biopsia por escisión, a través del cual las células tumorales se sembraron en la cámara anterior y se diseminaron a la superficie corneal posterior, el ángulo, el iris, el cuerpo ciliar y el cristalino 2). Patológicamente, los hallazgos se asemejaban a una forma maligna de crecimiento epitelial hacia abajo (epithelial downgrowth).
En el carcinoma mucoepidermoide, la tinción de mucina revela células epiteliales escamosas displásicas y células caliciformes malignas. Cuando el componente de mucina es predominante, se considera que la agresividad clínica es relativamente baja.
La radioterapia se está considerando como una opción de tratamiento para OSSN y SCC 1).
Es un tratamiento que combina verteporfina y láser 1). En un estudio piloto, se logró la desaparición del tumor en el 100% de los SCC conjuntivales, sin recurrencia durante el período de observación 1). Sin embargo, el alto costo, las instalaciones limitadas y la necesidad de capacitación especializada son barreras para su adopción generalizada.
Zein et al. (2024) administraron cuatro inyecciones intramusculares de la vacuna contra el VPH 9-valente (Gardasil-9) con intervalos de 6 semanas a un paciente con OSSN papilar recurrente (VPH positivo, p16 positivo) después de dos resecciones 4). Se observó una dramática reducción del tumor después de la tercera inyección, y la HR-OCT confirmó mejoría en el engrosamiento epitelial y la hiperreflectividad. Sin embargo, no se logró la curación y se administraron adicionalmente 5-FU tópico y mitomicina C.
Este es el primer informe mundial del uso de la vacuna contra el VPH para el tratamiento de OSSN 4), y se está investigando como una opción terapéutica futura. Se presume que el mecanismo terapéutico de la vacuna implica la supresión de las oncoproteínas E6/E7 específicas del VPH 4).