膠狀
半透明隆起性腫塊:最常見的形態。結膜血管呈髮夾樣走向。
營養血管:異常擴張迂曲的營養動脈提示惡性增生 1)。

該術語由Lee等人於1995年提出,涵蓋起源於角膜、結膜和角膜緣的非複合型鱗狀上皮腫瘤1)。它是眼表最常見的非色素性腫瘤;在一項單中心研究中,OSSN佔771例非黑色素細胞性結膜腫瘤的23%(179例)1)。
OSSN包括以下病變:
發生率的地理差異很大。在高緯度地區為0.02/10萬,而在赤道附近的低緯度地區則達到3.5/10萬1)。全球年齡標準化發生率為0.26/10萬/年,且呈增加趨勢1)。非洲發生率最高(3.4/10萬/年),HIV和HPV感染的高頻率是原因之一1)。
在西半球,好發於60歲以上的白人男性,但在非洲和亞洲部分地區,HIV感染者中的年輕人也會發病,且病程更具侵襲性1)。
AJCC第8版根據原發腫瘤(T)、區域淋巴結(N)和遠端轉移(M)對OSSN進行分類1)。
| 分類 | 定義 |
|---|---|
| Tis | 原位癌(侷限於上皮內) |
| T1 | 侷限於結膜,未侵犯鄰近結構 |
| T2 | 侵犯鄰近眼部結構(角膜、穹窿、淚阜、鞏膜、眼球) |
| T3 | 侵犯眼眶、鼻竇或眼瞼 |
| T4 | 侵犯中樞神經系統或遠端部位 |
未治療的SCC可能導致眼眶侵犯(約10%)、區域淋巴結轉移,罕見遠端轉移,死亡率報告為8%至24% 1)。
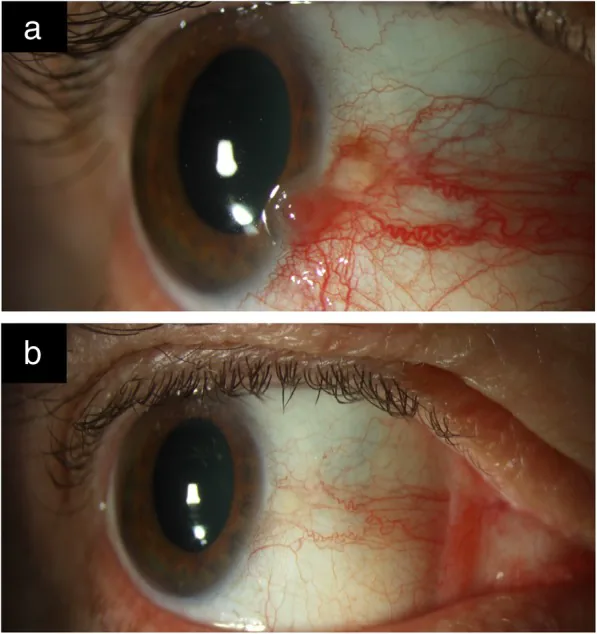
OSSN病變通常無症狀,偶然發現。有症狀時,主要表現為充血、異物感和眼刺激症狀 2)。也可能伴隨疼痛。視力下降見於腫瘤波及角膜或眼內浸潤的病例。
單側血管性腫塊最為常見,好發於眼裂間(鼻側或顳側)的角膜緣附近 1)。多累及角膜和球結膜,眼瞼結膜發病罕見 1)。白種人呈黃粉色,有色人種可伴有色素沉著 1)3)。
膠狀
半透明隆起性腫塊:最常見的形態。結膜血管呈髮夾樣走向。
營養血管:異常擴張迂曲的營養動脈提示惡性增生 1)。
白斑狀
表面白色化、增厚:因過度角化導致的腫瘤表面角化。
乾燥外觀:呈現不透明的白色調,與膠凍狀相反。
乳頭狀
乳頭狀增生:已知與HPV相關的形態4)。
結節狀表面:可能呈疣狀外觀。
結節潰瘍型
罕見但具侵襲性:強烈提示浸潤性腫瘤的形態1)。
潰瘍形成:預後較其他類型差。
角膜受累時呈半透明、灰色磨玻璃樣外觀,並呈流蘇狀或偽足樣擴展。
眼內浸潤罕見,但可表現為前房白色腫塊、前房炎症或續發性青光眼2)。
OSSN的病因是多因素的。主要危險因子如下1)。
因為HIV感染導致的免疫抑制削弱了腫瘤免疫監視機制。HIV陽性者OSSN風險增加10~13倍3),且可在年輕時發病。在非洲,HIV與HPV的合併感染被認為是疾病增加的原因之一1)。
OSSN的確診依靠切除切片或切開切片的組織學檢查(黃金標準)1)。小於4小時的小腫瘤適用切除切片,大於等於4小時的大腫瘤適用切開切片。
診斷輔助可使用玫瑰紅、麗絲胺綠、亞甲藍、甲苯胺藍等特殊染色1)。玫瑰紅可將凋亡或代謝不活躍的上皮細胞染成鮮明的粉紅色,使腫瘤輪廓更清晰1)。
主要診斷方式總結如下。
| 檢查方法 | 特點 |
|---|---|
| 活檢(組織檢查) | 黃金標準。可評估浸潤深度。 |
| HR-OCT | 非侵入性。特徵為上皮增厚和高反射。 |
| IVCM | 細胞層級評估。操作繁瑣。 |
| 印跡細胞學 | 非侵入性,但僅評估表面組織。 |
OSSN與翼狀胬肉和瞼裂斑的鑑別尤其重要1)。兩者可能共存,導致診斷困難。其他鑑別診斷包括角膜血管翳、光化性角化病、化膿性肉芽腫、結膜痣和惡性黑色素瘤。
僅憑臨床所見有時難以鑑別。HR-OCT上的上皮增厚和高反射表現,以及玫瑰紅或亞甲藍的特殊染色可為鑑別提供線索1)。確診需要切片檢查。
OSSN的治療根據腫瘤大小、浸潤深度和患者因素個別化1)。據報導,手術切除和局部化學治療療效相當1)。
無接觸技術+冷凍療法是黃金標準1)。
如果切除邊緣陽性,建議術後輔助化學治療1)2)。在沒有冷凍療法和術後化學治療的情況下,眼內浸潤的風險增加2)。
Pike等人(2023)報告了一例OSSN病例,切除後未進行冷凍療法或化學治療,通過全層角膜緣缺損發生眼內播散(前房腫塊形成),最終導致眼球摘除2)。這強調了無接觸技術、冷凍療法和術後化學治療的重要性。
局部化學治療既可作為單一療法,也可作為術後輔助治療使用1)。
絲裂黴素C
5-FU
5-氟尿嘧啶:一種嘧啶類似物,抑制S期DNA和RNA合成1)。
有效率:高。復發率最高達20%。比絲裂黴素C和IFN便宜。
給藥方法:使用1%滴眼液,每週給藥、停藥3週的週期。
IFNα-2b
干擾素α-2b:具有抗增殖、抗病毒和免疫調節作用1)。
有效率:80%~100%。通過結膜下注射(100萬IU/mL)或滴眼給藥。
特點:副作用少,但價格昂貴且需要冷藏保存。
其他藥物治療包括抗VEGF藥物(貝伐珠單抗、雷珠單抗),對結膜病變顯示出有希望的結果,但對角膜病變的效果不明確,需要大規模試驗1)。HPV相關患者可能使用西多福韋1)。
基於AJCC第8版的治療方法如下所示1)。
以下因子與復發相關1)。
據報導,單獨化療(MMC、5-FU、IFNα-2b)的療效與手術相當1)。根據腫瘤大小、浸潤深度、患者全身狀況和順從性選擇。對於大於4個鐘點的病灶、多發性或復發性病例,局部化療可能更有優勢。
OSSN被認為起源於角膜緣幹細胞1)。大多數原發性結膜惡性腫瘤出現在眼瞼裂間的角膜緣附近,該區域幹細胞分裂活躍1)。
組織學上,浸潤性SCC中惡性鱗狀上皮細胞穿透基底膜並在間質內增殖1)。CIN I至III根據上皮內異型增生的範圍分類。全層上皮異型增生(CIN III)與原位癌同義1)。
眼內浸潤罕見,但可通過以下途徑發生2):
Pike等人(2023)的病例中,切除活檢後形成全層角膜緣缺損,腫瘤細胞通過該路徑播散至前房,並擴散至角膜後面、房角、虹膜、睫狀體和晶狀體2)。病理學表現類似於惡性上皮向下生長。
在黏液表皮樣癌中,黏液染色顯示異型增生的鱗狀上皮細胞和惡性杯狀細胞。當黏液成分佔優勢時,臨床侵襲性被認為相對較低。
放射治療正在被考慮作為OSSN和SCC的治療選擇1)。
這是一種結合維替泊芬和雷射的治療方法1)。在一項先導研究中,結膜SCC的腫瘤消失率達到100%,且在觀察期間無復發1)。然而,高成本、設施有限以及需要專業訓練是普及的障礙。
Zein等人(2024)對一名兩次切除後復發的乳頭狀OSSN(HPV陽性、p16陽性)患者,每6週肌肉注射一次9價HPV疫苗(Gardasil-9),共4次4)。第三次注射後觀察到腫瘤顯著縮小,HR-OCT證實上皮增厚和高反射性改善。但未達到根治,隨後進行了額外的5-FU和絲裂黴素C點眼治療。
這是全球首次報導將HPV疫苗用於OSSN治療4),作為未來的治療選擇正在研究中。治療機制推測為抑制HPV特異性E6/E7癌蛋白4)。