Gelatinoso
Massa rilevata semitrasparente: forma più comune. I vasi congiuntivali mostrano un decorso a forcina.
Vasi nutritivi: arterie nutritive anormalmente dilatate e tortuose suggeriscono una crescita maligna 1).

Termine proposto da Lee et al. nel 1995, comprende i tumori epiteliali squamosi non compositi di cornea, congiuntiva e limbo 1). È il tumore non pigmentato più frequente della superficie oculare; in uno studio monocentrico, le OSSN rappresentavano il 23% (179 casi) di 771 tumori congiuntivali non melanocitari 1).
Le OSSN includono le seguenti lesioni:
L’incidenza varia notevolmente in base alla regione geografica. Nelle regioni ad alta latitudine è di 0,02/100.000, mentre vicino all’equatore raggiunge 3,5/100.0001). Il tasso di incidenza standardizzato per età a livello mondiale è di 0,26/100.000 all’anno ed è in aumento1). L’Africa ha il tasso più alto (3,4/100.000 all’anno), a cui contribuisce l’elevata frequenza di infezioni da HIV e HPV1).
Nell’emisfero occidentale, si verifica prevalentemente in uomini bianchi di età superiore ai 60 anni, ma in Africa e in alcune parti dell’Asia si manifesta anche in giovani adulti con infezione da HIV e ha un decorso più aggressivo1).
L’8ª edizione dell’AJCC classifica gli OSSN in base al tumore primario (T), ai linfonodi regionali (N) e alle metastasi a distanza (M)1).
| Classificazione | Definizione |
|---|---|
| Tis | Carcinoma in situ (limitato all’epitelio) |
| T1 | Limitato alla congiuntiva, senza invasione delle strutture adiacenti |
| T2 | Invasione delle strutture oculari adiacenti (cornea, fornice, caruncola, sclera, bulbo) |
| T3 | Invasione dell’orbita, dei seni paranasali o delle palpebre |
| T4 | Invasione del sistema nervoso centrale o di siti distanti |
I SCC non trattati possono causare invasione orbitaria (circa il 10%), metastasi ai linfonodi regionali e, raramente, metastasi a distanza, con un tasso di mortalità riportato dell’8-24% 1).
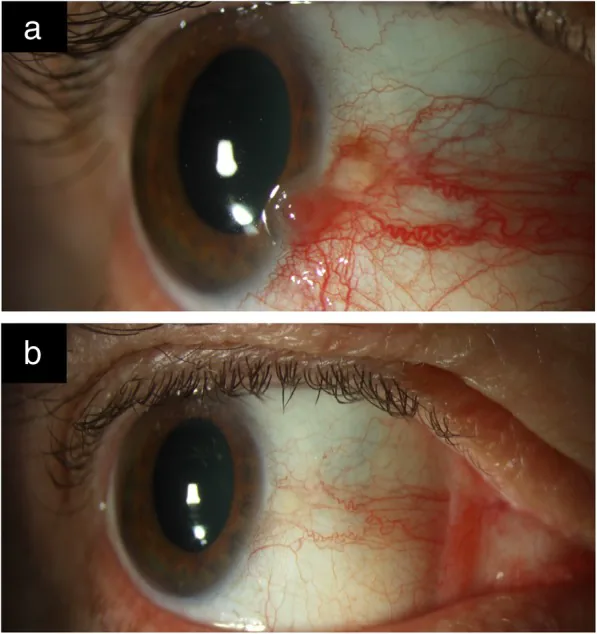
Le lesioni OSSN sono spesso asintomatiche e scoperte incidentalmente. Se presenti, i sintomi sono principalmente arrossamento, sensazione di corpo estraneo e irritazione oculare 2). Può essere presente anche dolore. La riduzione dell’acuità visiva si verifica quando il tumore si estende alla cornea o in caso di infiltrazione intraoculare.
La presentazione più comune è una massa unilaterale vascolarizzata, che si verifica preferenzialmente vicino al limbo nella zona interpalpebrale (lato nasale o temporale) 1). Colpisce principalmente la cornea e la congiuntiva bulbare, raramente la congiuntiva palpebrale 1). Nelle persone di razza bianca è di colore giallo-rosato, mentre nelle persone di colore può essere pigmentata 1)3).
Gelatinoso
Massa rilevata semitrasparente: forma più comune. I vasi congiuntivali mostrano un decorso a forcina.
Vasi nutritivi: arterie nutritive anormalmente dilatate e tortuose suggeriscono una crescita maligna 1).
Leucoplasico
Sbiancamento e ispessimento della superficie: cheratinizzazione della superficie tumorale dovuta a ipercheratosi.
Aspetto secco : presenta una tonalità bianca opaca, in contrasto con l’aspetto gelatinoso.
Papillare
Proliferazione papillare : forma associata all’HPV 4).
Superficie nodulare : può avere un aspetto verrucoso.
Nodulo-ulcerativo
Raro ma invasivo : forma fortemente suggestiva di neoplasia infiltrante 1).
Ulcerazione : prognosi peggiore rispetto ad altre forme.
L’estensione alla cornea si presenta con un aspetto traslucido, grigiastro, a vetro smerigliato, con progressione frangiata o a pseudopodi.
L’infiltrazione intraoculare è rara, ma può manifestarsi come massa bianca in camera anteriore, flogosi della camera anteriore o glaucoma secondario 2).
Sì. In particolare nelle persone di colore HIV-positive, è stato riportato che il CIN può imitare una lesione pigmentata 3). Anche in assenza di reperti tipici di OSSN, una lesione congiuntivale pigmentata in soggetti HIV-positivi deve includere l’OSSN nella diagnosi differenziale.
L’eziologia dell’OSSN è multifattoriale. I principali fattori di rischio sono elencati di seguito 1).
Ciò è dovuto all’immunosoppressione causata dall’infezione da HIV, che riduce la sorveglianza immunitaria antitumorale. Nei soggetti HIV-positivi, il rischio di OSSN aumenta di 10-13 volte3) e la malattia può insorgere in giovane età. In Africa, la coinfezione da HIV e HPV è considerata un fattore che contribuisce all’aumento della malattia1).
La diagnosi definitiva di OSSN si basa sull’esame istologico di una biopsia escissionale o incisionale (gold standard)1). Per piccoli tumori inferiori a 4 ore è indicata la biopsia escissionale, per grandi tumori superiori a 4 ore è appropriata la biopsia incisionale.
Per coadiuvare la diagnosi vengono utilizzate colorazioni speciali come il rosa bengala, il verde lissamina, il blu di metilene e il blu di toluidina 1). Il rosa bengala colora in rosa brillante le cellule epiteliali apoptotiche o metabolicamente inattive, chiarendo i contorni del tumore 1).
Le principali modalità diagnostiche sono riassunte di seguito.
| Metodo di esame | Caratteristiche |
|---|---|
| Biopsia (esame tissutale) | Gold standard. Consente anche di valutare la profondità di invasione |
| HR-OCT | Non invasivo. Ispessimento epiteliale e iperriflettività caratteristici |
| IVCM | Valutazione a livello cellulare. Manipolazione complessa |
| Citologia per impronta | Non invasivo ma valuta solo i tessuti superficiali |
L’OSSN deve essere distinto in particolare dallo pterigio e dalla pinguecola 1). La loro coesistenza può rendere la diagnosi difficile. Altre diagnosi differenziali includono panno corneale, cheratosi attinica, granuloma piogenico, nevo congiuntivale e melanoma maligno.
In alcuni casi la sola presentazione clinica non consente una diagnosi differenziale. L’ispessimento epiteliale e l’iper-riflettività all’HR-OCT, insieme alle colorazioni speciali con rosa bengala o blu di metilene, forniscono indizi per la diagnosi differenziale1). Per una diagnosi definitiva è necessaria una biopsia.
Il trattamento della OSSN viene personalizzato in base alle dimensioni del tumore, al grado di invasione e ai fattori legati al paziente1). L’efficacia dell’escissione chirurgica e della chemioterapia topica è risultata equivalente1).
La tecnica no-touch con crioterapia rappresenta il gold standard1).
In caso di margini di resezione positivi, si raccomanda la chemioterapia adiuvante post-operatoria1)2). Senza crioterapia e senza chemioterapia post-operatoria, il rischio di invasione intraoculare aumenta2).
Pike et al. (2023) hanno descritto un caso di OSSN in cui, dopo escissione senza crioterapia né chemioterapia, si è verificata una disseminazione intraoculare (formazione di una massa in camera anteriore) attraverso un difetto limbare a tutto spessore, che ha reso necessaria l’enucleazione2). Gli autori sottolineano l’importanza della tecnica no-touch, della crioterapia e della chemioterapia post-operatoria.
La chemioterapia topica viene utilizzata sia come monoterapia sia come terapia adiuvante post-operatoria1).
Mitomicina C
Mitomicina C: collirio allo 0,02-0,04%. Agisce formando legami crociati con il DNA, inducendo la morte delle cellule tumorali.
Tasso di efficacia: 80–100%. Il tempo di scomparsa tende ad essere più breve rispetto all’IFN1).
Effetti collaterali: dolore oculare, perdita delle cellule staminali limbari, rischio di stenosi del punto lacrimale.
5-FU
5-fluorouracile: analogo pirimidinico che inibisce la sintesi di DNA e RNA nella fase S1).
Tasso di efficacia: elevato. Tasso di recidiva fino al 20%. Meno costoso di mitomicina C e IFN.
Modalità di somministrazione: collirio all’1% in cicli di 1 settimana di trattamento e 3 settimane di pausa.
IFNα-2b
Interferone alfa-2b: possiede effetti antiproliferativi, antivirali e immunomodulatori1).
Tasso di efficacia: 80–100%. Somministrato per iniezione sottocongiuntivale (1 milione UI/mL) o come collirio.
Caratteristiche: pochi effetti collaterali ma costoso e richiede conservazione in frigorifero.
Tra le altre terapie farmacologiche, gli anti-VEGF (bevacizumab, ranibizumab) mostrano risultati promettenti per le lesioni congiuntivali, ma l’effetto sulle lesioni corneali non è chiaro e sono necessari studi su larga scala1). Nei pazienti correlati all’HPV può essere utilizzato il cidofovir1).
L’approccio terapeutico basato sull’8ª edizione dell’AJCC è mostrato di seguito1).
I seguenti fattori sono coinvolti nella recidiva1).
L’efficacia della sola chemioterapia (MMC, 5-FU, IFNα-2b) è riportata come equivalente alla chirurgia1). La scelta dipende dalle dimensioni e dal grado di infiltrazione del tumore, nonché dalle condizioni generali e dall’aderenza del paziente. Per lesioni di oltre 4 ore, multiple o recidivanti, la chemioterapia locale può essere vantaggiosa.
Si ritiene che l’OSSN abbia origine dalle cellule staminali limbari 1). La maggior parte dei tumori maligni congiuntivali primari compare vicino al limbo nella rima palpebrale, dove la divisione delle cellule staminali è attiva 1).
Istologicamente, nel SCC invasivo, le cellule squamose maligne attraversano la membrana basale e proliferano nello stroma 1). La CIN da I a III è classificata in base all’estensione della displasia intraepiteliale. La displasia che interessa tutto lo spessore dell’epitelio (CIN III) è sinonimo di carcinoma in situ 1).
L’infiltrazione intraoculare è rara ma può verificarsi attraverso le seguenti vie 2):
Nel caso di Pike et al. (2023), dopo una biopsia escissionale si è formato un difetto limbare a tutto spessore, attraverso il quale le cellule tumorali si sono disseminate nella camera anteriore, diffondendosi alla superficie posteriore della cornea, all’angolo, all’iride, al corpo ciliare e al cristallino 2). Patologicamente, l’aspetto era simile a una forma maligna di epithelial downgrowth.
Nel carcinoma mucoepidermoide, la colorazione per la mucina evidenzia cellule squamose displastiche e cellule caliciformi maligne. Quando la componente mucinosa è predominante, l’aggressività clinica è considerata relativamente bassa.
La radioterapia è considerata un’opzione terapeutica per OSSN e SCC 1).
Si tratta di un trattamento che combina verteporfina e laser 1). In uno studio pilota, si è ottenuta la scomparsa del tumore nel 100% dei casi di SCC congiuntivale, senza recidive durante il periodo di follow-up 1). Tuttavia, i costi elevati, la disponibilità limitata delle strutture e la necessità di una formazione specialistica rappresentano ostacoli alla sua diffusione.
Zein et al. (2024) hanno somministrato 4 iniezioni intramuscolari del vaccino anti-HPV 9-valente (Gardasil-9) a intervalli di 6 settimane a un paziente con OSSN papillare recidivante (HPV-positivo, p16-positivo) dopo due resezioni 4). Dopo la terza iniezione si è osservata una drammatica riduzione del tumore e l’HR-OCT ha confermato un miglioramento dell’ispessimento epiteliale e dell’iperriflettività. Tuttavia, non si è ottenuta la guarigione completa e sono stati somministrati ulteriori colliri a base di 5-FU e mitomicina C.
Questa è la prima segnalazione mondiale dell’applicazione del vaccino anti-HPV nel trattamento dell’OSSN 4) e la ricerca prosegue come futura opzione terapeutica. Si ipotizza che il meccanismo d’azione terapeutico del vaccino sia la soppressione delle oncoproteine E6/E7 specifiche dell’HPV 4).