
转移性脉络膜肿瘤
一目了然的要点
Section titled “一目了然的要点”1. 什么是转移性脉络膜肿瘤?
Section titled “1. 什么是转移性脉络膜肿瘤?”全身各脏器发生的恶性肿瘤可能转移至眼内。转移部位多为葡萄膜组织,尤其好发于脉络膜。虹膜或睫状体转移罕见。
脉络膜是眼内血流量最多的组织,具有易捕获血行运送的肿瘤细胞的解剖学背景。转移灶好发于后极部,可为单发或多发。约四分之一的病例出现双眼转移。
原发灶的分布存在性别差异。男性中最常见的原发灶是肺癌,女性中最常见的是乳腺癌。此外,也有来自肾癌、消化道癌和前列腺癌转移的报道。乳腺癌在原发灶治疗后,经过较长时间才可能发生葡萄膜转移。
按原发灶分类的频率(性别差异)
Section titled “按原发灶分类的频率(性别差异)”| 性别 | 最常见的原发灶 | 其他原发灶 |
|---|---|---|
| 男性 | 肺癌 | 肾癌、消化道癌、前列腺癌 |
| 女性 | 乳腺癌 | 肺癌、肾癌、消化道癌 |
与三大脉络膜肿瘤的鉴别
Section titled “与三大脉络膜肿瘤的鉴别”转移性脉络膜肿瘤在脉络膜的三大主要肿瘤(恶性黑色素瘤、血管瘤、转移性肿瘤)中具有独特的外观。
| 恶性黑色素瘤 | 血管瘤 | 转移性肿瘤 | |
|---|---|---|---|
| 色调 | 黑、灰、褐色 | 橙红色 | 黄白色 |
| 形状 | 穹隆状 | 梭形 | 板状 |
| 视网膜脱离 | 无至中度 | 无至轻度 | 显著 |
| 生长 | 相对缓慢 | 无 | 快速 |
男性中,肺癌是最常见的转移来源;女性中,乳腺癌最常见。此外,肾癌、消化道癌和前列腺癌的转移也有报道。约四分之一的病例出现双眼转移。乳腺癌可能在原发灶治疗后很长时间才发现眼内转移。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”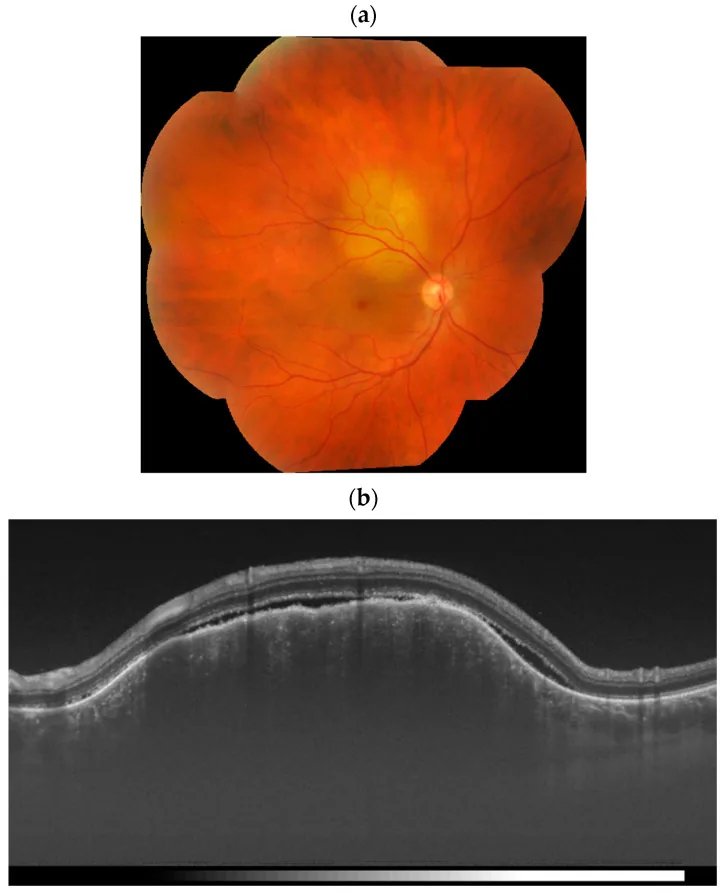
在脉络膜转移中,肿瘤伴随的浆液性视网膜脱离会引起以下症状:
- 视野缺损:与视网膜脱离范围相应的视野缺失。
- 视力下降:累及黄斑时显著下降。
- 视物变形:物体看起来扭曲,由视网膜移位引起。
虹膜转移则呈现不同的症状。
- 视物模糊和视力下降:由肿瘤出血引起。
- 前房混浊:虹膜肿瘤来源的炎症细胞流入前房。
临床所见(脉络膜转移)
Section titled “临床所见(脉络膜转移)”眼底检查时,表现为相对扁平、边界清晰的黄白色病变。随着进展,病变隆起,可能难以与其他脉络膜肿瘤鉴别。病变正上方或周围有明显的浆液性视网膜脱离。
呈板状形态的原因是肿瘤细胞在脉络膜毛细血管板中被捕获,并沿血管横向生长。随之,色素上皮(RPE)细胞也受到损伤,导致渗出性(浆液性)视网膜脱离。
荧光眼底造影(FA)所见
Section titled “荧光眼底造影(FA)所见”- 早期至中期:肿瘤内颗粒状强荧光。
- 后期:转变为弥漫性不规则强荧光。
- 肿瘤周围:有时可见带状弱荧光边缘。
3. 原因与风险因素
Section titled “3. 原因与风险因素”原发灶产生的肿瘤细胞通过血行播散至全身,并到达眼内。眼球内脉络膜血流最丰富,因此肿瘤细胞易被捕获,成为转移的好发部位。
肿瘤细胞在脉络膜毛细血管板的毛细血管网中被捕获后,局部增殖。在此过程中,RPE受损,引发渗出性视网膜脱离。
主要风险因素
Section titled “主要风险因素”- 恶性肿瘤病史:尤其需注意肺癌、乳腺癌、肾癌、消化道癌、前列腺癌病史者。
- 进展期全身性恶性肿瘤:作为远处转移的一部分发生眼内转移。
- 乳腺癌治疗后长期经过:治疗后数年甚至十数年后可能出现眼转移。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”恶性肿瘤病史和治疗史是诊断的关键。特征性眼底表现(黄白色扁平病变伴明显浆液性视网膜脱离)结合恶性肿瘤病史,几乎可以确诊转移性脉络膜肿瘤。
在肺癌中,眼底转移灶有时比原发灶更早被发现。部分患者因视力下降就诊眼科,进一步检查后发现全身恶性肿瘤。
眼底检查:确认黄白色扁平至板状病变及明显浆液性视网膜脱离。同时进行裂隙灯显微镜检查。
超声断层检查(B超):确认板状眼球壁增厚和浆液性视网膜脱离。肿瘤高度通常较低,形态扁平,与恶性黑色素瘤不同。
荧光眼底造影(FA):颗粒状高荧光→弥漫性高荧光的模式,以及肿瘤周围低荧光带支持诊断。
OCT/SS-OCTA:有助于评估肿瘤内部结构和视网膜脱离。扫频源OCT血管成像(SS-OCTA)可显示肿瘤内发夹环状异常血管,提高诊断图像质量1)。
原发灶不明时的全身检查:
- FDG-PET:全面搜索全身恶性肿瘤。
- 血清肿瘤标志物(CEA、器官特异性标志物):作为筛查进行。
- 影像学检查(胸部CT、腹部超声等):寻找主要原发灶。
| 疾病 | 鉴别要点 |
|---|---|
| 脉络膜恶性黑色素瘤 | 黑至褐色,隆起较高。浆液性视网膜脱离为中度 |
| 脉络膜血管瘤 | 橙红色,纺锤形。无生长或缓慢生长 |
| 脉络膜骨瘤 | 骨样高回声。超声显示声影 |
在肺癌中,眼底的转移灶有时比原发灶更早被发现。患者因视力下降就诊眼科,发现眼底转移性病变,进而通过全身检查确诊肺癌。作为视力下降和视野异常的原因,需考虑转移性脉络膜肿瘤进行鉴别诊断。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗方针的确定
Section titled “治疗方针的确定”当发现葡萄膜转移时,多数情况下预后较差。并非所有病例都适合治疗,评估全身状况和预期寿命是第一步。治疗方针需与原发灶的负责科室协作决定。
如果原发灶的治疗(化疗、分子靶向治疗、免疫治疗)预期有效,则优先进行全身治疗。全身治疗有时也能使眼内转移灶缩小。近年来,随着分子靶向药物和免疫检查点抑制剂的引入,长期生存的病例逐渐增多。
眼部局部放射治疗
Section titled “眼部局部放射治疗”眼部局部放射治疗无论原发灶的放射敏感性如何,均可期待一定效果。标准照射剂量为眼部40-50 Gy。放射治疗常能使浆液性视网膜脱离消退和转移灶缩小,有望改善视力。
如果预期寿命允许,放射治疗是基本方针;如果能够立即进行全身药物治疗,也可以优先进行全身治疗。
抗VEGF疗法
Section titled “抗VEGF疗法”有病例报告显示抗VEGF药物(如阿柏西普玻璃体内注射)可控制肿瘤。在一例38岁女性乳腺癌视神经转移病例中,阿柏西普玻璃体内注射治疗实现了肿瘤控制,视力从20/50改善至20/251)。然而,目前抗VEGF疗法在眼转移方面的系统性证据有限,需要根据具体病例进行考虑。
放射治疗(眼部40-50 Gy)通常可使浆液性视网膜脱离消退和转移灶缩小,有望改善视力。全身化疗或分子靶向治疗也有报告可缩小眼转移灶。但治疗效果因人而异,也取决于全身状况和疾病进展程度。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”血行转移与脉络膜捕获
Section titled “血行转移与脉络膜捕获”原发灶的肿瘤细胞通过血行播散至全身。在眼球内,脉络膜是血流量最丰富的组织,脉络膜毛细血管床的结构形成了易于捕获肿瘤细胞的环境。
脉络膜毛细血管的管径较大,肿瘤细胞容易在此处被捕获。捕获后,肿瘤细胞沿血管横向增殖,因此病变呈板状形态。这是转移性脉络膜肿瘤的形态学特征。
RPE损伤与渗出性视网膜脱离
Section titled “RPE损伤与渗出性视网膜脱离”随着肿瘤细胞增殖,上方的色素上皮(RPE)细胞受损。RPE通过Bruch膜与脉络膜毛细血管相邻,肿瘤的机械压迫或代谢障碍会损害RPE功能。
RPE功能受损导致脉络膜液体渗漏至视网膜下腔,形成渗出性(浆液性)视网膜脱离。这种视网膜脱离是视野缺损、视力下降和视物变形的主要原因。转移性脉络膜肿瘤的特征是明显的浆液性视网膜脱离,这有助于与其他脉络膜肿瘤鉴别。
转移部位的分布
Section titled “转移部位的分布”在眼内转移中,脉络膜转移最为常见,好发于后极部。虹膜和睫状体转移罕见。转移灶可为单发,也可在同一眼内出现多个病灶。约四分之一的病例发生双眼转移。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”SS-OCTA影像诊断的进展
Section titled “SS-OCTA影像诊断的进展”扫频源OCT血管成像(SS-OCTA)为转移性脉络膜肿瘤的诊断影像评估提供了新见解。已有报道显示其能够显示肿瘤内发夹环状的异常血管结构,对于无创评估肿瘤血管结构具有价值1)。该技术可补充传统荧光眼底造影,有助于详细掌握肿瘤内血管。
分子靶向药物和免疫疗法对眼转移的效果
Section titled “分子靶向药物和免疫疗法对眼转移的效果”随着肺癌中EGFR抑制剂、ALK抑制剂和PD-1/PD-L1抑制剂的普及,已有报道全身治疗有效时眼转移得到控制。在乳腺癌中,抗HER2疗法的发展可能有助于增加长期生存病例。
针对眼局部的抗VEGF疗法(如阿柏西普)对转移性脉络膜肿瘤已有病例报告水平的发现1),但目前尚无系统的随机对照试验证据。需要根据每个病例的全身状况和肿瘤性质进行适应症判断。
个体化影像诊断与治疗监测
Section titled “个体化影像诊断与治疗监测”OCT和超声检查的进步使治疗监测更加精细。通过定量追踪浆液性视网膜脱离的消退和肿瘤的扁平化,可以更精确地评估放射治疗和全身治疗的效果。
8. 参考文献
Section titled “8. 参考文献”- Zhou N, Liang L, Wei W. Swept-source OCT angiography of presumed optic nerve metastasis from breast carcinoma. Ophthalmology. 2023;130(9):e52.
- Cennamo G, Montorio D, Carosielli M, Romano MR, Cennamo G. Multimodal Imaging in Choroidal Metastasis. Ophthalmic Res. 2021;64(3):411-416. PMID: 33142285.
- Singh A, Malik D, Singh S, Vyas VJ. Choroidal metastasis in pancreatic adenocarcinoma. J Cancer Res Ther. 2022;18(1):263-265. PMID: 35381796.
