
تومور متاستاتیک کوروئید
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”1. متاستاز کوروئید چیست؟
Section titled “1. متاستاز کوروئید چیست؟”تومورهای بدخیم ایجاد شده در اندامهای مختلف بدن ممکن است به داخل چشم متاستاز دهند. شایعترین محل متاستاز بافت یووه آ است و به ویژه کوروئید شایعترین محل است. متاستاز به عنبیه و جسم مژگانی نادر است.
کوروئید بافتی با بیشترین جریان خون در چشم است و زمینه آناتومیکی برای به دام افتادن سلولهای توموری حمل شده از طریق جریان خون فراهم میکند. متاستازها اغلب در قطب خلفی رخ میدهند و میتوانند تک یا چندتایی باشند. حدود یکچهارم موارد متاستاز دوطرفه دارند.
توزیع تومور اولیه بر اساس جنسیت متفاوت است. در مردان، شایعترین متاستاز از ریه و در زنان از پستان است. همچنین متاستاز از کلیه، دستگاه گوارش و پروستات گزارش شده است. در سرطان پستان، متاستاز به یووهآ ممکن است مدتها پس از درمان تومور اولیه رخ دهد.
فراوانی بر اساس تومور اولیه (جنسیت)
Section titled “فراوانی بر اساس تومور اولیه (جنسیت)”| جنسیت | شایعترین تومور اولیه | سایر تومورهای اولیه |
|---|---|---|
| مرد | ریه | کلیه، دستگاه گوارش، پروستات |
| زن | پستان | ریه، کلیه، دستگاه گوارش |
تشخیص افتراقی از سه تومور اصلی مشیمیه
Section titled “تشخیص افتراقی از سه تومور اصلی مشیمیه”تومور متاستاتیک مشیمیه ظاهری منحصربهفرد در میان سه تومور اصلی مشیمیه (ملانوم بدخیم، همانژیوم، تومور متاستاتیک) دارد.
| ملانوم بدخیم | همانژیوم | تومور متاستاتیک | |
|---|---|---|---|
| رنگ | سیاه، خاکستری، قهوهای | نارنجی-قرمز | زرد-سفید |
| شکل | برجسته | دوکی شکل | صفحهای |
| جداشدگی شبکیه | بدون تا متوسط | بدون تا خفیف | شدید |
| رشد | نسبتاً آهسته | بدون | سریع |
در مردان، سرطان ریه و در زنان، سرطان پستان شایعترین منابع متاستاز هستند. متاستاز از سرطانهای کلیه، دستگاه گوارش و پروستات نیز گزارش شده است. در حدود یکچهارم موارد، متاستاز در هر دو چشم دیده میشود. در سرطان پستان، متاستاز داخل چشمی ممکن است مدتها پس از درمان تومور اولیه کشف شود.
2. علائم اصلی و یافتههای بالینی
Section titled “2. علائم اصلی و یافتههای بالینی”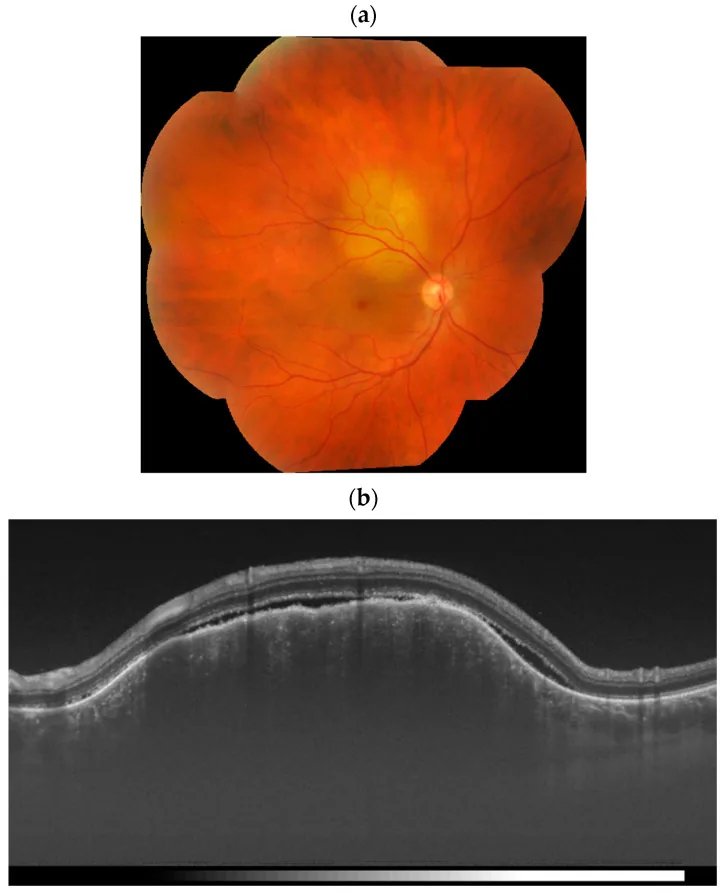
علائم ذهنی
Section titled “علائم ذهنی”در متاستاز مشیمیه، جداشدگی سروزی شبکیه ناشی از تومور علائم زیر را ایجاد میکند:
- نقص میدان بینایی: از دست دادن میدان بینایی متناسب با ناحیه جداشدگی شبکیه.
- کاهش دید: در صورت درگیری ماکولا، کاهش شدید دید.
- دگرنمایی: اشیاء خمیده به نظر میرسند که ناشی از جابجایی شبکیه است.
در متاستاز عنبیه، علائم متفاوتی بروز میکند:
- تاری دید و کاهش دید: ناشی از خونریزی از تومور.
- کدورت اتاق قدامی: سلولهای التهابی ناشی از تومور عنبیه به اتاق قدامی نشت میکنند.
یافتههای بالینی (متاستاز مشیمیه)
Section titled “یافتههای بالینی (متاستاز مشیمیه)”در معاینه فوندوس، ضایعه نسبتاً مسطح، زرد-سفید با مرزهای واضح دیده میشود. با پیشرفت، ضایعه برجسته میشود و گاهی تشخیص آن از سایر تومورهای مشیمیه دشوار میگردد. جداشدگی سروزی شبکیه قابل توجه در بالای ضایعه یا اطراف آن وجود دارد.
دلیل شکل صفحهای این است که سلولهای توموری در لایه مویرگی کوروئید گیر افتاده و در امتداد عروق به صورت جانبی رشد میکنند. به دنبال آن، سلولهای اپیتلیوم رنگدانهای (RPE) نیز آسیب دیده و جداشدگی شبکیه اگزوداتیو (سروزی) ایجاد میشود.
یافتههای آنژیوگرافی فلورسئین (FA)
Section titled “یافتههای آنژیوگرافی فلورسئین (FA)”- مرحله اولیه تا میانی: هیپرفلورسانس دانهای درون تومور.
- مرحله پایانی: تبدیل به هیپرفلورسانس منتشر و نامنظم.
- اطراف تومور: ممکن است حاشیهای کمفلورسانس به صورت نواری دیده شود.
3. علل و عوامل خطر
Section titled “3. علل و عوامل خطر”مکانیسم متاستاز
Section titled “مکانیسم متاستاز”سلولهای توموری از محل اولیه از طریق جریان خون در سراسر بدن پخش شده و به داخل چشم میرسند. از آنجایی که جریان خون در کوروئید چشم بیشترین است، سلولهای توموری به راحتی در آن گیر افتاده و این ناحیه به محل شایع متاستاز تبدیل میشود.
سلولهای توموری پس از گیر افتادن در شبکه مویرگی لایه مویرگی کوروئید، در محل تکثیر مییابند. در این فرآیند، RPE آسیب دیده و جداشدگی شبکیه اگزوداتیو ایجاد میشود.
عوامل خطر اصلی
Section titled “عوامل خطر اصلی”- سابقه بدخیمی: به ویژه افرادی با سابقه سرطان ریه، پستان، کلیه، دستگاه گوارش و پروستات باید احتیاط کنند.
- بدخیمی سیستمیک پیشرفته: متاستاز داخل چشمی به عنوان بخشی از متاستاز دوردست رخ میدهد.
- دوره طولانی پس از درمان سرطان پستان: ممکن است متاستاز چشمی چندین سال تا دهها سال پس از درمان ظاهر شود.
4. روشهای تشخیص و آزمایش
Section titled “4. روشهای تشخیص و آزمایش”نکات تشخیصی
Section titled “نکات تشخیصی”بررسی سابقه و درمان تومور بدخیم عامل تعیینکننده تشخیص است. ترکیب یافتههای مشخص فوندوس (ضایعات مسطح زرد-سفید همراه با جداشدگی شدید سروزی شبکیه) و سابقه تومور بدخیم، تشخیص تومور متاستاتیک مشیمیه را تقریباً قطعی میکند.
در سرطان ریه، گاهی متاستاز فوندوس زودتر از تومور اولیه کشف میشود. ممکن است بیمار به دلیل کاهش بینایی به چشمپزشک مراجعه کند و در نتیجه بررسیهای بیشتر، تومور بدخیم سیستمیک تشخیص داده شود.
آزمایشهای لازم
Section titled “آزمایشهای لازم”معاینه فوندوس: تأیید ضایعات مسطح تا صفحهای زرد-سفید و جداشدگی شدید سروزی شبکیه. همچنین معاینه با لامپ شکافی انجام میشود.
سونوگرافی (B-mode): ضخیم شدن صفحهای دیواره چشم و جداشدگی سروزی شبکیه تأیید میشود. ارتفاع تومور معمولاً کم است و در مقایسه با ملانوم بدخیم، شکلی مسطح دارد.
آنژیوگرافی فلورسین (FA): الگوی هیپرفلورسانس دانهای → هیپرفلورسانس منتشر و ناحیه هیپوفلورسانس اطراف تومور از تشخیص حمایت میکند.
OCT و SS-OCTA: برای ارزیابی ساختار داخلی تومور و جداشدگی شبکیه مفید است. در swept-source OCT angiography (SS-OCTA)، عروق غیرطبیعی به شکل حلقه سنجاقسر در داخل تومور گزارش شده است که به بهبود اطلاعات تصویربرداری تشخیصی کمک میکند 1).
جستجوی سیستمیک در صورت نامشخص بودن تومور اولیه:
- FDG-PET: جستجوی جامع تومورهای بدخیم در سراسر بدن.
- مارکرهای تومور سرم (CEA و مارکرهای اختصاصی اندام): به عنوان غربالگری انجام میشود.
- تصویربرداری (CT قفسه سینه، سونوگرافی شکم و غیره): جستجوی تومورهای اولیه اصلی.
تشخیص افتراقی
Section titled “تشخیص افتراقی”| بیماری | نکات افتراقی |
|---|---|
| ملانوم بدخیم مشیمیه | سیاه تا قهوهای و برجسته. جداشدگی سروزی شبکیه متوسط |
| همانژیوم مشیمیه | نارنجی-قرمز و دوکی شکل. بدون رشد یا رشد آهسته |
| استئوم مشیمیه | پراکندگی استخوانی. سایه صوتی در سونوگرافی |
در سرطان ریه، گاهی متاستازهای فوندوس قبل از تومور اولیه کشف میشوند. مواردی وجود دارد که بیمار با شکایت کاهش بینایی به چشم پزشک مراجعه کرده، ضایعات متاستاتیک در فوندوس یافت میشود و سپس با بررسی سیستمیک، سرطان ریه تشخیص داده میشود. تشخیص افتراقی با در نظر گرفتن تومورهای متاستاتیک مشیمیه به عنوان علت کاهش بینایی و نقص میدان بینایی مهم است.
5. درمان استاندارد
Section titled “5. درمان استاندارد”تعیین استراتژی درمان
Section titled “تعیین استراتژی درمان”هنگامی که متاستاز به یووه آشکار میشود، در بسیاری از موارد پیشآگهی زندگی نامطلوب است. همه موارد لزوماً کاندید درمان نیستند و ارزیابی وضعیت عمومی و پیشآگهی زندگی اولین گام است. استراتژی درمان با همکاری تیم مسئول تومور اولیه تعیین میشود.
درمان سیستمیک
Section titled “درمان سیستمیک”در صورت انتظار اثر درمانی (شیمیدرمانی، داروهای هدفمند، ایمونوتراپی) بر تومور اولیه، درمان سیستمیک اولویت دارد. درمان سیستمیک ممکن است باعث کاهش اندازه متاستازهای داخل چشمی شود. اخیراً با معرفی داروهای هدفمند و مهارکنندههای ایست بازرسی ایمنی، مواردی از بقای طولانی مدت مشاهده میشود.
رادیوتراپی موضعی چشم
Section titled “رادیوتراپی موضعی چشم”پرتو درمانی موضعی به چشم، صرف نظر از حساسیت پرتوی تومور اولیه، میتواند مؤثر باشد. دوز استاندارد پرتو 40 تا 50 گری به چشم است. پرتو درمانی اغلب باعث پسرفت جداشدگی سروزی شبکیه و کاهش اندازه متاستازها میشود و بهبود بینایی مورد انتظار است.
اگر امید به زندگی وجود داشته باشد، اصل اساسی انجام پرتودرمانی است و در صورت امکان انجام درمان دارویی سیستمیک، میتوان آن را در اولویت قرار داد.
درمان ضد VEGF
Section titled “درمان ضد VEGF”گزارشهای موردی از کنترل تومور با داروهای ضد VEGF (مانند تزریق داخل زجاجیهای آفلیبرسپت) وجود دارد. در یک مورد متاستاز عصب بینایی از سرطان پستان در یک زن 38 ساله، درمان با تزریق داخل زجاجیهای آفلیبرسپت منجر به کنترل تومور و بهبود دید از 20/50 به 20/25 شد 1). با این حال، شواهد سیستماتیک برای درمان ضد VEGF در متاستازهای چشمی در حال حاضر محدود است و بررسی مورد به مورد ضروری است.
پرتودرمانی (40-50 گری به چشم) اغلب منجر به پسرفت جداشدگی سروزی شبکیه و کوچک شدن متاستاز میشود و بهبود بینایی قابل انتظار است. درمان با شیمیدرمانی سیستمیک یا داروهای هدفمند مولکولی نیز کوچک شدن متاستاز چشمی را گزارش کرده است. با این حال، اثر درمانی بسته به فرد و وضعیت عمومی و پیشرفت بیماری متفاوت است.
6. پاتوفیزیولوژی و مکانیسم دقیق بروز
Section titled “6. پاتوفیزیولوژی و مکانیسم دقیق بروز”متاستاز هماتوژن و گیر افتادن در مشیمیه
Section titled “متاستاز هماتوژن و گیر افتادن در مشیمیه”سلولهای توموری از تومور اولیه از طریق جریان خون در سراسر بدن پخش میشوند. در داخل چشم، مشیمیه بافتی با بیشترین جریان خون است و ساختار بستر مویرگی (صفحه مویرگی مشیمیه) محیطی را ایجاد میکند که سلولهای توموری به راحتی در آن گیر میافتند.
مویرگهای صفحه مویرگی مشیمیه قطر زیادی دارند و سلولهای توموری به راحتی در آنجا گیر میافتند. پس از گیر افتادن، سلولهای توموری در امتداد رگها به صورت جانبی تکثیر میشوند و ضایعه شکل صفحهای به خود میگیرد. این ویژگی مورفولوژیکی تومورهای متاستاتیک مشیمیه است.
آسیب RPE و جداشدگی اگزوداتیو شبکیه
Section titled “آسیب RPE و جداشدگی اگزوداتیو شبکیه”با تکثیر سلولهای توموری، سلولهای اپیتلیوم رنگدانهدار (RPE) که در بالا قرار دارند آسیب میبینند. RPE از طریق غشای بروخ با صفحه مویرگی مشیمیه در تماس است و فشار مکانیکی و اختلال متابولیک ناشی از تومور عملکرد RPE را مختل میکند.
اختلال در عملکرد RPE منجر به نشت مایع از مشیمیه به فضای زیر شبکیه و تشکیل جداشدگی اگزوداتیو (سروزی) شبکیه میشود. این جداشدگی شبکیه علت اصلی نقص میدان بینایی، کاهش بینایی و دگرسانی تصویر است. در تومورهای متاستاتیک مشیمیه، جداشدگی سروزی شبکیه به طور مشخصی رخ میدهد که یک ویژگی افتراقی از سایر تومورهای مشیمیه است.
توزیع محلهای متاستاز
Section titled “توزیع محلهای متاستاز”در میان متاستازهای داخل چشمی، متاستاز کوروئید شایعترین است و تمایل به بروز در قطب خلفی دارد. متاستاز به عنبیه و جسم مژگانی نادر است. ضایعات متاستاتیک ممکن است به صورت منفرد یا چندگانه در یک چشم دیده شوند. در حدود یکچهارم موارد، متاستاز به صورت دوطرفه رخ میدهد.
7. تحقیقات جدید و چشمانداز آینده (گزارشهای در مرحله تحقیق)
Section titled “7. تحقیقات جدید و چشمانداز آینده (گزارشهای در مرحله تحقیق)”پیشرفت در تشخیص تصویربرداری با SS-OCTA
Section titled “پیشرفت در تشخیص تصویربرداری با SS-OCTA”آنژیوگرافی توموگرافی همدوسی نوری با منبع جاروب (SS-OCTA) بینش جدیدی در ارزیابی تصویربرداری تشخیصی تومورهای متاستاتیک کوروئید ارائه میدهد. گزارش شده است که میتواند ساختارهای عروقی غیرطبیعی به شکل حلقه سنجاقسر (hairpin loop) را در داخل تومور نشان دهد و برای ارزیابی غیرتهاجمی ساختار عروقی تومور مفید است1). این روش میتواند آنژیوگرافی فلورسئین معمولی را تکمیل کرده و به درک دقیقتر عروق داخل تومور کمک کند.
اثر داروهای هدفمند مولکولی و ایمونوتراپی بر متاستازهای چشمی
Section titled “اثر داروهای هدفمند مولکولی و ایمونوتراپی بر متاستازهای چشمی”با گسترش استفاده از مهارکنندههای EGFR، مهارکنندههای ALK و مهارکنندههای PD-1/PD-L1 برای سرطان ریه، کنترل متاستازهای چشمی همراه با پاسخ به درمان سیستمیک گزارش شده است. در سرطان پستان، توسعه درمان ضد HER2 ممکن است به افزایش موارد بقای طولانیمدت کمک کرده باشد.
درمان ضد VEGF موضعی چشمی (مانند آفلیبرسپت) برای تومورهای متاستاتیک کوروئید در سطح گزارش موردی شواهدی دارد1)، اما در حال حاضر شواهد حاصل از کارآزماییهای تصادفیسازی شده سیستماتیک وجود ندارد. تصمیمگیری برای استفاده باید با در نظر گرفتن وضعیت عمومی بیمار و ماهیت تومور در هر مورد انجام شود.
شخصیسازی تشخیص تصویربرداری و پایش درمان
Section titled “شخصیسازی تشخیص تصویربرداری و پایش درمان”پیشرفت در OCT و سونوگرافی، پایش اثر درمان را دقیقتر کرده است. با پیگیری کمی پسرفت جداشدگی سروزی شبکیه و مسطح شدن تومور، میتوان اثر پرتودرمانی و درمان سیستمیک را با دقت بیشتری ارزیابی کرد.
8. منابع
Section titled “8. منابع”- Zhou N, Liang L, Wei W. Swept-source OCT angiography of presumed optic nerve metastasis from breast carcinoma. Ophthalmology. 2023;130(9):e52.
- Cennamo G, Montorio D, Carosielli M, Romano MR, Cennamo G. Multimodal Imaging in Choroidal Metastasis. Ophthalmic Res. 2021;64(3):411-416. PMID: 33142285.
- Singh A, Malik D, Singh S, Vyas VJ. Choroidal metastasis in pancreatic adenocarcinoma. J Cancer Res Ther. 2022;18(1):263-265. PMID: 35381796.
