病毒阳性梅克尔细胞癌
梅克尔细胞多瘤病毒相关:约占所有病例的80%。病毒癌蛋白使RB1和p53失活。具有高免疫原性,是T细胞靶向治疗的基础1)。
细胞起源:有多种学说,包括真皮成纤维细胞、前/前B淋巴细胞和表皮祖细胞1)。

梅克尔细胞癌是一种罕见的神经内分泌肿瘤,起源于表皮基底层的梅克尔细胞。梅克尔细胞是弗里德里希·梅克尔于1875年发现的感觉细胞,参与轻触觉以及形状和质地的辨别。
年发病率为每10万人0.23例。约43-50%的病例发生在头颈部,其中5-10%发生在眼睑1)。从2000年到2013年,梅克尔细胞癌病例数增加了95%,远高于所有实体肿瘤(15%)和黑色素瘤(56%)的增长率1)。这归因于人口老龄化、免疫抑制患者增加以及诊断技术的提高。
在眼睑上,它特征性地发生在睫毛线处,呈红色,皮肤紧张有光泽。由于生长迅速且易通过淋巴转移,需要及时诊断和治疗。
年发病率为每10万人0.23例,在皮肤恶性肿瘤中属于罕见。但近年来快速增长,2000年至2013年病例数增加了95%1)。
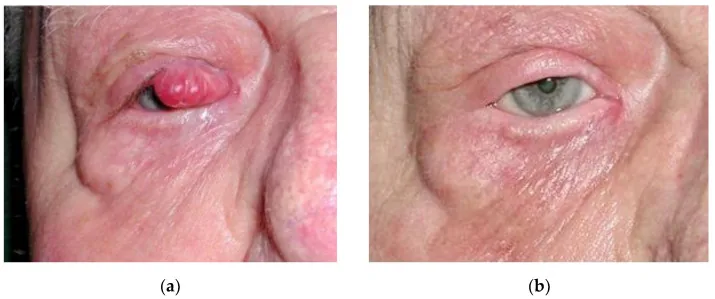
Merkel细胞癌通常无痛,早期自觉症状不明显。常因快速增大的皮肤结节而被发现。
Merkel细胞癌多表现为紫红色、无痛性单发结节。诊断辅助可采用AEIOU标准。
| 标准 | 内容 |
|---|---|
| Asymptomatic(无症状) | 无症状(无压痛) |
| Expanding rapidly(快速扩大) | 快速扩大 |
| Immunosuppression(免疫抑制) | 免疫抑制状态 |
| Older than 50(年龄>50岁) | 50岁以上 |
| UV暴露部位 | 紫外线暴露部位 |
89%的梅克尔细胞癌患者符合3项或以上标准,52%符合4项或以上。
眼周最常发生于上眼睑睫毛线附近。形成红色、圆顶状结节,伴有扩张的肿瘤血管。部分或完全睫毛脱落和表面毛细血管扩张是其特点。
诊断时,多达37%有淋巴结转移,6-12%有远处转移。触诊耳前、下颌下和颈部淋巴结至关重要。
病毒阳性梅克尔细胞癌
梅克尔细胞多瘤病毒相关:约占所有病例的80%。病毒癌蛋白使RB1和p53失活。具有高免疫原性,是T细胞靶向治疗的基础1)。
细胞起源:有多种学说,包括真皮成纤维细胞、前/前B淋巴细胞和表皮祖细胞1)。
病毒阴性梅克尔细胞癌
紫外线突变相关:高突变负荷。表达紫外线诱导的DNA新抗原,免疫原性高1)。
细胞起源:起源于携带大量紫外线突变的角化细胞/表皮祖细胞。有与鳞状细胞癌形成碰撞肿瘤的报道1)。
梅克尔细胞多瘤病毒是一种几乎普遍存在的病毒,也存在于正常皮肤中,但发展为梅克尔细胞癌的情况极为罕见,一生中大约每3000人中有1人1)。病毒基因组整合到宿主中和大T抗原突变这两个事件必须发生在同一细胞中。
肿瘤细胞胞质稀少,核大圆形,染色质细分散,核分裂象多见。在表皮下形成大的巢状结构。乍看类似淋巴瘤,但通过免疫染色鉴别。
| 标志物 | 梅克尔细胞癌 | 小细胞肺癌 |
|---|---|---|
| 细胞角蛋白20(CK20,点状) | 阳性 | 阴性 |
| 神经元特异性烯醇化酶(NSE) | 阳性 | 阳性 |
| S-100 | 阴性 | 阴性 |
| TTF-1 | 阴性至阳性 | 阳性 |
细胞角蛋白20的点状(核周点状模式)阳性是默克尔细胞癌最具特征性的发现,并且与泛细胞角蛋白共表达2)。据报道,细胞角蛋白20在默克尔细胞癌中100%阳性。电子显微镜下可见细胞质内具有电子致密核心的神经内分泌颗粒。
即使临床无淋巴结转移的患者,前哨淋巴结活检也可在三分之一病例中发现微转移1)。前哨淋巴结活检阳性患者的复发风险约为阴性患者的3倍(3年复发率:60% vs 20%),这对制定监测计划至关重要1)。
FDG PET/CT基线影像学检查可使约六分之一(16.8%)的患者分期上调1)。与黑色素瘤(<1%)相比,隐匿性转移的发生率显著更高。
免疫组织化学染色是关键。细胞角蛋白20核周点状阳性是默克尔细胞癌的特异性表现,而小细胞肺癌细胞角蛋白20阴性、TTF-1阳性2)。
治疗的基础是手术切除和病理淋巴结评估。身体其他部位推荐1-2cm切缘,但眼周可接受约5mm的保守切缘2)。采用莫氏显微手术或冰冻切片确认切缘阴性。
对于眼睑皮肤和睑板有粘连浸润的病例,需参照皮脂腺癌进行眼睑全层切除和重建。确认切缘阴性后,有时会在切除面追加2-3次冷冻凝固(冻融)。无法耐受根治性切除的患者可选择放射治疗。
术后辅助放射治疗
适应证:NCCN指南推荐所有分期在手术切除后4-6周内进行辅助放疗,可显著降低5年局部复发风险。
剂量:通常50-66Gy2)。眼周需注意对眼部结构的影响。
根治性放射治疗
适应证:不适合手术患者的一线治疗。默克尔细胞癌对放射线高度敏感,有时可单独使用放疗。
单次照射:单次8 Gy照射的缓解率超过94%。适用于老年或体弱患者的替代选择1)。
传统的铂类药物联合依托泊苷化疗初始缓解率高,但缓解持续时间短(多数在90天内进展),且未显示生存改善1)。
免疫检查点抑制剂已成为晚期梅克尔细胞癌的标准全身治疗:
作为一线治疗,缓解率为55-62%,显著高于化疗1)。与化疗不同,缓解通常是持久的(持续数年)。无论病毒状态如何,均可预期有效。
梅克尔细胞癌的发生有两条主要通路。
在病毒阳性的梅克尔细胞癌中,梅克尔细胞多瘤病毒的癌蛋白(截短的大T抗原和小T抗原)使RB1和p53失活,并激活Myc信号通路1)。在病毒阴性的梅克尔细胞癌中,紫外线诱导的突变直接导致这些通路失调。两种类型中,“PARCB”因子(p53、Akt1、RB1、c-Myc和Bcl2的异常)驱动神经内分泌分化1)。
梅克尔细胞癌倾向于不连续扩散,即使病理学切缘阴性也可能发生局部复发1)。增加复发风险的六个因素包括:1)慢性T细胞免疫抑制,2)肿瘤直径>1厘米,3)淋巴血管侵犯,4)前哨淋巴结活检阳性,5)切缘阳性,6)原发部位在头颈部1)。
检测针对梅克尔细胞多瘤病毒癌蛋白的循环抗体可作为预后指标。血清阴性患者的复发风险比血清阳性患者高约42%1)。在血清阳性患者中,抗体滴度的变化可用于早期发现复发,该方法已被NCCN指南采纳为监测工具1)。
据报道,术前(新辅助)免疫检查点抑制剂可使约50%的局部晚期梅克尔细胞癌患者实现快速肿瘤缩小1)。需要根据具体病例进行评估。
约半数晚期梅克尔细胞癌患者对抗PD-1/PD-L1治疗无法获得持久疗效1)。应对原发性或获得性耐药是最大的未满足需求,许多临床试验正在进行中。
循环肿瘤DNA(ctDNA)分析正在被开发为一种有前景的新工具,用于早期检测病毒阴性梅克尔细胞癌患者的复发1)。基于分期的复发风险计算器(merkelcell.org/recur)也有助于个体化监测。