متفرقة (الأكثر شيوعًا)
نمط الوراثة: غير وراثي (متفرق)
توزع الآفات: أحادي العين، شبكية محيطية
المسار السريري: عادة غير تقدمي، بدون أعراض
المضاعفات الجهازية: لا يوجد

الورم الوعائي الكهفي الشبكي (retinal cavernous hemangioma) هو تشوه وعائي شبكي يتكون من تجمع أوردة متوسعة منخفضة التدفق. عادة ما يكون غير وراثي، أحادي العين، غير تقدمي، ويحدث بشكل منفرد في الشبكية المحيطية. وقد تم الإبلاغ عن حالات تشمل رأس العصب البصري أو البقعة، وحالات وراثية سائدة تترافق مع تشوهات جلدية وعصبية وكبدية.
هذا المرض ليس ورمًا بالمعنى الدقيق، بل يُصنف ضمن التشوهات الوعائية. وهو عبارة عن كتلة وعائية مكونة من خلايا بطانية وخلايا عضلية ملساء وخلايا سدوية، وليس تكاثرًا لخلية واحدة. وفقًا لتصنيف الجمعية الدولية لدراسة التشوهات الوعائية (ISSVA)، يُصنف ضمن التشوهات الوريدية منخفضة التدفق (venous malformation)، وهو أيضًا ضمن أمراض دليل إدارة الأورام الوعائية والتشوهات الوعائية.
متفرقة (الأكثر شيوعًا)
نمط الوراثة: غير وراثي (متفرق)
توزع الآفات: أحادي العين، شبكية محيطية
المسار السريري: عادة غير تقدمي، بدون أعراض
المضاعفات الجهازية: لا يوجد
عائلية (وراثة جسمية سائدة)
نمط الوراثة: جسمية سائدة
توزع الآفات: أحادي أو ثنائي العين، متعدد
المسار السريري: قد توجد مضاعفات دماغية وجلدية وكبدية
المضاعفات الجهازية: ورم وعائي كهفي دماغي (CCM)، ورم وعائي جلدي، ورم وعائي كبدي
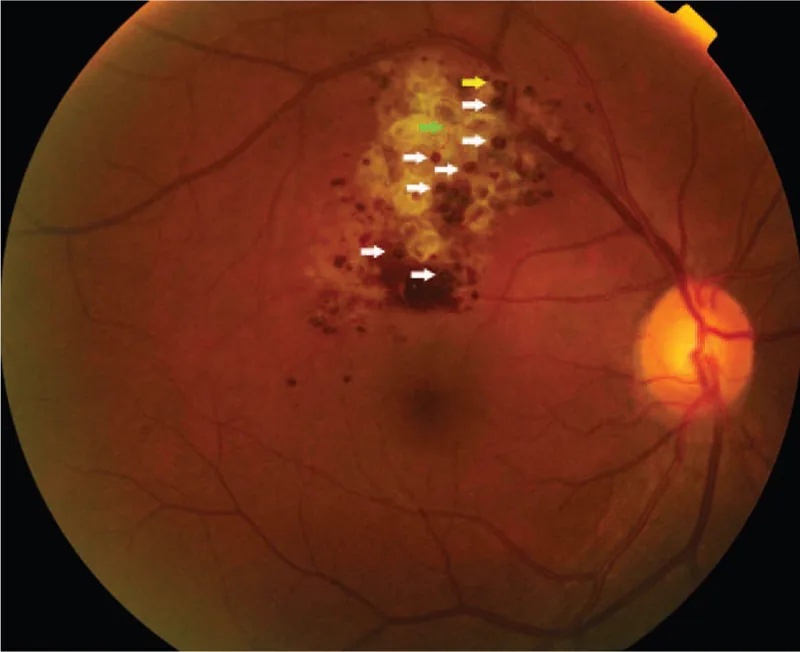
عندما تقتصر الآفة على المنطقة المحيطية، عادة ما تكون بدون أعراض، وغالبًا ما تُكتشف بالصدفة أثناء فحص قاع العين. في الحالات التي تمتد فيها الآفة إلى رأس العصب البصري أو البقعة، قد يحدث ضعف في الرؤية وعيوب في المجال البصري. إذا تشكل غشاء ليفي متكاثر فوق الورم وتسبب في نضح أو نزيف نتيجة الجر، فإن التأثير على الوظيفة البصرية يصبح واضحًا.
تعتبر نتائج فحص قاع العين الأكثر أهمية في تشخيص هذا المرض. فيما يلي النتائج المميزة.
تصوير الأوعية بالفلوريسين هو الفحص الأكثر فائدة للتشخيص التفريقي. فيما يلي النتائج المميزة.
في التصوير المقطعي التوافقي البصري (OCT)، يظهر الورم ككتلة مرتفعة عالية الانعكاس تشبه الكيس تبرز من الطبقات الداخلية للشبكية. في تصوير الأوعية بالتصوير المقطعي التوافقي البصري (OCT-A)، يُظهر الورم تدفقًا دمويًا ضعيفًا داخليًا، مما يؤكد خصائصه كتشوه وعائي منخفض التدفق.
الآلية الدقيقة لتكون الورم الوعائي الكهفي الشبكي لم تُفهم بالكامل بعد. يُعتقد أن السبب هو خلل في تكوين الأوعية الدموية خلال المرحلة الجنينية، أي تغير ورمي عيوبي موضعي في الجهاز الوريدي. لم يتم تحديد أي عوامل خطر بيئية للحالات المتفرقة حتى الآن.
في الحالات العائلية (وراثة جسمية سائدة)، توجد خلفية وراثية مشتركة مع الورم الوعائي الكهفي الدماغي (CCM). تم تحديد ثلاثة جينات مسببة للورم الوعائي الكهفي الدماغي، وتم الإبلاغ عن ارتباطها بتشوهات وعائية جهازية تشمل إصابة العين1).
| الجين | الاسم الآخر | البروتين المشفر | الوظيفة الرئيسية |
|---|---|---|---|
| CCM1 | KRIT1 | Krev interaction trapped 1 | التصاق الخلايا واستتباب البطانة الوعائية |
| CCM2 | MGC4607 | Malcavernin | الارتباط بـ CCM1 ونقل الإشارات |
| CCM3 | PDCD10 | موت الخلية المبرمج 10 | تنظيم موت الخلايا المبرمج ونفاذية الأوعية الدموية |
تشارك هذه الطفرات الجينية في التصاق الخلايا البطانية الوعائية، نقل الإشارات، وتنظيم النفاذية، مما يؤدي إلى توسع الأوردة وضعف جدار الأوعية الدموية2).
بيانات معدل الإصابة الدقيقة محدودة، لكن الورم الوعائي الكهفي الشبكي يعتبر مرضًا نادرًا3). يبلغ معدل انتشار الورم الوعائي الكهفي الدماغي في السكان 0.1-0.5%، لكن نسبة المصابين بآفات العين أقل. لا توجد بيانات واضحة عن العمر أو الجنس الأكثر إصابة. الحالات العائلية نادرة، لكن تم الإبلاغ عن عدة عائلات مصابة بأورام وعائية في الدماغ والجلد والكبد.
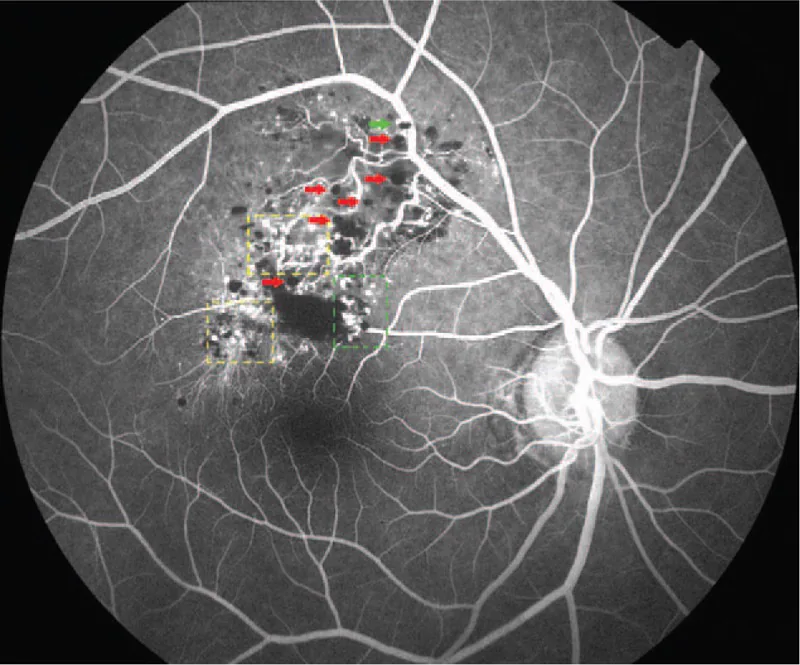
يعتمد التشخيص بشكل أساسي على النتائج المميزة لفحص قاع العين (كتلة متعددة الأكياس حمراء داكنة تشبه عنقود العنب) ونتائج تصوير الأوعية الدموية بالفلوريسين (علامة الغطاء الفلوري، نمط امتلاء وريدي مع تسرب فلوري ضعيف). في الحالات النموذجية، لا حاجة للخزعة ويمكن التشخيص سريريًا.
في الورم الوعائي الكهفي الشبكي العائلي (وراثي سائد)، هناك ارتباط وراثي بالورم الوعائي الكهفي الدماغي (CCM). طفرات جينات CCM1 وCCM2 وCCM3 هي سبب مشترك، مما يؤدي إلى تشوهات وعائية متعددة في الشبكية والدماغ والجلد والكبد. في الحالات العائلية، التصوير بالرنين المغناطيسي المعزز بالتباين للدماغ إلزامي لاستبعاد آفات دماغية غير مكتشفة (قد تسبب الصرع أو النزف الدماغي). في الحالات المتفرقة، لم يثبت ارتباط بآفات دماغية.
أهم تشخيص تفريقي للورم الوعائي الكهفي الشبكي هو الورم الوعائي الشعري الشبكي (مرض فون هيبل لينداو). يعتبر تصوير الأوعية بالفلوريسئين النقطة الأهم للتمييز بين المرضين.
| المرض | المنظر القاعي | تصوير الأوعية بالفلوريسئين | المضاعفات الجهازية | العلاج |
|---|---|---|---|---|
| الورم الوعائي الكهفي الشبكي | كتلة حمراء داكنة متعددة الأكياس (تشبه عنقود العنب) | امتلاء وريدي بطيء، علامة القبة المضيئة، تسرب ضئيل | الورم الوعائي الكهفي الدماغي (عائلي) | عادةً المراقبة |
| ورم وعائي شعيري شبكي (مرض فون هيبل لينداو) | ورم شفاف برتقالي محمر مع أوعية دموية مغذية ومصرفة متوسعة | امتلاء سريع في الطور الشرياني، تسرب فلوريسيني قوي | أورام VHL (مثل سرطان الخلايا الكلوية) | ليزر - جراحة - مضاد VEGF |
| مرض كوتس | انفصال شبكي نضحي، تمدد وعائي شعيري | تسرب قوي من التمددات الوعائية الشعرية | لا يوجد (شائع عند الأطفال) | ليزر - جراحة |
| ورم شبكي وعائي متكاثر | كتلة صفراء بيضاء في المحيط | امتلاء تدريجي، تسرب | لا يوجد | ليزر - علاج ضوئي ديناميكي |
كلا المرضين عبارة عن آفات وعائية في الشبكية، ولكن يمكن تمييزهما بوضوح من خلال تصوير الأوعية بالفلوريسين. في الورم الوعائي الشبكي الشعري (مرض فون هيبل-لينداو)، يتميز الورم البرتقالي المحمر مع أوعية دموية مغذية ومصرفة متوسعة، وفي تصوير الأوعية بالفلوريسين، يمتلئ بسرعة من الطور الشرياني مع تسرب قوي للفلوريسين. في المقابل، يتميز الورم الوعائي الكهفي الشبكي بالامتلاء البطيء في الطور الوريدي وعلامة الغطاء الفلوريسيني، مع تسرب ضئيل للفلوريسين حتى في المراحل المتأخرة. في فحص قاع العين، يظهر الورم الوعائي الكهفي الشبكي ككتلة حمراء داكنة متعددة الأكياس تشبه عنقود العنب، وعادة ما يكون التمييز ممكنًا.
الورم الوعائي الكهفي الشبكي غير تقدمي، وعادة لا يحتاج إلى علاج. قد يتشكل غشاء ليفي تكاثري فوق الآفة، مما قد يسبب انصبابًا أو نزيفًا نتيجة الجر. في الحالات غير المصحوبة بأعراض أو مضاعفات، يتم إجراء متابعة دورية بفحص قاع العين.
يتم النظر في العلاج في حالة حدوث المضاعفات التالية.
جراحة الزجاجية: في حالة حدوث انفصال الشبكية الجري أو نزيف زجاجي ناتج عن الغشاء الليفي التكاثري، يتم النظر في جراحة الزجاجية. نظرًا لأنها تشوه وعائي منخفض التدفق، فإن خطر النزيف أثناء الجراحة وبعدها يعادل خطر جراحة الشبكية العامة. معظم الأدبيات هي تقارير حالات، والأدلة واسعة النطاق محدودة4).
التخثير الضوئي بالليزر: نظرًا لأنه تشوه وعائي منخفض التدفق، فإن الاستجابة للتخثير الضوئي ضعيفة. لا يُوصى به حاليًا بشكل فعال.
في الحالات العائلية، لا تقتصر الإدارة على علاج آفات العين فحسب، بل تشمل أيضًا الإدارة العصبية للورم الكهفي الدماغي. بالنسبة لآفات الدماغ، إذا كانت بدون أعراض، فإن المتابعة هي الأساس، ولكن في حالة ظهور نوبات صرع أو أعراض عصبية، يتم النظر في العلاج الدوائي أو التدخل الجراحي5).
عادة لا يحتاج إلى علاج. إنه تشوه وعائي غير تقدمي، وفي الحالات بدون أعراض، تكون المتابعة الدورية بفحص قاع العين هي السياسة الأساسية. فقط عند حدوث مضاعفات جر الشريط الليفي (انفصال الشبكية الجري أو نزف الجسم الزجاجي) يصبح استئصال الزجاجية مناسبًا. التخثير الضوئي بالليزر غير فعال بسبب انخفاض التدفق، ولا يتم إجراؤه بشكل عام. في الحالات العائلية، بالإضافة إلى متابعة العيون، يلزم الإدارة الجهازية للأورام الكهفية الدماغية.
الورم الكهفي الشبكي ليس ورمًا بل تشوه وعائي. إنه كتلة وعائية مكونة من خلايا بطانية وعائية وخلايا عضلية ملساء وخلايا خلالية، وليس تكاثرًا لخلية واحدة (أي تكاثر ورمي)، وهذه هي السمة الأساسية. في تصنيف ISSVA (الجمعية الدولية لتشوهات الأوعية) لعام 2018، يُصنف ضمن التشوهات الوريدية منخفضة التدفق (venous malformation)، ويتم تمييزه عن التشوه الشرياني الوريدي (عالي التدفق)6).
في الحالات العائلية (وراثة جسمية سائدة)، تلعب الطفرات المفقودة للوظيفة في جينات CCM دورًا مركزيًا. ينظم CCM1 (KRIT1) مسار الإنتغرين المسؤول عن الالتصاق بين الخلايا، ويعمل CCM2 (malcavernin) كبروتين سقالة لـ CCM1. يشارك CCM3 (PDCD10) في تنظيم موت الخلايا المبرمج ونفاذية الأوعية2). تسبب هذه الطفرات انهيار الالتصاق بين الخلايا البطانية الوعائية → التحول البطاني اللحمي المتوسط (endothelial-to-mesenchymal transition) → توسع الأوعية وزيادة النفاذية.
في الحالات المتفرقة (غير الوراثية)، يُشتبه في وجود خلل موضعي في تكوين الأوعية بسبب طفرة جسدية (somatic mutation). يُعتقد أن خللًا أثناء عملية تكوين الأوعية الشبكية في المرحلة الجنينية يؤدي إلى توسع وريدي متعدد الكيسات يشبه عنقود العنب، لكن الآلية التفصيلية لا تزال غير معروفة إلى حد كبير.
كونه تشوهًا وريديًا وعائيًا منخفض التدفق يحدد الخصائص السريرية لهذا المرض. نظرًا لانخفاض تدفق الدم، تنشأ الخصائص التالية:
قد يتكون غطاء دبقي (gliotic cap) أو غشاء ليفي تكاثري على سطح التشوه الوعائي (جهة الجسم الزجاجي). يمكن أن يؤدي انكماش هذا الغشاء إلى انفصال الشبكية الجري أو نزف الجسم الزجاجي. الغشاء الليفي التكاثري ليس ورميًا، بل هو تكاثر تفاعلي ثانوي.
يتقدم فهم الآليات الجزيئية للطفرات الجينية لـ CCM. أظهرت التجارب الحيوانية أن مثبطات إشارات Rho/ROCK ومثبطات مسار PI3K/Akt/mTOR نتائج واعدة في نماذج الورم الكهفي الدماغي 7). يتطلب تطبيقها على آفات العين مزيدًا من البحث.
أصبحت اختبارات اللوحات الجينية المتعددة باستخدام التسلسل من الجيل التالي (NGS) شائعة، وتُستخدم في التشخيص النهائي للحالات العائلية، وتشخيص الحاملين، والاستشارة الوراثية للعائلات. كما يتراكم تفسير المتغيرات المرضية للطفرات الجينية لـ CCM 1).
فيما يتعلق بإدارة المضاعفات الجرية عن طريق جراحة الجسم الزجاجي، تتراكم الأدبيات على مستوى تقارير الحالات وسلاسل الحالات 4,8). لا توجد تجارب عشوائية محكومة واسعة النطاق، وهناك حاجة لدراسات مستقبلية.
Fischer A, Zalvide J, Faurobert E, et al. Cerebral cavernous malformations: from CCM genes to endothelial cell homeostasis. Trends Mol Med. 2013;19(5):302-308.
Couteulx SL, Jung HH, Labauge P, et al. Truncating mutations in CCM1, encoding KRIT1, cause hereditary cavernous angiomas. Nat Genet. 1999;23(2):189-193.
Gass JDM. Cavernous hemangioma of the retina. A neuro-oculocutaneous syndrome. Am J Ophthalmol. 1971;71(4):799-814.
Messmer EP, Font RL, Laqua H, et al. Cavernous hemangioma of the retina. Immunohistochemical and ultrastructural observations. Arch Ophthalmol. 1984;102(3):413-418.
Haller JA Jr, Dortz J, Goldberg MF. Familial retinal cavernous hemangiomas. Arch Ophthalmol. 1979;97(5):879-883.
ISSVA Classification of Vascular Anomalies. International Society for the Study of Vascular Anomalies. 2018 update. Available at: https://www.issva.org.
Lewis RA, Cohen BH, Wise GN. Cavernous haemangioma of the retina and optic disc. A report of three cases and a review of the literature. Br J Ophthalmol. 1975;59(8):422-434.
Shields JA, Shields CL, Timmers E, et al. Spectrum of vitreoretinal surgery. Retina. 1992;12(1):1-11.