بلوک مردمک
شکل عنبیه: برآمدگی قدامی عنبیه محیطی (iris bombé)
عمق اتاق قدامی: بهویژه در قسمت محیطی کم عمق است
PI: مسدود یا انجام نشده
داروهای میوتیک: مؤثر

گلوکوم بدخیم (malignant glaucoma) وضعیتی از افزایش فشار داخل چشم همراه با اتاق قدامی بسیار کم عمق است که به طور معمول پس از جراحی فیلتراسیون در چشمهای مبتلا به گلوکوم زاویه بسته رخ میدهد. تصور میشود که ناشی از چرخش قدامی جسم مژگانی و جریان غیرطبیعی زلالیه به داخل حفره زجاجیه باشد که منجر به جابجایی قدامی زجاجیه و بسته شدن زاویه میشود. این بیماری همچنین به عنوان سندرم انحراف زلالیه (aqueous misdirection syndrome)، گلوکوم بلوک جسم مژگانی (ciliary block glaucoma) و گلوکوم بلوک مستقیم عدسی (direct lens block glaucoma) شناخته میشود و نامهای متعددی دارد. کد ICD-10 آن H40.8 است.
این یک مفهوم بیماری تاریخی است که اولین بار توسط فون گریف در سال ۱۸۶۹ به عنوان اتاق قدامی کم عمق مقاوم به درمان پس از جراحی فیلتراسیون گزارش شد 3). پس از آن، مفهوم پاتوفیزیولوژیکی که زلالیه به جای مسیر قدامی طبیعی به سمت عقب (به سمت حفره زجاجیه) منحرف میشود، تثبیت شد و نام aqueous misdirection (انحراف زلالیه) به طور گسترده مورد استفاده قرار گرفت. اگرچه بیشتر در چشمهای مبتلا به گلوکوم زاویه بسته پس از جراحی فیلتراسیون دیده میشود، اما از نظر بالینی مهم است که میتواند پس از هر نوع جراحی داخل چشمی از جمله جراحی آب مروارید رخ دهد.
در راهنمای بالینی گلوکوم (ویرایش پنجم)، مکانیسم افزایش فشار داخل چشمی در گلوکوم زاویه بسته ثانویه به چهار دسته زیر تقسیم شده است 6).
گلوکوم بدخیم در دسته سوم یعنی «جابجایی قدامی بافتهای پشت عدسی» طبقهبندی میشود. در ویرایش پنجم EGS، معادل «مکانیسم فشار از پشت» است 5).
بروز پس از جراحی فیلتراسیون ۰.۶ تا ۴٪ گزارش شده است 5). در زنان شایعتر است و معمولاً یک طرفه رخ میدهد. بیشتر پس از جراحی فیلتراسیون در چشمهای مبتلا به گلوکوم زاویه بسته اولیه دیده میشود، اما میتواند پس از هر نوع جراحی داخل چشمی از جمله جراحی آب مروارید رخ دهد 5). عوامل خطر شامل محور کوتاه چشم (کمتر از ۲۱ میلیمتر)، دوربینی بالا (بیش از ۶+ دیوپتر) و سابقه گلوکوم زاویه بسته اولیه است 5). موارد نادری از بروز خودبهخودی بدون سابقه جراحی نیز گزارش شده است. در ترابکولکتومی برای گلوکوم زاویه بسته، احتمال ایجاد گلوکوم بدخیم همراه با اتاق قدامی کم عمق و جداشدگی مشیمیه پس از جراحی نسبتاً بالا شناخته شده است 6).
در بلوک مردمک، به دلیل اختلال در عبور زلالیه از لبه مردمک، عنبیه محیطی به سمت جلو برآمده میشود (iris bombé). در مقابل، در انحراف زلالیه، زلالیه در پشت عدسی در حفره زجاجیه تجمع مییابد و در نتیجه اتاق قدامی به طور یکنواخت کم عمق میشود. برای بلوک مردمک، داروهای میوتیک مؤثر هستند، اما در انحراف زلالیه، داروهای میوتیک منع مصرف دارند.
در موارد شروع حاد، علائم زیر بروز میکند.
علائم متغیر (fluctuant) هستند و ممکن است هفتهها تا سالها پس از جراحی آب مروارید ظاهر شوند3). در مراحل اولیه، فشار داخل چشم ممکن است در محدوده طبیعی باقی بماند که تشخیص را به تأخیر میاندازد5). در صورت افزایش ناگهانی فشار داخل چشم، تصویر بالینی مشابه حمله حاد گلوکوم ایجاد شده و کاهش بینایی به سرعت پیشرفت میکند.
تشخیص بر اساس ترکیبی از یافتههای زیر انجام میشود. علاوه بر افزایش فشار داخل چشم، الگوی تغییر عمق اتاق قدامی در تشخیص افتراقی مهمترین عامل است.
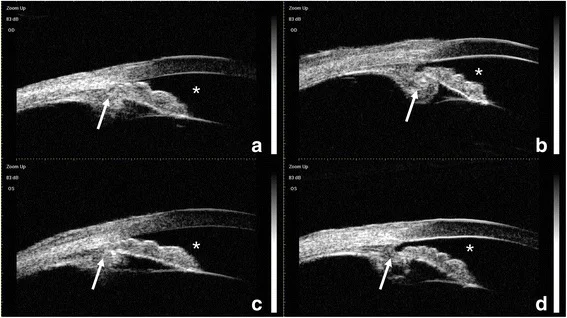
در توموگرافی انسجام نوری بخش قدامی (AS-OCT)، یافتههایی شبیه plateau iris (قسمت مرکزی عنبیه صاف اما زاویه بسته) به دلیل جابجایی قدامی کمپلکس CTR-IOL گزارش شده است2). در میکروسکوپ اولتراسوند بیومیکروسکوپی (UBM) میتوان جابجایی قدامی کمپلکس کپسول عدسی-IOL و چرخش قدامی یا ناهنجاری موقعیت جسم مژگانی را مستقیماً تأیید کرد4). UBM با وضوح بالا (۲۰-۶۰ میکرومتر) ساختارهای بخش قدامی مانند عنبیه و جسم مژگانی را با جزئیات نشان میدهد، بنابراین در موارد مشکوک به گلوکوم بدخیم باید به طور فعال انجام شود.
UBM و OCT بخش قدامی برای روشن شدن پاتوفیزیولوژی مفید هستند و به ویژه با بررسی سابقه جراحی، باید ناهنجاری موقعیت جسم مژگانی ارزیابی شود.
شایعترین عامل محرک، جراحی داخل چشمی است5).
چشمهای کوچکتر خطر بیشتری دارند5).
در صورت بروز در یک چشم، خطر بروز در چشم مقابل نیز افزایش مییابد 3). از آنجایی که خطر بدون توجه به سابقه گلوکوم افزایش مییابد، پیگیری منظم چشم مقابل اهمیت دارد.
عوامل خطر اصلی در زیر خلاصه شده است.
| عامل خطر | مثال |
|---|---|
| شکل چشم | محور کوتاه (<21 میلیمتر)، دوربینی شدید (>+6 D)، اتاق قدامی کم عمق |
| جراحی | جراحی فیلتراسیون، جراحی آب مروارید، قرار دادن CTR |
| دارو | توپیرامات، SSRI |
توپیرامات نفوذپذیری عروق مشیمیه-جسم مژگانی را افزایش داده و باعث تورم جسم مژگانی و چرخش قدامی آن میشود 1). در چشمهای پرخطر مانند میکروفتالمی، میتواند محرک جریان اشتباه زلالیه باشد. SSRIها نیز از طریق اثر میدریاتیک ممکن است در چشمهای با زاویه باریک باعث بسته شدن زاویه شوند.
گلوکوم بدخیم یک تشخیص افتراقی است و تنها پس از رد سیستماتیک بلوک مردمک، خونریزی یا جداشدگی مشیمیه، خونریزی فوق مشیمیه و سایر مکانیسمهای بسته شدن زاویه، تشخیص داده میشود 4). این بیماری با یک مقدار آزمایش یا یافته تصویربرداری خاص تأیید نمیشود، بلکه با ترکیبی از سیر بالینی و چندین یافته آزمایشگاهی به طور جامع ارزیابی میشود.
در اوایل پس از جراحی گلوکوم با زاویه بسته، در صورت بروز اتاق قدامی بسیار کم عمق و فشار بالای چشم، به این بیماری مشکوک شوید. جداشدگی مشیمیه هموراژیک یافتههای مشابهی در لامپ اسلیت نشان میدهد و هر دو میتوانند باعث فشار بالا شوند، اما با یافتههای فوندوس قابل افتراق هستند. در موارد ایدیوپاتیک، به دلیل عدم سابقه جراحی، تشخیص دشوارتر است و تأیید موقعیت غیرطبیعی جسم مژگانی با UBM کلید تشخیص است.
نقاط افتراق بین بلوک مردمک و جریان اشتباه زلالیه در زیر خلاصه شده است.
بلوک مردمک
شکل عنبیه: برآمدگی قدامی عنبیه محیطی (iris bombé)
عمق اتاق قدامی: بهویژه در قسمت محیطی کم عمق است
PI: مسدود یا انجام نشده
داروهای میوتیک: مؤثر
انحراف زجاجیه-اتاق قدامی
شکل عنبیه: عنبیه به طور کلی به سمت جلو جابجا شده است
عمق اتاق قدامی: به طور یکنواخت کم عمق تا از بین رفته 5)
PI: باز است
داروهای میوتیک: منع مصرف (تشدید)
سایر تشخیصهای افتراقی به شرح زیر است. همه میتوانند باعث اتاق قدامی کم عمق و فشار بالای چشم شوند، اما مکانیسم بروز متفاوت است، بنابراین برنامه درمانی نیز متفاوت است.
رویکرد گام به گام شامل درمان دارویی → لیزر → جراحی اساس درمان است. ابتدا با درمان دارویی سعی در رفع بلوک جسم مژگانی میشود؛ در صورت عدم پاسخ، لیزر درمانی و در صورت عدم موفقیت، جراحی انجام میشود. هدف نهایی درمان ایجاد وضعیتی است که در آن هیچ بلوکی بین اتاق خلفی و قدامی وجود نداشته باشد (unicameral eye: چشم تکحفرهای) و از عود جلوگیری شود.
ترکیب سهگانه داروهای آنتیکولینرژیک (میدریاتیک و شلکننده جسم مژگانی)، مهارکنندههای تولید زلالیه (قطره و خوراکی) و عوامل اسمزی (وریدی) توصیه میشود5).
| دارو | روش مصرف | مکانیسم اثر |
|---|---|---|
| قطره آتروپین 1% | 1 تا 3 بار در روز | شلکننده جسم مژگانی و میدریاتیک |
| قطره تیمولول 0.5% | 2 بار در روز | مهار تولید زلالیه (بتا بلوکر) |
| قرص دیاموکس 250 میلیگرم | 2 قرص، دو بار در روز بعد از غذا | مهار تولید زلالیه (مهارکننده خوراکی کربنیک آنهیدراز) |
| انفوزیون مانیتول | تجویز داخل وریدی | کاهش حجم زجاجیه |
آتروپین با افزایش کشش رباطهای مژگانی، عدسی را به سمت عقب حرکت میدهد و باعث میشود زلالیهای که به حفره زجاجیه رفته است به سمت جلو بازگردد. سیکلوپنتولات نیز میتواند به عنوان جایگزین آتروپین استفاده شود5).
قطرههای چشمی مهارکننده تولید زلالیه (مسدودکنندههای بتا و مهارکنندههای آنهیدراز کربنیک) همراه با انفوزیون داروهای اسمزی استفاده میشوند6). داروهای اسمزی حجم زجاجیه را کاهش میدهند، اما اثر درمانی آنها موقتی است و بنابراین به عنوان آمادهسازی قبل از جراحی در نظر گرفته میشوند6).
نرخ پاسخ به درمان دارویی حدود ۵۰٪ (در عرض ۵ روز) گزارش شده است، اما میزان عود با دارو به تنهایی بالاست5). حتی اگر با درمان دارویی عمق اتاق قدامی افزایش یابد و فشار چشم نرمال شود، قطع قطره آتروپین اغلب منجر به عود میشود، بنابراین ممکن است نیاز به ادامه قطره آتروپین به عنوان درمان نگهدارنده طولانیمدت باشد. درمان دارویی صرفاً یک اقدام اولیه است و درمان قطعی اغلب نیاز به مداخله لیزری یا جراحی دارد.
در چشمهای شبهفاکیک، کپسولوتومی خلفی با لیزر Nd:YAG انجام میشود و سپس با تغییر فوکوس به پشت کپسول خلفی، ۱۰ تا ۲۰ شلیک با انرژی ۳-۴ میلیژول برای شکستن غشای زجاجیه قدامی اعمال میشود. با ایجاد مسیری برای زلالیه بین حفره زجاجیه و اتاق قدامی، سعی در رفع بلوک میشود. در صورت موفقیت، بهبود عمق اتاق قدامی و کاهش فشار چشم بلافاصله یا روز بعد حاصل میشود.
در چشمهای شبهفاکیک یا آفاکیک، ویتروتومی قدامی یا کپسولوتومی با لیزر YAG یا جراحی انتخاب میشود6) (سطح شواهد 2C).
فتوکواگولاسیون سیکلوبادی با لیزر دیود را میتوان در هر مرحله از درمان در نظر گرفت5). این روش باعث نکروز انعقادی و آتروفی زوائد مژگانی میشود و ممکن است منجر به تخریب سطح مشترک مژگانی-زجاجیه و چرخش خلفی جسم مژگانی شود3). با این حال، شرایط تابش لازم برای تخریب سطح مشترک مژگانی-زجاجیه هنوز مشخص نشده است.
در صورت عدم پاسخ کافی به درمان دارویی و لیزری، یا در موارد عود، جراحی انجام میشود. ویترکتومی همراه با ویتروتومی قدامی برای رفع پاتوفیزیولوژی مهم است6) (سطح شواهد 2C).
ویترکتومی از طریق پارس پلانا (PPV) انجام میشود 5). در برخی موارد، برداشتن لنز نیز همزمان انجام میشود 6) (2C). با برداشتن لنز، یک چشم تکحفرهای (unicameral eye) ایجاد میشود و بلوک بین اتاق خلفی و قدامی به طور کامل برطرف میشود تا از عود جلوگیری شود.
zonulo-hyaloido-vitrectomy (برداشتن عنبیه-رباط زین-غشاء زجاجیه قدامی) مؤثر است 5). از طریق بخش ایریدکتومی محیطی به اتاق قدامی دسترسی پیدا کرده و رباط زین اطراف کپسول لنز و غشاء زجاجیه قدامی برداشته میشود. این روش یک مسیر ارتباطی دائمی بین حفره زجاجیه و اتاق قدامی ایجاد میکند.
در ویترکتومی همراه با باز کردن غشاء زجاجیه قدامی، در برخی موارد برای درمان غشاء زجاجیه قدامی در محیطترین ناحیه، نیاز به ایریدکتومی وجود دارد 6) (2C). اگر غشاء زجاجیه قدامی و رباط زین به اندازه کافی درمان نشوند، بلوک بین حفره زجاجیه و اتاق قدامی باقی میماند و احتمال عود وجود دارد. در چشمهای دارای لنز طبیعی، با برداشتن همزمان لنز، تماس بین زوائد مژگانی و استوای لنز برطرف شده و یک چشم تکحفرهای ایجاد میشود.
گزارش شده است که ترکیب برداشتن CTR، ویترکتومی قدامی و فیکساسیون داخل صلبیه IOL مؤثر بوده است 2).
اشتباه مسیر زلالیه یک زاویه بسته ناشی از مکانیسم فشار از پشت لنز است. داروهای میوتیک با انقباض عضله مژگانی، برجستگی قدامی جسم مژگانی را تشدید کرده و بلوک مژگانی را بدتر میکنند، بنابراین منع مصرف دارند 6). در مقابل، داروهای سیکلوپلژیک-میدریاتیک مانند آتروپین با شل کردن عضله مژگانی، تنش رباط زین را افزایش داده و لنز را به سمت عقب حرکت میدهند که برای رفع بلوک مؤثر است.
درگیری یک چشم به طور معنیداری خطر درگیری چشم مقابل را افزایش میدهد 3). این خطر صرف نظر از سابقه گلوکوم افزایش مییابد، بنابراین ارزیابی منظم فشار داخل چشم و عمق اتاق قدامی در چشم مقابل مهم است.
مکانیسم دقیق بروز گلوکوم بدخیم به طور کامل شناخته نشده است، اما دو فرضیه زیر مطرح شده است 5).
فرضیه اتساع کوروئید
مکانیسم اصلی: افزایش حجم مشیمیه باعث مقاومت در برابر حرکت مایع از عقب به جلو میشود5)
نتیجه: زلالیه در حفره زجاجیه تجمع یافته و دیافراگم عنبیه-عدسی را به سمت جلو میراند
نظریه بلوک جسم مژگانی
مکانیسم اصلی: تماس غیرطبیعی آناتومیک بین زوائد مژگانی و استوای عدسی (یا IOL) و غشای زجاجیه قدامی
نتیجه: یک «چرخه بدخیم» ایجاد میشود که به عنوان یک دریچه یکطرفه عمل کرده و از خروج قدامی زلالیه جلوگیری میکند
پیشرفت پاتولوژی را میتوان با آبشار زیر درک کرد. در چشم طبیعی، زلالیه تولید شده در جسم مژگانی از اتاق خلفی از طریق مردمک به اتاق قدامی جریان یافته و از طریق ترابکول زاویه تخلیه میشود. در گلوکوم بدخیم، این مسیر جریان مختل میشود.
قطره آتروپین عضله مژگانی را شل کرده، تنش زونولهای مژگانی را افزایش داده و عدسی را به سمت عقب حرکت میدهد. این امر میتواند باعث شود زلالیهای که به حفره زجاجیه رفته است به سمت جلو بازگردد.
از سوی دیگر، داروهای میوتیک مانند پیلوکارپین عضله مژگانی را منقبض میکنند. این انقباض زونولهای مژگانی را شل کرده و عدسی را به سمت جلو هل میدهد و همچنین برجستگی قدامی جسم مژگانی را تشدید میکند، بنابراین بلوک مژگانی بدتر میشود 6). بنابراین، داروهای میوتیک در گلوکوم بدخیم منع مصرف دارند.
در چشمهای شبهعدسی، قطر افقی کمپلکس IOL-کپسول از عدسی طبیعی بزرگتر است و احتمال تماس با زوائد مژگانی بیشتر است 4). بخشی از زلالیه تولید شده در زوائد مژگانی به سمت عقب (حفره زجاجیه) ترشح میشود. اگر غشای هیالوئید قدامی intact باشد، خروج مایع به سمت جلو مختل شده، گرادیان فشار ایجاد شده و اتاق قدامی کم عمق میشود.
حتی در چشمهایی که سابقه ویترکتومی دارند، در صورت باقی ماندن غشای هیالوئید قدامی، امکان بروز گزارش شده است 4). در موارد عود با شیفت میوپیک بیش از 3 دیوپتر، ترکیب گونیوسینشیالیز، ایریدکتومی و زونولو-هیالوئیدکتومی باعث بهبود رفرکشن و فشار چشم شد 4). بنابراین، در هنگام ویترکتومی، پاکسازی کامل غشای هیالوئید قدامی تا محیطیترین نواحی برای پیشگیری از عود ضروری است.
توپیرامات نفوذپذیری عروق مشیمیه-جسم مژگانی را افزایش داده و باعث تورم جسم مژگانی و مشیمیه و چرخش قدامی جسم مژگانی میشود 1). در میکروفتالمی، به دلیل ضخامت صلبیه، اختلال در تخلیه وریدهای گردابی اضافه شده و خطر افیوژن یووهآ بیشتر افزایش مییابد 1).
با قرار دادن CTR، کپسول عدسی بزرگ و ضخیم شده و کمپلکس CTR-IOL به طور محیطی با جسم مژگانی و عنبیه خلفی تماس پیدا میکند 2). این امر فضای جسم مژگانی را فشرده کرده و مقاومت در برابر حرکت زلالیه از عقب به جلو را افزایش میدهد. قطر بزرگ کمپلکس CTR-IOL تا حدی جابجایی قدامی را محدود میکند، بنابراین ممکن است با حفظ عمق اتاق قدامی، انسداد زاویه شبیه plateau iris رخ دهد 2). این یافته غیرمعمول با تصویر کلاسیک گلوکوم بدخیم یعنی «اتاق قدامی کم عمق یکنواخت» متفاوت است، بنابراین ارزیابی دقیق مورفولوژی زاویه با AS-OCT کلید تشخیص است.
چیان و همکاران (2021) یک مورد از اشتباه هدایت زلالیه (aqueous misdirection) را گزارش کردند که تنها علامت اولیه آن نزدیکبینی (myopic surprise) پس از جراحی آب مروارید بود 3). فشار داخل چشم تا حدود سه سال پس از جراحی در محدوده طبیعی باقی ماند و تشخیص به تأخیر افتاد. حتی اگر عمق اتاق قدامی در بیومتری طبیعی به نظر برسد، در چشمهای با محور کوتاه ممکن است خطای اندازهگیری رخ دهد، بنابراین در صورت مشاهده نزدیکبینی، باید اشتباه هدایت زلالیه را در تشخیص افتراقی در نظر گرفت.
استفنسون و همکاران (2023) موردی را گزارش کردند که در یک چشم با سابقه ویترکتومی، جراحی آب مروارید و کاشت عنبیه مصنوعی، همراه با تغییر نزدیکبینی (myopic shift) بیش از 3 دیوپتر، اشتباه هدایت زلالیه رخ داد 4). این نشان میدهد که حتی پس از ویترکتومی، اگر غشای زجاجیه قدامی باقی بماند، ممکن است بیماری ایجاد شود. گونیوسینکیالیز (goniosynechialysis) همراه با ایریدکتومی و زونولو-هیالوئیدکتومی (zonulo-hyaloidectomy) باعث بهبود انکسار و فشار داخل چشم شد.
گوتو و همکاران (2024) برای اولین بار با استفاده از AS-OCT، بسته شدن زاویه ثانویه ناشی از جابجایی قدامی کمپلکس CTR-IOL را مشخص کردند 2). آنها یک نمای غیرمعمول شبیه plateau iris را گزارش کردند که در آن عمق اتاق قدامی حفظ شده بود و نشان دادند که AS-OCT برای تشخیص بسته شدن زاویه ثانویه پس از جراحی آب مروارید و کاشت CTR مفید است.
یک رویکرد مرحلهای شامل دارودرمانی → لیزر Nd:YAG → سیکلودیود (cyclodiode) → جراحی پیشنهاد شده است 3). سیکلودیود باعث انعقاد نکروز و آتروفی زوائد مژگانی میشود و ممکن است تخریب سطح مشترک زجاجیه-جسم مژگانی و چرخش خلفی جسم مژگانی را ایجاد کند. با این حال، شرایط تابش لازم برای تخریب سطح مشترک زجاجیه-جسم مژگانی هنوز مشخص نشده است و در صورت عدم پاسخ کافی به دارو و لیزر، جراحی برای ایجاد یک اتاق تک حفرهای (unicameral eye) همچنان گزینه درمانی نهایی است 3).