Blocco pupillare
Morfologia dell’iride : Bombamento anteriore dell’iride periferica (iris bombé)
Profondità della camera anteriore : Particolarmente superficiale in periferia
PI : Ostruito o non eseguito
Miotici : Efficaci

Il glaucoma maligno (malignant glaucoma) è una condizione di ipertensione oculare con camera anteriore molto poco profonda, che si verifica tipicamente dopo chirurgia filtrante per glaucoma ad angolo chiuso. Si ritiene che sia causato da una rotazione anteriore del corpo ciliare e da un flusso anomalo di umore acqueo nella cavità vitreale, con conseguente spostamento anteriore del vitreo e blocco angolare. È anche chiamato sindrome da deviazione dell’umore acqueo (aqueous misdirection syndrome), glaucoma da blocco ciliare (ciliary block glaucoma) o glaucoma da blocco diretto del cristallino (direct lens block glaucoma), con diversi nomi in uso. Il codice ICD-10 è H40.8.
Nel 1869, Von Graefe riportò per la prima volta questo concetto storico di malattia come camera anteriore poco profonda refrattaria dopo chirurgia filtrante 3). Successivamente, è stato stabilito il concetto fisiopatologico che l’umore acqueo viene deviato posteriormente (verso la cavità vitrea) invece che attraverso il normale percorso anteriore, e il termine “aqueous misdirection” (deviazione dell’umore acqueo) è ampiamente utilizzato. Si incontra più comunemente negli occhi con glaucoma ad angolo chiuso dopo chirurgia filtrante, ma è clinicamente importante che possa verificarsi dopo qualsiasi intervento chirurgico intraoculare, inclusa la chirurgia della cataratta.
Nelle linee guida cliniche per il glaucoma (5a edizione), i meccanismi di aumento della pressione intraoculare nel glaucoma secondario ad angolo chiuso sono classificati in quattro categorie 6).
Il glaucoma maligno è classificato nella terza categoria sopra: “spostamento anteriore dei tessuti posteriori al cristallino”. Nella 5a edizione dell’EGS, corrisponde al “meccanismo di spinta posteriore” 5).
L’incidenza dopo chirurgia filtrante è dello 0,6–4% 5). È più comune nelle donne e di solito si presenta unilateralmente. È più frequente dopo chirurgia filtrante per glaucoma primario ad angolo chiuso, ma può verificarsi dopo qualsiasi intervento chirurgico intraoculare, inclusa la chirurgia della cataratta 5). I fattori di rischio includono un asse oculare corto (inferiore a 21 mm), ipermetropia elevata (+6 D o più) e una storia di glaucoma primario ad angolo chiuso 5). Sono stati riportati rari casi idiopatici senza storia chirurgica. È noto che la trabeculectomia per il glaucoma ad angolo chiuso ha un rischio relativamente alto di causare glaucoma maligno con camera anteriore poco profonda e distacco coroidale nel periodo postoperatorio 6).
Nel blocco pupillare, l’ostruzione del flusso dell’umore acqueo al margine pupillare provoca un bombamento anteriore dell’iride periferica (iris bombé). D’altra parte, nella deviazione dell’umore acqueo, l’accumulo di umore acqueo nella cavità vitrea dietro il cristallino rende la camera anteriore uniformemente poco profonda, questa è la differenza. I miotici sono efficaci per il blocco pupillare, ma sono controindicati nella deviazione dell’umore acqueo.
In caso di esordio acuto si manifestano i seguenti sintomi.
I sintomi sono fluttuanti e possono manifestarsi da settimane ad anni dopo l’intervento di cataratta 3). Inizialmente la pressione intraoculare può rimanere entro i limiti normali, ritardando la diagnosi 5). In caso di aumento brusco della pressione intraoculare, il quadro clinico è simile a un attacco acuto di glaucoma, con rapida riduzione della vista.
La diagnosi si basa sulla combinazione dei seguenti segni. Oltre all’aumento della pressione intraoculare, il pattern di variazione della profondità della camera anteriore è il più importante per la diagnosi differenziale.
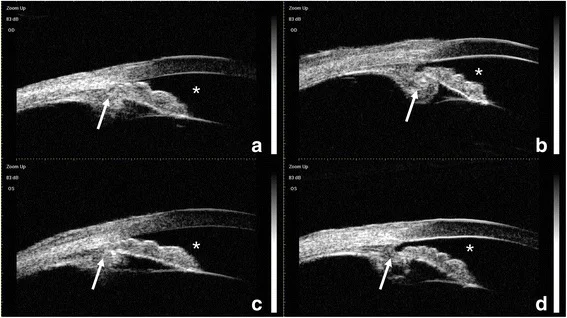
La tomografia a coerenza ottica del segmento anteriore (AS-OCT) può mostrare un aspetto simile a plateau iris (parte centrale dell’iride piatta ma angolo chiuso) associato a una deviazione anteriore del complesso CTR-IOL (anello di tensione capsulare-lente intraoculare) 2). L’ecografia biomicroscopica (UBM) consente di visualizzare direttamente la deviazione anteriore del complesso sacco capsulare-IOL e la rotazione anteriore o la malposizione del corpo ciliare 4). L’UBM ha un’alta risoluzione di 20-60 μm e può visualizzare in dettaglio le strutture del segmento anteriore come iride e corpo ciliare; pertanto, dovrebbe essere eseguita attivamente nei casi sospetti di glaucoma maligno.
L’UBM e l’OCT del segmento anteriore sono utili per chiarire la patogenesi. In particolare, valutare la presenza di malposizione del corpo ciliare, tenendo conto della storia chirurgica.
Il fattore scatenante più comune è la chirurgia intraoculare 5).
Più piccolo è l’occhio, maggiore è il rischio 5).
In caso di insorgenza monolaterale, aumenta anche il rischio di sviluppare la malattia nell’occhio controlaterale 3). Il rischio è aumentato indipendentemente dalla storia di glaucoma, quindi è importante un follow-up regolare dell’occhio controlaterale.
I principali fattori di rischio sono riassunti di seguito.
| Fattore di rischio | Esempi |
|---|---|
| Morfologia oculare | Asse corto (<21 mm), ipermetropia elevata (>+6 D), camera anteriore poco profonda |
| Chirurgia | Chirurgia filtrante, chirurgia della cataratta, posizionamento di CTR |
| Farmaci | Topiramato, SSRI |
Il topiramato aumenta la permeabilità vascolare del corpo ciliare e della coroide, causando gonfiore del corpo ciliare e rotazione anteriore 1). Negli occhi ad alto rischio come la microftalmia, ciò può innescare un glaucoma maligno. Anche gli SSRI possono indurre la chiusura dell’angolo in occhi con angolo stretto attraverso il loro effetto midriatico.
Il glaucoma maligno è una diagnosi di esclusione; viene posta solo dopo aver sistematicamente escluso il blocco pupillare, l’emorragia o distacco coroidale, l’emorragia sopracoroideale e altri meccanismi di chiusura dell’angolo 4). Non è una malattia che può essere confermata da un singolo valore di laboratorio o di imaging; la diagnosi si basa sul decorso clinico e sulla combinazione di più reperti.
Sospettare questa malattia in caso di camera anteriore estremamente bassa e ipertensione oculare nel periodo post-operatorio precoce dopo chirurgia del glaucoma ad angolo chiuso. Il distacco coroidale emorragico mostra reperti simili alla lampada a fessura e può anch’esso causare ipertensione, ma può essere differenziato in base al fundus. Nei casi idiopatici, l’assenza di anamnesi chirurgica rende la diagnosi più difficile; la conferma di una posizione anomala del corpo ciliare mediante UBM è la chiave diagnostica.
I punti di differenziazione tra blocco pupillare e glaucoma maligno sono riassunti di seguito.
Blocco pupillare
Morfologia dell’iride : Bombamento anteriore dell’iride periferica (iris bombé)
Profondità della camera anteriore : Particolarmente superficiale in periferia
PI : Ostruito o non eseguito
Miotici : Efficaci
Blocco ciliare (glaucoma maligno)
Morfologia dell’iride : Iride complessivamente spostata in avanti
Profondità della camera anteriore : Uniformemente superficiale o assente5)
PI : Pervio
Miotici : Controindicati (peggioramento)
Le altre diagnosi differenziali sono le seguenti. Tutte possono causare camera anteriore superficiale e ipertensione oculare, ma i meccanismi patogenetici sono diversi, quindi anche le strategie terapeutiche sono differenti.
L’approccio di base è graduale: terapia farmacologica → trattamento laser → trattamento chirurgico. Si tenta prima di risolvere il blocco ciliare con farmaci; se non risponde, si passa al laser, e se ancora inefficace, alla chirurgia. L’obiettivo finale è creare un occhio unicamerale (unicameral eye) in cui non possa verificarsi un blocco tra la camera posteriore e anteriore, prevenendo le recidive.
Si raccomanda la triplice associazione di un parasimpaticolitico (midriatico e rilassante ciliare), un inibitore della produzione di umore acqueo (collirio e orale) e un agente iperosmolare (infusione)5).
| Farmaco | Posologia | Meccanismo d’azione |
|---|---|---|
| Collirio di atropina 1% | 1-3 volte al giorno | Rilassamento ciliare e midriasi |
| Collirio di timololo 0,5% | 2 volte al giorno | Inibizione della produzione di umore acqueo (beta-bloccante) |
| Compresse di Diamox 250 mg | 2 compresse in 2 dosi dopo i pasti | Inibizione della produzione di umore acqueo (IAC orale) |
| Infusione di mannitolo | Somministrazione endovenosa | Riduzione del volume vitreale |
L’atropina aumenta la tensione della zonula ciliare, sposta il cristallino posteriormente e consente all’umore acqueo che è rifluito nella cavità vitrea di tornare anteriormente. Il ciclopentolato può essere utilizzato come alternativa all’atropina5).
Si associano colliri che inibiscono la produzione di umore acqueo (beta-bloccanti, inibitori dell’anidrasi carbonica) e un’infusione di agente iperosmolare6). L’agente iperosmolare riduce il volume vitreale, ma il suo effetto terapeutico è temporaneo, pertanto è considerato un trattamento preoperatorio6).
Il tasso di risposta alla terapia farmacologica è di circa il 50% (entro 5 giorni), ma il tasso di recidiva con i soli farmaci è elevato5). Anche se la camera anteriore si approfondisce e la pressione intraoculare si normalizza con la terapia farmacologica, la recidiva è frequente alla sospensione dei colliri di atropina, pertanto può essere necessario continuare l’atropina come terapia di mantenimento a lungo termine. La terapia farmacologica è solo un trattamento iniziale; il trattamento curativo spesso richiede un intervento laser o chirurgico.
Negli occhi pseudofachici si esegue una capsulotomia posteriore con laser Nd:YAG, quindi si sposta il fuoco posteriormente alla capsula posteriore e si applicano 10-20 colpi con energia di 3-4 mJ per frammentare la membrana ialoidea anteriore. Creando un passaggio per l’umore acqueo tra la cavità vitrea e la camera anteriore, si tenta di risolvere il blocco. In caso di successo, si osserva un miglioramento della profondità della camera anteriore e una riduzione della pressione intraoculare immediatamente o il giorno successivo.
Negli occhi pseudofachici o afachici si sceglie il laser YAG o una ialoidotomia anteriore chirurgica o una capsulotomia del cristallino6) (livello di evidenza 2C).
La ciclofotocoagulazione con laser a diodi può essere presa in considerazione in qualsiasi fase del trattamento5). Provoca necrosi da coagulazione e atrofia dei processi ciliari e può portare alla distruzione dell’interfaccia ciliare-vitreale e a una rotazione posteriore del corpo ciliare3). Tuttavia, le condizioni di irradiazione necessarie per distruggere l’interfaccia ciliare-vitreale non sono ancora state stabilite.
In caso di efficacia insufficiente del trattamento farmacologico o laser, o in caso di recidiva, si ricorre alla chirurgia. È importante eseguire una vitrectomia con ialoidotomia anteriore per risolvere la patologia6) (livello di evidenza 2C).
Si esegue una vitrectomia pars plana (PPV) 5). Talvolta viene associata anche l’estrazione del cristallino 6) (2C). L’estrazione del cristallino crea un occhio unicamerale, eliminando completamente il blocco tra la camera posteriore e quella anteriore e prevenendo la recidiva.
La zonulo-ialoideo-vitrectomia (resezione di iride, zonula di Zinn e membrana ialoidea anteriore) è efficace 5). Si accede alla camera anteriore attraverso un’iridectomia periferica e si resecano la zonula di Zinn intorno al sacco capsulare e la membrana ialoidea anteriore. Questa tecnica crea una via di comunicazione permanente tra la cavità vitreale e la camera anteriore.
Nella vitrectomia con incisione della membrana ialoidea anteriore, in alcuni casi è necessaria un’iridectomia per trattare la parte più periferica della membrana ialoidea anteriore 6) (2C). Se la membrana ialoidea anteriore e la zonula di Zinn non vengono trattate adeguatamente, rimane un blocco tra la cavità vitreale e la camera anteriore, che può portare a recidiva. Nell’occhio fachico, l’asportazione simultanea del cristallino elimina il contatto tra i processi ciliari e l’equatore del cristallino, creando un occhio unicamerale.
Esistono segnalazioni che la combinazione di rimozione del CTR, vitrectomia anteriore e fissazione sclerale dell’IOL sia stata efficace 2).
Il glaucoma maligno è un angolo chiuso dovuto a un meccanismo di spinta posteriore del cristallino. I miotici contraggono il muscolo ciliare, favorendo la protrusione anteriore del corpo ciliare e aggravando il blocco ciliare, quindi sono controindicati 6). Al contrario, i midriatici-cicloplegici come l’atropina rilassano il muscolo ciliare, aumentano la tensione della zonula e spostano il cristallino posteriormente, risultando efficaci per risolvere il blocco.
Il coinvolgimento unilaterale aumenta significativamente il rischio per l’occhio controlaterale 3). Il rischio è aumentato indipendentemente dalla storia di glaucoma, pertanto è importante una valutazione regolare della pressione intraoculare e della profondità della camera anteriore dell’occhio controlaterale.
Il meccanismo esatto del glaucoma maligno non è completamente chiarito, ma sono state proposte due ipotesi 5).
Teoria dell'espansione coroidale
Meccanismo principale: L’aumento di volume della coroide crea resistenza al movimento del fluido da dietro in avanti5)
Risultato: L’umore acqueo si accumula nella cavità vitrea, spingendo in avanti il diaframma irido-cristallino
Teoria del blocco ciliare
Meccanismo principale: Contatto anatomico anomalo tra i processi ciliari e l’equatore del cristallino (o IOL) e la membrana ialoide anteriore
Risultato: Si instaura un « ciclo maligno » che agisce come una valvola unidirezionale, impedendo il deflusso anteriore dell’umore acqueo
La progressione patologica può essere compresa attraverso la seguente cascata. In un occhio normale, l’umore acqueo prodotto dal corpo ciliare fluisce dalla camera posteriore attraverso la pupilla nella camera anteriore e defluisce attraverso il trabecolato dell’angolo. Nel glaucoma maligno, questo percorso è interrotto.
L’instillazione di atropina rilassa il muscolo ciliare, aumenta la tensione della zonula e sposta il cristallino posteriormente. Ciò può consentire all’umore acqueo che è finito nella cavità vitrea di tornare anteriormente.
D’altra parte, i miotici come la pilocarpina contraggono il muscolo ciliare. Questa contrazione rilassa la zonula, spinge il cristallino in avanti e favorisce la protrusione anteriore del corpo ciliare, aggravando il blocco ciliare 6). Pertanto, i miotici sono controindicati nel glaucoma maligno.
Nell’occhio pseudofachico, il diametro orizzontale del complesso IOL-sacco capsulare è maggiore di quello del cristallino naturale, rendendolo più suscettibile al contatto con i processi ciliari 4). Parte dell’umore acqueo prodotto dai processi ciliari viene secreto posteriormente (nella cavità vitrea). Se la membrana ialoidea anteriore è intatta, il deflusso del liquido in avanti è ostacolato, creando un gradiente pressorio e un assottigliamento della camera anteriore.
È stato riportato che la malattia può insorgere anche in occhi con precedente vitrectomia, se la membrana ialoidea anteriore persiste 4). In un caso di recidiva con uno shift miopico superiore a 3 D, una combinazione di goniosinechiolisi, iridectomia e zonulo-ialoidectomia ha ripristinato la refrazione e la pressione intraoculare 4). Pertanto, durante la vitrectomia è essenziale asportare completamente la membrana ialoidea anteriore e trattare fino alla periferia più estrema per prevenire la recidiva.
Il topiramato aumenta la permeabilità dei vasi corioidei ciliari, causando gonfiore del corpo ciliare e della coroide e una rotazione anteriore del corpo ciliare 1). Nella microftalmia, l’ispessimento sclerale ostacola il drenaggio delle vene vorticose, aumentando ulteriormente il rischio di versamento uveale 1).
Il posizionamento del CTR provoca l’espansione e l’ispessimento del sacco capsulare, e il complesso CTR-IOL entra in contatto circonferenziale con il corpo ciliare e l’iride posteriore 2). Ciò comprime lo spazio ciliare e aumenta la resistenza al movimento dell’umore acqueo da dietro in avanti. Il grande diametro del complesso CTR-IOL limita parzialmente lo spostamento anteriore, quindi la profondità della camera anteriore può essere mantenuta mentre si verifica un blocco angolare simile a un plateau dell’iride 2). Questa presentazione atipica differisce dall’immagine classica del glaucoma maligno con una «camera anteriore uniformemente bassa», pertanto la valutazione dettagliata della morfologia angolare mediante AS-OCT è la chiave per la diagnosi.
Chean et al. (2021) hanno riportato un caso di deviazione acquosa (myopic surprise) manifestatasi esclusivamente come spostamento miopico dopo chirurgia della cataratta 3). La pressione intraoculare è rimasta entro limiti normali per circa tre anni dopo l’intervento, ritardando la diagnosi. Anche se la profondità della camera anteriore misurata biometricamente appare normale, possono verificarsi errori di misurazione negli occhi con asse corto. Pertanto, in presenza di spostamento miopico, la deviazione acquosa dovrebbe essere inclusa nella diagnosi differenziale.
Stephenson et al. (2023) hanno riportato un caso di deviazione acquosa con uno spostamento miopico superiore a 3 D in un occhio con precedenti di vitrectomia, chirurgia della cataratta e impianto di iride artificiale 4). Hanno dimostrato che anche dopo vitrectomia, se la membrana ialoidea anteriore è preservata, la condizione può insorgere. La goniosinechiolisi + iridectomia + zonulo-ialoidectomia hanno ripristinato la rifrazione e la pressione intraoculare.
Goto et al. (2024) hanno caratterizzato per la prima volta con AS-OCT un blocco angolare secondario dovuto a uno spostamento anteriore del complesso CTR-IOL 2). Hanno riportato un’immagine atipica simile a un iris a plateau con profondità della camera anteriore preservata, dimostrando l’utilità dell’AS-OCT nel rilevare il blocco angolare secondario dopo chirurgia della cataratta con impianto di CTR.
È stato proposto un approccio graduale (terapia farmacologica → laser Nd:YAG → ciclodiode → chirurgia) 3). Il ciclodiode provoca necrosi da coagulazione e atrofia dei processi ciliari, che possono portare alla distruzione dell’interfaccia ciliare-vitreale e a una rotazione posteriore del corpo ciliare. Tuttavia, le condizioni di irradiazione necessarie per distruggere l’interfaccia ciliare-vitreale non sono ancora state stabilite. Se i farmaci e il laser sono insufficienti, la chirurgia per creare un occhio unicamerale rimane l’opzione terapeutica finale 3).