Bloqueo pupilar
Morfología del iris: Abombamiento anterior del iris periférico (iris bombé)
Profundidad de la cámara anterior: Especialmente superficial en la periferia
PI: Ocluido o no realizado
Mióticos: Efectivos

El glaucoma maligno es una condición de presión intraocular elevada con una cámara anterior marcadamente poco profunda, que ocurre típicamente después de una cirugía de filtración en ojos con glaucoma de ángulo cerrado. Se cree que resulta del cierre angular causado por el desplazamiento anterior del vítreo debido a la rotación anterior del cuerpo ciliar y la entrada anormal de humor acuoso en la cavidad vítrea. También se denomina síndrome de mala dirección del humor acuoso, glaucoma por bloqueo ciliar o glaucoma por bloqueo directo del cristalino, y se utilizan múltiples términos de manera intercambiable. El código ICD-10 es H40.8.
Reportado por primera vez por Von Graefe en 1869 como una cámara anterior poco profunda refractaria después de la cirugía de filtración, este es un concepto de enfermedad histórico 3). Posteriormente, se estableció el concepto fisiopatológico de que el humor acuoso se desvía hacia atrás (hacia la cavidad vítrea) en lugar de seguir la vía anterior normal, y el término “desviación acuosa” (aqueous misdirection) se ha utilizado ampliamente. Se encuentra con mayor frecuencia en ojos con glaucoma de ángulo cerrado después de la cirugía de filtración, pero es clínicamente importante que puede ocurrir después de cualquier cirugía intraocular, incluida la cirugía de cataratas.
Las Guías de Práctica Clínica para el Glaucoma (5.ª edición) clasifican los mecanismos de elevación de la presión intraocular en el glaucoma de ángulo cerrado secundario en las siguientes cuatro categorías 6).
El glaucoma maligno se clasifica en la tercera categoría, “movimiento anterior de tejidos posteriores al cristalino”. Corresponde al “mecanismo de empuje posterior” en la 5.ª edición de la EGS 5).
La incidencia después de la cirugía de filtración se reporta entre 0.6 y 4% 5). Es más común en mujeres y generalmente ocurre de forma unilateral. Es más frecuente después de la cirugía de filtración en ojos con glaucoma primario de ángulo cerrado, pero puede ocurrir después de cualquier cirugía intraocular, incluida la cirugía de cataratas 5). Los factores de riesgo incluyen longitud axial corta (<21 mm), hipermetropía alta (≥+6 D) y antecedentes de glaucoma primario de ángulo cerrado 5). También se han reportado casos espontáneos raros sin cirugía previa. Se sabe que la trabeculectomía para el glaucoma de ángulo cerrado tiene un riesgo relativamente alto de causar glaucoma maligno postoperatorio, junto con cámara anterior poco profunda y desprendimiento coroideo 6).
En el bloqueo pupilar, la obstrucción del flujo acuoso en el borde pupilar hace que el iris periférico se abombe hacia adelante (iris bombé). En contraste, en la desviación acuosa, el humor acuoso se acumula en la cavidad vítrea desde detrás del cristalino, lo que resulta en una cámara anterior uniformemente poco profunda. Los mióticos son efectivos para el bloqueo pupilar, pero están contraindicados en la desviación acuosa.
En el inicio agudo, se presentan los siguientes síntomas.
Los síntomas son fluctuantes y pueden manifestarse semanas a años después de la cirugía de cataratas 3). En etapas tempranas, la presión intraocular puede permanecer dentro del rango normal, lo que retrasa el diagnóstico 5). Cuando la presión intraocular se eleva rápidamente, el cuadro clínico se asemeja a un ataque agudo de glaucoma, con progresión rápida de la pérdida de visión.
El diagnóstico se realiza mediante una combinación de los siguientes hallazgos. Además de la elevación de la presión intraocular, el patrón de cambio en la profundidad de la cámara anterior es el más importante para el diagnóstico diferencial.
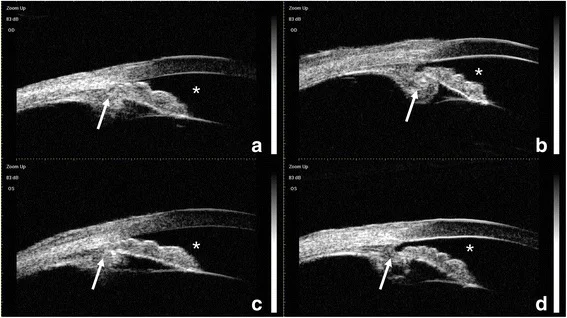
La tomografía de coherencia óptica del segmento anterior (AS-OCT) ha mostrado hallazgos similares a iris en meseta (iris central plano pero ángulo ocluido) asociados con el desplazamiento anterior del complejo CTR (anillo de tensión capsular)-IOL 2). La biomicroscopía ultrasónica (UBM) puede confirmar directamente el desplazamiento anterior del complejo saco capsular-IOL y la rotación anterior o anomalías posicionales del cuerpo ciliar 4). La UBM tiene una alta resolución de 20–60 μm y puede visualizar en detalle las estructuras del segmento anterior como el iris y el cuerpo ciliar, por lo que debe realizarse activamente en casos sospechosos de glaucoma maligno.
La UBM y la OCT del segmento anterior son útiles para dilucidar la fisiopatología. En particular, mientras se confirma la presencia o ausencia de antecedentes quirúrgicos, se debe evaluar si existe alguna anomalía posicional del cuerpo ciliar.
El desencadenante más común es la cirugía intraocular 5).
Los ojos más pequeños tienen mayor riesgo 5).
Si ocurre en un ojo, el riesgo de desarrollarlo en el ojo contralateral también aumenta 3). Dado que el riesgo se eleva independientemente de los antecedentes de glaucoma, es importante el seguimiento regular del ojo contralateral.
Los principales factores de riesgo se resumen a continuación.
| Factor de riesgo | Ejemplo específico |
|---|---|
| Morfología ocular | Longitud axial corta (<21 mm), hipermetropía alta (>+6 D), cámara anterior poco profunda |
| Cirugía | Cirugía filtrante, cirugía de cataratas, colocación de CTR |
| Medicación | Topiramato, ISRS |
El topiramato aumenta la permeabilidad vascular del cuerpo ciliar y la coroides, causando hinchazón del cuerpo ciliar y rotación hacia adelante 1). En ojos de alto riesgo como los de microftalmia, puede desencadenar desviación acuosa. Los ISRS también pueden inducir cierre angular en ojos con ángulos estrechos a través de un efecto midriático.
El glaucoma maligno es un diagnóstico de exclusión, que se establece solo después de descartar sistemáticamente el bloqueo pupilar, la hemorragia/desprendimiento coroideo, la hemorragia supracoroidea y otros mecanismos de cierre angular 4). No es una enfermedad que pueda confirmarse solo con valores de laboratorio o hallazgos de imagen específicos; se requiere una evaluación integral que combine la evolución clínica y múltiples hallazgos exploratorios.
Sospeche esta afección cuando se produzca una cámara anterior extremadamente poco profunda y presión intraocular alta en el postoperatorio temprano de cirugía de glaucoma de ángulo cerrado. El desprendimiento coroideo hemorrágico muestra hallazgos similares en la lámpara de hendidura y también puede causar presión intraocular alta, pero puede diferenciarse mediante el examen de fondo de ojo. En casos idiopáticos, el diagnóstico es más difícil debido a la ausencia de antecedentes quirúrgicos, y la confirmación de la posición anormal del cuerpo ciliar mediante UBM es clave para el diagnóstico.
Los puntos diferenciales entre el bloqueo pupilar y la desviación acuosa se resumen a continuación.
Bloqueo pupilar
Morfología del iris: Abombamiento anterior del iris periférico (iris bombé)
Profundidad de la cámara anterior: Especialmente superficial en la periferia
PI: Ocluido o no realizado
Mióticos: Efectivos
Desviación del humor acuoso
Morfología del iris: El iris está desplazado hacia adelante en su totalidad
Profundidad de la cámara anterior: Uniformemente superficial a ausente5)
PI: Permeable
Mióticos: Contraindicados (empeoran)
Otros diagnósticos diferenciales incluyen los siguientes. Todos pueden causar cámara anterior superficial y presión intraocular alta, pero la estrategia de tratamiento difiere porque la patogenia es diferente.
El enfoque escalonado de medicación → terapia láser → cirugía es fundamental. Primero se intenta aliviar el bloqueo ciliar con medicación; si no responde, se realiza terapia láser; si aún es ineficaz, se procede a la cirugía. El objetivo final del tratamiento es crear un estado en el que no se produzca bloqueo entre la cámara posterior y la anterior (ojo unicameral) y prevenir la recurrencia.
Se recomienda la combinación de un parasimpaticolítico (midriático / ciclopléjico), un supresor de la producción de humor acuoso (colirio y oral) y un agente hiperosmótico (intravenoso) 5).
| Fármaco | Posología | Mecanismo de acción |
|---|---|---|
| Atropina colirio al 1% | 1–3 veces al día | Cicloplejía / midriasis |
| Timolol colirio al 0.5% | Dos veces al día | Supresión del humor acuoso (bloqueo beta) |
| Comprimidos de Diamox 250 mg | 2 comprimidos, divididos en 2 dosis después de las comidas | Supresión del humor acuoso (CAI oral) |
| Infusión de manitol | Administración intravenosa | Reducción del volumen vítreo |
La atropina aumenta la tensión de las zónulas, moviendo el cristalino hacia atrás, y provoca que el humor acuoso que ha pasado a la cavidad vítrea regrese hacia adelante. El ciclopentolato también se puede usar como alternativa a la atropina 5).
Se utilizan gotas oftálmicas que suprimen la producción de humor acuoso (betabloqueantes, inhibidores de la anhidrasa carbónica) en combinación con infusión intravenosa de agentes hiperosmóticos 6). Los agentes hiperosmóticos reducen el volumen vítreo, pero su efecto terapéutico es temporal, por lo que se consideran un tratamiento preoperatorio 6).
La tasa de respuesta a la farmacoterapia es de aproximadamente el 50% (dentro de 5 días), pero la tasa de recurrencia con medicación sola es alta 5). Incluso si la farmacoterapia profundiza la cámara anterior y normaliza la presión intraocular, la recurrencia es frecuente al suspender las gotas de atropina, por lo que puede ser necesario continuar con atropina como terapia de mantenimiento a largo plazo. La farmacoterapia es solo una medida inicial; el tratamiento definitivo a menudo requiere intervención con láser o cirugía.
En ojos pseudofáquicos, se realiza una capsulotomía posterior con láser Nd:YAG, y luego se desplaza el foco detrás de la cápsula posterior, administrando de 10 a 20 disparos con energía de 3-4 mJ para romper la membrana vítrea anterior. Al crear un pasaje para el humor acuoso entre la cavidad vítrea y la cámara anterior, se alivia el bloqueo. Si tiene éxito, se obtiene una mejora en la profundidad de la cámara anterior y una reducción de la presión intraocular inmediatamente o al día siguiente.
En ojos pseudofáquicos o afáquicos, se seleccionan la incisión con láser YAG o la incisión quirúrgica de la membrana vítrea anterior y la capsulotomía 6) (nivel de evidencia 2C).
La ciclofotocoagulación con láser de diodo se puede considerar en cualquier etapa del tratamiento 5). Provoca necrosis por coagulación y atrofia de los procesos ciliares, lo que puede llevar a la destrucción de la interfaz ciliar-vítrea y a la rotación posterior del cuerpo ciliar 3). Sin embargo, las condiciones de irradiación necesarias para destruir la interfaz ciliar-vítrea no están establecidas.
Si el tratamiento farmacológico y con láser son insuficientes, o en casos recurrentes, se realiza cirugía. Es importante resolver la condición mediante vitrectomía con incisión de la membrana vítrea anterior 6) (nivel de evidencia 2C).
Se realiza vitrectomía pars plana (PPV) 5). En algunos casos también se realiza extracción del cristalino 6) (2C). Al combinar la extracción del cristalino, se crea un ojo unicameral, aliviando completamente el bloqueo entre la cámara posterior y la anterior para prevenir la recurrencia.
La zonulo-hialoideo-vitrectomía (irido-zonulo-hialoidectomía anterior) es efectiva 5). Se aborda desde la iridectomía periférica hacia la cámara anterior, y se extirpan las zónulas alrededor del saco capsular y la membrana hialoidea anterior. Este procedimiento crea una comunicación permanente entre la cavidad vítrea y la cámara anterior.
En la vitrectomía con hialoidotomía anterior, algunos casos requieren iridectomía para tratar la membrana hialoidea anterior más periférica 6) (2C). Si la membrana hialoidea anterior y las zónulas no se tratan suficientemente, queda un bloqueo entre la cavidad vítrea y la cámara anterior, lo que puede llevar a recurrencia. En ojos fáquicos, el cristalino también se extrae simultáneamente para aliviar el contacto entre los procesos ciliares y el ecuador del cristalino, creando un ojo unicameral.
Hay un informe de que la combinación de extracción del CTR, vitrectomía anterior y fijación escleral del IOL fue efectiva 2).
La desviación acuosa es un cierre angular debido a un mecanismo de empuje posterior del cristalino. Los mióticos contraen el músculo ciliar, promoviendo la protrusión anterior del cuerpo ciliar y empeorando el bloqueo ciliar, por lo que están contraindicados 6). En contraste, los agentes midriáticos-ciclopléjicos como la atropina relajan el músculo ciliar, aumentan la tensión de las zónulas y mueven el cristalino hacia atrás, lo que es efectivo para aliviar el bloqueo.
La aparición unilateral aumenta significativamente el riesgo en el ojo contralateral 3). El riesgo se eleva independientemente de antecedentes de glaucoma, por lo que es importante la evaluación regular de la presión intraocular y la profundidad de la cámara anterior en el ojo contralateral.
El mecanismo exacto del glaucoma maligno no se ha dilucidado completamente, pero se han propuesto las siguientes dos hipótesis 5).
Teoría de la expansión coroidea
Mecanismo principal: El aumento del volumen coroideo genera resistencia al movimiento del líquido de posterior a anterior 5)
Resultado: El humor acuoso se acumula en la cavidad vítrea, empujando el diafragma iris-cristalino hacia adelante
Teoría del bloqueo ciliar
Mecanismo principal: Contacto anatómico anormal entre los procesos ciliares y el ecuador del cristalino (o LIO) o la membrana hialoidea anterior
Resultado: Se establece un “ciclo maligno” que actúa como una válvula unidireccional, bloqueando la salida anterior del humor acuoso
La progresión de la enfermedad se puede entender mediante la siguiente cascada. En un ojo normal, el humor acuoso producido por el cuerpo ciliar fluye desde la cámara posterior a través de la pupila hacia la cámara anterior y sale a través de la malla trabecular del ángulo. En el glaucoma maligno, esta vía se interrumpe.
Las gotas oftálmicas de atropina relajan el músculo ciliar, aumentan la tensión de las zónulas y desplazan el cristalino hacia atrás. Esto puede permitir que el humor acuoso que ha pasado a la cavidad vítrea regrese hacia adelante.
Por el contrario, los mióticos como la pilocarpina contraen el músculo ciliar. Esta contracción relaja las zónulas, empuja el cristalino hacia adelante y promueve aún más la rotación anterior del cuerpo ciliar, empeorando el bloqueo ciliar 6). Por lo tanto, los mióticos están contraindicados en el glaucoma maligno.
En ojos pseudofáquicos, el diámetro horizontal del complejo LIO-saco capsular es mayor que el del cristalino natural, lo que facilita el contacto con los procesos ciliares 4). Parte del humor acuoso producido por los procesos ciliares se secreta hacia atrás (cavidad vítrea). Si la membrana hialoidea anterior está intacta, se impide el flujo de líquido hacia adelante, creando un gradiente de presión y disminuyendo la profundidad de la cámara anterior.
Se ha informado que incluso en ojos con antecedentes de vitrectomía, la condición puede desarrollarse si la membrana hialoidea anterior permanece 4). En un caso recurrente con un desplazamiento miópico de 3 D o más, una combinación de goniosinequiolisis, iridectomía y zonulo-hialoidectomía restauró la refracción y la presión intraocular 4). Por lo tanto, durante la vitrectomía, la eliminación completa de la membrana hialoidea anterior, incluidas las áreas más periféricas, es esencial para prevenir la recurrencia.
El topiramato aumenta la permeabilidad de los vasos coroideos ciliares, causando hinchazón del cuerpo ciliar y la coroides y rotación anterior del cuerpo ciliar 1). En la microftalmía, el deterioro del drenaje de las venas vorticosas debido al engrosamiento escleral aumenta aún más el riesgo de efusión uveal 1).
La colocación de un CTR expande y engrosa el saco capsular, y el complejo CTR-LIO contacta circunferencialmente con el cuerpo ciliar y el iris posterior 2). Esto comprime el surco ciliar, aumentando la resistencia al flujo de humor acuoso de posterior a anterior. Debido a que el gran diámetro del complejo CTR-LIO limita parcialmente el desplazamiento anterior, puede presentarse con un cierre angular similar a plateau iris mientras se mantiene la profundidad de la cámara anterior 2). Este hallazgo atípico difiere de la apariencia clásica del glaucoma maligno con cámara anterior uniformemente poco profunda, por lo que la evaluación detallada de la morfología angular mediante AS-OCT es clave para el diagnóstico.
Chean et al. (2021) reportaron un caso de maldirección acuosa que se presentó con sorpresa miópica (myopic surprise) como único signo inicial después de la cirugía de cataratas 3). La presión intraocular se mantuvo dentro del rango normal durante aproximadamente tres años después de la operación, lo que retrasó el diagnóstico. Incluso si la profundidad de la cámara anterior parece normal en la biometría, pueden ocurrir errores de medición en ojos con eje axial corto, por lo que cuando se observa un desplazamiento miópico, se debe incluir la maldirección acuosa en el diagnóstico diferencial.
Stephenson et al. (2023) reportaron un caso de maldirección acuosa con un desplazamiento miópico de 3 D o más en un ojo con antecedentes de vitrectomía, cirugía de cataratas e implante de iris artificial 4). Demostraron que incluso después de la vitrectomía, si la membrana hialoidea anterior permanece, aún puede ocurrir, y la refracción y la presión intraocular se recuperaron después de goniosinequiolisis + iridectomía + zonulo-hialoidectomía.
Goto et al. (2024) caracterizaron por primera vez el cierre angular secundario debido al desplazamiento anterior del complejo CTR-IOL mediante AS-OCT 2). Reportaron una apariencia atípica similar a iris en plateau con profundidad de cámara anterior preservada, demostrando la utilidad de la AS-OCT en la detección del cierre angular secundario después de cirugía de cataratas con implante de CTR.
Se ha propuesto un enfoque escalonado de medicación → láser Nd:YAG → ciclodiodo → cirugía 3). El ciclodiodo causa necrosis por coagulación y atrofia de los procesos ciliares, pudiendo alterar la interfaz cilio-vítrea y provocar una rotación posterior del cuerpo ciliar. Sin embargo, las condiciones de irradiación necesarias para alterar la interfaz cilio-vítrea no están establecidas, y cuando la medicación y el láser por sí solos son insuficientes, la cirugía para crear un ojo unicameral sigue siendo la opción de tratamiento final 3).