瞳孔阻滞
虹膜形态:周边虹膜向前膨隆(iris bombé)
前房深度:周边部特别浅
PI:闭塞或未施行
缩瞳药:有效

恶性青光眼是一种伴有明显浅前房的高眼压状态,典型发生于闭角型青光眼眼滤过手术后。推测是由于睫状体前旋和房水异常流入玻璃体腔导致玻璃体前移,从而引起房角关闭。也称为房水迷流综合征、睫状体阻滞性青光眼或直接晶状体阻滞性青光眼,多种名称混用。ICD-10编码为H40.8。
1869年Von Graefe首次将其报告为滤过手术后难治性浅前房,这是一个历史性的疾病概念3)。随后,房水不沿正常前向路径而是被错误地引导至后方(玻璃体腔侧)的病理概念得以确立,“aqueous misdirection”(房水迷流)这一名称被广泛使用。最常见于滤过手术后的闭角型青光眼,但临床上重要的是,它可能发生在任何内眼手术后,包括白内障手术。
青光眼诊疗指南(第5版)将继发性房角关闭性青光眼的眼压升高机制分为以下四类6)。
恶性青光眼属于上述第三类“晶状体后方组织的前移”。在EGS第5版中相当于“后推机制”5)。
滤过手术后的发生率为0.6%~4%5)。多见于女性,通常单眼发病。最常见于原发性闭角型青光眼滤过手术后,但也可能发生在任何内眼手术后,包括白内障手术5)。危险因素包括短眼轴(<21 mm)、高度远视(≥+6 D)和原发性闭角型青光眼病史5)。罕见无手术史的自发性病例也有报道。已知闭角型青光眼行小梁切除术后,发生浅前房、脉络膜脱离以及恶性青光眼的风险相对较高6)。
瞳孔阻滞时,瞳孔缘房水流通受阻导致周边虹膜向前膨隆(iris bombé)。而房水迷流时,房水从晶状体后方积聚在玻璃体腔,因此前房均匀变浅。缩瞳药对瞳孔阻滞有效,但对房水迷流是禁忌的。
急性发作时出现以下症状。
症状具有波动性,可能在白内障术后数周至数年才显现3)。早期眼压可能仍在正常范围内,导致诊断延迟5)。眼压急剧升高时,临床表现类似急性青光眼发作,视力下降迅速进展。
通过以下体征的组合进行诊断。除眼压升高外,前房深度的变化模式在鉴别诊断中最为重要。
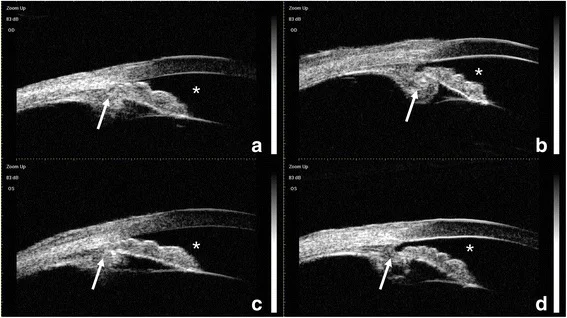
前段光学相干断层扫描(AS-OCT)显示,CTR(囊袋张力环)-IOL复合体前移可导致类似高褶虹膜的表现(虹膜中央平坦但房角关闭)2)。超声生物显微镜(UBM)可直接确认晶状体囊-IOL复合体前移及睫状体前旋或位置异常4)。UBM分辨率高达20–60 μm,可详细显示虹膜、睫状体等前段结构,因此对疑似恶性青光眼的病例应积极进行此项检查。
UBM和前段OCT检查有助于阐明病理生理机制,尤其应在确认手术史的同时评估是否存在睫状体位置异常。
最常见的诱因是内眼手术5)。
眼球越小,风险越高5)。
如果单眼发病,对侧眼的发病风险也会增加3)。无论是否有青光眼病史,风险都会升高,因此对侧眼的定期随访很重要。
主要风险因素总结如下。
| 风险因素 | 具体例子 |
|---|---|
| 眼球形态 | 短眼轴(<21 mm)、高度远视(>+6 D)、浅前房 |
| 手术 | 滤过手术、白内障手术、CTR植入 |
| 药物 | 托吡酯、SSRI |
托吡酯可增加睫状体脉络膜的血管通透性,导致睫状体肿胀和向前旋转1)。在小眼球等高危眼中,可能诱发房水迷流。SSRI也可能通过散瞳作用诱发窄房角眼的房角关闭。
恶性青光眼是排除性诊断,必须在系统排除瞳孔阻滞、脉络膜出血/脱离、脉络膜上腔出血及其他闭角机制后才能确诊4)。该病不能仅凭特定检查值或影像学表现确诊,需要结合临床病程和多项检查结果综合判断。
闭角型青光眼术后早期出现极浅前房和高眼压时,应怀疑本病。出血性脉络膜脱离可呈现类似的裂隙灯显微镜表现,且均可导致高眼压,但可通过眼底检查鉴别。特发性病例因无手术史,诊断更为困难,UBM确认睫状体位置异常是诊断的关键。
瞳孔阻滞与房水迷流的鉴别要点总结如下。
瞳孔阻滞
虹膜形态:周边虹膜向前膨隆(iris bombé)
前房深度:周边部特别浅
PI:闭塞或未施行
缩瞳药:有效
房水误流
虹膜形态:虹膜整体向前移位
前房深度:均匀变浅至消失5)
PI:通畅
缩瞳药:禁忌(加重病情)
其他鉴别诊断包括以下疾病。这些疾病均可导致浅前房和高眼压,但由于发病机制不同,治疗方案也不同。
基本采用药物疗法→激光疗法→手术治疗的阶梯式方法。首先尝试药物疗法解除睫状体阻滞,无效则进行激光治疗,仍无效则逐步进行手术治疗。治疗的最终目标是建立后房与前房之间不会发生阻滞的状态(单房眼),防止复发。
推荐联合使用副交感神经阻断药(散瞳/睫状肌松弛药)、房水生成抑制剂(滴眼和口服)以及高渗剂(静脉滴注)5)。
| 药物 | 用法 | 作用机制 |
|---|---|---|
| 阿托品滴眼液1% | 每日1~3次滴眼 | 睫状肌松弛/散瞳 |
| 噻吗洛尔滴眼液0.5% | 每日2次滴眼 | 房水生成抑制(β阻滞) |
| 醋唑磺胺片250 mg | 2片,分2次饭后服用 | 房水生成抑制(口服CAI) |
| 甘露醇静脉滴注 | 静脉给药 | 缩小玻璃体容积 |
阿托品可增加睫状小带的张力,使晶状体向后移动,并促使进入玻璃体腔的房水向前回流。也可使用环喷托酯作为阿托品的替代品5)。
抑制房水生成的眼药水(β受体阻滞剂、碳酸酐酶抑制剂)与高渗剂静脉滴注联合使用6)。高渗剂可缩小玻璃体容积,但其治疗效果是暂时的,因此被视为术前处理6)。
药物治疗的有效率约为50%(5天内),但单用药物复发率高5)。即使药物治疗使前房加深、眼压恢复正常,停用阿托品眼药水后也常复发,因此可能需要长期维持使用阿托品眼药水。药物治疗仅为初始措施,根治性治疗通常需要激光或手术干预。
在人工晶状体眼中,进行Nd:YAG激光后囊膜切开,然后将焦点移至后囊膜后方,以3-4 mJ的能量发射10-20次,破坏前玻璃体膜。通过在玻璃体腔和前房之间建立房水通道,解除阻滞。如果成功,即刻至次日可观察到前房深度改善和眼压下降。
在人工晶状体眼或无晶状体眼中,可选择YAG激光或手术前玻璃体膜切开和囊膜切开术6)(证据等级2C)。
二极管激光睫状体光凝术可在治疗的任何阶段考虑5)。它引起睫状突的凝固坏死和萎缩,可能导致睫状体-玻璃体界面的破坏和睫状体向后旋转3)。然而,破坏睫状体-玻璃体界面所需的照射条件尚未确定。
如果药物和激光治疗效果不佳,或复发,则进行手术。通过前玻璃体膜切开的玻璃体切除术来解除病情至关重要6)(证据等级2C)。
进行经睫状体扁平部玻璃体切除术(PPV)5)。有时也联合晶状体摘除术6)(2C)。通过联合晶状体摘除,创建单房眼,完全解除后房与前房之间的阻滞,防止复发。
zonulo-hyaloido-vitrectomy(虹膜-晶状体悬韧带-前玻璃体膜切除术)是有效的5)。从周边虹膜切除处向前房方向进入,切除晶状体囊周围的悬韧带和前玻璃体膜。该术式在玻璃体腔和前房之间建立永久性交通通道。
在伴有前玻璃体膜切开的玻璃体切除术中,有些病例需要虹膜切除以处理最周边的前玻璃体膜6)(2C)。如果前玻璃体膜和悬韧带处理不充分,玻璃体腔和前房之间会残留阻滞,可能导致复发。在有晶状体眼中,同时摘除晶状体可解除睫状突与晶状体赤道部的接触,创建单房眼。
有报告称,CTR取出、前玻璃体切除和IOL巩膜内固定的组合是有效的2)。
房水迷流是晶状体后方推挤机制引起的闭角。缩瞳药收缩睫状肌,促进睫状体前突,加重睫状体阻滞,因此是禁忌的6)。相比之下,阿托品等散瞳睫状肌麻痹药可松弛睫状肌,增加悬韧带张力,使晶状体后移,从而有效解除阻滞。
单眼发病会显著增加对侧眼的风险3)。无论是否有青光眼病史,风险都会升高,因此定期评估对侧眼的眼压和前房深度很重要。
恶性青光眼的确切发病机制尚未完全阐明,但提出了以下两种假说5)。
脉络膜膨胀说
主要机制:脉络膜容积增大,对液体从后方向前方的移动产生阻力5)
结果:房水积聚在玻璃体腔,将虹膜-晶状体隔膜向前推
睫状体阻滞学说
主要机制:睫状突与晶状体(或人工晶状体)赤道部、前玻璃体膜之间的异常解剖接触
结果:形成“恶性循环”,起到单向阀的作用,阻碍房水向前流出
病情的进展可通过以下级联理解。正常眼中,睫状体产生的房水从后房经瞳孔流入前房,然后通过房角的小梁网流出。在恶性青光眼中,这一通路被破坏。
阿托品滴眼液可松弛睫状肌,增加悬韧带张力,使晶状体向后移动。这可能导致进入玻璃体腔的房水有机会向前回流。
相反,毛果芸香碱等缩瞳药会收缩睫状肌。这种收缩会松弛悬韧带,将晶状体向前推,并进一步促进睫状体前旋,从而加重睫状环阻滞6)。因此,缩瞳药在恶性青光眼中是禁忌的。
在人工晶状体眼中,IOL-囊袋复合体的水平直径大于天然晶状体,更容易接触睫状突4)。睫状突产生的部分房水向后(玻璃体腔)分泌。如果前玻璃体膜完整,前向液体流出受阻,产生压力梯度,导致前房变浅。
据报道,即使有玻璃体切除术史的眼,如果前玻璃体膜残留,也可能发病4)。在一例伴有3 D以上近视漂移的复发病例中,联合房角粘连分离术、虹膜切除术和晶状体悬韧带-玻璃体膜切除术恢复了屈光和眼压4)。因此,玻璃体切除术时应充分清除前玻璃体膜,包括最周边区域,这对预防复发至关重要。
托吡酯可增加睫状体脉络膜血管的通透性,导致睫状体和脉络膜肿胀以及睫状体前旋1)。在小眼球症中,巩膜增厚导致的涡静脉引流障碍进一步增加了葡萄膜渗出的风险1)。
植入CTR会使囊袋扩张增厚,CTR-IOL复合体全周接触睫状体和虹膜后表面2)。这会压迫睫状沟,增加房水从后向前流动的阻力。由于CTR-IOL复合体的大直径部分限制了前向移位,可能表现为前房深度保持的虹膜高坪型房角关闭2)。这种非典型表现不同于恶性青光眼典型的均匀浅前房,因此使用AS-OCT详细评估房角形态是诊断的关键。
Chean等人(2021)报告了一例白内障术后以近视漂移(myopic surprise)为唯一早期体征的房水迷流病例3)。术后约三年内眼压正常,导致诊断延迟。即使生物测量显示前房深度看似正常,短眼轴眼也可能出现测量误差,因此当出现近视漂移时,应将房水迷流纳入鉴别诊断。
Stephenson等人(2023)报告了一例既往有玻璃体切除术、白内障手术和人工虹膜植入术史的眼,出现3 D以上的近视漂移并伴有房水迷流的病例4)。他们表明,即使玻璃体切除术后,如果前玻璃体膜残留,仍可能发病,通过房角粘连分离术+虹膜切除术+晶状体悬韧带-玻璃体切除术,屈光和眼压得以恢复。
Goto等人(2024)首次使用AS-OCT描述了CTR-IOL复合体前移导致的继发性房角关闭的特征2)。他们报告了一种非典型的高原虹膜样表现,前房深度保持不变,表明AS-OCT在检测白内障手术联合CTR植入术后继发性房角关闭方面具有价值。
已提出药物→Nd:YAG激光→睫状体光凝→手术的阶梯式方法3)。睫状体光凝可引起睫状突的凝固坏死和萎缩,可能破坏睫状体-玻璃体界面并导致睫状体向后旋转。然而,破坏睫状体-玻璃体界面所需的照射条件尚未确定,当药物和激光单独治疗不足时,创建单腔眼的手术仍然是最终的治疗选择3)。