引起瞳孔阻滞型青光眼的药物
具有散瞳/调节麻痹作用的药物:去氧肾上腺素、托吡卡胺、环喷托酯、阿托品1)
具有抗胆碱作用的全身用药:三环类抗抑郁药、抗精神病药(奥氮平)、苯二氮卓类(地西泮)、抗组胺药1, 2)
具有交感神经刺激作用的药物:肾上腺素、地匹福林、鼻腔减充血剂(含去氧肾上腺素)、非法兴奋剂(可卡因、摇头丸)2)
其他:肉毒杆菌毒素(眼周注射)、丙吡胺(抗心律失常药)

药物诱发性急性房角关闭青光眼(drug-induced AACG)是使用局部或全身药物后诱发急性房角关闭的眼科急症1)。若治疗不及时,可因不可逆的视神经损伤导致永久性视力丧失。
易发生急性房角关闭的患者具有远视、短眼轴、浅前房、窄房角等解剖特征1)。窄房角的患病率在白人中约为3.8%,在亚洲人中约为8.5%1)。其他危险因素包括高龄、女性、家族史以及对侧眼AACG病史1)。
药物诱发性AACG的发病机制大致分为瞳孔阻滞型和非瞳孔阻滞型1)。瞳孔阻滞是最常见的机制,但需排除继发性原因(如高褶虹膜、晶状体源性、晶状体后等)3)。
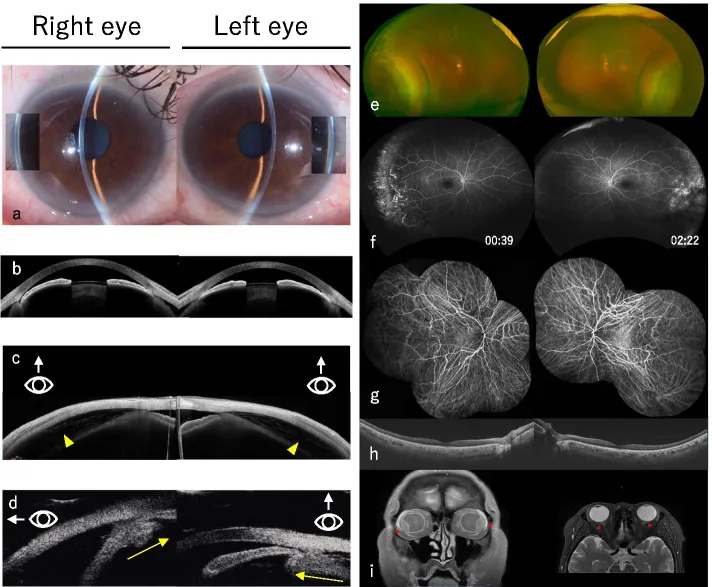
急性发作的症状包括突然的单侧剧烈眼痛、充血、头痛、恶心/呕吐、视物模糊、光周围虹视症(光晕)2)。全身症状如剧烈头痛、恶心、呕吐可能显著出现,有时被误诊为神经系统或消化系统疾病2)。眼压可升至40–80 mmHg。
| 所见 | 特征 |
|---|---|
| 眼压 | 显著升高(40–80 mmHg) |
| 角膜 | 水肿(以上皮性为主) |
| 瞳孔 | 中度散大,对光反射减弱 |
| 前房 | 浅(伴虹膜膨隆) |
| 结膜 | 睫状充血,静脉淤血 |
| 晶状体 | 青光眼斑 |
房角镜检查可见广泛的虹膜与小梁网接触(ITC)3)。对侧眼的房角检查也通常显示闭角型青光眼的风险征象3)。当角膜水肿导致房角镜检查困难时,AS-OCT或超声生物显微镜检查是有用的2)。
在一例奥氮平诱发的AAC病例中,用药一周后,右眼眼压为51 mmHg,出现微囊性角膜水肿、中度固定性瞳孔散大、虹膜膨隆伴浅前房1)。超声生物显微镜证实360度房角关闭,未观察到脉络膜渗出1)。
药物诱发的AACG根据诱发机制可分为瞳孔阻滞型和非瞳孔阻滞型。
| 药物分类 | 代表药物 | 机制 |
|---|---|---|
| 散瞳药/睫状肌麻痹药 | 去氧肾上腺素、托吡卡胺 | 瞳孔阻滞 |
| 三环类抗抑郁药 | 阿米替林、丙咪嗪 | 瞳孔阻滞 |
| SSRI | 帕罗西汀、艾司西酞普兰 | 瞳孔阻滞/葡萄膜渗漏 |
| 抗精神病药 | 奥氮平 | 瞳孔阻滞 |
| 抗癫痫药 | 托吡酯 | 非瞳孔阻滞 |
| 支气管扩张药 | 异丙托溴铵 | 瞳孔阻滞 |
引起瞳孔阻滞型青光眼的药物
具有散瞳/调节麻痹作用的药物:去氧肾上腺素、托吡卡胺、环喷托酯、阿托品1)
具有抗胆碱作用的全身用药:三环类抗抑郁药、抗精神病药(奥氮平)、苯二氮卓类(地西泮)、抗组胺药1, 2)
具有交感神经刺激作用的药物:肾上腺素、地匹福林、鼻腔减充血剂(含去氧肾上腺素)、非法兴奋剂(可卡因、摇头丸)2)
其他:肉毒杆菌毒素(眼周注射)、丙吡胺(抗心律失常药)
非瞳孔阻滞型的致病药物
托吡酯:因睫状体上腔渗出、睫状体前旋、晶状体膨胀导致前房变浅。通常在用药开始2周内发病,几乎均为双眼性2, 3)
磺胺类药物:因晶状体膨隆、视网膜水肿、脉络膜渗出导致继发性前房变浅
SSRI(部分):艾司西酞普兰、文拉法辛已被报道伴有葡萄膜渗出的双眼性房角关闭2)
抗凝药:自发性脉络膜出血导致虹膜-晶状体隔前移
具有散瞳或调节麻痹作用的药物,可在具有浅前房、厚晶状体等解剖易感因素的眼睛中诱发APACA2)。这是因为散瞳会增强瞳孔阻滞和房角拥挤2)。具体包括SSRI抗抑郁药、三环类抗抑郁药、鼻腔减充血剂(含抗组胺药)、抗胆碱能药、交感神经兴奋药、止吐药2)。
雾化吸入支气管扩张剂(异丙托溴铵、沙丁胺醇)也可诱发急性房角关闭3)。全身麻醉期间或麻醉后也可能发生急性房角关闭3)。
大致分为两种机制。瞳孔阻滞型由具有散瞳作用的药物(交感神经兴奋药、抗胆碱能药、三环类抗抑郁药、SSRI、抗精神病药、苯二氮卓类、支气管扩张剂)引起。非瞳孔阻滞型中,托吡酯和磺胺类药物引起睫状体水肿、脉络膜渗出,将虹膜-晶状体隔向前推挤,从而诱发房角关闭。两种情况均在有解剖易感因素(浅前房、窄房角、远视眼)的患者中风险更高。
药物诱发性AACG的诊断需要评估临床表现并详细询问用药史。由于急性房角关闭中有很高比例是由外用或全身药物诱发的,因此必须确认包括处方药和非处方药在内的完整用药史3)。
房角镜检查应在双眼进行2)。即使角膜水肿导致患眼房角镜检查困难,对侧眼的发现也有助于诊断2)。
**眼前段光学相干断层扫描(AS-OCT)和超声生物显微镜(UBM)**即使在角膜水肿的情况下也能评估前房深度、房角形态和睫状体状态2)。超声生物显微镜特别有助于识别睫状体肿胀或旋转,这对非瞳孔阻滞型的诊断很重要。
为鉴别继发性原因,如果对侧眼表现为开角、深前房,患眼角膜相对透明,或存在虹膜新生血管,则需注意2)。
综合评估用药史、晶状体状态、房角和虹膜解剖以及急性房角关闭的侧别(单侧/双侧)有助于明确病因。双侧急性房角关闭罕见,但提示可能存在药物相关机制,如托吡酯或SSRIs2)。
药物诱导的AACG的治疗首先应优先快速降低眼压,并根据病因机制进行干预2)。
药物治疗
乙酰唑胺:当眼压≥40mmHg时建议立即给药。呕吐或需要快速起效时,首选静脉注射(10mg/kg)3)。
甘露醇:当对乙酰唑胺反应不足时考虑使用。以15-20%溶液静脉注射0.5-1.5g/kg3)。
毛果芸香碱:滴用1-2%滴眼液。括约肌缺血时无效,眼压下降后可能出现缩瞳3)。
类固醇滴眼液:频繁给药(每日4-6次)以减轻炎症3)。
激光和手术治疗
在一例奥氮平诱发的AAC病例中,使用噻吗洛尔0.5%和溴莫尼定0.15%滴眼液、口服乙酰唑胺、毛果芸香碱2%后,行Nd:YAG激光虹膜切开术,次日眼压从51 mmHg降至20 mmHg,视力从6/200恢复至20/301)。对侧眼也进行了预防性激光虹膜切开术1)。
全身用药(乙酰唑胺、甘露醇)在老年或合并其他疾病的患者中需谨慎,可能引起从感觉异常、意识错乱到肺水肿、急性肾衰竭等严重副作用2)。
瞳孔阻滞是药物诱发性AACG最常见的机制3)。具有交感神经刺激或副交感神经阻断作用的药物诱发散瞳时,虹膜与晶状体的接触面积增加1)。这增加了房水从后房经瞳孔流向前房的阻力,导致后房压力超过前房压力3)。
后房压力升高导致虹膜向前膨隆(虹膜膨隆),周边虹膜覆盖小梁网,阻塞房水流出通道,引起眼压急剧升高3)。括约肌和开大肌同时激活的中等散瞳状态风险最高3)。
在奥氮平病例中,弱的抗胆碱作用诱发散瞳,在解剖学易感眼中发生瞳孔阻滞1)。非典型抗精神病药引起的闭角型青光眼罕见,与SSRI和三环类抗抑郁药相比报告较少1)。
托吡酯和磺胺类药物可因特异质药物反应引起睫状体上腔渗出3)。这导致睫状体向前旋转,晶状体悬韧带松弛和晶状体膨胀,使整个虹膜-晶状体隔膜前移,堵塞房角2)。
这种机制可发生于开角或窄角患者。文拉法辛和艾司西酞普兰引起的伴有葡萄膜渗出的双眼急性房角关闭也有报道2)。
高坪虹膜形态是指位置靠前的睫状突将周边虹膜向前推,在散瞳时直接堵塞房角3)。如果解除瞳孔阻滞后眼压仍高,应怀疑高坪虹膜参与。
瞳孔阻滞型是由于散瞳使虹膜与晶状体接触增加,阻碍房水从后房流入前房,导致虹膜向前膨隆堵塞房角。散瞳药、抗胆碱药和拟交感神经药是原因,激光虹膜切开术有效。而非瞳孔阻滞型是由托吡酯或磺胺类药物引起的睫状体水肿和脉络膜渗出,将整个虹膜-晶状体隔膜向前推。虹膜切开术无效,停用致病药物和睫状肌麻痹剂是治疗核心。双眼发病强烈提示非瞳孔阻滞型。
2025年发布的国际共识中,提出了术语**APACA(急性原发性房角关闭发作)**用于急性原发性房角关闭发作2)。该术语强调了疾病的急性和紧急性质,并明确了与继发性原因的区别2)。100%一致同意快速降低眼压应优先于准确诊断2)。
共识声明以88.24%的同意率确认,具有散瞳和睫状肌麻痹作用的药物可在有解剖易感性的眼中诱发APACA2)。对高危患者处方此类药物时需谨慎,详细的用药史是重要的诊断线索2)。
诊断性药物散瞳在一般人群中是安全的,散瞳不足导致眼底疾病漏诊的风险远高于诱发房角关闭的风险3)。对于接受过适当预防性治疗(激光虹膜切开术)的房角关闭病史患者,散瞳通常是安全的3)。散瞳后预防性使用毛果芸香碱缩瞳应避免,因为这可能导致瞳孔固定于中等散瞳位,增加房角关闭风险3)。