引起瞳孔阻滯型青光眼的藥物
具有散瞳/調節麻痺作用的藥物:去氧腎上腺素、托吡卡胺、環噴托酯、阿托品1)
具有抗膽鹼作用的全身用藥:三環抗憂鬱藥、抗精神病藥(奧氮平)、苯二氮平類(地西泮)、抗組織胺藥1, 2)
具有交感神經刺激作用的藥物:腎上腺素、地匹福林、鼻腔充血解除劑(含去氧腎上腺素)、非法興奮劑(古柯鹼、搖頭丸)2)
其他:肉毒桿菌毒素(眼周注射)、丙吡胺(抗心律不整藥)

藥物誘發性急性隅角閉鎖青光眼(drug-induced AACG)是使用局部或全身藥物後誘發急性隅角閉鎖的眼科急症1)。若治療延遲,可能因不可逆的視神經損傷導致永久性視力喪失。
易發生急性隅角閉鎖的患者具有遠視、短眼軸、淺前房、窄隅角等解剖特徵1)。窄隅角的盛行率在白人中約為3.8%,在亞洲人中約為8.5%1)。其他危險因子包括高齡、女性、家族史以及對側眼AACG病史1)。
藥物誘發性AACG的發病機轉大致分為瞳孔阻塞型和非瞳孔阻塞型1)。瞳孔阻塞是最常見的機制,但需排除繼發性原因(如高褶虹膜、水晶體源性、水晶體後等)3)。
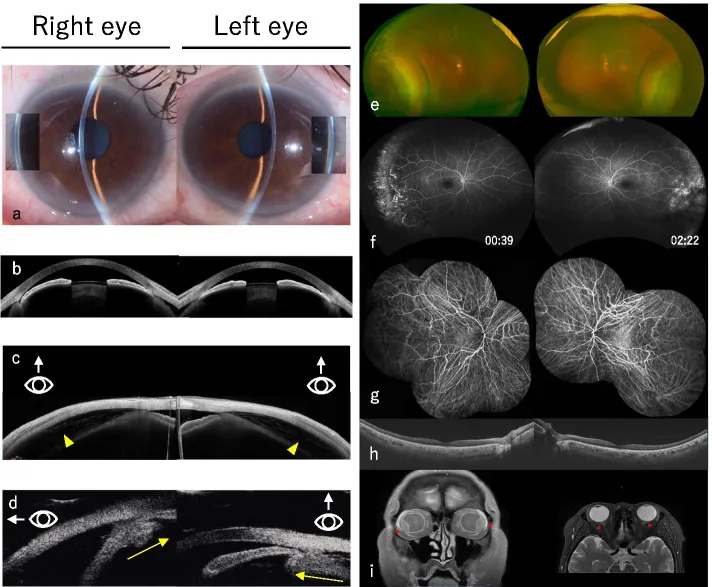
急性發作的症狀包括突然的單側劇烈眼痛、充血、頭痛、噁心/嘔吐、視物模糊、光周圍虹視症(光暈)2)。全身症狀如劇烈頭痛、噁心、嘔吐可能顯著出現,有時被誤診為神經系統或消化系統疾病2)。眼壓可升至40–80 mmHg。
| 所見 | 特徵 |
|---|---|
| 眼壓 | 顯著升高(40–80 mmHg) |
| 角膜 | 水腫(以上皮性為主) |
| 瞳孔 | 中度散大,對光反射減弱 |
| 前房 | 淺(伴虹膜膨隆) |
| 結膜 | 睫狀充血,靜脈淤血 |
| 水晶體 | 青光眼斑 |
隅角鏡檢查可見廣泛的虹膜與小樑網接觸(ITC)3)。對側眼的隅角檢查也通常顯示閉塞隅角的風險徵象3)。當角膜水腫導致隅角鏡檢查困難時,AS-OCT或超音波生物顯微鏡檢查是有用的2)。
在一例奧蘭扎平誘發的AAC病例中,用藥一週後,右眼眼壓為51 mmHg,出現微囊性角膜水腫、中度固定性瞳孔散大、虹膜膨隆伴淺前房1)。超音波生物顯微鏡證實360度隅角閉塞,未觀察到脈絡膜滲出1)。
藥物誘發的AACG根據誘發機制可分為瞳孔阻塞型和非瞳孔阻塞型。
| 藥物分類 | 代表藥物 | 機制 |
|---|---|---|
| 散瞳藥/睫狀肌麻痺藥 | 去氧腎上腺素、托吡卡胺 | 瞳孔阻塞 |
| 三環抗憂鬱藥 | 阿米替林、丙咪嗪 | 瞳孔阻塞 |
| SSRI | 帕羅西汀、艾司西酞普蘭 | 瞳孔阻滯/葡萄膜滲出 |
| 抗精神病藥 | 奧氮平 | 瞳孔阻滯 |
| 抗癲癇藥 | 托吡酯 | 非瞳孔阻滯 |
| 支氣管擴張藥 | 異丙托溴銨 | 瞳孔阻滯 |
引起瞳孔阻滯型青光眼的藥物
具有散瞳/調節麻痺作用的藥物:去氧腎上腺素、托吡卡胺、環噴托酯、阿托品1)
具有抗膽鹼作用的全身用藥:三環抗憂鬱藥、抗精神病藥(奧氮平)、苯二氮平類(地西泮)、抗組織胺藥1, 2)
具有交感神經刺激作用的藥物:腎上腺素、地匹福林、鼻腔充血解除劑(含去氧腎上腺素)、非法興奮劑(古柯鹼、搖頭丸)2)
其他:肉毒桿菌毒素(眼周注射)、丙吡胺(抗心律不整藥)
非瞳孔阻滯型的致病藥物
托吡酯:因睫狀體上腔滲出、睫狀體前旋、水晶體膨脹導致前房變淺。通常在給藥開始2週內發病,幾乎均為雙眼性2, 3)
磺胺類藥物:因水晶體膨隆、視網膜水腫、脈絡膜滲出導致繼發性前房變淺
SSRI(部分):艾司西酞普蘭、文拉法辛已被報告伴有葡萄膜滲出的雙眼性隅角閉塞2)
抗凝血藥:自發性脈絡膜出血導致虹膜-水晶體膈前移
具有散瞳或調節麻痺作用的藥物,可在具有淺前房、厚水晶體等解剖易感因素的眼睛中誘發APACA2)。這是因為散瞳會增強瞳孔阻滯和隅角擁擠2)。具體包括SSRI抗憂鬱藥、三環抗憂鬱藥、鼻腔充血解除劑(含抗組織胺藥)、抗膽鹼藥、交感神經興奮藥、止吐藥2)。
霧化吸入支氣管擴張劑(異丙托溴銨、沙丁胺醇)也可誘發急性隅角閉塞3)。全身麻醉期間或麻醉後也可能發生急性隅角閉塞3)。
大致分為兩種機制。瞳孔阻滯型由具有散瞳作用的藥物(交感神經興奮藥、抗膽鹼藥、三環抗憂鬱藥、SSRI、抗精神病藥、苯二氮平類、支氣管擴張劑)引起。非瞳孔阻滯型中,托吡酯和磺胺類藥物引起睫狀體水腫、脈絡膜滲出,將虹膜-水晶體膈向前推擠,從而誘發隅角閉塞。兩種情況均在有解剖易感因素(淺前房、窄隅角、遠視眼)的患者中風險更高。
藥物誘發性AACG的診斷需要評估臨床表現並詳細詢問用藥史。由於急性隅角閉塞中有很高比例是由外用或全身藥物誘發的,因此必須確認包括處方藥和非處方藥在內的完整用藥史3)。
隅角鏡檢查應在雙眼進行2)。即使角膜水腫導致患眼隅角鏡檢查困難,對側眼的發現也有助於診斷2)。
**前眼部光學同調斷層掃描(AS-OCT)和超音波生物顯微鏡(UBM)**即使在角膜水腫的情況下也能評估前房深度、隅角形態和睫狀體狀態2)。超音波生物顯微鏡特別有助於識別睫狀體腫脹或旋轉,這對非瞳孔阻滯型的診斷很重要。
為鑑別繼發性原因,如果對側眼表現為開角、深前房,患眼角膜相對透明,或存在虹膜新生血管,則需注意2)。
綜合評估用藥史、水晶體狀態、隅角和虹膜解剖以及急性隅角閉鎖的側別(單側/雙側)有助於明確病因。雙側急性隅角閉鎖罕見,但提示可能存在藥物相關機制,如托吡酯或SSRIs2)。
藥物誘導的AACG的治療首先應優先快速降低眼壓,並根據病因機制進行干預2)。
藥物治療
乙醯唑胺:當眼壓≥40mmHg時建議立即給藥。嘔吐或需要快速起效時,首選靜脈注射(10mg/kg)3)。
甘露醇:當對乙醯唑胺反應不足時考慮使用。以15-20%溶液靜脈注射0.5-1.5g/kg3)。
毛果芸香鹼:滴用1-2%滴眼液。括約肌缺血時無效,眼壓下降後可能出現縮瞳3)。
類固醇滴眼液:頻繁給藥(每日4-6次)以減輕炎症3)。
雷射手術治療
在一例奧氮平誘發的AAC病例中,使用噻嗎洛爾0.5%和溴莫尼定0.15%眼藥水、口服乙醯唑胺、毛果芸香鹼2%後,進行Nd:YAG雷射虹膜切開術,次日眼壓從51 mmHg降至20 mmHg,視力從6/200恢復至20/301)。對側眼也進行了預防性雷射虹膜切開術1)。
全身性藥物(乙醯唑胺、甘露醇)在老年或合併其他疾病的患者中需謹慎,可能引起從感覺異常、意識混亂到肺水腫、急性腎衰竭等嚴重副作用2)。
瞳孔阻滯是藥物誘發性AACG最常見的機轉3)。具有交感神經刺激或副交感神經阻斷作用的藥物誘發散瞳時,虹膜與水晶體的接觸面積增加1)。這增加了房水從後房經瞳孔流向前房的阻力,導致後房壓力超過前房壓力3)。
後房壓力升高導致虹膜向前膨隆(虹膜膨隆),周邊虹膜覆蓋小樑網,阻塞房水流出通道,引起眼壓急劇升高3)。括約肌和開大肌同時激活的中等散瞳狀態風險最高3)。
在奧氮平病例中,弱的抗膽鹼作用誘發散瞳,在解剖學易感眼中發生瞳孔阻滯1)。非典型抗精神病藥引起的隅角閉鎖青光眼罕見,與SSRI和三環抗憂鬱藥相比報告較少1)。
托吡酯和磺胺類藥物可因特異體質藥物反應引起睫狀體上腔滲出3)。這導致睫狀體向前旋轉,水晶體懸韌帶鬆弛和水晶體膨脹,使整個虹膜-水晶體隔膜前移,堵塞隅角2)。
這種機制可發生於開角或窄角患者。文拉法辛和艾司西酞普蘭引起的伴有葡萄膜滲出的雙眼急性隅角閉塞也有報導2)。
高坪虹膜形態是指位置靠前的睫狀突將周邊虹膜向前推,在散瞳時直接堵塞隅角3)。如果解除瞳孔阻滯後眼壓仍高,應懷疑高坪虹膜參與。
瞳孔阻滯型是由於散瞳使虹膜與水晶體接觸增加,阻礙房水從後房流入前房,導致虹膜向前膨隆堵塞隅角。散瞳藥、抗膽鹼藥和擬交感神經藥是原因,雷射虹膜切開術有效。而非瞳孔阻滯型是由托吡酯或磺胺類藥物引起的睫狀體水腫和脈絡膜滲出,將整個虹膜-水晶體隔膜向前推。虹膜切開術無效,停用致病藥物和睫狀肌麻痺劑是治療核心。雙眼發病強烈提示非瞳孔阻滯型。
2025年發布的國際共識中,提出了術語**APACA(急性原發性隅角閉塞發作)**用於急性原發性隅角閉塞發作2)。該術語強調了疾病的急性和緊急性質,並明確了與繼發性原因的區別2)。100%一致同意快速降低眼壓應優先於準確診斷2)。
共識聲明以88.24%的同意率確認,具有散瞳和睫狀肌麻痺作用的藥物可在有解剖易感性的眼中誘發APACA2)。對高風險患者處方此類藥物時需謹慎,詳細的用藥史是重要的診斷線索2)。
診斷性藥物散瞳在一般人群中是安全的,散瞳不足導致眼底疾病漏診的風險遠高於誘發隅角閉塞的風險3)。對於接受過適當預防性治療(雷射虹膜切開術)的隅角閉塞病史患者,散瞳通常是安全的3)。散瞳後預防性使用毛果芸香鹼縮瞳應避免,因為這可能導致瞳孔固定於中等散瞳位,增加隅角閉塞風險3)。