早期发病机制

外伤性青光眼(包括房角后退性青光眼)
1. 什么是外伤性青光眼?
Section titled “1. 什么是外伤性青光眼?”外伤性青光眼是由眼外伤引起的继发性青光眼。可由钝性(非穿孔性)外伤、穿通性外伤、化学外伤或放射线外伤引起。涉及开角型和闭角型两种机制 2)。尤其在钝性外伤后,可通过前房积血、房角后退、血影细胞性青光眼、晶状体脱位引起的瞳孔阻滞等多种机制导致眼压升高。
在急性期,房水生成功能常受影响,因此即使房水流出通道受损,眼压也不一定升高。此外,急性期眼压升高的机制涉及前房积血、炎症、晶状体损伤等多种因素同时参与。而且,可能在受伤后数年至十余年迟发性发病,因此长期随访必不可少 2)3)。
按外伤类型和发病时间的分类如下所示。
| 分类 | 发病时间 | 主要机制 |
|---|---|---|
| 钝性外伤·早期 | 受伤后即刻至数周 | 前房积血、小梁网破坏、外伤性虹膜炎 |
| 钝性外伤·迟发 | 数月至数十年 | 房角后退、血影细胞性青光眼、小梁网瘢痕化 |
| 穿通性外伤 | 急性至慢性 | 虹膜前粘连、上皮植入、铁锈症 |
| 化学性外伤 | 急性至慢性 | 炎症和瘢痕化导致的流出道障碍 |
| 放射性外伤 | 迟发性 | 视网膜缺血和新生血管性青光眼 |
房角后退的概念最早由Collins于1892年报道。1949年,D’Ombrain指出外伤与单眼青光眼的关联,1962年Wolf和Zimmer首次系统性地通过6个病例展示了外伤、房角后退和青光眼发病的连锁关系。后续研究将房角后退性青光眼确立为继发性开角型青光眼的代表性类型。
钝性眼外伤后房角后退和青光眼发病的主要流行病学数据如下所示。
- 非穿孔性眼外伤眼中,高达60% 发生房角后退。
- 伴有外伤性前房积血的病例中,房角后退的发生率为 60–100%。
- Girkin等人对美国眼损伤登记处的分析显示,钝性外伤后6个月的外伤性青光眼发病率约为 3.4% 6)。
- Kaufman和Tolpin对31只眼进行的10年前瞻性研究显示,房角后退病例中长期进展为青光眼的约占 6% 7)。
- 当房角后退范围达到 180度或以上 时,10年内 6–20% 的病例会发展为青光眼。
- 发病时间从数天到数年不等,有报告称最晚可在 50年后 发病。
- 约50%的ARG患者对侧眼也会发生开角型青光眼,提示存在体质易感性5)。
常见致伤原因包括运动(球类外伤、拳击、球拍等)、格斗、暴力袭击、交通事故和职业伤害。在儿童中,还需鉴别家庭内的撞击和虐待。婴幼儿和儿童中,如果前房出血持续超过两周,可能导致形觉剥夺性弱视,因此需要比成人更早的积极干预。钝性外伤导致的闭合性眼球损伤被认为是一系列病变,包括前房出血、虹膜根部离断、房角后退、晶状体偏位、视网膜震荡和眼底挫伤。
许多研究报告男性占优势,这反映了致伤原因(运动和暴力袭击多见于男性)。年龄分布以青中年多见,但由于迟发性发病,受伤年龄与发病年龄之间常有较大差距。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”急性期眼压升高时,患者会因角膜水肿出现视物模糊、眼痛和恶心。伴有前房出血时会出现视力下降和畏光。眼压急剧升高可引起头痛和呕吐,有时会被误诊为急性闭角型青光眼发作。慢性期高眼压无症状进展,常在视野缺损加重后才被发现。
房角后退本身没有自觉症状。合并前房出血时会出现相应症状。广泛的睫状体分离可导致低眼压性黄斑病变,引起视力下降。
前房出血:钝性外伤最常见的并发症。轻症时仅在裂隙灯显微镜下可见前房内有微量血液;中症时出现水平面(液平)。重症时前房充满血块,颜色从鲜红色变为暗红色或黑色。当前房完全被黑褐色血液占据时,称为8球前房出血(黑球前房出血),如果持续存在,需要早期手术干预。
前房积血的严重程度通常分为I级(前房积血少于1/3)、II级(1/3至1/2)、III级(超过1/2)和IV级(完全性,8球状)。级别越高,继发性出血、高眼压和角膜血染的发生率越高。每日记录积血的高度,以客观评估出血量的变化。视诊时,新鲜出血呈鲜红色,随时间推移变为暗红色和黑褐色,最终观察到黄橙色的纤维蛋白凝块。
房角后退:房角镜检查可见睫状体带增宽。从虹膜根部到巩膜突的距离增加,睫状体呈宽大的深灰色带状。由睫状体纵行肌和环形肌之间的撕裂引起。
角膜血染:严重前房积血伴持续高眼压时,角膜后表面被血液染色。即使出血消退后也可能导致永久性视力损害,因此需要早期进行前房冲洗。
血影细胞:玻璃体出血后1至4周,变性的红细胞作为卡其色小泡出现在前房。大量时可形成假性前房积脓。
睫状体分离:睫状体从巩膜脱离的状态。房水流入脉络膜上腔,导致持续性低眼压。长期存在可引发低眼压性黄斑病变。
虹膜根部离断:虹膜根部从巩膜突脱离。裂隙灯显微镜检查可见新月形或半月形裂隙。如果断裂范围广泛并伴有瞳孔偏位,可导致视力下降或单眼复视。常伴有晶状体悬韧带断裂导致的玻璃体脱出。
外伤性瞳孔散大:钝性外力导致瞳孔括约肌断裂,瞳孔散大。对光反射和近反射均减弱或消失。对1%盐酸毛果芸香碱滴眼液无反应或反应减弱。裂隙灯显微镜检查可见瞳孔缘切迹样不规则。需与头部外伤引起的动眼神经麻痹鉴别,检查有无上睑下垂和眼球运动障碍。
晶状体异常:可包括晶状体震颤(phacodonesis)所提示的半脱位、完全脱位或外伤性白内障。晶状体脱位可导致瞳孔阻滞或晶状体溶解性青光眼。
眼压的双相性:受伤后即刻,由于睫状体房水生成功能下降,眼压可能轻度降低;随后,房角后退导致睫状体血管破裂,血液成分阻塞小梁网,引起眼压急剧升高。本症的特点是受伤后眼压可表现为低、正常或高三种状态。
钝性眼外伤的特征性表现
Section titled “钝性眼外伤的特征性表现”以下是钝性眼外伤后常与房角后退并存的表现。
| 表现 | 部位 | 意义 |
|---|---|---|
| 虹膜括约肌断裂 | 虹膜 | 外伤的直接征象 |
| 福修斯环 | 晶状体前囊 | 虹膜色素印迹 |
| 虹膜根部离断 | 虹膜根部 | 重度外伤的指标 |
| 前房积血 | 前房 | 常合并房角后退 |
| 血影细胞 | 前房 | 玻璃体出血后1~4周 |
3. 原因和风险因素
Section titled “3. 原因和风险因素”钝挫伤导致眼压升高的机制
Section titled “钝挫伤导致眼压升高的机制”迟发性机制
穿通伤导致眼压升高的机制
Section titled “穿通伤导致眼压升高的机制”在穿通伤中,除前房积血和晶状体脱位外,还涉及以下机制。
- 虹膜后粘连引起的瞳孔阻滞
- 晶状体溶解性青光眼
- 上皮植入(epithelial downgrowth)
- 铁锈症(siderosis bulbi)导致的小梁网损伤(眼内异物残留时)
- 长期浅前房引起的虹膜前粘连
化学伤与放射伤
Section titled “化学伤与放射伤”碱或强酸引起的化学伤中,炎症导致的瞳孔阻滞、虹膜前粘连以及小梁网组织本身的炎症和瘢痕化是眼压升高的原因。尤其是碱烧伤,对眼内深部渗透性强,容易引起严重的前段损伤和继发性青光眼。放射伤可因视网膜缺血导致新生血管性青光眼。
青光眼化的风险因素
Section titled “青光眼化的风险因素”钝挫伤后房角后退进展为青光眼的风险增加因素包括:
- 后退范围:180度以上(部分作者认为240度以上)
- 房角色素沉着增加
- 基线眼压升高
- 晶状体偏位
- 对侧眼的青光眼表现:约50%的房角后退性青光眼患者对侧眼也会发生开角型青光眼,提示原本有青光眼易感因素的眼中,外伤加速了病程 5)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”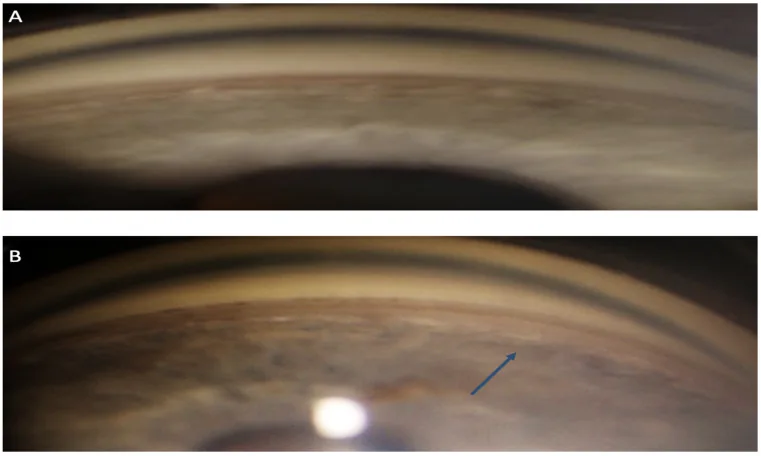
问诊内容包括受伤机制(外力方向、强度、受伤时间)、既往史、用药史(抗凝药使用情况)、全身疾病(镰状细胞病家族史、出血倾向)。
基本检查包括视力检查、对光反射检查、非接触式或压平眼压计测量眼压、裂隙灯显微镜检查。评估前房积血量、晶状体位置异常、虹膜离断的有无、前房内炎症细胞和闪辉的程度。若前房积血量大,还需检查对侧眼的间接对光反射。进行Seidel试验(荧光素染色下观察角膜伤口渗漏)以排除角膜穿孔。
眼底检查应在生理性散瞳或无散瞳眼底相机下进行,以避免散瞳诱发出血。评估有无玻璃体积血、视网膜震荡(commotio retinae)、脉络膜破裂、视网膜脱离。
若出现严重的结膜水肿、前房积血、低眼压、结膜下出血,应怀疑眼球破裂,立即进行影像学检查(CT)。需避免过度压迫眼球,原则上不使用压平眼压计和超声生物显微镜(UBM)。
房角镜检查是诊断房角后退的金标准。确认睫状体带增宽以及从虹膜根部到巩膜突的距离增加。必须与对侧眼(未受伤眼)进行比较4)。由于正常眼也可能有较宽的睫状体带,因此通过与健侧眼并列观察才能确认病理性增宽。
日常诊疗中使用间接房角镜(Goldmann房角镜、Zeiss四面镜)。房角开大度的评估采用Shaffer-Kanski分类、Scheie分类、Spaeth分类。Shaffer-Kanski分类将房角开大度分为0~4级,4级(35~45度)表示最大开大,无房角关闭可能;0级(无法观察)表示关闭状态。直接房角镜(Koeppe、Swan-Jacob等)用于手术时或婴幼儿检查。
房角镜检查时,除了记录房角开放程度和色素沉着程度外,还应详细记录周边虹膜前粘连(PAS)、Sampaolesi线、房角新生血管、残留硅油、房角结节、前房积血、房角后退、房角发育异常以及青光眼术后房角变化等所见。外伤眼常观察到房角色素沉着增加,这被认为是青光眼化的危险因素之一。
前房积血残留期间,因存在再出血风险,受伤后1~2周内应避免房角镜检查。出血消退后进行详细的房角评估。
| 检查 | 适应症 | 注意事项 |
|---|---|---|
| CT / X线 | 眼内异物探查 | 对金属异物的检出有用 |
| MRI | 非金属异物的评估 | 怀疑含铁异物时禁忌 |
| B超 | 前房积血导致眼底无法窥见时 | 门诊可简便实施 |
| 超声生物显微镜(UBM) | 评估睫状体分离和睫状体水肿 | 接触式,穿孔性外伤禁忌 |
| 眼前节OCT | 房角结构的定量评估 | 非接触、安全,睫状体不可见 |
UBM可以观察从虹膜根部到睫状体的细微结构,因此对评估睫状体分离和房角后退很有用。眼前节OCT是非接触、非侵入性的,分辨率高,但难以观察睫状体。
当表现为单眼开角型青光眼时,与以下疾病的鉴别很重要:
- 激素性青光眼(单眼局部使用激素史)
- UGH综合征(葡萄膜炎-青光眼-前房积血综合征)
- ICE综合征(虹膜角膜内皮综合征)
- 颈动脉海绵窦瘘
- 假性剥脱性青光眼
- 色素性青光眼
- 视网膜母细胞瘤(儿童,与非外伤性前房积血鉴别)
第5版青光眼诊疗指南指出,继发性开角型青光眼中,房水流出阻力主要位于小梁网的病因包括外伤、葡萄膜炎、晶状体物质、眼内异物等4)。该指南明确说明,房角镜检查可见“外伤性改变如房角分离或睫状体带增宽(房角后退)”,强调了房角镜检查的重要性4)。
本病的诊断需要确定眼压升高的机制和原发病因,治疗原发病因是治疗策略的第一步。由于多种机制常并存,需要全面评估整个眼球的创伤性改变,包括前房积血、虹膜炎、晶状体异常、视网膜挫伤、脉络膜破裂等。
长期随访的考虑
Section titled “长期随访的考虑”对于有钝性眼外伤史的患者,建议伤后至少每年进行一次眼压测量、房角镜检查、视乳头评估和视野检查。特别是房角后退达180度以上的病例,最好终身随访。同时应注意对侧眼的眼压和视神经变化。
使用光学相干断层扫描(OCT)测量视网膜神经纤维层(RNFL)厚度和视乳头周围神经节细胞复合体(GCC)厚度,可在早期视野异常出现之前检测到青光眼性视神经病变,因此对长期随访有用。标准视野检查采用Humphrey 24-2或30-2 SITA Standard,每年进行1-2次。由于单次眼压测量不能反映昼夜波动,对于异常值或怀疑进展的病例应进行昼夜波动测量。
5. 标准治疗方法
Section titled “5. 标准治疗方法”急性期的保守治疗(前房积血的管理)
Section titled “急性期的保守治疗(前房积血的管理)”外伤性前房积血以休息和药物治疗为主。患者应保持坐位或床头抬高30-45度休息。禁止剧烈运动,儿童或前房积血平面超过前房1/3至1/2的病例建议住院治疗。
急性期的药物治疗基于以下方案。
- 散瞳药:阿托品滴眼液(1%)每日1次睡前(消炎和减轻房角压力)
- 类固醇滴眼液:倍他米松(0.1% Rinderon)每日4次
- 止血药:卡巴克络(Adona片 30mg)每次1片,每日3次,饭后服用
- 降眼压药(眼压升高时):
- β受体阻滞剂:噻吗洛尔(0.5% Timoptol)每日2次
- 碳酸酐酶抑制剂:乙酰唑胺(250mg 迪阿莫克斯)2片,每日2次
- 补钾:门冬氨酸钾(300mg 阿斯帕拉)2片,每日2次
- 高渗剂:眼压急剧升高时静脉滴注甘露醇
盐酸毛果芸香碱绝对禁忌。它不仅会加重炎症,还会扩大房角,增加出血和再出血,并可能诱发恶性青光眼。前列腺素类药物也可能增强急性炎症,因此急性期应避免使用。
使用散瞳药(阿托品)的目的是通过麻痹睫状肌减轻疼痛、减少对房角的机械应力,并预防虹膜后粘连。为避免过度散瞳导致周边房角变窄,首选阿托品而非其他强效散瞳药。
局部皮质类固醇滴眼液(如倍他米松)有助于平息虹膜炎、抑制小梁网炎症并预防再出血。但在类固醇反应阳性者中,眼压可能升高,因此用药后需频繁测量眼压。如果出现眼压升高,考虑改用较弱的类固醇,如氯替泼诺或氟米龙。
眼压耐受时间指南
Section titled “眼压耐受时间指南”在健康的年轻患者中,眼压50 mmHg可耐受5天,35 mmHg可耐受7天,对视神经的风险可接受。如果已存在青光眼性视神经病变、前房积血严重或有角膜血染风险,则无需等待上述时间,应迅速进行前房冲洗。
前房冲洗的适应证和时机
Section titled “前房冲洗的适应证和时机”在以下情况下进行手术前房冲洗:
- 最大药物治疗下眼压控制不佳
- 持续的全前房积血(8球积血)
- 角膜血染的迹象
- 再出血
前房冲洗的最佳时机是伤后第4天左右,此时再出血风险较低,血凝块已部分与眼组织分离。手术通过角膜侧切口使用前房灌注针(Simcoe针)进行。如果血凝块大且硬,可用镊子取出或用玻璃体切割器切除并吸出。
再出血易发生于伤后3~7天,发生率报道为5%~10%2)。再出血通常比初次出血量更大,并发症风险也增加。有报道称抗纤溶药物(如氨甲环酸)对预防再出血有效,但对视力预后的影响尚不明确2)。
外伤后炎症消退后的眼压升高与小梁网瘢痕化和虹膜前粘连有关。当多种降眼压药物控制不佳时,需考虑手术3)。
药物治疗
房水生成抑制剂:β受体阻滞剂、碳酸酐酶抑制剂、α2受体激动剂有效。
前列腺素类似物:急性炎症消退后可使用。其优点是通过增加葡萄膜巩膜流出通道,绕过功能不全的小梁网2)。
禁忌:毛果芸香碱(缩瞳药)因会加重房角后退,故禁用。
激光治疗
氩激光小梁成形术(ALT):有报道称长期降眼压效果不佳。
选择性激光小梁成形术(SLT):对IRIS注册库中560例患者的分析显示,18个月时失败率为48%,高于一般人群(41%)5)。
手术治疗
由于外伤或反复手术导致结膜粘连和瘢痕化,滤过手术常较困难。在某些情况下,Ahmed青光眼阀或Baerveldt青光眼植入物等引流管植入术可作为首选3)。难治性病例也可选择睫状体破坏术(经巩膜睫状体光凝术、内镜下睫状体光凝术)。
在鬼影细胞性青光眼中,除了使用降眼压药物外,还建议通过前房冲洗和玻璃体手术清除鬼影细胞2)。如果存在晶状体偏位或损伤,则需要摘除晶状体。如果存在瞳孔阻滞,应同时进行激光虹膜切开术或晶状体摘除术。
外伤眼常伴有结膜和Tenon囊瘢痕化以及眼前段解剖结构改变,因此手术难度高于一般青光眼手术。术前评估结膜活动性、虹膜、晶状体和睫状体结构,以及了解现有伤口和人工晶状体固定状态,在计划阶段至关重要。根据术中所见灵活选择手术方式,并确保术后长期管理,将影响预后。
睫状体分离(cyclodialysis cleft)所致低眼压的治疗
Section titled “睫状体分离(cyclodialysis cleft)所致低眼压的治疗”对于睫状体分离引起的持续性低眼压,首先进行保守的药物治疗。
- 阿托品滴眼液(1%)每日1次,睡前使用
- 氟米龙滴眼液(0.1%氟美瞳)每日4次
如果药物治疗无效,则考虑手术治疗。可选择的方法包括:对分离区进行氩激光光凝、睫状体透热凝固、经巩膜冷冻凝固、巩膜扣带术、睫状体分离直接缝合、前部玻璃体手术等。如果低眼压性黄斑病变持续存在,及时的手术干预可改善视力预后。
小范围(1-2个钟点)的睫状体分离有时可通过自然闭合或药物治疗缓解,但广泛分离仅靠被动观察难以愈合。近年来,有报道采用前部玻璃体手术联合气体填充、直接缝合闭合、内镜下激光光凝等微创技术。治疗方法的选择需考虑分离范围、眼内状态和角膜透明度。
再出血容易在受伤后3至7天发生,发生率据报道为5-10%2)。这与初始血凝块开始退缩和溶解的时间一致。再出血通常比初次出血量更大,并发症风险也增加。保持安静、使用散瞳药物、考虑停用抗凝药物很重要。对于儿童或前房出血超过前房1/3至1/2的情况,建议住院管理。
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”钝性外伤的力学
Section titled “钝性外伤的力学”钝性外伤时,眼球壁变形,对附着在内的虹膜睫状体产生牵拉力或剥离力。微细组织损伤破坏血-房水屏障,炎症细胞游出至前房。瞳孔括约肌受损导致外伤性散瞳。
最易受损的部位是虹膜附着于睫状体的薄弱部分。此处断裂导致虹膜根部离断,瞳孔移位。稍向巩膜侧的睫状体内出现裂隙则形成房角后退,进一步在巩膜侧睫状体从巩膜剥离则形成睫状体分离。这些病变尤其容易发生前房积血。
房角后退的发生机制
Section titled “房角后退的发生机制”钝性外力导致前房内压急剧升高时,角膜缘伸展,房水向后房和房角移动。这使虹膜根部受到牵拉,在睫状肌的纵行肌(Brücke肌)和环行肌(Müller肌)之间发生断裂。即房角后退是睫状体与虹膜一起向后移动的状态,也称为房角分离。
外力足够大时,睫状体动脉破裂导致前房积血。外伤性前房积血中房角后退发生率高达60-100%的原因在于这一共同的发病机制。即房角后退和前房积血并非独立病变,而是同一外力造成的连续性组织损伤。睫状体内动脉破裂导致前房内急剧出血,短时间内前房内压升高,可能对侧角膜内皮造成继发性损伤。
损伤部位的组织学特征如下:睫状体环行肌(Müller肌)位于内侧(晶状体侧),纵行肌(Brücke肌)位于外侧(巩膜侧)。两肌之间存在结缔组织层,这是力学上最薄弱的部位。钝性外力导致眼球前后缩短和随之而来的赤道部扩张,对睫状体施加强大的剪切力,结果在该结缔组织层产生裂隙。
眼压升高的机制
Section titled “眼压升高的机制”- 前房积血相关的红细胞、纤维蛋白和血小板阻塞小梁网
- Schlemm管直接损伤导致的早期眼压峰值
- 炎症产物和细胞碎片导致房水流出阻力增加
- 小梁网和Schlemm管瘢痕化、纤维化导致房水流出阻力慢性增加
- 由于睫状肌对巩膜突的张力丧失导致施莱姆管狭窄
- 覆盖小梁网的玻璃样膜增生
- 虹膜前粘连导致的继发性房角关闭
EGS指南将钝挫伤引起的继发性开角型青光眼列为:小梁网损伤、瘢痕化、炎症、红细胞和碎屑阻塞、房角后退、晶状体源性青光眼2)。强调外伤后经过极长时间才可能出现眼压升高2)。组织学上,在房角后退病例的小梁网中观察到不连续的玻璃样膜样物质增生,这种结构被认为长期增加房水流出阻力。
小梁网的瘢痕化在受伤后逐渐进展,受伤时正常的房水流出功能在数年至数十年间下降。因此,即使受伤后眼压正常,也不能排除将来发生青光眼的可能性。定期测量眼压以及评估视神经和视野是长期管理的关键。
血影细胞性青光眼的机制
Section titled “血影细胞性青光眼的机制”玻璃体出血后,如果红细胞在玻璃体中停留数周,细胞内容物大部分被吸收,形成仅含变性血红蛋白(海因茨小体)的中空胞体(血影细胞)。血影细胞与正常红细胞相比变形能力降低,无法通过小梁网,导致阻塞2)。当前玻璃体界面破坏且玻璃体与前房之间有交通时,血影细胞会移动到前房。由于前房内高氧分压和快速循环,仅前房出血不易形成血影细胞2)。
晶状体相关性青光眼
Section titled “晶状体相关性青光眼”外伤导致晶状体囊破裂,晶状体物质漏出,沉积在小梁网上导致眼压升高(晶状体溶解性青光眼)。主要机制是吞噬晶状体皮质的巨噬细胞阻塞小梁网。也可能发生对晶状体蛋白的III型过敏反应(晶状体过敏性青光眼)。
穿通性外伤特有的机制
Section titled “穿通性外伤特有的机制”上皮植入是指通过穿通创口进入前房的上皮细胞覆盖小梁网、角膜内皮和虹膜前面,阻碍房水流出。治疗极为困难,有时选择切除受累组织并冷冻治疗,但预后不良。
纤维植入是指通过穿通创口成纤维细胞向前房内增殖的病变,其进展比上皮植入缓慢,但同样难以治疗。
铁锈症(siderosis bulbi)是指含铁眼内异物溶出的铁离子对房角细胞、晶状体上皮、视网膜色素上皮等细胞产生毒性作用的全层性病变。特别是沉积在房角会导致慢性房水流出障碍。电生理检查(ERG)早期即可发现b波振幅降低,是全层性损伤的指标。早期摘除眼内异物对预防至关重要。
睫状体分离导致的低眼压黄斑病变
Section titled “睫状体分离导致的低眼压黄斑病变”睫状体分离时,形成从睫状体到脉络膜上腔的房水引流通道(葡萄膜巩膜流出通道的侧支),导致持续性低眼压。长期存在会引起视网膜脉络膜皱襞和黄斑水肿,导致低眼压黄斑病变(hypotony maculopathy)和视力障碍。关闭分离部位需要睫状体缝合、透热凝固或玻璃体手术等外科治疗。
低眼压黄斑病变的发病机制是眼压降低导致眼球壁变形,引起视网膜下液移动、脉络膜皱襞和视乳头水肿,损害黄斑部光感受器功能。如果眼压低于6 mmHg并持续数周,可能导致不可逆的视力下降,因此早期诊断和治疗至关重要。治疗目标是使眼压恢复到10 mmHg以上,阻止解剖学变化的进展。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”Ahmed青光眼阀的睫状沟植入法
Section titled “Ahmed青光眼阀的睫状沟植入法”外伤性青光眼涉及多种机制,需要根据个体情况确定眼压升高的原因并制定治疗策略2)。近年来,有报道将Ahmed青光眼阀(AGV)的引流管植入睫状沟的技术,与前房植入相比,具有角膜内皮细胞损失较少的优点1)。然而,根据Asaoka等人的研究,传统简单植入法首次尝试的成功率仅为54%,4.4%的病例甚至无法完成睫状沟植入1)。
Nitta等人(2023)报道了一种使用23G针头制作可靠引导通道的4-0尼龙引导法1)。与21G/23G针头引导法相比,该方法由于水平植入,虹膜干扰风险较低,并可排除引流管误入玻璃体腔的风险。即使在散瞳不良或人工晶体晃动眼中也能实现准确的睫状沟植入1)。
病例报告(Nitta 等 2023)1):对一名88岁女性房角后退性青光眼患者施行了本手术。患者合并假性剥脱综合征,瞳孔散大不良(最大瞳孔直径3.5 mm),并有轻度IOL晃动。术前眼压40 mmHg,术后1个月眼压降至10 mmHg(未使用眼药水),未观察到角膜内皮细胞密度减少。
在外伤性青光眼的管理中,预计在以下领域将取得临床研究进展。
- 构建房角后退程度与青光眼发病风险的预测模型
- 开发前房出血后小梁网损伤的无创评估方法
- 确立外伤眼的最佳手术策略(引流管植入术 vs 滤过手术 vs MIGS)
- 明确血影细胞性青光眼的早期干预标准
- 扩大微创青光眼手术(MIGS)在外伤性青光眼中的适应证
- 利用仿生材料进行小梁网重建的基础研究
- 利用人工智能自动分析房角图像并检测房角后退
- 阐明遗传易感性与外伤性青光眼发病的关联(对侧眼青光眼发病机制)
这些研究动向有望为伤后个体化医疗和长期预后改善做出贡献。
8. 参考文献
Section titled “8. 参考文献”-
Nitta K, Akiyama H. A New Technique Using a 4-0 Nylon Thread as a Guide for Easy and Precise Tube Insertion of Ahmed Glaucoma Valve Implant Into Ciliary Sulcus. Cureus. 2023;15(2):e34854.
-
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2021;105(Suppl 1):1-169.
-
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
-
日本緑内障学会 緑内障診療ガイドライン作成委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
-
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. Ophthalmology. 2021;128(1):P71-P150.
-
Girkin CA, McGwin G Jr, Long C, et al. Glaucoma after ocular contusion: a cohort study of the United States Eye Injury Registry. J Glaucoma. 2005;14(6):470-473.
-
Kaufman JH, Tolpin DW. Glaucoma after traumatic angle recession. A ten-year prospective study. Am J Ophthalmol. 1974;78(4):648-654.
-
Wiggins RE Jr, Vaphiades M, Crouch ER Jr. Sickle cell trait and secondary glaucoma following ocular trauma. J Ocul Pharmacol Ther. 1995;11(2):201-205.
