解剖学易感因素

急性青光眼发作(急性原发性闭角型青光眼)
1. 什么是急性青光眼发作?
Section titled “1. 什么是急性青光眼发作?”急性青光眼发作是一种眼科急症,由于房角快速关闭导致眼压突然且严重升高。眼压常达40–80 mmHg,若数小时内未进行适当处理,将发生不可逆的视神经损伤。它被认为是眼科医疗中最紧急的疾病之一。
亚太青光眼学会(APGS)和亚太眼科教授学会(AAPPO)在2025年国际共识中提议将术语统一为急性原发性房角关闭发作(APACA)1)。该术语强调疾病的急性和紧急性,并有意排除“青光眼”一词,因为及时治疗可能预防青光眼性视神经病变1)。APGS 2025小组投票以94.11%的同意率采纳。
流行病学上,该病在华人及亚洲人群中最为常见,年发病率报道为每10万人6至16例1)。而欧美白人的发病率仅为每10万人2至4.1例,亚洲人高出约3至4倍1, 14)。Day等人的系统综述报告了欧洲裔人群中原发性闭角型青光眼的患病率,揭示了显著的种族差异14)。此外,亚洲患者的视功能预后较欧美患者差。Aung等人在新加坡的长期随访研究显示,在4至10年的随访中,17.8%的患眼失明,47.8%出现青光眼性视神经病变,57%的矫正视力低于6/9斯内伦1, 7)。在日本,多治见研究显示40岁以上人群中原发性闭角型青光眼(PACG)的患病率为0.6%,而久米岛研究为2.2%,存在地区差异,尤其是冲绳县闭角型青光眼频率较高2)。根据Quigley等人的全球估计,到2020年,全球原发性闭角型青光眼患者人数将达到约2100万,其中亚洲地区占大部分10)。
发作发生在解剖学上具有易感因素的眼睛,并叠加某种诱因。典型情况是短眼轴、浅前房、远视的老年女性,在使用抗胆碱能药物或散瞳药后,或因长时间低头工作或夜间自然散瞳而诱发。动物实验表明,当眼压持续在50 mmHg以上超过12小时时,视网膜神经纤维、神经节细胞和视神经会发生不可逆损伤1),因此从发病到开始治疗的时间对视力预后影响很大。
急性发作的概念在历史上早已被认识,传统上使用了多种名称,如“急性闭角型青光眼(AACG)”、“急性青光眼发作”、“急性闭角危象(AACC)”和“急性原发性房角关闭(APAC)”等1)。APGS 2025为整理这些混杂术语,将APACA定为推荐术语,明确了其急性、紧急性和原发性1)。此外,特意不包含“青光眼”一词,暗示通过及时治疗有可能避免青光眼性视神经病变1)。但需注意,即使眼压恢复正常,缺血再灌注损伤仍可能导致视网膜神经节细胞持续丢失1)。
本病发病越晚,预后越差。在老年患者中,合并症多、就诊延迟、就诊时眼压高的病例,仅靠传统药物治疗往往无法获得足够的眼压下降1)。学历、从症状出现到治疗的时间、就诊时眼压已被确定为失明的独立危险因素1),因此公众教育活动和快速治疗可及性成为公共卫生挑战。
在APGS 2025共识1.3中,“急性青光眼发作是眼科急症,必须立即降低眼压”这一表述以100%的同意率获得通过1)。此外,共识1.9以100%的同意率确认“虽然准确诊断很重要,但临床怀疑本病时应优先快速降低眼压”1)。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”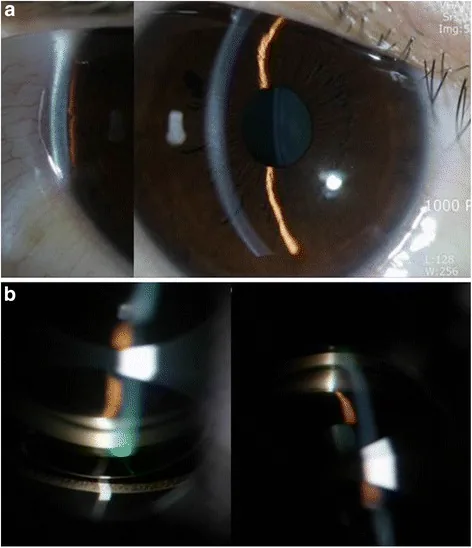
急性青光眼发作的特点是主观症状和客观体征均十分剧烈。然而,也存在缺乏所有表现的非典型病例,经验不足的临床医生可能会漏诊1)。
主观症状(三联征)
Section titled “主观症状(三联征)”随着眼压急剧升高,出现以下强烈的主观症状。
- 剧烈眼痛:单侧眼球或眼眶深部的剧痛
- 同侧头痛:放射至前额或颞部
- 恶心呕吐:消化道症状突出,有时被误诊为急性胃肠炎或蛛网膜下腔出血1)
- 视物模糊和视力下降:由于角膜水肿
- 虹视(光晕):看到光源周围有彩虹色光环
- 结膜充血
当全身症状如剧烈头痛、恶心、呕吐先出现时,存在被误诊为神经系统疾病或消化系统疾病的风险1)。APGS 2025强调这些全身症状是重要的诊断线索1)。
| 所见 | 特征 |
|---|---|
| 眼压 | 显著升高(40–80 mmHg)1) |
| 角膜 | 上皮水肿导致雾状混浊 |
| 前房 | 极浅(前节OCT显示ACD约1.3–1.5 mm) |
| 瞳孔 | 中度散大,对光反射减弱或消失 |
| 结膜 | 睫状充血及结膜血管淤血 |
| 房角 | 广泛房角关闭(双眼确认) |
| 晶状体 | 青光眼斑(晶状体上皮缺血性坏死)1) |
| 视盘 | 急性期可见视盘水肿、静脉怒张、视盘出血 |
中等度散瞳是瞳孔括约肌和开大肌同时被激活的位置,此时相对性瞳孔阻滞和瞳孔缘虹膜-晶状体接触达到最大。此外,严重的眼压升高导致瞳孔括约肌缺血,光反射消失。APGS 2025共识1.6推荐使用Goldmann压平眼压计测量和记录眼压1)。
慢性闭角型青光眼(CACG)的眼压升高为20–30 mmHg的中等程度,充血轻微或缺如,自觉症状不明显,以此与急性发作相区别。
3. 原因与风险因素
Section titled “3. 原因与风险因素”急性青光眼发作的发病涉及解剖学易感因素和诱发因素两个方面。
发病诱因
散瞳药:眼科检查时使用的滴眼液,如托吡卡胺、去氧肾上腺素等1)。
抗胆碱药:胃镜检查前用药、安眠药、抗精神病药等1)。
三环类抗抑郁药、SSRI:由于中枢性副交感神经阻断和散瞳作用1)。
鼻腔减充血剂:含抗组胺药、含去氧肾上腺素的药物1)。
拟交感神经药、止吐药:均通过散瞳作用增强瞳孔阻滞和房角拥挤1)。
生活场景诱因:长时间阅读、缝纫等低头姿势,暗室或夜间自然散瞳。
APGS 2025共识1.8以88.24%的同意率确认,具有散瞳和睫状肌麻痹作用的药物可在有解剖易感性的眼中诱发APACA1)。详细的用药史是诊断的重要线索。
进一步细分解剖因素,随着年龄增长晶状体终生增厚是决定性的。远视眼眼轴短、前房浅,更容易受到晶状体增厚的影响。增厚的晶状体将整个虹膜向前推,这称为晶状体因素。此外,瞳孔缘虹膜-晶状体接触增加,导致房水流出阻力增大,相对性瞳孔阻滞进展。组织学和影像学研究表明,随着年龄增长,睫状突位置前移,久米岛研究证实这是闭角型眼的特征2)。Wang等人的定量虹膜参数研究表明,虹膜厚度、虹膜曲率和虹膜面积与窄角显著相关,前段OCT图像分析证实虹膜前膨越明显的病例发作风险越高12)。
近视眼通常被认为发作风险较低,但并非绝对。Yong等人的横断面研究中,427例房角关闭患者中有94例患有近视,其中11例(11.7%)近视超过-5.0 D1)。APGS 2025共识4.1以94.11%的同意率采纳,近视眼不能完全排除房角关闭发作1)。风险主要取决于前房浅等解剖易感性,而非屈光或眼轴长度1)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”急性青光眼发作的诊断主要基于急性眼压升高与自觉症状及他觉体征相结合的临床诊断。APGS 2025共识1.6以94.11%的同意率采纳了“APACA是基于症状和体征的临床诊断”1)。然而,为与其他导致严重眼压升高的疾病鉴别,需要进行多项检查。
- 视力
- 眼压测量(Goldmann压平眼压计):APGS 2025推荐使用该眼压计进行测量和记录1)
- 角膜内皮细胞检查(镜面显微镜):激光虹膜切开术前的必需评估,内皮细胞计数低的病例激光后发生大疱性角膜病变的风险高2)
- 眼前节OCT:定量前房深度。发作时前房深度可浅至1.3–1.5 mm,可观察到角膜与虹膜几乎接触的表现。
- 眼轴长度测量:支持短眼轴(通常小于22 mm)
- 双眼房角镜检查:APGS 2025共识1.10以100%同意率认为双眼房角镜检查是必需的1)。即使患眼因角膜水肿观察困难,对侧眼的发现也有助于诊断1)
- 屈光检查(双眼):典型为远视性屈光。近视性屈光异常需考虑继发性青光眼的可能。
- 眼底检查(双眼):排除糖尿病视网膜病变、Vogt-小柳-原田病等继发性青光眼的病因。
当角膜水肿导致房角镜检查困难时,眼前段OCT和**超声生物显微镜(UBM)**很有用1)。特别是UBM可以评估睫状突和虹膜背面的形态,在诊断虹膜高褶和晶状体半脱位方面表现出色2)。此外,B型超声有助于排除脉络膜出血、脉络膜脱离、玻璃体出血等后段病变,对于药物和激光治疗无效的非典型病例是必需的1)。APGS 2025推荐这些影像学检查,但也明确指出不应为了检查而延迟降低眼压1)。
可能与急性青光眼发作混淆的疾病包括以下1)。
- 恶性青光眼:由睫状体前旋或房水异常流入玻璃体腔导致玻璃体前移引起。通过手术史和UBM表现鉴别。
- 继发性闭角型青光眼
- 新生血管性青光眼:如有虹膜新生血管(虹膜红变)表现则怀疑1)。
- 葡萄膜炎性青光眼如Posner-Schlossman综合征:尽管眼压升高,角膜相对透明,这是一个线索1)。
- 前部晶状体半脱位:当患眼浅前房、高眼压,但对侧眼为开角、深前房时怀疑1)。
在APGS 2025共识1.7中,以94.11%的同意率通过,当对侧眼为开角、深前房,患眼角膜相对透明,或观察到虹膜新生血管时,应积极怀疑继发性原因1)。当发现这些表现时,需要排除晶状体半脱位和新生血管性青光眼等可能改变侵入性治疗适应证的疾病。
5. 标准治疗方法
Section titled “5. 标准治疗方法”急性青光眼发作的治疗核心是急性期快速降低眼压和解除相对性瞳孔阻滞。发作解除后,长期管理对于适当的眼压控制和预防复发至关重要。青光眼诊疗指南第5版推荐将晶状体重建术作为APAC的一线治疗 2)。
发作时,应同时迅速给予以下药物。
| 药物 | 剂量和用法 | 作用和注意事项 |
|---|---|---|
| 20%甘露醇(高渗剂) | 1.0–2.0 g/kg 静脉滴注30–60分钟 2) | 眼压最低值出现在60–90分钟后,持续4–6小时。肾功能不全时有急性肾衰竭风险,心力衰竭/肺充血时有肺水肿风险 2) |
| 甘油(10%甘油) | 300–500 mL 静脉滴注45–90分钟 2) | 眼压最低值出现在30–135分钟后,持续约5小时。代谢产生葡萄糖;糖尿病患者慎用 2) |
| 1–2%毛果芸香碱盐酸盐 | 每小时滴眼2–3次 2) | 通过缩瞳解除瞳孔阻滞。在括约肌麻痹病例中,可能无法获得缩瞳,反而因睫状体前移有加重瞳孔阻滞的风险 2) |
| 乙酰唑胺 | 10 mg/kg口服或静脉注射2) | 通过抑制房水生成降低眼压。注意代谢性酸中毒和低钾血症。 |
| β受体阻滞剂滴眼液 | 每日两次 | 抑制房水生成 |
| α2受体激动剂滴眼液 | 每日2-3次 | 抑制房水生成并部分促进流出 |
| 0.1%倍他米松滴眼液 | 每日四次2) | 缓解发作时的炎症 |
| 盐酸阿普可乐定滴眼液 | 虹膜切开术前1小时和术后即刻 | 预防术后一过性眼压升高 |
使用毛果芸香碱需要谨慎判断。如果因高眼压导致瞳孔括约肌缺血,即使频繁给药也无法获得缩瞳效果,并且睫状肌的前移反而会加重瞳孔阻滞2)。初次给药时必须确认是否有缩瞳效果。全身吸收也可能引起腹痛等副交感神经刺激症状2)。
全身使用高渗药物在老年或合并其他疾病的患者中风险尤其高。细胞外液量急剧增加会给循环系统带来负担,在心力衰竭或肺淤血患者中可能导致肺水肿2)。甘露醇经肾排泄,因此在肾功能不全患者中,血浆渗透压升高和循环血容量增加可能导致急性肾衰竭2)。此外,发作时患者常已因呕吐而脱水,甘露醇的利尿作用可能进一步加重脱水2)。甘油在代谢过程中产生葡萄糖,每升含637千卡能量,因此糖尿病患者使用需谨慎2)。APGS 2025也指出,静脉注射乙酰唑胺和甘露醇可能引起从感觉异常、意识错乱到致死性肺水肿、急性肾衰竭等严重副作用,因此在老年或合并其他疾病的患者中,更希望采用替代治疗1)。
激光虹膜切开术(LPI)
Section titled “激光虹膜切开术(LPI)”当药物使眼压充分下降、角膜变透明后,进行激光虹膜切开术(laser peripheral iridotomy: LPI)。LPI是解除相对性瞳孔阻滞的根本治疗,在青光眼诊疗指南第5版中推荐等级为1A2)。
LPI的要点如下:
- 在角膜充分透明后进行。 通过不透明的角膜进行激光照射发生大疱性角膜病变的风险很高2)。
- 激光选择: 单独使用氩激光总能量大,角膜内皮损伤风险高,因此推荐单独使用Nd:YAG激光或氩激光联合YAG激光。
- 术前和术后立即使用阿普拉可乐定滴眼液: 预防术后一过性眼压升高。
- 照射部位: 安装虹膜切开接触镜(如Abraham、Pollak),照射虹膜最周边部。最好选择上眼睑能遮盖的位置,避免12点钟方向,因为气泡容易聚集在那里。
标准激光设置包括:氩激光第一阶段Stretch(200–400 μm,200 mW,0.2秒,2–10发)以伸展虹膜,第二阶段Thinner(50 μm,800–1000 mW,0.02秒,直至即将穿孔,考虑到内皮损伤,最好少于100发),以及Nd:YAG第三阶段(2.0–4.0 mJ,1–2发)完成穿孔。LPI的并发症包括前房出血、局限性白内障、再闭塞和大疱性角膜病变。
晶状体重建术
Section titled “晶状体重建术”青光眼诊疗指南第5版推荐**晶状体重建术(超声乳化吸除+人工晶状体植入)**作为APAC的一线治疗(推荐等级1A),认为其既能从根本上解除瞳孔阻滞,又能有效开放房角2)。但急性期的晶状体摘除术易发生并发症,因此建议由熟练的术者进行(推荐等级1B)2)。
APGS 2025指出,传统的“LPI后观察等待”方法存在重大局限性1)。Aung等人对亚洲人的长期随访显示,在110只LPI成功的眼中,64只眼(58.1%)出现慢性眼压升高,其中26例(40.6%)通过药物控制,但36例(56.3%)需要小梁切除术,2例(1.8%)失明1, 7)。此外,Aung等人的另一份报告分析了亚洲急性原发性房角关闭患者的长期眼压结局,表明仅靠LPI实现长期眼压控制的比例有限13)。基于这些证据,结论是单独LPI不足以进行长期管理,应尽早进行晶状体重建术1)。
英国的一项5年随访研究显示,即使在白种人群中,早期晶状体重建术与单独LPI相比,失明减少86%,眼压升高减少93%,药物需求减少69%,改善显著1)。APGS 2025共识3.2–3.3达成一致:早期晶状体重建术比单独LPI具有更好的长期效果,并且对APACA眼以较低的阈值进行晶状体重建术是合适的1)。共识3.4指出,发作解除后1–3个月进行晶状体重建术是最佳时机,等待更长时间会增加PAS形成和进展为慢性闭角型青光眼(CACG)的风险1)。
EAGLE试验是一项随机对照试验,展示了透明晶状体摘除术治疗原发性房角关闭疾病的长期结果。该试验纳入原发性房角关闭青光眼或眼压>30 mmHg的原发性房角关闭患者,随访36个月,结果显示早期晶状体摘除组在眼压控制、生活质量评分和成本效益方面均优于传统治疗组6)。Husain等人的随机对照试验比较了急性原发性房角关闭眼的一次性超声乳化术与激光周边虹膜切开术,2年随访显示超声乳化术组在眼压控制、周边前粘连减少和药物需求方面均更优8)。此外,Lai等人的前瞻性病例系列报告指出,对合并白内障的原发性房角关闭青光眼眼进行超声乳化术后,眼压、用药数量和房角开放程度均显著改善11)。Tham等人的另一项随机对照试验比较了药物治疗未控制的慢性原发性房角关闭青光眼(无白内障)的超声乳化术与小梁切除术,发现超声乳化术组术后并发症更少,长期眼压控制率相当或更优9)。
日本青光眼诊疗指南第5版也基于这些国际证据,明确将晶状体摘除术(推荐等级1A)列为原发性房角关闭青光眼和原发性房角关闭的治疗方法2)。美国眼科学会的《原发性房角关闭疾病优选实践模式》(2026年版)也将激光治疗和晶状体摘除术作为原发性房角关闭疾病的主要治疗选择3)。欧洲青光眼学会(EGS)第6版指南(2025年版)也更新了包括房角关闭疾病在内的青光眼诊疗标准框架4)。
APGS 2025推荐的替代治疗
Section titled “APGS 2025推荐的替代治疗”APGS 2025指出,传统的“药物→激光周边虹膜切开术→必要时小梁切除术或超声乳化术”的阶梯式方法对于迟发性或高眼压病例效果不足,并提出以下替代治疗作为早期选择1)。
氩激光周边虹膜成形术(ALPI)
激光瞳孔成形术(LPP)
机制:使用532 nm倍频激光烧灼瞳孔缘的虹膜,使其向外收缩,解除瞳孔阻滞。
优点:即使角膜透明度差也可施行;在3点和9点方向操作,即使患者伴有疼痛或恶心也易于操作。
证据:LPP单独或联合ALPI可在发作后2小时内显著降低眼压。
APGS 2025共识2.6以88.23%的同意率通过1)
前房穿刺(ACP)
机制:用30G针头或穿刺刀从3点或9点方向刺入,排出房水而不抽吸。由于30G针头的内腔摩擦,眼压自然稳定在12–15 mmHg 1)
优点:立即恢复正常眼压。即使在没有氩激光设备或熟练操作者的机构也可施行。
证据:在初始眼压低于60 mmHg的APACA眼中,比甘露醇输注在视力改善方面更优,且未观察到严重并发症1)
APGS 2025共识2.7以94.12%的同意率通过1)
角膜压陷(corneal indentation)
机制:使用小直径4镜房角镜(如Posner、Sussman等)或光滑的指尖通过眼睑压迫角膜,暂时开放房角,促进房水流出。
适应症:在眼科设备有限的地区进行初始处理。
APGS 2025共识4.4以88.23%的同意率通过1)
另一方面,对于药物无法控制的APACA眼,APGS 2025建议避免进行紧急小梁切除术和紧急晶状体乳化术1)。对于药物未控制的APACA眼,单独进行小梁切除术的成功率有限,据报道合格成功率为56.2%,完全成功率仅为9.4%1)。此外,在“hot and angry”状态的眼中进行晶状体乳化术,存在严重并发症的风险,如角膜水肿导致视野不佳、浅前房、小且变形的瞳孔、无张力虹膜导致脱出风险以及术中炎症等1)。
对侧眼(僚眼)管理
Section titled “对侧眼(僚眼)管理”由于原发性闭角型青光眼是双眼性疾病,单眼急性发作的患者对侧眼发作风险极高。青光眼诊疗指南第5版推荐对侧眼窄角进行预防性激光虹膜切开术和晶状体摘除术,推荐等级为1A2)。APGS 2025共识2.3以100%的同意率采纳了在治疗发作眼期间、直至可行LPI之前,对侧眼开始使用毛果芸香碱滴眼液1)。
实用治疗流程
Section titled “实用治疗流程”典型的处理流程如下2):
- 评估视力、眼压、角膜内皮细胞、前段OCT、眼轴长度、双眼房角镜、屈光度和眼底
- 20%甘露醇1.0~2.0 g/kg静脉滴注30~60分钟(注意肾功能障碍)
- 开始频繁滴用1~2%毛果芸香碱(务必确认缩瞳效果)
- 联合使用乙酰唑胺、β受体阻滞剂滴眼液和倍他米松滴眼液
- 对侧眼开始使用毛果芸香碱滴眼液
- 角膜透明后行LPI(术前和术后立即滴用阿普拉可乐定盐酸盐)
- 术后处方示例:0.1%倍他米松滴眼液每日4次 + 根据眼压使用青光眼滴眼液和碳酸酐酶抑制剂
- 次日用前段OCT评估房角开放程度;若PAS残留或眼压持续升高,迅速转诊至可行晶状体重建术的机构
- 发作解除后1~3个月计划晶状体重建术
- 对侧眼的预防性LPI或晶状体重建术
对于无法当天进行急诊手术的医疗机构,现实的做法是首先通过药物治疗和LPI缓解发作,然后在发作后1至3个月内进行晶状体重建手术1, 2)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”急性青光眼发作的主要机制是相对性瞳孔阻滞,可能涉及高褶虹膜机制或脉络膜扩张。
相对性瞳孔阻滞与晶状体因素
Section titled “相对性瞳孔阻滞与晶状体因素”虹膜背面与晶状体前面在瞳孔缘处生理性接触,房水从后房经瞳孔流入前房。随着年龄增长,晶状体增厚并前移,瞳孔缘处的虹膜-晶状体接触增强,房水流出阻力增加。这称为相对性瞳孔阻滞。当后房压力超过前房压力时,虹膜向前凸出,几乎完全覆盖小梁网,导致眼压急剧升高1)。
远视眼眼轴短、前房浅,晶状体增厚的影响更为显著。一旦发生瞳孔阻滞,后房压力升高使虹膜进一步向前膨隆,同时眼压升高引起的虹膜实质水肿进一步加重瞳孔阻滞,形成恶性循环。这样在数小时内眼压可达40–80 mmHg。
中度散瞳的危险
Section titled “中度散瞳的危险”瞳孔阻滞在中度散瞳时最为严重。在此位置,瞳孔括约肌和开大肌均被激活,虹膜最为松弛,与晶状体前面广泛接触1)。因此,抗胆碱药或拟交感神经药引起的药物性散瞳、暗环境、强烈应激等导致的自然散瞳均可诱发发作。相反,完全散瞳或完全缩瞳时瞳孔阻滞程度相对较小。
高褶虹膜机制
Section titled “高褶虹膜机制”少数情况下也存在由高褶虹膜机制引起的发作。虹膜根部向前弯曲,散瞳时睫状体从后方机械性地推起虹膜根部,直接阻塞房角。高褶虹膜时,中央前房深度相对保持,但周边房角呈锐角狭窄。UBM显示虹膜中央平坦,根部增厚并向前弯曲,睫状突前移和睫状沟消失是其特点。激光虹膜切开术后眼压仍高时,应怀疑高褶虹膜机制参与,考虑追加激光房角成形术(LGP)或晶状体摘除术2)。
脉络膜扩张的参与
Section titled “脉络膜扩张的参与”影像学研究表明,脉络膜扩张可能升高后房压力,将虹膜-晶状体隔膜向前推,从而缩小前房角1)。然而,APGS 2025共识1.5“脉络膜扩张是APACA的启动因素”仅获得41.17%的同意,未成立1)。因果关系和贡献度的量化需要未来大规模影像学研究。
缺血性损伤和青光眼斑
Section titled “缺血性损伤和青光眼斑”眼压急剧升高导致瞳孔括约肌缺血,光反射消失。晶状体上皮也发生缺血性坏死,在瞳孔区留下白色混浊。这称为青光眼斑,是提示既往发作史的重要所见1)。
视神经病变可因发作时高眼压引起的机械性和缺血性损伤,以及眼压正常化后的缺血再灌注损伤而进展1)。APGS 2025明确指出,即使眼压得到控制,视网膜神经节细胞丢失仍可能持续1)。因此,不能认为“眼压降下来就放心了”,需要长期随访视神经和视野。
炎症和前房反应
Section titled “炎症和前房反应”APACA眼出现明显的前房炎症。高眼压导致虹膜毛细血管蛋白渗漏、瞳孔括约肌和开大肌缺血坏死、内皮细胞损伤导致房水蛋白增加,这些在前房中表现为炎症细胞和纤维素。APGS 2025共识2.2以100%同意通过,即APACA眼呈现严重炎症,因此应联合使用局部及必要时全身抗炎治疗1)。炎症消退对于预防LPI后大疱性角膜病变、预防瞳孔粘连以及为早期晶状体重建手术做准备均很重要。
急性发作后可能残留各种并发症。典型的包括:对光反射消失的麻痹性瞳孔散大、青光眼斑、虹膜实质色素释放、局限性白内障、周边虹膜前粘连(PAS)形成、以及角膜内皮细胞数量减少。已知LPI后大疱性角膜病变在角膜滴状变性、糖尿病、有急性发作史或角膜内皮细胞已减少的病例中更常见2)。因此,术前角膜内皮细胞检查是必需的,在内皮细胞数量减少的病例中,应考虑选择手术周边虹膜切除术2)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”急性青光眼发作的治疗范式在2020年代后期正在发生重大变化。除了传统的“药物治疗→LPI”之外,APGS指南2025提出了以下新的治疗策略1)。
- 早期替代治疗:在早期阶段积极选择ALPI、LPP或ACP,可以在30分钟内将眼压降至安全范围,同时避免全身药物的副作用1, 5)
- 早期晶状体重建术:鉴于单独LPI后高达58%的CACG转化率,应在发作解除后1-3个月更积极地选择晶状体重建术1)
- 联合房角粘连分离术(GSL):当存在伴有广泛PAS的CACG成分时,也正在考虑将GSL或房角切开术与晶状体重建术联合使用的选项1)
- 结膜下地塞米松:一项随机对照试验报告,在常规治疗基础上加用结膜下地塞米松可提高眼压降低效果和治疗成功率1)。给药途径和剂量的优化是未来的课题
- 资源有限地区的应对:在无法使用氩激光的地区,角膜压陷法已被提议作为一种可行的选择1)
另一方面,未解决的争议点也很多。晶状体重建术的最佳时机、MIGS(微创青光眼手术)在闭角型青光眼中的作用、新的药物联合疗法、以及基于影像的发病预测模型等,都需要通过大规模前瞻性研究进行验证1)。
8. 参考文献
Section titled “8. 参考文献”- Chan PP, Zhang X, Aung T, et al. Controversies, consensuses, and guidelines for acute primary angle closure attack (APACA) by the Asia-Pacific Glaucoma Society (APGS) and the Academy of Asia-Pacific Professors of Ophthalmology (AAPPO). Asia Pac J Ophthalmol (Phila). 2025;14(6):100223. PMID: 40615047. doi:10.1016/j.apjo.2025.100223.
- 日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Gedde SJ, Chopra V, Vinod K, Bowden EC, Kolomeyer NN, Challa P, et al.; American Academy of Ophthalmology Preferred Practice Pattern Glaucoma Committee. Primary Angle-Closure Disease Preferred Practice Pattern. Ophthalmology. 2026;133(4):P153-P201. PMID: 41665581. doi:10.1016/j.ophtha.2025.12.030.
- Pazos M, Traverso CE, Viswanathan A; European Glaucoma Society. European Glaucoma Society - Terminology and guidelines for glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):1-212. PMID: 41026937. doi:10.1136/bjophthalmol-2025-egsguidelines.
- Lam DS, Lai JS, Tham CC, Chua JK, Poon AS. Argon laser peripheral iridoplasty versus conventional systemic medical therapy in treatment of acute primary angle-closure glaucoma: a prospective, randomized, controlled trial. Ophthalmology. 2002;109(9):1591-6.
- Azuara-Blanco A, Burr J, Ramsay C, et al. Effectiveness of early lens extraction for the treatment of primary angle-closure glaucoma (EAGLE): a randomised controlled trial. Lancet. 2016;388(10052):1389-1397.
- Aung T, Friedman DS, Chew PT, et al. Long-term outcomes in Asians after acute primary angle closure. Ophthalmology. 2004;111(8):1464-9.
- Husain R, Gazzard G, Aung T, et al. Initial management of acute primary angle closure: a randomized trial comparing phacoemulsification with laser peripheral iridotomy. Ophthalmology. 2012;119(11):2274-81.
- Tham CC, Kwong YY, Baig N, Leung DY, Li FC, Lam DS. Phacoemulsification versus trabeculectomy in medically uncontrolled chronic angle-closure glaucoma without cataract. Ophthalmology. 2013;120(1):62-7.
- Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006;90(3):262-7.
- Lai JS, Tham CC, Chan JC. The clinical outcomes of cataract extraction by phacoemulsification in eyes with primary angle-closure glaucoma (PACG) and co-existing cataract: a prospective case series. J Glaucoma. 2006;15(1):47-52.
- Wang B, Sakata LM, Friedman DS, et al. Quantitative iris parameters and association with narrow angles. Ophthalmology. 2010;117(1):11-17.
- Aung T, Ang LP, Chan SP, Chew PT. Acute primary angle-closure: long-term intraocular pressure outcome in Asian eyes. Am J Ophthalmol. 2001;131(1):7-12.
- Day AC, Baio G, Gazzard G, et al. The prevalence of primary angle closure glaucoma in European derived populations: a systematic review. Br J Ophthalmol. 2012;96(9):1162-7.
