急性发作时的所见
眼压:超过40 mmHg,有时可达80 mmHg1)2)
角膜:可见实质水肿和微囊性水肿2)
瞳孔:中度散大,对光反射减弱或消失2)3)
前房:中央部保持一定深度,但周边部变浅。伴有前房炎症 2)
青光眼斑:晶状体前囊下坏死。提示既往发作的所见 2)
房角:可见广泛的虹膜与小梁网接触 2)3)

闭角型青光眼(ACG)是由于前房角发生并置性或粘连性关闭,导致房水流出受阻,引起眼压升高和视神经损害的一组疾病1)2)。原发性和继发性均可表现为急性发作或慢性病程。
原发性闭角疾病(PACD)按以下阶段分类1):
40岁以上患病率增加1)4)。在Tajimi研究中,PACG的患病率为0.6%,而在Kumejima研究中为2.2%,存在地区差异。东亚人和因纽特人的患病率特别高4)。女性更常见4)。
原发性闭角型青光眼的患病率在不同种族和民族间差异很大4)。东亚人和因纽特人的患病率最高4)。这被认为是由眼轴长度、前房深度、晶状体厚度和角膜曲率等解剖特征的人种差异所致。即使在日本国内也存在地区差异,Tajimi(0.6%)和Kumejima(2.2%)之间相差约3.7倍。
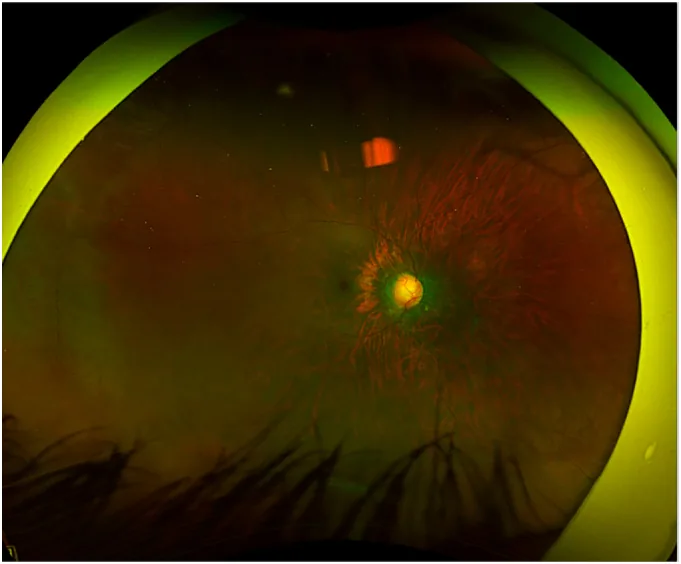
仅有解剖性窄角或慢性闭角的情况下通常无症状。直到末期才意识到视力下降和视野缺损。
急性闭角发作时出现剧烈症状1)2)。出现视力下降、视物模糊和虹视(灯光周围有光晕)1)2)。伴有剧烈眼痛和头痛,有时会出现恶心、呕吐等迷走神经症状1)2)。
急性发作时的所见
眼压:超过40 mmHg,有时可达80 mmHg1)2)
角膜:可见实质水肿和微囊性水肿2)
瞳孔:中度散大,对光反射减弱或消失2)3)
前房:中央部保持一定深度,但周边部变浅。伴有前房炎症 2)
青光眼斑:晶状体前囊下坏死。提示既往发作的所见 2)
房角:可见广泛的虹膜与小梁网接触 2)3)
继发性ACG的鉴别所见
| 风险因素 | 概述 |
|---|---|
| 远视 | 眼轴短导致浅前房 4) |
| 年龄增长 | 晶状体厚度增加1)4) |
| 女性 | 较男性更常见4) |
| 亚洲/因纽特人种 | 解剖学特征4) |
| 家族史 | 眼轴长度和屈光的遗传4) |
| 浅前房、短眼轴、厚晶状体 | 解剖学易感因素4) |
继发性原因多种多样1)2)。大致分为将虹膜从后方推向前方的机制(如晶状体膨胀、晶状体脱位、睫状体脉络膜渗出、房水引流异常、后部眼内肿瘤等)和将虹膜拉向小梁网的机制(如炎性膜收缩、ICE综合征、纤维增殖等)。
在药物诱发的ACG中,托吡酯等磺胺类药物可引起睫状体脉络膜渗出,导致睫状体前旋和虹膜-晶状体隔前移,从而引起房角关闭6)7)8)。据报道,乙酰唑胺也可引起类似的特异性反应10)。
托吡酯引起睫状体脉络膜渗出,导致睫状体前旋和虹膜-晶状体隔前移,从而引起双眼急性房角关闭6)7)8)。通常在用药后2周内发生,但停药后也可能发生6)。UBM可显示睫状体前旋和脉络膜渗出8)。治疗包括停用托吡酯、阿托品滴眼液、类固醇滴眼液和降眼压药物6)7)。激光虹膜切开术无效,缩瞳剂因加重病情而禁忌使用。
房角镜检查是诊断ACG的金标准1)2)。使用压迫式房角镜鉴别并置性关闭与粘连性关闭。原发性ACG上方易形成PAS,而炎症性继发性ACG下方易形成PAS。
UBM(超声生物显微镜)可评估睫状体的形态、位置以及有无脉络膜渗出,有助于查找继发性ACG的原因8)10)。眼前段OCT用于房角结构的客观定量评估。
van Herick法评估前房深度是一种简便的窄房角筛查方法1)。如果角膜厚度与周边前房深度之比小于1/4,则应进行房角镜检查1)。
若怀疑药物诱导性ACG,应进行UBM和B超检查以确认睫状体脉络膜渗出6)8)10)。若怀疑合并视网膜色素变性,应进行全视野视网膜电图检查5)。在ARB(常染色体隐性遗传性卵黄样黄斑营养不良)中,EOG显示特征性的光上升消失9)。
急性原发性房角关闭的治疗按以下顺序进行1):
LPI是解除瞳孔阻滞的有效一线治疗方法1)2)。需在角膜足够透明时进行1)。通过不透明角膜进行激光照射有发生大疱性角膜病变的风险1)。若一眼确诊为原发性闭角型青光眼/原发性房角关闭,则对另一眼进行预防性LPI1)。
晶状体摘除可从根本上解除瞳孔阻滞1)。可获得房角开放和眼压下降效果1)。若周边前粘连(PAS)范围广泛,则眼压下降效果有限1)。
对于高坪虹膜,仅行LPI不够,需行激光虹膜成形术(激光周边虹膜成形术)以收缩虹膜根部1)。晶状体摘除以开放房角也有效1)。
| 治疗方法 | 适应症 |
|---|---|
| LPI | 瞳孔阻滞1) |
| 晶状体摘除 | 瞳孔阻滞、晶状体因素1) |
| ALPI | 高褶虹膜1) |
| 房角粘连分离术 | 广泛PAS(≥50%)1) |
继发性ACG中,治疗原发病最为优先1)2)。药物诱发性病例中,停用致病药物最为重要,同时使用阿托品滴眼液放松睫状肌和类固醇抗炎6)7)8)。缩瞳药因促进晶状体前移而禁忌。恶性青光眼中,阿托品滴眼液和玻璃体切除术是治疗核心1)。
晶状体摘除可从根本上解除瞳孔阻滞1)。摘除晶状体可使前房加深、房角增宽。在有白内障手术指征的病例中,可期待一举两得的效果。但如果已形成广泛PAS,降眼压效果有限,建议联合房角粘连分离术1)。急性期晶状体摘除并发症风险高,应由经验丰富的手术者进行1)。
大多数原发性闭角型青光眼由相对性瞳孔阻滞引起1)2)3)。房水从后房流向前房的阻力增加导致虹膜向前膨隆,阻塞小梁网1)。瞳孔阻滞的风险在中等散瞳时最大3)。
原发性房角关闭的成因涉及多种机制1):(1)相对性瞳孔阻滞,(2)高褶虹膜,(3)晶状体因素(年龄增长导致晶状体厚度增加),(4)晶状体后因素(睫状体、脉络膜、玻璃体)1)。
在高褶虹膜构型中,位置靠前的睫状突将虹膜根部向前推,尽管中央前房深度正常,仍导致房角关闭1)。
推挤机制
瞳孔阻滞型:晶状体膨胀、晶状体脱位或小球形晶状体导致虹膜向前推挤2)3)。虹膜后粘连引起的绝对性瞳孔阻滞2)
睫状体脉络膜型:药物(托吡酯)引起的睫状体脉络膜渗出和睫状体前旋6)7)8)。后段肿瘤或浆液性视网膜脱离引起的推挤
房水引流异常型:玻璃体前移导致整个前房变浅。也称为恶性青光眼1)
牵拉机制
炎性膜收缩:葡萄膜炎相关的周边虹膜前粘连形成。虹膜新生血管引起的纤维血管膜收缩2)
ICE综合征:角膜内皮异常增殖导致小梁网阻塞1)
外伤/手术相关:上皮植入、纤维增殖、虹膜嵌顿于伤口2)
Lu等人报告了三例年轻视网膜色素变性(RP)患者合并PACG的病例5)。RP患者发生ACG的风险比一般人群高3.64倍5)。短眼轴、晶状体厚度增加和悬韧带脆弱是ACG的解剖学易感因素5)。在合并PACG的RP患者中发现了ZNF408基因的新突变5)。建议RP患者定期进行房角镜检查和眼压监测5)。
托吡酯诱发性ACG的多例病例报告已积累6)7)8)。典型病例在用药后1-2周双眼发病,机制为睫状体脉络膜渗出及随后的睫状体前旋8)。Tyagi等人报告了两例表现为前房积脓性葡萄膜炎和脉络膜脱离的病例,表明托吡酯可引起严重的眼内炎症7)。有报告称停药后仍可能发病6)。
Kaisari等人的文献综述显示,自1956年以来已有23例乙酰唑胺诱发的近视化报告10)。中位剂量500 mg给药后中位24小时发病,约1/3合并房角关闭10)。该反应是剂量非依赖性的特异质反应,首次给药也可发生10)。停药并使用睫状肌麻痹剂后,中位5天完全恢复10)。
常染色体隐性遗传性卵黄样黄斑营养不良(ARB)中超过50%合并闭角型青光眼9)。Raja等人报告了一例38岁女性ARB合并ACG患者出现进展性视神经病变,仅行激光周边虹膜切开术(LPI)难以控制眼压,因此实施了微脉冲经巩膜睫状体光凝术9)。
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2021.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
- American Academy of Ophthalmology. Primary Angle-Closure Disease Preferred Practice Pattern®. 2020.
- Lu Z, Wang L, Ying X, et al. Bilateral angle closure glaucoma with retinitis pigmentosa in young patients: case series. BMC Ophthalmology. 2023;23:458.
- Alzendi NA, Badawi AH, Alhazzaa B, et al. Topiramate-induced angle closure glaucoma: two unique case reports. Saudi J Ophthalmol. 2020;34:202-204.
- Tyagi M, Behera S, Senthil S, et al. Topiramate induced bilateral hypopyon uveitis and choroidal detachment: a report of two cases and review of literature. BMC Ophthalmology. 2021;21:287.
- AlNaqeeb O, Aljohani S, Alshehri A. Topiramate-induced acute bilateral angle closure glaucoma confirmed by ultrasound biomicroscopy. Saudi J Ophthalmol. 2020;34:316-318.
- Raja V, Manthravadi SK, Anjanamurthy R. Angle-closure glaucoma associated with autosomal recessive bestrophinopathy. Indian J Ophthalmol. 2022;70:2657-2658.
- Kaisari E, Abouzeid H, Magnin L, et al. Acute myopic shift after a single dose of acetazolamide: a case report and review of the literature. Klin Monatsbl Augenheilkd. 2024;241:554-558.