瞳孔阻塞
虹膜形態:周邊虹膜向前膨隆(iris bombé)
前房深度:周邊部特別淺
PI:阻塞或未施行
縮瞳藥:有效

惡性青光眼是一種伴有明顯淺前房的高眼壓狀態,典型發生於閉鎖隅角青光眼眼濾過手術後。推測是由於睫狀體前旋和房水異常流入玻璃體腔導致玻璃體前移,從而引起隅角閉塞。也稱為房水誤導症候群、睫狀體阻滯性青光眼或直接水晶體阻滯性青光眼,多種名稱混用。ICD-10編碼為H40.8。
1869年Von Graefe首次將其報告為濾過手術後難治性淺前房,這是一個歷史性的疾病概念3)。隨後,房水不沿正常前向路徑而是被錯誤地引導至後方(玻璃體腔側)的病理概念得以確立,“aqueous misdirection”(房水迷流)這一名稱被廣泛使用。最常見於濾過手術後的閉角型青光眼,但臨床上重要的是,它可能發生在任何內眼手術後,包括白內障手術。
青光眼診療指引(第5版)將續發性隅角關閉性青光眼的眼壓升高機轉分為以下四類6)。
惡性青光眼屬於上述第三類「水晶體後方組織的前移」。在EGS第5版中相當於「後推機轉」5)。
濾過手術後的發生率為0.6%~4%5)。多見於女性,通常單眼發病。最常見於原發性閉角型青光眼濾過手術後,但也可能發生在任何內眼手術後,包括白內障手術5)。危險因子包括短眼軸(<21 mm)、高度遠視(≥+6 D)和原發性閉角型青光眼病史5)。罕見無手術史的特發性病例也有報告。已知閉角型青光眼行小樑切除術後,發生淺前房、脈絡膜剝離以及惡性青光眼的風險相對較高6)。
瞳孔阻滯時,瞳孔緣房水流通受阻導致周邊虹膜向前膨隆(iris bombé)。而房水迷流時,房水從水晶體後方積聚在玻璃體腔,因此前房均勻變淺。縮瞳藥對瞳孔阻滯有效,但對房水迷流是禁忌的。
急性發作時出現以下症狀。
症狀具有波動性,可能在白內障術後數週至數年才顯現3)。早期眼壓可能仍在正常範圍內,導致診斷延遲5)。眼壓急劇升高時,臨床表現類似急性青光眼發作,視力下降迅速進展。
透過以下徵象的組合進行診斷。除眼壓升高外,前房深度的變化模式在鑑別診斷中最為重要。
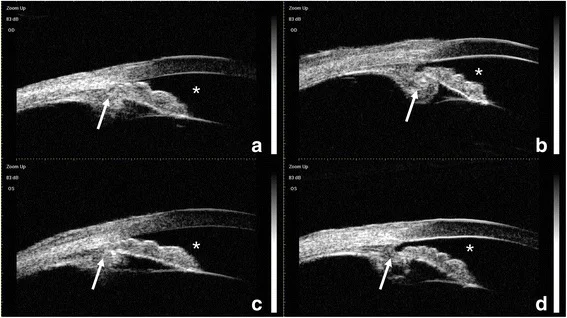
前段光學同調斷層掃描(AS-OCT)顯示,CTR(囊袋張力環)-IOL複合體前移可導致類似高褶虹膜之表現(虹膜中央平坦但隅角關閉)2)。超音波生物顯微鏡(UBM)可直接確認水晶體囊-IOL複合體前移及睫狀體前旋或位置異常4)。UBM解析度達20–60 μm,可詳細顯示虹膜、睫狀體等前段結構,因此對疑似惡性青光眼之病例應積極進行此項檢查。
UBM及前段OCT檢查有助於闡明病理生理機制,尤其應在確認手術史之同時評估是否存在睫狀體位置異常。
最常見之誘因為內眼手術5)。
眼球越小,風險越高5)。
如果單眼發病,對側眼的發病風險也會增加3)。無論是否有青光眼病史,風險都會升高,因此對側眼的定期追蹤很重要。
主要風險因素總結如下。
| 風險因素 | 具體例子 |
|---|---|
| 眼球形態 | 短眼軸(<21 mm)、高度遠視(>+6 D)、淺前房 |
| 手術 | 濾過手術、白內障手術、CTR植入 |
| 藥物 | 托吡酯、SSRI |
托吡酯可增加睫狀體脈絡膜的血管通透性,導致睫狀體腫脹和向前旋轉1)。在小眼球等高風險眼中,可能誘發房水誤導。SSRI也可能透過散瞳作用誘發窄隅角眼的隅角閉塞。
惡性青光眼是排除性診斷,必須在系統排除瞳孔阻塞、脈絡膜出血/剝離、脈絡膜上腔出血及其他閉角機制後才能確診4)。此病不能僅憑特定檢查值或影像學表現確診,需結合臨床病程和多項檢查結果綜合判斷。
閉角型青光眼術後早期出現極淺前房和高眼壓時,應懷疑本病。出血性脈絡膜剝離可呈現類似的裂隙燈顯微鏡表現,且均可導致高眼壓,但可透過眼底檢查鑑別。特發性病例因無手術史,診斷更為困難,UBM確認睫狀體位置異常是診斷的關鍵。
瞳孔阻塞與房水誤導的鑑別要點總結如下。
瞳孔阻塞
虹膜形態:周邊虹膜向前膨隆(iris bombé)
前房深度:周邊部特別淺
PI:阻塞或未施行
縮瞳藥:有效
房水誤導
虹膜形態:虹膜整體向前偏移
前房深度:均勻變淺至消失5)
PI:暢通
縮瞳藥:禁忌(惡化)
其他鑑別診斷包括以下疾病。這些疾病均可導致淺前房和高眼壓,但由於發病機制不同,治療方針也不同。
基本採用藥物療法→雷射治療→手術治療的階段性方法。首先嘗試藥物療法解除睫狀體阻滯,無效則進行雷射治療,仍無效則逐步進行手術治療。治療的最終目標是建立後房與前房之間不會發生阻滯的狀態(單房眼),防止復發。
建議聯合使用副交感神經阻斷藥(散瞳/睫狀肌鬆弛藥)、房水生成抑制劑(點眼和口服)以及高滲透壓劑(靜脈滴注)5)。
| 藥物 | 用法 | 作用機轉 |
|---|---|---|
| 阿托品點眼液1% | 每日1~3次點眼 | 睫狀肌鬆弛/散瞳 |
| 噻嗎洛爾點眼液0.5% | 每日2次點眼 | 房水生成抑制(β阻斷) |
| 乙醯唑胺片250 mg | 2錠,分2次飯後服用 | 房水生成抑制(口服CAI) |
| 甘露醇點滴 | 靜脈注射 | 縮小玻璃體容積 |
阿托品可增加睫狀小帶的張力,使水晶體向後移動,並促使進入玻璃體腔的房水向前回流。也可使用環噴托酯作為阿托品的替代品5)。
抑制房水生成的眼藥水(β阻斷劑、碳酸酐酶抑制劑)與高滲透壓藥物點滴合併使用6)。高滲透壓藥物可縮小玻璃體容積,但其治療效果是暫時的,因此被視為術前處置6)。
藥物治療的有效率約為50%(5天內),但單獨用藥的復發率高5)。即使藥物治療使前房加深、眼壓恢復正常,停用阿托品眼藥水後也常復發,因此可能需要長期維持使用阿托品眼藥水。藥物治療僅為初始措施,根治性治療通常需要雷射或手術介入。
在人工水晶體眼中,進行Nd:YAG雷射後囊切開,然後將焦點移至後囊後方,以3-4 mJ的能量發射10-20次,破壞前玻璃體膜。透過在玻璃體腔和前房之間建立房水通道,解除阻滯。如果成功,即刻至次日可觀察到前房深度改善和眼壓下降。
在人工水晶體眼或無水晶體眼中,可選擇YAG雷射或手術前玻璃體膜切開和水晶體囊切開術6)(證據等級2C)。
二極體雷射睫狀體光凝固可在治療的任何階段考慮5)。它引起睫狀突的凝固壞死和萎縮,可能導致睫狀體-玻璃體介面的破壞和睫狀體向後旋轉3)。然而,破壞睫狀體-玻璃體介面所需的照射條件尚未確定。
如果藥物和雷射治療效果不佳,或復發,則進行手術。透過前玻璃體膜切開的玻璃體切除術來解除病情至關重要6)(證據等級2C)。
進行經睫狀體扁平部玻璃體切除術(PPV)5)。有時也合併水晶體摘除術6)(2C)。透過合併水晶體摘除,建立單房眼,完全解除後房與前房之間的阻滯,防止復發。
zonulo-hyaloido-vitrectomy(虹膜-水晶體懸韌帶-前玻璃體膜切除術)是有效的5)。從周邊虹膜切除處向前房方向進入,切除水晶體囊周圍的懸韌帶和前玻璃體膜。此術式在玻璃體腔和前房之間建立永久性交通通道。
在伴有前玻璃體膜切開的玻璃體切除術中,有些病例需要虹膜切除以處理最周邊的前玻璃體膜6)(2C)。如果前玻璃體膜和懸韌帶處理不充分,玻璃體腔和前房之間會殘留阻滯,可能導致復發。在有水晶體眼中,同時摘除水晶體可解除睫狀突與水晶體赤道部的接觸,建立單房眼。
有報告指出,CTR取出、前玻璃體切除和IOL鞏膜內固定的組合是有效的2)。
房水誤導是水晶體後方推擠機制引起的閉角。縮瞳藥收縮睫狀肌,促進睫狀體前突,加重睫狀體阻滯,因此是禁忌的6)。相比之下,阿托品等散瞳睫狀肌麻痺藥可鬆弛睫狀肌,增加懸韌帶張力,使水晶體後移,從而有效解除阻滯。
單眼發病會顯著增加對側眼的風險3)。無論是否有青光眼病史,風險都會升高,因此定期評估對側眼的眼壓和前房深度很重要。
惡性青光眼的確切發病機轉尚未完全闡明,但提出了以下兩種假說5)。
脈絡膜膨脹說
主要機轉:脈絡膜容積增大,對液體從後方向前方的移動產生阻力5)
結果:房水積聚在玻璃體腔,將虹膜-水晶體隔膜向前推
睫狀體阻滯學說
主要機轉:睫狀突與水晶體(或人工水晶體)赤道部、前玻璃體膜之間的異常解剖接觸
結果:形成「惡性循環」,起到單向閥的作用,阻礙房水向前流出
病情的進展可透過以下級聯理解。正常眼中,睫狀體產生的房水從後房經瞳孔流入前房,然後通過房角的小樑網流出。在惡性青光眼中,這一通路被破壞。
阿托品眼藥水可放鬆睫狀肌,增加懸韌帶張力,使水晶體向後移動。這可能使進入玻璃體腔的房水有機會向前回流。
相反地,毛果芸香鹼等縮瞳藥會收縮睫狀肌。這種收縮會放鬆懸韌帶,將水晶體向前推,並進一步促進睫狀體前旋,從而加重睫狀環阻滯6)。因此,縮瞳藥在惡性青光眼中是禁忌的。
在人工水晶體眼中,IOL-囊袋複合體的水平直徑大於天然水晶體,更容易接觸睫狀突4)。睫狀突產生的部分房水向後(玻璃體腔)分泌。如果前玻璃體膜完整,前向液體流出受阻,產生壓力梯度,導致前房變淺。
據報導,即使有玻璃體切除術史的眼睛,如果前玻璃體膜殘留,也可能發病4)。在一例伴有3 D以上近視漂移的復發病例中,聯合隅角黏連分離術、虹膜切除術和晶狀體懸韌帶-玻璃體膜切除術恢復了屈光和眼壓4)。因此,玻璃體切除術時應充分清除前玻璃體膜,包括最周邊區域,這對預防復發至關重要。
托吡酯可增加睫狀體脈絡膜血管的通透性,導致睫狀體和脈絡膜腫脹以及睫狀體前旋1)。在小眼球症中,鞏膜增厚導致的渦靜脈引流障礙進一步增加了葡萄膜滲出的風險1)。
植入CTR會使囊袋擴張增厚,CTR-IOL複合體全周接觸睫狀體和虹膜後表面2)。這會壓迫睫狀溝,增加房水從後向前流動的阻力。由於CTR-IOL複合體的大直徑部分限制了前向移位,可能表現為前房深度保持的虹膜高坪型隅角關閉2)。這種非典型表現不同於惡性青光眼典型的均勻淺前房,因此使用AS-OCT詳細評估隅角形態是診斷的關鍵。
Chean等人(2021)報告了一例白內障術後以近視漂移(myopic surprise)為唯一早期徵象的房水誤導病例3)。術後約三年內眼壓正常,導致診斷延遲。即使生物測量顯示前房深度看似正常,短眼軸眼也可能出現測量誤差,因此當出現近視漂移時,應將房水誤導納入鑑別診斷。
Stephenson等人(2023)報告了一例既往有玻璃體切除術、白內障手術和人工虹膜植入術史的眼,出現3 D以上的近視漂移並伴有房水誤導的病例4)。他們表明,即使玻璃體切除術後,如果前玻璃體膜殘留,仍可能發病,通過房角粘連分離術+虹膜切除術+晶狀體懸韌帶-玻璃體切除術,屈光和眼壓得以恢復。
Goto等人(2024)首次使用AS-OCT描述了CTR-IOL複合體前移導致的繼發性房角關閉的特徵2)。他們報告了一種非典型的高原虹膜樣表現,前房深度保持不變,表明AS-OCT在檢測白內障手術聯合CTR植入術後繼發性房角關閉方面具有價值。
已提出藥物→Nd:YAG雷射→睫狀體光凝→手術的階梯式方法3)。睫狀體光凝可引起睫狀突的凝固壞死和萎縮,可能破壞睫狀體-玻璃體界面並導致睫狀體向後旋轉。然而,破壞睫狀體-玻璃體界面所需的照射條件尚未確定,當藥物和雷射單獨治療不足時,創建單腔眼的手術仍然是最終的治療選擇3)。