Bloc pupillaire
Morphologie de l’iris : Bombement antérieur de l’iris périphérique (iris bombé)
Profondeur de la chambre antérieure : Particulièrement peu profonde en périphérie
PI : Obstrué ou non réalisé
Myotiques : Efficaces

Le glaucome malin (malignant glaucoma) est un état d’hypertension oculaire avec une chambre antérieure très peu profonde, survenant typiquement après une chirurgie filtrante pour un glaucome par fermeture de l’angle. On pense qu’il est dû à une rotation antérieure du corps ciliaire et à un flux anormal d’humeur aqueuse dans la cavité vitréenne, entraînant un déplacement antérieur du vitré et une fermeture de l’angle. Il est également appelé syndrome de mauvaise direction de l’humeur aqueuse (aqueous misdirection syndrome), glaucome par bloc ciliaire (ciliary block glaucoma) ou glaucome par bloc direct du cristallin (direct lens block glaucoma), avec plusieurs noms en usage. Le code CIM-10 est H40.8.
En 1869, Von Graefe a rapporté pour la première fois ce concept historique de maladie comme une chambre antérieure peu profonde réfractaire après une chirurgie de filtration 3). Par la suite, le concept physiopathologique selon lequel l’humeur aqueuse est déviée vers l’arrière (côté du corps vitré) plutôt que par la voie antérieure normale a été établi, et le terme « aqueous misdirection » (déviation de l’humeur aqueuse) est largement utilisé. On le rencontre le plus souvent dans les yeux atteints de glaucome à angle fermé après une chirurgie de filtration, mais il est cliniquement important de noter qu’il peut survenir après toute chirurgie intraoculaire, y compris la chirurgie de la cataracte.
Dans les directives cliniques pour le glaucome (5e édition), les mécanismes d’élévation de la pression intraoculaire dans le glaucome secondaire à angle fermé sont classés en quatre catégories 6).
Le glaucome malin est classé dans la troisième catégorie ci-dessus : « déplacement antérieur des tissus en arrière du cristallin ». Dans la 5e édition de l’EGS, cela correspond au « mécanisme de poussée postérieure » 5).
L’incidence après chirurgie de filtration est de 0,6 à 4 % 5). Elle est plus fréquente chez les femmes et survient généralement de manière unilatérale. Elle est plus fréquente après une chirurgie de filtration pour un glaucome primitif à angle fermé, mais peut survenir après toute chirurgie intraoculaire, y compris la chirurgie de la cataracte 5). Les facteurs de risque comprennent un axe oculaire court (moins de 21 mm), une hypermétropie élevée (+6 D ou plus) et des antécédents de glaucome primitif à angle fermé 5). De rares cas idiopathiques sans antécédents chirurgicaux ont été rapportés. On sait que la trabéculectomie pour le glaucome à angle fermé a un risque relativement élevé de provoquer un glaucome malin avec une chambre antérieure peu profonde et un décollement choroïdien en postopératoire 6).
Dans le bloc pupillaire, l’obstruction de l’écoulement de l’humeur aqueuse au niveau du bord pupillaire provoque un bombement antérieur de l’iris périphérique (iris bombé). En revanche, dans la déviation de l’humeur aqueuse, l’accumulation d’humeur aqueuse dans la cavité vitréenne depuis l’arrière du cristallin rend la chambre antérieure uniformément peu profonde, ce qui est différent. Les myotiques sont efficaces pour le bloc pupillaire, mais ils sont contre-indiqués dans la déviation de l’humeur aqueuse.
En cas de début aigu, les symptômes suivants se manifestent.
Les symptômes sont fluctuants et peuvent apparaître plusieurs semaines à plusieurs années après la chirurgie de la cataracte 3). Au début, la pression intraoculaire peut rester dans les limites normales, ce qui retarde le diagnostic 5). En cas d’élévation brutale de la pression intraoculaire, le tableau clinique ressemble à une crise de glaucome aigu, avec une baisse rapide de l’acuité visuelle.
Le diagnostic repose sur la combinaison des signes suivants. Outre l’élévation de la pression intraoculaire, le profil de modification de la profondeur de la chambre antérieure est le plus important pour le diagnostic différentiel.
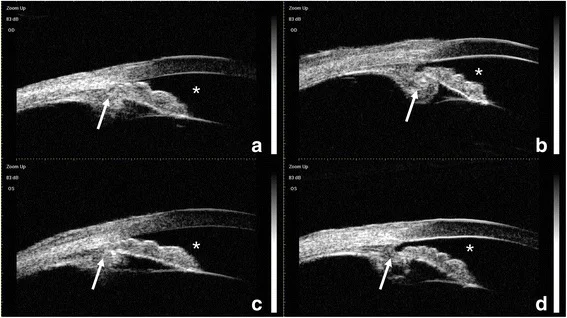
La tomographie par cohérence optique du segment antérieur (AS-OCT) peut montrer un aspect de plateau iris (partie centrale de l’iris plate mais angle fermé) associé à une déviation antérieure du complexe CTR-IOL (anneau de tension capsulaire-implant intraoculaire) 2). L’échographie biomicroscopique (UBM) permet de visualiser directement la déviation antérieure du complexe sac capsulaire-IOL et la rotation antérieure ou la malposition du corps ciliaire 4). L’UBM, avec une résolution élevée de 20 à 60 μm, permet de visualiser en détail les structures du segment antérieur telles que l’iris et le corps ciliaire ; elle doit donc être réalisée activement en cas de suspicion de glaucome malin.
L’UBM et l’OCT du segment antérieur sont utiles pour élucider la pathologie. Il est important d’évaluer la présence d’une malposition du corps ciliaire, tout en vérifiant les antécédents chirurgicaux.
Le facteur déclenchant le plus fréquent est la chirurgie intraoculaire 5).
Plus l’œil est petit, plus le risque est élevé 5).
En cas d’atteinte unilatérale, le risque de développer la maladie dans l’œil controlatéral augmente également 3). Le risque est accru indépendamment des antécédents de glaucome, d’où l’importance d’un suivi régulier de l’œil controlatéral.
Les principaux facteurs de risque sont résumés ci-dessous.
| Facteurs de risque | Exemples |
|---|---|
| Morphologie oculaire | Axes courts (<21 mm), forte hypermétropie (>+6 D), chambre antérieure peu profonde |
| Chirurgie | Chirurgie filtrante, chirurgie de la cataracte, pose de CTR |
| Médicaments | Topiramate, ISRS |
Le topiramate augmente la perméabilité vasculaire du corps ciliaire et de la choroïde, provoquant un gonflement du corps ciliaire et une rotation antérieure 1). Dans les yeux à haut risque comme la microphtalmie, cela peut déclencher un glaucome malin. Les ISRS peuvent également induire une fermeture de l’angle chez les yeux à angle étroit par leur effet mydriatique.
Le glaucome malin est un diagnostic d’exclusion : il n’est posé qu’après avoir systématiquement exclu un bloc pupillaire, une hémorragie ou décollement choroïdien, une hémorragie suprachoroïdienne et d’autres mécanismes de fermeture de l’angle 4). Il ne s’agit pas d’une maladie pouvant être confirmée par une seule valeur de test ou imagerie ; le diagnostic repose sur une combinaison de l’évolution clinique et de multiples résultats d’examens.
Suspecter cette maladie en cas de chambre antérieure extrêmement peu profonde et d’hypertension oculaire survenant précocement après une chirurgie du glaucome à angle fermé. Le décollement choroïdien hémorragique présente des signes similaires à la lampe à fente et peut également entraîner une hypertension oculaire, mais le fond d’œil permet de les différencier. Dans les cas idiopathiques, l’absence d’antécédents chirurgicaux rend le diagnostic plus difficile, et la confirmation d’une position anormale du corps ciliaire par UBM est la clé du diagnostic.
Les points de différenciation entre le bloc pupillaire et le glaucome malin sont résumés ci-dessous.
Bloc pupillaire
Morphologie de l’iris : Bombement antérieur de l’iris périphérique (iris bombé)
Profondeur de la chambre antérieure : Particulièrement peu profonde en périphérie
PI : Obstrué ou non réalisé
Myotiques : Efficaces
Blocage ciliaire (malin)
Morphologie de l’iris : Iris déplacé vers l’avant dans son ensemble
Profondeur de la chambre antérieure : Uniformément peu profonde à absente5)
PI : Perméable
Myotiques : Contre-indiqués (aggravation)
Les autres diagnostics différentiels sont les suivants. Tous peuvent entraîner une chambre antérieure peu profonde et une hypertension oculaire, mais les mécanismes pathogéniques diffèrent, donc les stratégies thérapeutiques sont également différentes.
L’approche de base est une progression par étapes : traitement médicamenteux → traitement laser → traitement chirurgical. On tente d’abord de lever le bloc ciliaire par des médicaments ; en cas d’échec, on passe au laser, puis à la chirurgie. L’objectif final est de créer un œil à chambre unique (unicameral eye) où aucun blocage entre la chambre postérieure et antérieure ne peut se produire, afin de prévenir les récidives.
L’association d’un anticholinergique (mydriatique et relaxant ciliaire), d’un inhibiteur de la production d’humeur aqueuse (collyre et oral) et d’un agent hyperosmolaire (perfusion) est recommandée5).
| Médicament | Posologie | Mécanisme d’action |
|---|---|---|
| Collyre à l’atropine 1% | 1 à 3 fois par jour | Relaxation ciliaire et mydriase |
| Collyre au timolol 0,5% | 2 fois par jour | Inhibition de la production d’humeur aqueuse (bêta-bloquant) |
| Comprimés de Diamox 250 mg | 2 comprimés en 2 prises après les repas | Inhibition de la production d’humeur aqueuse (IAC oral) |
| Perfusion de mannitol | Administration intraveineuse | Réduction du volume vitréen |
L’atropine augmente la tension de la zonule ciliaire, déplace le cristallin vers l’arrière et permet à l’humeur aqueuse qui a reflué dans la cavité vitréenne de revenir vers l’avant. Le cyclopentolate peut également être utilisé comme alternative à l’atropine5).
On associe des collyres inhibant la production d’humeur aqueuse (bêta-bloquants, inhibiteurs de l’anhydrase carbonique) et une perfusion d’agent hyperosmolaire6). L’agent hyperosmolaire réduit le volume vitréen, mais son effet thérapeutique est temporaire, il est donc considéré comme un traitement préopératoire6).
Le taux de réponse au traitement médicamenteux est d’environ 50 % (dans les 5 jours), mais le taux de récidive avec les médicaments seuls est élevé5). Même si la chambre antérieure s’approfondit et la pression intraoculaire se normalise sous traitement médicamenteux, la récidive est fréquente à l’arrêt des collyres atropiniques, il peut donc être nécessaire de poursuivre l’atropine en traitement d’entretien à long terme. Le traitement médicamenteux n’est qu’une mesure initiale ; le traitement curatif nécessite souvent une intervention au laser ou chirurgicale.
Chez les patients pseudophakes, on réalise une capsulotomie postérieure au laser Nd:YAG, puis on décale le foyer en arrière de la capsule postérieure et on applique 10 à 20 tirs avec une énergie de 3 à 4 mJ pour fragmenter la membrane hyaloïdienne antérieure. En créant un passage pour l’humeur aqueuse entre la cavité vitréenne et la chambre antérieure, on vise à lever le bloc. En cas de succès, on observe une amélioration de la profondeur de la chambre antérieure et une baisse de la pression intraoculaire immédiatement ou le lendemain.
Chez les patients pseudophakes ou aphakes, on choisit le laser YAG ou une hyaloïdotomie antérieure chirurgicale ou une capsulotomie du cristallin6) (niveau de preuve 2C).
La cyclophotocoagulation au laser diode peut être envisagée à n’importe quel stade du traitement5). Elle provoque une nécrose de coagulation et une atrophie des procès ciliaires, et peut entraîner une destruction de l’interface ciliaire-vitréen et une rotation postérieure du corps ciliaire3). Cependant, les conditions d’irradiation nécessaires pour détruire l’interface ciliaire-vitréen ne sont pas encore établies.
En cas d’efficacité insuffisante du traitement médicamenteux ou laser, ou en cas de récidive, on a recours à la chirurgie. Il est important de réaliser une vitrectomie avec hyaloïdotomie antérieure pour résoudre la pathologie6) (niveau de preuve 2C).
Une vitrectomie pars plana (PPV) est réalisée 5). Une extraction du cristallin peut être associée 6) (2C). L’extraction du cristallin permet de créer un œil unicaméral, supprimant complètement le bloc entre la chambre postérieure et la chambre antérieure pour prévenir la récidive.
La zonulo-hyaloido-vitrectomie (résection de l’iris, de la zonule de Zinn et de la membrane hyaloïde antérieure) est efficace 5). On aborde la chambre antérieure par une iridectomie périphérique et on résèque la zonule de Zinn autour du sac capsulaire et la membrane hyaloïde antérieure. Cette technique crée une voie de communication permanente entre la cavité vitréenne et la chambre antérieure.
Dans la vitrectomie avec incision de la membrane hyaloïde antérieure, une iridectomie peut être nécessaire pour traiter la membrane hyaloïde antérieure la plus périphérique 6) (2C). Si la membrane hyaloïde antérieure et la zonule de Zinn ne sont pas suffisamment traitées, un bloc persiste entre la cavité vitréenne et la chambre antérieure, pouvant entraîner une récidive. Dans l’œil phaque, l’ablation simultanée du cristallin supprime le contact entre les procès ciliaires et l’équateur du cristallin, créant un œil unicaméral.
Des rapports indiquent que la combinaison de l’ablation du CTR, de la vitrectomie antérieure et de la fixation sclérale de l’IOL a été efficace 2).
Le glaucome malin est un angle fermé dû à un mécanisme de poussée postérieure du cristallin. Les myotiques contractent le muscle ciliaire, favorisant la protrusion antérieure du corps ciliaire et aggravant le bloc ciliaire, ils sont donc contre-indiqués 6). En revanche, les cycloplégiques mydriatiques comme l’atropine relâchent le muscle ciliaire, augmentent la tension de la zonule et déplacent le cristallin vers l’arrière, ce qui est efficace pour lever le bloc.
L’atteinte unilatérale augmente significativement le risque pour l’œil controlatéral 3). Le risque est accru indépendamment des antécédents de glaucome, il est donc important d’évaluer régulièrement la pression intraoculaire et la profondeur de la chambre antérieure de l’œil controlatéral.
Le mécanisme exact du glaucome malin n’est pas complètement élucidé, mais deux hypothèses ont été proposées 5).
Théorie de l'expansion choroïdienne
Mécanisme principal : L’augmentation du volume choroïdien résiste au mouvement du liquide de l’arrière vers l’avant5)
Résultat : L’humeur aqueuse s’accumule dans la cavité vitréenne, poussant le diaphragme irido-cristallinien vers l’avant
Théorie du bloc ciliaire
Mécanisme principal : Contact anatomique anormal entre les procès ciliaires et l’équateur du cristallin (ou LIO) ainsi que la membrane hyaloïde antérieure
Résultat : Un « cycle malin » s’établit, agissant comme une valve unidirectionnelle qui empêche l’écoulement antérieur de l’humeur aqueuse
La progression pathologique peut être comprise par la cascade suivante. Dans un œil normal, l’humeur aqueuse produite par le corps ciliaire s’écoule de la chambre postérieure à travers la pupille vers la chambre antérieure, puis sort par le trabéculum de l’angle. Dans le glaucome malin, cette voie est perturbée.
L’instillation d’atropine relâche le muscle ciliaire, augmente la tension de la zonule et déplace le cristallin vers l’arrière. Cela peut permettre à l’humeur aqueuse qui s’est accumulée dans la cavité vitréenne de revenir vers l’avant.
En revanche, les myotiques comme la pilocarpine contractent le muscle ciliaire. Cette contraction relâche la zonule, pousse le cristallin vers l’avant et favorise la protrusion antérieure du corps ciliaire, aggravant ainsi le bloc ciliaire 6). Par conséquent, les myotiques sont contre-indiqués dans le glaucome malin.
Dans l’œil pseudophaque, le diamètre horizontal du complexe IOL-sac est plus grand que celui du cristallin naturel, ce qui le rend plus susceptible d’entrer en contact avec les procès ciliaires 4). Une partie de l’humeur aqueuse produite par les procès ciliaires est sécrétée vers l’arrière (cavité vitréenne). Si la membrane hyaloïde antérieure est intacte, l’écoulement du liquide vers l’avant est entravé, créant un gradient de pression et un amincissement de la chambre antérieure.
Même dans les yeux ayant subi une vitrectomie, la persistance de la membrane hyaloïde antérieure peut entraîner l’apparition de la maladie 4). Dans un cas de récidive avec un décalage myopique de plus de 3 D, une combinaison de goniosynéchie (goniosynechialysis), d’iridectomie et de zonulo-hyaloidectomie a permis de restaurer la réfraction et la pression intraoculaire 4). Par conséquent, lors d’une vitrectomie, il est essentiel de disséquer complètement la membrane hyaloïde antérieure et de traiter jusqu’à la périphérie la plus extrême pour prévenir la récidive.
Le topiramate augmente la perméabilité des vaisseaux choroïdiens ciliaires, provoquant un gonflement du corps ciliaire et de la choroïde ainsi qu’une rotation antérieure du corps ciliaire 1). Dans la microphtalmie, l’épaississement scléral entrave le drainage des veines vortiqueuses, augmentant encore le risque d’épanchement uvéal 1).
La mise en place d’un CTR provoque l’expansion et l’épaississement du sac capsulaire, et le complexe CTR-IOL entre en contact circonférentiel avec le corps ciliaire et l’iris postérieur 2). Cela comprime l’espace ciliaire et augmente la résistance au déplacement de l’humeur aqueuse de l’arrière vers l’avant. Le grand diamètre du complexe CTR-IOL limite partiellement le déplacement antérieur, de sorte que la profondeur de la chambre antérieure peut être maintenue tout en présentant une occlusion angulaire de type plateau iris 2). Cette présentation atypique diffère de l’image classique du glaucome malin avec une « chambre antérieure uniformément peu profonde », ce qui fait de l’évaluation détaillée de la morphologie angulaire par AS-OCT la clé du diagnostic.
Chean et al. (2021) ont rapporté un cas de déviation aqueuse (myopic surprise) se manifestant uniquement par une myopisation après chirurgie de la cataracte 3). La pression intraoculaire est restée normale pendant environ trois ans après l’opération, ce qui a retardé le diagnostic. Même si la profondeur de la chambre antérieure mesurée par biométrie semble normale, des erreurs de mesure peuvent survenir dans les yeux à axe court. Par conséquent, en cas de myopisation, la déviation aqueuse doit être incluse dans le diagnostic différentiel.
Stephenson et al. (2023) ont rapporté un cas de déviation aqueuse avec un décalage myopique de plus de 3 D dans un œil ayant subi une vitrectomie, une chirurgie de la cataracte et une implantation d’iris artificiel 4). Ils ont montré que même après vitrectomie, si la membrane hyaloïde antérieure persiste, la déviation aqueuse peut survenir. La goniosynéchie + iridectomie + zonulo-hyaloidectomie a rétabli la réfraction et la pression intraoculaire.
Goto et al. (2024) ont caractérisé pour la première fois par AS-OCT un blocage angulaire secondaire dû à un déplacement antérieur du complexe CTR-IOL 2). Ils ont rapporté une image atypique ressemblant à un iris plateau avec une profondeur de chambre antérieure préservée, montrant l’utilité de l’AS-OCT pour détecter un blocage angulaire secondaire après chirurgie de la cataracte avec pose de CTR.
Une approche par étapes (traitement médicamenteux → laser Nd:YAG → cyclodiode → chirurgie) a été proposée 3). Le cyclodiode provoque une nécrose de coagulation et une atrophie des procès ciliaires, pouvant entraîner une destruction de l’interface ciliaire-vitréenne et une rotation postérieure du corps ciliaire. Cependant, les conditions d’irradiation nécessaires pour détruire l’interface ciliaire-vitréenne ne sont pas encore établies. Si les médicaments et le laser sont insuffisants, la chirurgie pour créer un œil unicaméral reste l’option thérapeutique finale 3).