
Ostéome chorọdien
1. Qu’est-ce que l’ostéome choroïdien ?
Section intitulée « 1. Qu’est-ce que l’ostéome choroïdien ? »L’ostéome choroïdien (choroidal osteoma) est une tumeur bénigne dans laquelle du tissu osseux hétérotopique se forme dans la choroïde. Il survient préférentiellement au pôle postérieur du fond d’œil et se présente comme une lésion jaune-blanc plate. La cause est inconnue ; des théories suggèrent une séparation osseuse (tissu osseux hétérotopique) ou une implication inflammatoire.
Au cours de l’évolution, une pigmentation, une atrophie de l’épithélium pigmentaire rétinien (EPR) et une décalcification peuvent survenir, modifiant l’aspect du fond d’œil selon le stade. La lésion a tendance à s’agrandir lentement mais finit par s’arrêter.
Épidémiologie
Section intitulée « Épidémiologie »- C’est une tumeur bénigne relativement rare, représentant une très petite partie de toutes les tumeurs intraoculaires.
- Elle est plus fréquente chez les jeunes femmes, et on suppose une implication de la sécrétion hormonale, mais la cause est inconnue.
- Elle peut survenir de manière bilatérale.
- Elle se développe préférentiellement au pôle postérieur (en particulier autour de la papille optique).
Stades d’évolution de la lésion
Section intitulée « Stades d’évolution de la lésion »Bien qu’il n’existe pas de classification claire, on distingue les stades d’évolution suivants.
| Stade | Caractéristiques |
|---|---|
| Initial | Lésion maculaire ou plate de couleur blanc-jaunâtre ou jaune-orangé au pôle postérieur. Presque pas de relief. |
| Avancé | Décalcification, dégénérescence et atrophie de l’EPR et des couches externes de la rétine, modifiant l’aspect du fond d’œil. |
| Avec CNV | Apparition de néovascularisation choroïdienne (NVC), entraînant une hémorragie rétinienne et une baisse de l’acuité visuelle. |
C’est une tumeur bénigne caractérisée par la formation de tissu osseux ectopique dans la choroïde. Elle survient préférentiellement au pôle postérieur et est légèrement plus fréquente chez les jeunes femmes. Aucun cas de malignisation ou de métastase n’a été rapporté, mais une extension à la macula peut entraîner une baisse de l’acuité visuelle. Il n’existe pas de traitement curatif, et la surveillance est la règle.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »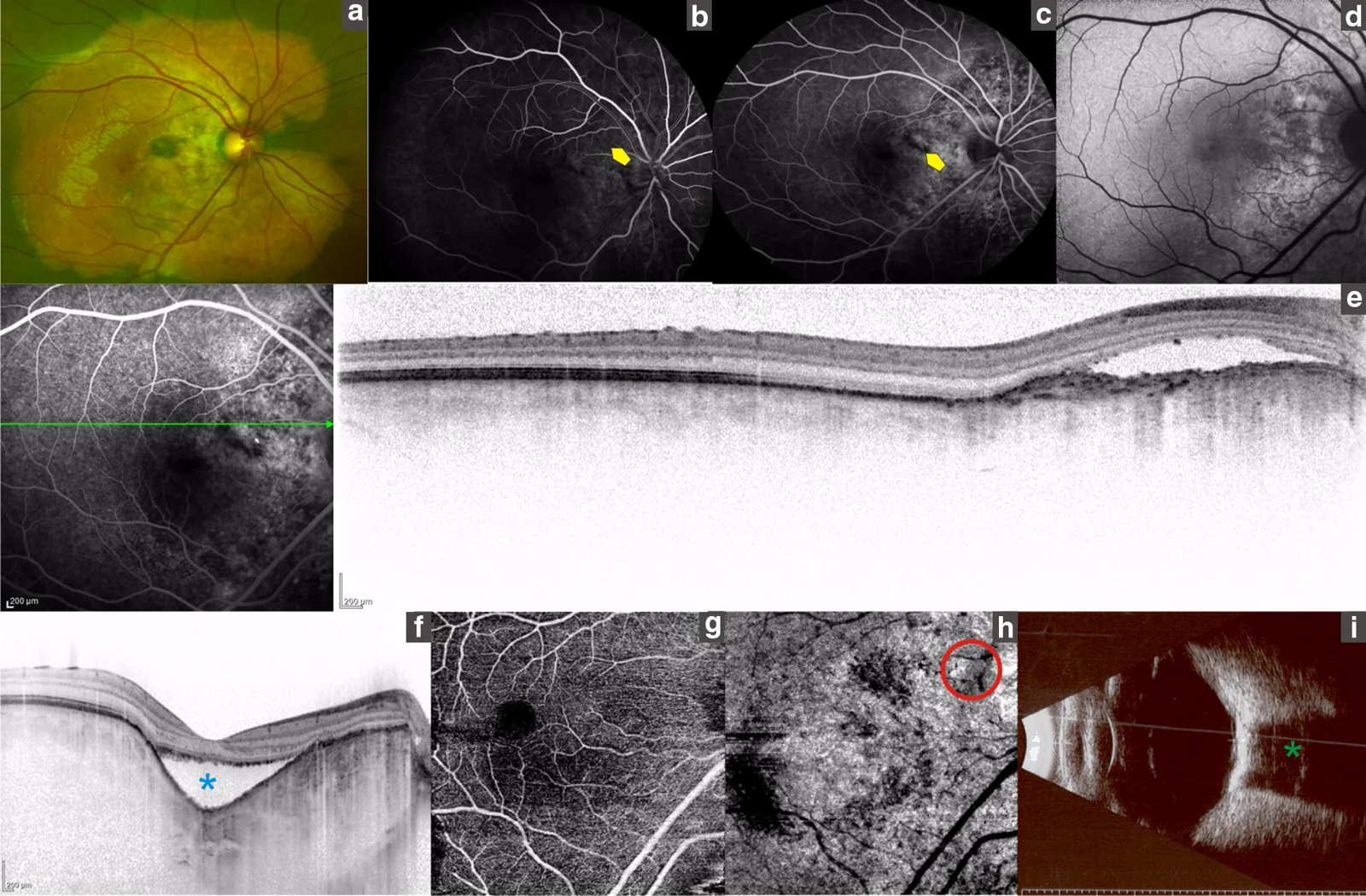
Symptômes subjectifs
Section intitulée « Symptômes subjectifs »- Déficit du champ visuel : survient en regard de la tumeur. Souvent peu perceptible au début.
- Baisse de l’acuité visuelle : une baisse importante survient lorsque la lésion atteint la macula.
- Hémorragie rétinienne et hémorragie du vitré : surviennent en cas de développement d’une NVC. Elles sont une cause de baisse brutale de l’acuité visuelle.
- Si la tumeur n’atteint pas la macula, les symptômes subjectifs peuvent être absents.
Signes du fond d’œil
Section intitulée « Signes du fond d’œil »Au pôle postérieur, en particulier autour de la papille optique, on observe les signes suivants :
- Lésion maculaire de couleur blanc-jaunâtre à jaune-orangé, presque sans relief. Peut être irrégulière.
- Observée comme une lésion surélevée plate, bien délimitée, de couleur blanc-jaunâtre. La surface de la tumeur est souvent accompagnée de fins vaisseaux.
- Avec la progression, une dégénérescence et une atrophie de l’EPR adjacent et des couches externes de la rétine se produisent, modifiant l’aspect du fond d’œil.
Signes d’imagerie
Section intitulée « Signes d’imagerie »Angiographie à la fluorescéine (FA) :
- Dès le début, on observe une hyperfluorescence tachetée et granuleuse correspondant à la tumeur.
- Au stade tardif, elle devient une hyperfluorescence diffuse.
- En cas de complication par une CNV, on note une fuite de fluorescéine.
Échographie en mode B :
- On observe une réflexion élevée en forme de plaque au niveau de la tumeur, avec une ombre acoustique postérieure (disparition ou atténuation de la réflexion).
TDM (élément clé pour le diagnostic définitif) :
- La zone tumorale présente une valeur d’atténuation élevée (haute densité) comparable à celle de l’os.
OCT :
- Utile pour évaluer la hauteur tumorale, la CNV et le liquide sous-rétinien.
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »Le mécanisme d’apparition de l’ostéome choroidien est inconnu. Actuellement, les hypothèses suivantes sont proposées.
- Théorie du choristome osseux : suppose une anomalie congénitale dans laquelle du tissu osseux ectopique se forme dans la choroïde.
- Théorie de l’implication inflammatoire : l’ossification se produirait à la suite d’une inflammation.
- Hypothèse hormonale : étant plus fréquente chez les jeunes femmes, une association avec la sécrétion hormonale est suspectée, mais le mécanisme précis n’est pas élucidé.
Aucun cas de malignité ou de métastase n’a été rapporté, et la tumeur elle-même suit une évolution bénigne.
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »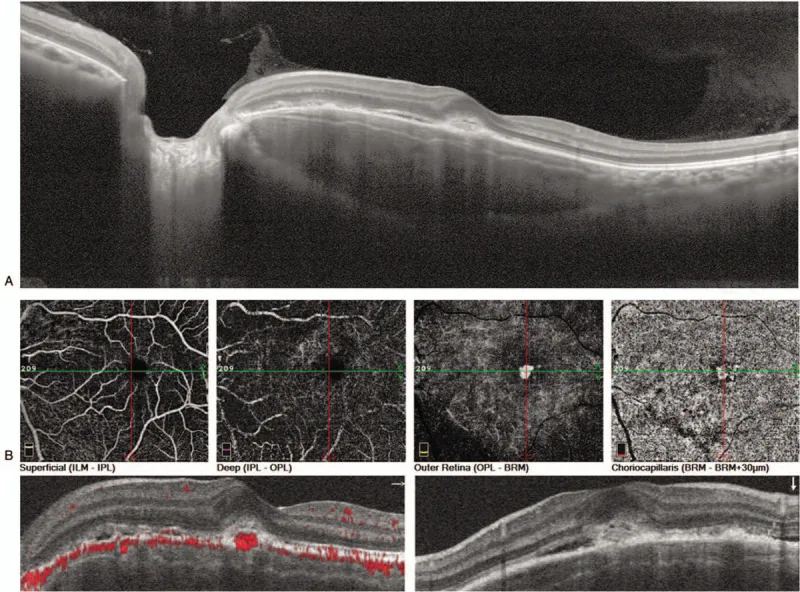
Points clés du diagnostic
Section intitulée « Points clés du diagnostic »Une lésion plate jaune-blanc au pôle postérieur (en particulier autour de la papille optique) est observée à l’examen du fond d’œil, et le diagnostic est confirmé par tomodensitométrie (TDM) et échographie.
- Examen du fond d’œil : lésion plate jaune-blanc à jaune-orange au pôle postérieur. Évaluer l’extension de la lésion, les modifications de l’EPR et la présence de NVC.
- TDM (diagnostic de confirmation) : une valeur d’atténuation élevée (haute densité) équivalente à celle de l’os au niveau de la tumeur est l’élément clé du diagnostic.
- Échographie : une image hyperéchogène en plaque avec un cône d’ombre postérieur est caractéristique et soutient le diagnostic.
- Angiographie à la fluorescéine (FA) : hyperfluorescence tachetée/granulaire précoce et hyperfluorescence diffuse tardive. En cas de NVC, une fuite de fluorescence s’ajoute.
- OCT : permet d’évaluer en détail les modifications de l’EPR et de la rétine neurosensorielle, le liquide sous-rétinien et la présence de NVC.
Diagnostic différentiel
Section intitulée « Diagnostic différentiel »Il est important de différencier l’ostéome choroïdien des maladies associées à une calcification.
| Maladie | Points clés du diagnostic différentiel |
|---|---|
| Rétinoblastome | Fréquent chez l’enfant. Tumeur blanche avec calcifications. Évaluation par TDM et échographie. |
| Astrocytome (associé à la sclérose tubéreuse) | Lésion blanche péripaillaire ou au pôle postérieur. Calcifications présentes. |
| Mélanome choroïdien malin | Élévation en dôme, pigmenté. Double circulation à l’angiographie. Faible échogénicité interne à l’échographie. |
| Métastase choroïdienne | Antécédent de tumeur maligne systémique. Lésions plates et multiples. Hyperfluorescence précoce à l’angiographie. |
| Hémangiome choroïdien | Couleur orange-rouge. Motif caractéristique à l’angiographie. Haute échogénicité à l’échographie. |
Le diagnostic définitif repose sur la mise en évidence d’une densité élevée équivalente à celle de l’os au scanner. Il est associé à une ombre acoustique à l’échographie. En cas de lésion blanchâtre et plate au pôle postérieur à l’examen du fond d’œil, suspecter cette maladie et réaliser un scanner et une échographie pour confirmation.
5. Traitement standard
Section intitulée « 5. Traitement standard »Principe de base : surveillance
Section intitulée « Principe de base : surveillance »Aucun traitement curatif n’étant établi, la surveillance est la règle. Il est important d’évaluer régulièrement l’extension de la tumeur et la présence de néovaisseaux. Tant que la macula n’est pas atteinte, l’impact sur la fonction visuelle est souvent mineur.
Traitement en cas de développement de CNV
Section intitulée « Traitement en cas de développement de CNV »En cas de confirmation d’une néovascularisation choroïdienne (CNV), les traitements symptomatiques suivants sont envisagés pour préserver la vision.
- Photocoagulation (laser) : réalisée pour la CNV. Les lésions extrafovéolaires sont les plus adaptées.
- Thérapie photodynamique (PDT) : utilisant la vertéporfine. Bien que non remboursée, une certaine efficacité a été rapportée.
- Injections intravitréennes d’anti-VEGF : ranibizumab, aflibercept, bevacizumab, etc. Non remboursées, mais une régression de la CNV est attendue.
L’indication et le choix du traitement sont déterminés individuellement en fonction de la localisation de la CNV, de l’acuité visuelle et du contexte du patient.
Il n’existe pas de traitement curatif ; la surveillance est la règle. En cas de développement d’une CNV entraînant une baisse de vision, un traitement symptomatique par PDT ou injections intravitréennes d’anti-VEGF peut être proposé. Ces traitements n’étant pas remboursés, la décision doit être prise après une discussion approfondie avec le médecin traitant.
6. Physiopathologie et mécanisme détaillé
Section intitulée « 6. Physiopathologie et mécanisme détaillé »Mécanisme de l’ossification hétérotopique
Section intitulée « Mécanisme de l’ossification hétérotopique »L’ostéome choroïdien est une ossification hétérotopique dans la choroïde. Le mécanisme par lequel du tissu osseux apparaît dans la choroïde normale n’est pas élucidé, mais les points suivants sont connus.
- La lésion s’étend progressivement mais a tendance à finir par s’arrêter.
- Étant plus fréquente chez les jeunes femmes, une implication hormonale est suspectée, mais le mécanisme moléculaire est inconnu.
- La théorie du choristome osseux suppose une migration aberrante de tissu osseux due à une anomalie embryonnaire.
- La théorie inflammatoire suppose une induction d’ossification après inflammation, mais un antécédent inflammatoire clair est souvent absent.
Décalcification
Section intitulée « Décalcification »Au cours de l’évolution, une décalcification de la tumeur peut survenir. Lorsqu’elle se produit, les limites de l’ostéome au fond d’œil deviennent floues et la couleur change. Certains rapports indiquent que la CNV est plus fréquente après la décalcification. La fréquence de la décalcification et son impact quantitatif sur le pronostic visuel font encore l’objet de collecte de cas.
Mécanisme de la déficience visuelle
Section intitulée « Mécanisme de la déficience visuelle »- L’EPR et les photorécepteurs situés directement au-dessus de la tumeur subissent une dégénérescence et une atrophie avec le temps.
- Lorsque la CNV se développe, les fuites vasculaires provoquent un liquide sous-rétinien et une hémorragie rétinienne, entraînant une baisse brutale de l’acuité visuelle.
- Si la macula est impliquée, les photorécepteurs de la fovéa sont endommagés, entraînant une baisse sévère de l’acuité visuelle. Une fois survenue, la récupération est difficile.
Pronostic
Section intitulée « Pronostic »- Tant que la macula n’est pas impliquée, il n’y a pas de déficience visuelle majeure.
- Si la lésion s’étend à la macula, une baisse sévère de l’acuité visuelle se produit et la récupération est peu probable.
- Dans les cas bilatéraux, même si la progression d’un œil est en avance, il faut surveiller l’évolution de l’autre œil.
- Aucun cas de transformation maligne ou de métastase n’a été rapporté.
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Application du traitement anti-VEGF à la CNV
Section intitulée « Application du traitement anti-VEGF à la CNV »Bien que non couvert par l’assurance maladie, l’injection intravitréenne d’anti-VEGF avec du ranibizumab ou de l’aflibercept est appliquée aux cas compliqués de CNV. Des rapports de cas et de petites séries ont rapporté une régression de la CNV et une amélioration de l’acuité visuelle, mais il n’existe actuellement aucun essai contrôlé randomisé concernant le protocole d’administration (intervalle, nombre de doses, combinaison avec d’autres traitements). L’accumulation de preuves à l’avenir est attendue.
Évaluation détaillée par OCT et OCT-A
Section intitulée « Évaluation détaillée par OCT et OCT-A »Les progrès de l’angiographie par tomographie par cohérence optique (OCT-A) permettent désormais une évaluation non invasive détaillée de la structure vasculaire de la CNV. L’évaluation quantitative de la CNV à l’aide de l’OCT-A dans l’ostéome chorọidien et son application au suivi sont des défis futurs.
Élucidation du mécanisme de décalcification
Section intitulée « Élucidation du mécanisme de décalcification »Le mécanisme moléculaire expliquant pourquoi la décalcification se produit et si la CNV est plus susceptible de se développer après la décalcification reste inconnu. Des recherches sont en cours pour étudier la relation avec les facteurs liés au métabolisme osseux (tels que RANKL et OPG).
8. Références
Section intitulée « 8. Références »- Shields CL, Sun H, Demirci H, et al. Factors predictive of tumor growth, tumor decalcification, choroidal neovascularization, and visual outcome in 74 eyes with choroidal osteoma. Arch Ophthalmol. 2005;123(12):1658-1666.
- Shields JA, Shields CL. Intraocular Tumors: An Atlas and Textbook. 3rd ed. Philadelphia: Wolters Kluwer; 2015.
- Tsui I, Gillies MC, Barlow R, et al. Photodynamic therapy for choroidal neovascularization complicating choroidal osteoma. Retina. 2006;26(7):804-810.
- Nadarajah S, Blumenkranz MS. Intravitreal bevacizumab for choroidal neovascularization secondary to choroidal osteoma. Retina. 2009;29(6):888-890.
