การฉีดยาต้าน VEGF เข้าในน้ำวุ้นตา เป็นการรักษาโดยการฉีดยาโดยตรงเข้าไปในช่องวุ้นตา เพื่อยับยั้งการทำงานของ VEGF (การสร้างเส้นเลือดใหม่และการเพิ่มการซึมผ่านของหลอดเลือด) ข้อบ่งชี้หลัก ได้แก่ โรคหลอดเลือดจอประสาทตา เช่น จอประสาทตา เสื่อมตามอายุ จอประสาทตา บวมจากเบาหวาน และหลอดเลือดดำจอประสาทตาอุดตัน
การรักษาด้วยยาต้าน VEGF มีความก้าวหน้าอย่างรวดเร็วในการประยุกต์ใช้ทางคลินิกในช่วงปี 2000
ปี เหตุการณ์ 2004 เริ่มการทดลองใช้ยาเบวาซิซูแมบ ในลูกตา 2006 FDA อนุมัติรานิบิซูแมบ (การทดลอง MARINA/ANCHOR) 12) 2011 FDA อนุมัติอะฟลิเบอร์เซปต์ (การทดลอง VIEW) 12) 2019 FDA อนุมัติโบรลูซิซูแมบ (การทดลอง HAWK/HARRIER) 10) 2022 FDA อนุมัติฟาริซิแมบ (การทดลอง TENAYA/LUCERNE/YOSEMITE/RHINE) 8)
จอประสาทตา เสื่อมชนิดเปียกตามอายุ (nAMD )เส้นเลือดใหม่ในคอรอยด์ (CNV )1) จอประสาทตา บวมจากเบาหวาน (DME)จอประสาทตา บวมที่เกิดจากจอตาเบาหวาน2) หลอดเลือดดำจอตาอุดตัน (RVO ) : จอประสาทตา บวมในหลอดเลือดดำจอตาส่วนกลางหรือแขนงอุดตัน6) จอตาเบาหวานชนิดงอกเส้นเลือด (PDR) : ช่วยเสริมหรือทดแทน PRP (รานิบิซูแมบ )5) เส้นเลือดใหม่ในคอรอยด์ จากสายตาสั้น ผิดปกติ (mCNV )แอฟลิเบอร์เซปต์ , รานิบิซูแมบ 4) โรคหลอดเลือดคอรอยด์ แบบโพลิป (PCV ) : โบรลูซิซูแมบ มีอัตราการยุบตัวของโพลิปสูง14) จอตาในทารกคลอดก่อนกำหนด (ROP ) : รานิบิซูแมบ 0.2 มก. (อนุมัติปี 2019), แอฟลิเบอร์เซปต์ 0.4 มก. (อนุมัติกันยายน 2022)3) จอประสาทตา ฝ่อแบบแผนที่ (GA)คอมพลีเมนต์ เยื่อบุตาอักเสบ (Endophthalmitis)
Q
การรักษาด้วยยาต้าน VEGF ใช้กับโรคอะไรบ้าง?
A
จอประสาทตา เสื่อมตามอายุ จอประสาทตา บวมจากเบาหวาน และหลอดเลือดดำจอตาอุดตัน เป็นสามโรคบ่งชี้หลัก ในทุกโรคเหล่านี้ VEGF ถูกผลิตมากเกินไป ทำให้เกิดเส้นเลือดใหม่และการซึมผ่านของหลอดเลือดเพิ่มขึ้น ซึ่งทำให้การมองเห็น ในบริเวณจอประสาทตา ลดลง โดยการฉีดยาต้าน VEGF เข้าไปในวุ้นตา โดยตรง จะยับยั้งกระบวนการทางพยาธิวิทยาเหล่านี้เพื่อปรับปรุงหรือรักษาการมองเห็น ในช่วงไม่กี่ปีที่ผ่านมา ข้อบ่งชี้ได้ขยายไปถึง PDR, mCNV , ROP และโรคหลอดเลือดคอรอยด์ แบบโพลิป
ชื่อยา ชื่อการค้า น้ำหนักโมเลกุล กลไกการออกฤทธิ์ ขนาดยา การอนุมัติ (ญี่ปุ่น) รานิบิซูแมบ ลูเซนทิส® 48 kDa ชิ้นส่วน Fab ที่ต้าน VEGF-A 0.5 มก. (AMD /RVO ), 0.3 มก. (DME) 2009 แอฟลิเบอร์เซปต์ อายลีอา® 115 kDa ยับยั้ง VEGF-A/B และ PlGF (ตัวรับล่อ) 2 มก. / 8 มก. (HD) 2012 เพกาพทานิบ แมคยูเจน® — แอปทาเมอร์ VEGF165 0.3 มก. 2008 โบรลูซิซูแมบ เบโอวู® 26 กิโลดาลตัน VEGF-A scFv 6 มก. พ.ศ. 2563 ฟาริซิแมบ วาบิสโม® 149 กิโลดาลตัน แอนติบอดีแบบคู่จำเพาะต่อ VEGF-A + Ang-2 6 มก. พ.ศ. 2566 เบวาซิซูแมบ อาวาสติน® 148 กิโลดาลตัน VEGF-A IgG แบบเต็มความยาว 1.25 มก. — (นอกข้อบ่งใช้)
รานิบิซูแมบ (ลูเซนทิส®)
น้ำหนักโมเลกุล : 48 kDa (ชิ้นส่วน Fab)
กลไกการออกฤทธิ์ : ยับยั้ง VEGF-A ทุกไอโซฟอร์ม
การทดลองหลัก : มีประสิทธิภาพใน AMD จากการทดลอง MARINA/ANCHOR เทียบเท่าเบวาซิซูแมบ ในการทดลอง CATT 12)
ลักษณะเด่น : สามารถให้ยาเสริมทุก 6 เดือนผ่าน PDS 98% ไม่ต้องฉีดรายเดือนหลังจาก 2 ปี ใน ROP ใช้ 40% ของขนาดผู้ใหญ่ (0.2 มก.) 12)
อะฟลิเบอร์เซปต์ (อายเลีย®)
น้ำหนักโมเลกุล : 115 kDa (โปรตีนฟิวชัน)
กลไกการออกฤทธิ์ : ยับยั้งสามปัจจัยพร้อมกัน: VEGF-A, VEGF-B และ PlGF มีความสัมพันธ์สูงสุดกับ VEGF-A โดย Kd = 0.49 pM
การทดลองหลัก : ไม่ด้อยกว่ารานิบิซูแมบ ในการทดลอง VIEW ขนาดสูง 8 มก. (HD) ให้ระยะห่างได้ถึง 16 สัปดาห์ 12, 13)
ลักษณะเด่น : สเปกตรัมการยับยั้ง VEGF กว้าง ใน ROP ใช้ 20% ของขนาดผู้ใหญ่ (0.4 มก.) 13)
โบรลูซิซูแมบ (บีโอวู®)
น้ำหนักโมเลกุล : 26 kDa (scFv เล็กที่สุดในยาที่มีอยู่)
กลไกการออกฤทธิ์ : โครงสร้าง scFv ทำให้ให้ยาได้ความเข้มข้นโมลาร์สูงกว่าอะฟลิเบอร์เซปต์ประมาณ 12 เท่า ซึมผ่านเนื้อเยื่อได้ดี
การทดลองหลัก : บรรลุความไม่ด้อยกว่าในการทดลอง HAWK/HARRIER มากถึง 55% รักษาระยะห่าง 12 สัปดาห์ 10)
ข้อควรระวัง : ใน HAWK/HARRIER มีรายงาน IOI, จอประสาทตา อักเสบ และจอประสาทตา อุดตัน ควรสังเกตอาการอักเสบหลังฉีด 10)
ฟาริซิแมบ (Vabysmo®)
น้ำหนักโมเลกุล : 149 kDa (แอนติบอดี IgG แบบสองความจำเพาะ)
กลไกการออกฤทธิ์ : ยับยั้ง VEGF-A และ Ang-2 (angiopoietin-2) พร้อมกัน เป็นยาที่มีเป้าหมายคู่ชนิดแรกของโลก
การทดลองหลัก : TENAYA/LUCERNE (nAMD ) สูงสุด Q16W ผู้ป่วย nAMD 63% บรรลุ Q16W ในปีที่สอง 8)
ลักษณะเด่น : ใน RVO (BALATON/COMINO ) อัตราการหายไปของการรั่วซึม FA สูงกว่า aflibercept 8)
เบวาซิซูแมบ (Avastin®)
น้ำหนักโมเลกุล : 148 kDa (IgG ความยาวเต็ม)
กลไกการออกฤทธิ์ : ยับยั้ง VEGF-A (การใช้แบบนอกข้อบ่งชี้ในจักษุวิทยา)
การทดลองหลัก : การทดลอง CATT แสดงประสิทธิภาพเทียบเท่า ranibizumab 12)
สถานะการใช้ : ต้นทุนต่ำกว่าอย่างมาก ใช้ผลิตภัณฑ์สำหรับฉีดเข้าหลอดเลือดดำซึ่งถูกแบ่งบรรจุอย่างปลอดเชื้อ
เพกาพทาเนีย (Macugen®)
กลไกการออกฤทธิ์ : อะพทาเมอร์จำเพาะต่อ VEGF165
สถานะปัจจุบัน : ยารุ่นแรกที่ได้รับการอนุมัติในปี 2008 ปัจจุบันยารุ่นใหม่เป็นหลัก มีส่วนช่วยในการสร้างแนวคิดการรักษาด้วย anti-VEGF ในระยะแรก
Q
ควรเลือกยาใด?
A
การเลือกขึ้นอยู่กับโรคที่เหมาะสม ระยะห่างการฉีดที่ต้องการ และความเสี่ยงของภาวะแทรกซ้อน โดยทั่วไปใน nAMD ยา aflibercept, faricimab และ brolucizumab เหนือกว่าในการยืดระยะห่างการฉีด ใน DME ยามาตรฐานคือ aflibercept และ faricimab ส่วน brolucizumab เมื่อพิจารณาความเสี่ยง IOI แล้ว มีข้อดีคืออัตราการหายของติ่งเนื้อสูงกว่าในผู้ป่วย PCV ส่วน faricimab สามารถฉีดได้สูงสุด Q16W (ทุก 16 สัปดาห์) ช่วยลดภาระการมาโรงพยาบาล ท้ายที่สุด แพทย์ผู้รักษาจะเป็นผู้ตัดสินใจอย่างครอบคลุม
Q
สามารถใช้ bevacizumab (Avastin) ได้หรือไม่?
A
ในสาขาจักษุวิทยา เป็นการใช้แบบนอกข้อบ่งชี้ (off-label) และต้องเตรียมยาฉีดเข้าหลอดเลือดดำให้ปราศจากเชื้อเพื่อใช้ทางตา การทดลอง CATT ยืนยันประสิทธิภาพในการปรับปรุงการมองเห็น ที่เทียบเท่ากับ ranibizumab และเนื่องจากต้นทุนต่ำกว่ามาก จึงถูกใช้อย่างแพร่หลายทั่วโลก อย่างไรก็ตาม ในญี่ปุ่นไม่มีประกันครอบคลุม และการใช้ขึ้นอยู่กับดุลยพินิจของสถานพยาบาล
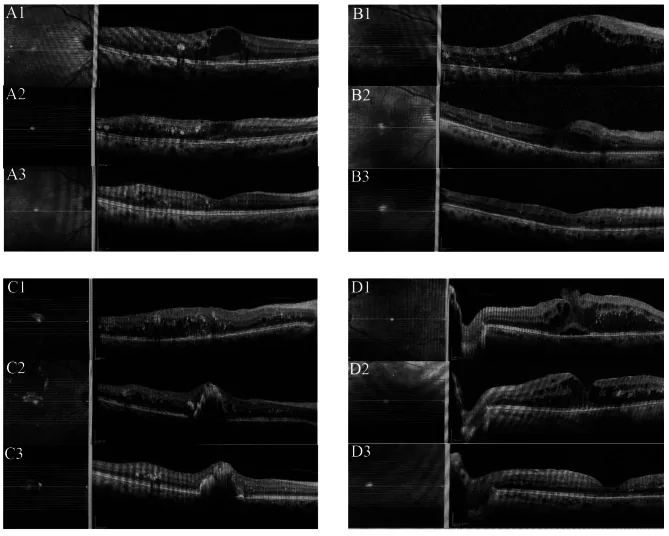
ภาพ OCT ก่อนและหลังการฉีด aflibercept เข้าแก้วตาเพื่อรักษาภาวะจอประสาทตาบวมจากเบาหวาน Koc H, Alpay A, Ugurbas SH. Comparison of the efficacy of intravitreal Anti-VEGF versus intravitreal dexamethasone implant in treatment resistant diabetic macular edema. BMC Ophthalmol. 2023 Mar 13;23(1):97. PM
CI D: PMC10009964. License: CC BY.
แสดงภาพตัดขวาง OCT ของจอประสาทตา ของผู้ป่วยที่มีภาวะจอประสาทตา บวมจากเบาหวานชนิดดื้อรักษา (DME) ก่อนฉีดเข้าแก้วตา (A1/B1/C1/D1) หลังฉีด aflibercept 3 ครั้ง (A2/B2/C2/D2) และหลังฉีด 6 ครั้ง (A3/B3/C3/D3) ซึ่งสอดคล้องกับผลการลดอาการบวมน้ำของจอประสาทตา ด้วยยาต้าน VEGF ที่กล่าวถึงในหัวข้อ “3. โรคที่บ่งชี้และสูตรการให้ยา”
การให้ยาต้าน VEGF ดำเนินการในสองระยะ: ระยะเริ่มต้นและระยะคงสภาพ
ระยะเริ่มต้น : เพื่อยับยั้งการดำเนินโรคอย่างรุนแรง ให้ยาแบบคงที่ 3-6 ครั้งต่อเดือน (แตกต่างกันไปตามโรคและยา)ระยะคงสภาพ มีสามวิธีดังนี้:
PRN (ตามความจำเป็น) : ตรวจทุกเดือน ให้ยาเฉพาะเมื่อมีสัญญาณของการกลับเป็นซ้ำการให้แบบคงที่ : ให้ยาอย่างสม่ำเสมอในช่วงเวลาคงที่ เช่น ทุก 2 เดือนหรือ 3 เดือนTreat and Extend (T&E) : หากไม่มีสัญญาณของกิจกรรม ให้ขยายช่วงห่างออกไป 2 สัปดาห์ หากกลับเป็นซ้ำ ให้缩短ช่วงห่าง
สำหรับ ranibizumab แนะนำให้ให้ยา 3 ครั้งในระยะเริ่มต้น (เดือนละครั้ง) ตามด้วย PRN ในระยะคงสภาพ สำหรับ aflibercept แนะนำให้ให้ยา 3 ครั้งในระยะเริ่มต้น (เดือนละครั้ง) ตามด้วยการให้แบบคงที่ทุก 2 เดือนหรือวิธี T&E ในช่วงไม่กี่ปีที่ผ่านมา วิธี T&E ถูกนำมาใช้ในหลายสถานพยาบาล
โรคที่บ่งชี้ ยาที่แนะนำ ระยะเริ่มต้น ระยะคงสภาพ nAMD (รานิบิซูแมบ ) ลูเซนทิส® 0.5 มก. เดือนละ 1 ครั้ง × 3 ครั้ง1) PRN (สังเกตทุกเดือน) nAMD (อะฟลิเบอร์เซปต์) ไอลีอา® 2 มก. เดือนละ 1 ครั้ง × 3 ครั้ง1) คงที่ทุก 2 เดือน หรือ T&E (สูงสุด 3 เดือน) nAMD (โบรลูซิซูแมบ ) เบโอวู® 6 มก. เดือนละ 1 ครั้ง × 3 ครั้ง ช่วงห่าง 8–12 สัปดาห์10) nAMD (ฟาริซิแมบ ) วาบิสโม® 6 มก. Q4W × 4 ครั้ง Q8W ถึง Q16W8) DME (อะฟลิเบอร์เซปต์) Eylea® 2 มก. เดือนละ 1 ครั้ง × 5 ครั้ง2) ทุก 2 เดือน DME (รานิบิซูแมบ ) Lucentis® 0.5 มก. เดือนละ 1 ครั้ง × 3 ครั้ง2) PRN DME (ฟาริซิแมบ ) Vabysmo® 6 มก. Q4W × 4–6 ครั้ง PTI (สูงสุด Q16W)8, 13) RVO อะฟลิเบอร์เซปต์/ฟาริซิแมบ Q4W × 6 เดือน PTI (สูงสุด Q16W)8) จอประสาทตาเสื่อมจากเบาหวาน ชนิด proliferativeรานิบิซูแมบ 0.3 มก.— ไม่ด้อยกว่า PRP 5) mCNV อะฟลิเบอร์เซปต์/รานิบิซูแมบ 1-3 ครั้งแรก PRN (อาจหายได้ครั้งเดียว) 4) ROP (รานิบิซูแมบ )ลูเซนทิส® 0.2 มก./0.02 มล. ครั้งแรก เพิ่มเมื่อกลับเป็นซ้ำ (ห่างกัน ≥1 เดือน) 3) ROP (อะฟลิเบอร์เซปต์)อายลีอา® 0.4 มก./0.01 มล. ครั้งแรก เพิ่มเมื่อกลับเป็นซ้ำ (ห่างกัน ≥1 เดือน) 3)
การจัดการ PCV (Polypoidal Choroidal Vasculopathy) : Brolucizumab เหนือกว่ายาอื่นในอัตราการหายของติ่งเนื้อประมาณ 79% และบรรลุการรักษาระยะห่าง 12 สัปดาห์ที่ 76% (48 สัปดาห์) 14) มีรายงานว่า Faricimab มีประสิทธิภาพแม้ในกรณี PCV ที่ดื้อต่อ ranibizumab 15)
การทดลอง BALATON (BRVO , n=553) 8) : Faricimab 6.0 มก. เทียบกับ aflibercept 2.0 มก. Q4W การเปลี่ยนแปลง BCVA ที่สัปดาห์ที่ 24 คือ +16.9 ตัวอักษร และ +17.5 ตัวอักษรตามลำดับ (บรรลุ non-inferiority, ขอบล่างของ CI 95.03% > -4 ตัวอักษร) การเปลี่ยนแปลง CST คือ -311.4 μm เทียบกับ -304.4 μm การปรับปรุง ≥15 ตัวอักษรใน faricimab 56.1% เทียบกับ aflibercept 60.4% อัตราการหายของการรั่วซึม FA คือ 33.6% ใน faricimab เทียบกับ 21.0% ใน aflibercept (p nominal=0.0023) แสดงให้เห็นว่า faricimab เหนือกว่าอย่างมีนัยสำคัญ
การทดลอง COMINO (CRVO /HRVO , n=729) 8) : สูตรเดียวกัน การเปลี่ยนแปลง BCVA ที่สัปดาห์ที่ 24 คือ +16.9 ตัวอักษร และ +17.3 ตัวอักษร (บรรลุ non-inferiority) การเปลี่ยนแปลง CST -461.6 μm เทียบกับ -448.8 μm การปรับปรุง ≥15 ตัวอักษรใน faricimab 56.6% เทียบกับ aflibercept 58.1% อัตราการหายของการรั่วซึม FA คือ 44.4% ใน faricimab เทียบกับ 30.0% ใน aflibercept (p nominal=0.0002) แสดงให้เห็นถึงความเหนือกว่าอย่างมีนัยสำคัญและผลการรักษาเสถียรภาพของหลอดเลือดผ่านการยับยั้ง Ang-2
ความปลอดภัยของ IOI ใน RVO (24 สัปดาห์) 8) : ในการทดลอง COMINO IOI เกิดขึ้นใน faricimab 2.2% เทียบกับ aflibercept 1.1% มีรายงาน uveitis รุนแรง 2 ราย (กลุ่ม faricimab) ไม่มีรายงาน retinal vasculitis ในการทดลองทั้ง BALATON/COMINO เหตุการณ์ APTC ใกล้เคียงกัน: BALATON faricimab 1.1% เทียบกับ aflibercept 1.5%, COMINO 1.1% เทียบกับ 1.4%
การรักษาเสริม (RVO ) : ในจอประสาทตา บวมจาก BRVO การรักษาแบบผสมผสานของ ranibizumab ร่วมกับเลเซอร์ไมโครพัลส์ระดับต่ำกว่าเกณฑ์กำลังถูกศึกษาเปรียบเทียบกับการรักษาเดี่ยว 11)
ยาต้าน VEGF ที่ได้รับการอนุมัติสำหรับการรักษา ROP (ณ เดือนธันวาคม 2022) มีสองชนิดดังต่อไปนี้ 3)
Ranibizumab (Lucentis®) 0.2 มก./0.02 มล. : 40% ของขนาดผู้ใหญ่ อนุมัติในปี 2019 เฉพาะรูปแบบขวดที่ได้รับการอนุมัติสำหรับ ROP Aflibercept (Eylea®) 0.4 มก./0.01 มล. : 20% ของขนาดผู้ใหญ่ อนุมัติในเดือนกันยายน 2022 เฉพาะรูปแบบขวดที่ได้รับการอนุมัติสำหรับ ROP การให้ซ้ำต้องมีระยะห่างอย่างน้อย 1 เดือน (ตามข้อกำหนดในเอกสารกำกับยา)
ข้อบ่งชี้ในการรักษา (ตามเกณฑ์การศึกษา ETROP ) 3) :
ROP โซน I ทุกรายที่มี plus diseaseROP โซน I ระยะ 3 ที่ไม่มี plus diseaseROP โซน II ระยะ 3 ที่มี plus diseaseROP ชนิดรุนแรง (A-ROP ): ดำเนินการโดยเร็วที่สุด
ข้อมูลการทดลองทางคลินิกหลัก 26, 28, 30) :
การทดลอง ยาและขนาด n อัตราความสำเร็จของการรักษา อัตราความสำเร็จของการเลเซอร์ หมายเหตุ BEAT-ROP 30) เบวาซิซูแมบ 0.625 มก.150 โซน I: การกลับเป็นซ้ำ 4% โซน I: การกลับเป็นซ้ำ 22% เบวาซิซูแมบ เหนือกว่าในโซน I RVRAINBOW26) รานิบิซูแมบ 0.2 มก.225 80.0% 66.2% สายตาสั้น ระดับสูงเมื่ออายุ 5 ปี: 8% เทียบกับเลเซอร์ 24%FIREFLEYE28) อะฟลิเบอร์เซปต์ 0.4 มก. 118 85.5% 82.1% ไม่ถึงเกณฑ์ไม่ด้อยกว่าแต่เกินเกณฑ์ 66%
ผลระยะยาวของการศึกษา RAINBOW 26, 29) : สายตาสั้น ระดับสูงเมื่ออายุ 5 ปีคือ 8% ในกลุ่มรานิบิซูแมบ 0.2 มก. เทียบกับ 24% ในกลุ่มเลเซอร์ (แตกต่างอย่างมีนัยสำคัญทางสถิติ) อัตราความผิดปกติของโครงสร้าง 1.5% ในกลุ่มรานิบิซูแมบ 0.2 มก. เทียบกับ 10% ในกลุ่มเลเซอร์ อัตราการฉีดซ้ำ 31% ระยะเวลาในการรักษาซ้ำ 4–16 สัปดาห์ (มัธยฐาน 8 สัปดาห์)
ผลติดตามของการศึกษา FIREFLEYE 28) : อัตราการกลับเป็นซ้ำ 21.9% อัตราการฉีดซ้ำ 17.8% ระยะเวลาเฉลี่ยจนถึงการฉีดซ้ำ 11 สัปดาห์ (4–17 สัปดาห์) ใน FIREFLEYE Next (ติดตามจนถึงอายุ 2 ปี) ไม่พบเหตุการณ์ไม่พึงประสงค์ที่เกี่ยวข้องกับการรักษาต่อการเจริญเติบโตทางร่างกายและพัฒนาการทางระบบประสาท
การเปรียบเทียบอัตราการกลับเป็นซ้ำระหว่างยา 3) :
Aflibercept: 13.9–28% (เวลาเฉลี่ยที่เกิดการกลับเป็นซ้ำ 11–14.2 สัปดาห์)
Ranibizumab: 20.8–83.0% (การกลับเป็นซ้ำเร็ว 5.9–9.3 สัปดาห์ → ต้องสังเกตอย่างระมัดระวังตั้งแต่ระยะแรก)
ข้อควรระวังสำหรับ A-ROP 3) : ใน A-ROP การรักษาด้วย anti-VEGF เพียงอย่างเดียวต้องได้รับการรักษาเพิ่มเติมใน 75.0–87.5% ของกรณี มีการกลับเป็นซ้ำเร็วภายใน 1–3 สัปดาห์หลังให้ยา หากกลับเป็นซ้ำภายใน 1 เดือน ให้ใช้เลเซอร์โฟโตโคแอกกูเลชันร่วมด้วย หากมีการเจริญของเนื้อเยื่อเส้นใยเป็นบริเวณกว้าง การรักษาด้วย anti-VEGF เพียงอย่างเดียวมีข้อห้าม (เสี่ยงต่อจอประสาทตาลอก ชนิด tractional เนื่องจากการหดตัว)
เทคนิคการฉีดสำหรับ ROP (ความแตกต่างจากผู้ใหญ่) 3) :
ตำแหน่งแทงเข็ม: 1.0–1.5 มม. ด้านหลังลิมบัส (แตกต่างจากผู้ใหญ่ที่ 3.5–4 มม. มาก ตำแหน่งเดียวกับผู้ใหญ่เสี่ยงต่อการทะลุจอประสาทตา )
ทิศทางเข็ม: ลงด้านล่าง (ไปทางด้านหลัง) (เนื่องจากเลนส์มีขนาดค่อนข้างใหญ่ การแทงเข้าสู่ศูนย์กลางเสี่ยงต่อการทะลุเลนส์)
ใช้เข็มขนาด 30 เกจหรือเล็กกว่า
ยืนยันขนาดยา: Ranibizumab 0.02 มล., Aflibercept 0.01 มล. (ตรวจสอบอย่างระมัดระวังเพื่อป้องกันการใช้ยาเกินขนาด)
การระงับความรู้สึก: ยาชาหยอดตา, ยาชาทางหลอดเลือดดำ, หรือยาสลบ ขึ้นอยู่กับสถานการณ์ของสถานพยาบาล
การติดตามผล 3) : หากหลอดเลือดจอประสาทตา ยังไม่ขยายไปถึง Zone III แนะนำให้ตรวจอวัยวะภายในดวงตาทุกสัปดาห์จนถึงสัปดาห์ที่ 17 หลังฉีด ตรวจอวัยวะภายในดวงตาเป็นระยะต่อไปเป็นเวลา 1 ปีหลังฉีด (มีรายงานจอประสาทตาลอก ชนิด tractional เกิดขึ้น 4–335 วันหลังฉีด)
Q
ยาชนิดใดมีประสิทธิภาพสูงสุดสำหรับจอประสาทตาบวมจากเบาหวาน?
A
ในการทดลอง Protocol T การมองเห็น ดีขึ้นมากที่สุดที่ 1 ปีด้วย aflibercept อย่างไรก็ตาม ในกลุ่มที่มีความรุนแรงน้อย (BCVA ≥ 20/40) ไม่มีความแตกต่างทางสถิติที่มีนัยสำคัญระหว่างยาทั้งสามชนิด 13) Faricimab ในการทดลอง YOSEMITE/RHINE แสดงการมองเห็น ดีขึ้นเทียบเท่า aflibercept แต่สามารถยืดระยะห่างการฉีดในระยะบำรุงรักษาได้มากขึ้น (บรรลุ Q16W 60–64% ในปีที่ 2) 8) เลือกยาตามภูมิหลังของผู้ป่วยและความต้องการเรื่องความถี่ในการมาโรงพยาบาล
Q
การรักษาด้วย anti-VEGF และเลเซอร์สำหรับจอประสาทตาในทารกคลอดก่อนกำหนดแตกต่างกันอย่างไร?
A
การรักษาด้วย anti-VEGF สามารถทำได้ในเวลาสั้นและมีการรุกรานน้อย และการทดลอง RAINBOW แสดงผลระยะยาวดีกว่าเลเซอร์ในแง่การรักษาลานสายตาและการป้องกันสายตาสั้น (สายตาสั้น รุนแรง 8% เทียบกับ 24% ที่อายุ 5 ปี) 26, 29) ในทางกลับกัน การรักษาด้วยเลเซอร์ ทำให้หลอดเลือดจอประสาทตา สมบูรณ์ได้ง่ายกว่าหลังการรักษา การรักษาด้วย anti-VEGF ต้องติดตามอวัยวะภายในดวงตาในระยะยาวโดยคำนึงถึงการกลับเป็นซ้ำ (ranibizumab 20–83%) และการทดลอง FIREFLEYE รายงานอัตราการกลับเป็นซ้ำ 21.9% 28) ใน A-ROP ที่มีการเจริญของเนื้อเยื่อเส้นใยเป็นบริเวณกว้าง การใช้ anti-VEGF เพียงอย่างเดียวอาจมีข้อห้าม 3)
การป้องกันการสับสนระหว่างผู้ป่วย ตา และยา : หลังจากตัดสินใจฉีด ให้ติดป้ายระบุตัวผู้ป่วยที่คอเพื่อยืนยันการยืนยันการแพ้ไอโอดีน : ตรวจสอบล่วงหน้าทุกครั้งการเตรียมวัสดุที่จำเป็น :
โพวิโดนไอโอดีน 10% สำหรับฆ่าเชื้อผิวหนัง
ยาหยอดตาชา, ยาหยอดตา PA ไอโอดีนที่เจือจางและปรับอุณหภูมิห้อง, ยาหยอดตาปฏิชีวนะ (ถ้าจำเป็น)
ผ้าก๊อซ, สำลีก้าน (3 อันสำหรับล้างตาและฉีด) และผ้าปิดแผลที่มีรูและเทป
เครื่องเปิดเปลือกตา, คาลิปเปอร์, คีมไมโครมีตะขอ
เข็มฉีดยาและสารละลายสำหรับฉีด (เมื่อใช้ขวด ให้ใช้กระบอกฉีด 1 มล. และเข็มดูดพร้อมตัวกรอง)
การชา : เนื่องจากอาจมีน้ำยาฆ่าเชื้อกระเด็นเข้าตาอีกข้าง ให้หยอด Benoxil® ทั้งสองตา จากนั้นหยอด Xylocaine® 4% ที่ตาที่จะฉีดสองครั้ง
ข้อควรระวังเกี่ยวกับการฆ่าเชื้อด้วย PA ไอโอดีน :
PA ไอโอดีนที่เพิ่งนำออกจากตู้เย็นมีประสิทธิภาพในการต้านเชื้อแบคทีเรียและเชื้อราลดลง ดังนั้นต้องแน่ใจว่าได้ปรับอุณหภูมิห้องแล้ว
เมื่อเก็บในภาชนะที่ไม่ปิดสนิทที่อุณหภูมิ 25°C อัตราส่วนของส่วนประกอบที่ออกฤทธิ์จะลดลงเหลือ 60% ภายใน 5 ชั่วโมง ห้ามใช้ PA ไอโอดีนที่ผ่านไปนาน
เพื่อยับยั้งแบคทีเรียและเชื้อรา ต้องใช้เวลาสัมผัสประมาณ 1 นาที ดังนั้นหลังจากล้างตา ให้หลับตาเพื่อให้แน่ใจว่ามีเวลาสัมผัสกับเยื่อบุตา อย่างเพียงพอ
มาตรการป้องกันแบคทีเรียในช่องปาก : ใช้ผ้าปิดแผลที่มีรูและสวมหน้ากากอนามัยสำหรับศัลยแพทย์ ผู้ช่วย และผู้ป่วยทุกคนเพื่อป้องกันละอองฝอย เนื่องจากแบคทีเรียในช่องปากเป็นสาเหตุหนึ่งของเยื่อบุตาอักเสบจากแบคทีเรีย จึงควรปิดช่องว่างระหว่างตาด้วยผ้าปิดแผลและหน้ากากเพื่อป้องกันไม่ให้ลมหายใจกระจายไปยังผิวตา
ระยะห่างในการแทงเข็มจากขอบตาดำผ่าตัดมีดังนี้ การปฏิบัติตามตำแหน่งแทงเข็มจะช่วยให้สามารถแทงเข้าสู่ส่วนแบนของซิลิอารีบอดี (ด้านหลังรอยพับซิลิอารี) ซึ่งป้องกันความเสียหายต่อเลนส์แก้วตา และเลือดออกในวุ้นตา
สภาพตา ระยะห่างจากขอบตาดำ ตาที่มีเลนส์แก้วตา 4 มม. (ส่วนแบนของซิลิอารีบอดี ) ตาที่ไม่มีเลนส์แก้วตา หรือมีเลนส์แก้วตาเทียม 3.5 มม. ทารกคลอดก่อนกำหนด (ROP ) 1.0-1.5 มม.
แทงเข็มไปทางศูนย์กลางของช่องวุ้นตา หากแทงใกล้ขอบตาดำเกินไป อาจทำให้รอยพับซิลิอารีเสียหายและเกิดเลือดออกในวุ้นตา และระยะห่างถึงเลนส์แก้วตา จะสั้นลง เพิ่มความเสี่ยงต่อความเสียหายของเลนส์แก้วตา
ติดผ้าปิดแผลที่มีรูและเปิดเปลือกตาด้วยเครื่องเปิดเปลือกตา
วัดระยะห่างในการแทงเข็มจากขอบตาดำโดยใช้คาลิปเปอร์
ตำแหน่งฉีดคือบริเวณด้านบนหรือด้านล่างของหู (เพื่อป้องกันการบาดเจ็บของกล้ามเนื้อเรกตัสแนวนอน)
ยึดลูกตาด้วยคีม และเลื่อนเยื่อบุตา ไปข้างหน้าเล็กน้อยก่อนฉีดเพื่อป้องกันการรั่วของของเหลวหลังจากถอนเข็ม
สอดเข็มสั้นขนาด 30G เกือบตั้งฉากกับตาขาว และฉีดยาช้าๆ (การฉีดเร็วทำให้ความดันลูกตา สูงขึ้นอย่างต่อเนื่อง)
หลังจากถอนเข็ม ให้กดบริเวณที่ฉีดด้วยสำลี
ทันทีหลังทำหัตถการ ตรวจสอบการมองเห็น (นับนิ้ว) หากไม่สามารถนับนิ้วได้ ให้ทำการเจาะช่องหน้าม่านตา
ใช้ยาหยอดตาปฏิชีวนะชนิดออกฤทธิ์กว้างต่อไปเป็นเวลา 3 วันหลังทำหัตถการ
Q
การฉีดเจ็บไหม?
A
เนื่องจากทำหลังจากการหยอดยาชาเฉพาะที่ (Benoxil® และ Xylocaine 4%) ความเจ็บปวดระหว่างฉีดจึงน้อยมาก อาจรู้สึกแสบจากน้ำยาฆ่าเชื้อ (PA iodine) แต่ยาหยอดตาโซเดียมไฮยาลูโรเนตมีประสิทธิภาพในการลดอาการไม่สบายหลังทำหัตถการในระยะแรก
เยื่อบุตาอักเสบ ติดเชื้อเป็นภาวะแทรกซ้อนที่ร้ายแรงที่สุด โดยมีอุบัติการณ์ประมาณ 0.027% ถึง 0.065% เมื่อเกิดขึ้น จำเป็นต้องได้รับการรักษาฉุกเฉินด้วยการฉีดยาเข้าแก้วตา (vancomycin 1.0 มก. + ceftazidime 2.0 มก.)
มาตรการป้องกันที่สำคัญที่สุด:
การฆ่าเชื้ออย่างเหมาะสมด้วยโพวิโดนไอโอดีน (ทำให้กลับสู่อุณหภูมิห้อง ใช้เวลาสัมผัสอย่างน้อย 1 นาที)
การใช้ผ้าปิดแผลที่มีรู (ป้องกันละอองแบคทีเรียจากช่องปาก)
สำหรับการใช้ยาหยอดตาปฏิชีวนะป้องกันหลังผ่าตัด การศึกษาหลายชิ้นแสดงว่าไม่ลดอุบัติการณ์ของเยื่อบุตาอักเสบ และหลักฐานประสิทธิภาพไม่สอดคล้องกัน
เป็นปฏิกิริยาการอักเสบภายในตาโดยไม่มีการติดเชื้อแบคทีเรีย รายงานว่าเป็นภาวะแทรกซ้อนที่พบได้ยากหลังการให้ยา anti-VEGF 7) เนื่องจากความถี่แตกต่างกันไปตามยา การเตรียม และรุ่นการผลิต จึงต้องให้ความสำคัญกับการแยกจากเยื่อบุตาอักเสบ ติดเชื้อ
ระยะเวลาที่เกิด: มักเกิดเร็วหลังการฉีด แต่จำเป็นต้องแยกจากเยื่อบุตาอักเสบ ติดเชื้อ 7) อาการสำคัญ: อาจทำให้เกิดความขุ่นของแก้วตา อักเสบในช่องหน้าตา และการมองเห็น ลดลง 7) การวินิจฉัยที่แน่นอน: การเพาะเชื้อให้ผลลบ (การตรวจ PCR เพื่อแยกเชื้อก่อโรคก็มีประโยชน์)ความแตกต่างตามยา: มีรายงานด้วย bevacizumab, ranibizumab และ aflibercept แต่ความถี่ของรายงานแตกต่างกันไปตามการศึกษาและสภาวะการเตรียม 7) การรักษา: ในกรณีที่ไม่รุนแรง มักให้การรักษาแบบประคับประคอง แต่หากไม่สามารถแยกเยื่อบุตาอักเสบ ติดเชื้อได้ ต้องตัดสินใจอย่างรวดเร็ว รวมถึงการเก็บตัวอย่างเพาะเชื้อ การฉีดยาปฏิชีวนะเข้าแก้วตา และการผ่าตัดแก้วตา 7)
ในการวิเคราะห์ผู้ป่วย 1,044 รายจาก IRIS Registry ผลลัพธ์ของการผ่าตัดแก้วตาตั้งแต่เนิ่นๆ สำหรับเยื่อบุตาอักเสบ หลังฉีดยาเข้าแก้วตาได้รับการศึกษาโดยใช้ข้อมูลขนาดใหญ่ 24)
เป็นที่ทราบกันว่า brolucizumab ทำให้เกิด IOI ด้วยความถี่ที่สูงกว่ายา anti-VEGF อื่นๆ
การศึกษา / ประชากร อุบัติการณ์ของ IOI หมายเหตุ HAWK/HARRIER (เกี่ยวข้องกับ IOI) มีรายงาน ระวังเหตุการณ์ไม่พึงประสงค์จากการอักเสบ รวมถึง vasculitis จอประสาทตา และการอุดตันของหลอดเลือด10) KESTREL (6 มก.) 3.7% (กลุ่มควบคุม 0.5%) การทดลอง DME10) MERLIN (ช่วง 4 สัปดาห์) 9.3% หยุดการทดลอง10) ผู้ป่วยชาวญี่ปุ่น รายงานในรายงานผู้ป่วยและข้อมูลหลังการวางตลาด ระมัดระวังในการประมาณความถี่ หลังวางตลาด (หลอดเลือดอักเสบ + การอุดตันร่วม) 3.73/10,000 การฉีด
IOI ส่วนใหญ่เกิดขึ้นภายใน 6 เดือนหลังการให้ยาครั้งแรก และหลังการฉีด 4 ครั้งหรือน้อยกว่า 10)
กลไก : มีการถกเถียงถึงความเป็นไปได้ของกลไกการอักเสบที่อาศัยแอนติบอดีต่อยาหรืออิมมูนคอมเพล็กซ์ 10, 25)
เยื่อบุตาอักเสบ (รายงานแรกของโลก)เยื่อบุตาอักเสบ ส่วนหลังหลังการให้ brolucizumab ในผู้ป่วยญี่ปุ่น 3 ราย ร่วมกับความดันลูกตา สูงขึ้นถึง 24-49 มม.ปรอท และหนึ่งรายลุกลามเป็นหลอดเลือดแดงจอตาอุดตันและหลอดเลือดอักเสบ 9)
การรักษา : การฉีด triamcinolone acetonide (STTA) ขนาด 5-20 มก. ใต้เยื่อบุตา หรือใต้ Tenon ได้ผลดี มีรายงานการรวมกับการป้องกันด้วย STTA เช่นกัน 20, 21)
อุบัติการณ์ของ IOI คือ 2.0% ใน nAMD , 1.3% ใน DME และ 1.4% ใน RVO ; ในกรณีฉีดสองตาพบ 8.5% 8) ในการสำรวจหลังวางตลาด หลอดเลือดจอตาอักเสบพบน้อย (0.17/10,000 การฉีด) แต่หลอดเลือดจอตาอักเสบชนิดอุดตันร่วมกับเลือดออก (HORV ) อาจนำไปสู่ผลลัพธ์ที่รุนแรง 8) มีการรวบรวมรายงานผู้ป่วยหลอดเลือดจอตาอักเสบและ IOI ที่เกี่ยวข้องกับ faricimab และในกรณีรุนแรง HORV เป็นปัญหาสำคัญ 16-18)
การฉีกขาดของ RPE เกิดขึ้นในกลุ่ม faricimab 2.7% ใน TENAYA และ 3.0% ใน LUCERNE โดยความสูงของ PED > 550 μm เป็นปัจจัยเสี่ยง 19)
ในผู้ป่วย ROP หลังการรักษาด้วย anti-VEGF เยื่อหุ้มเส้นเลือดฝอยอาจหดตัวอย่างรวดเร็วทำให้เกิดจอตาลอกแบบดึงรั้ง (TRD) ภาวะแทรกซ้อนนี้เรียกว่า crunch syndrome 27)
กลไก : การยับยั้ง VEGF ทำให้กิจกรรมของ TGF-β เพิ่มขึ้นสัมพัทธ์ TGF-β ส่งเสริมการเกิดพังผืดและการปรับเปลี่ยนเมทริกซ์นอกเซลล์ ทารกคลอดก่อนกำหนดอยู่ในช่วงที่ TGF-β สูงตามสรีรวิทยา และการให้ anti-VEGF จะขยายความไม่สมดุล 27) การป้องกัน : ประเมินการเปลี่ยนแปลงแบบพังผืดอย่างรอบคอบก่อนการรักษา หากมีการเจริญของเนื้อเยื่อพังผืดอย่างกว้างขวางร่วมกับมีเลือดคั่ง ไม่ควรให้การรักษาด้วย anti-VEGF เพียงอย่างเดียว 3) ภาวะแทรกซ้อนระยะหลัง : มีรายงานจอตาลอกแบบดึงรั้งเกิดขึ้น 4-335 วันหลังการฉีด ดังนั้นการตรวจอวัยวะภายในตาเป็นประจำเป็นเวลา 1 ปีหลังฉีดจึงจำเป็น 3)
หลังการรักษาด้วย anti-VEGF อาจไม่เกิดการสร้างหลอดเลือดจอประสาทตา อย่างสมบูรณ์ และอาจเกิดหลอดเลือด shunt และรูปแบบการแตกแขนงที่ผิดปกติที่รอยต่อระหว่างหลอดเลือดและบริเวณไร้หลอดเลือด 27) จำเป็นต้องติดตามผลระยะยาว (เพื่อประเมินความเสี่ยงของการกลับเป็นซ้ำและภาวะแทรกซ้อนระยะหลัง) การตรวจ fluorescein angiography มีประโยชน์ในการประเมินการพัฒนาปกติของหลอดเลือดจอประสาทตา
การบาดเจ็บเลนส์แก้วตา : การลุกลามของต้อกระจก ป้องกันโดยปฏิบัติตามระยะการแทง (4 มม. ในตาที่มีเลนส์แก้วตา )การบาดเจ็บจอประสาทตา : จอประสาทตาลอก ชนิดมีรอยฉีกขาด ป้องกันโดยการแทงเข็มสั้น 30G อย่างเหมาะสมการบาดเจ็บซิลิอารีบอดี : เลือดออกในน้ำวุ้นตา ป้องกันโดยปฏิบัติตามตำแหน่งและทิศทางการแทง
ความดันลูกตา สูงชั่วคราวทันทีหลังฉีดเกิดขึ้นในผู้ป่วยทุกรายที่ได้รับการฉีด การฉีด 0.05 มล. ทำให้ความดันลูกตา เพิ่มขึ้นทันทีเป็น 50 มม.ปรอท แต่โดยทั่วไปสามารถกลับคืนได้ ในผู้ป่วยที่มีประวัติโรคต้อหิน ต้องระวังความดันลูกตา สูงที่คงอยู่ และหากจำเป็นให้ลดความดันโดยการเจาะช่องหน้าลูกตา
ตามทฤษฎีแล้วมีความเสี่ยงต่อโรคหลอดเลือดสมองและกล้ามเนื้อหัวใจตาย ในการทดลอง HAWK สำหรับ brolucizumab พบ ATE 1.1-1.4% 10) ในผู้ป่วยที่มีประวัติ ต้องใช้ยาด้วยความระมัดระวัง
Q
หลังฉีด ควรไปพบแพทย์เมื่อมีอาการใด?
A
หากมีอาการต่อไปนี้ ให้ไปพบจักษุแพทย์ทันที: ① การมองเห็น ลดลงอย่างกะทันหัน ② ปวดตา หรือตาแดง มากขึ้น ③ จำนวนจุดลอยตัวเพิ่มขึ้นอย่างชัดเจน ④ มีสารคัดหลั่ง อาการเหล่านี้อาจบ่งบอกถึงเยื่อบุตาอักเสบ ติดเชื้อหรือการอักเสบภายในลูกตา (IOI) โดยเฉพาะอย่างยิ่งต้องระวังภายใน 24-72 ชั่วโมงหลังฉีด
Q
หากเกิด IOI กับ brolucizumab ควรทำอย่างไร?
A
หากมีการมองเห็น ลดลงอย่างกะทันหัน จุดลอยตัวแย่ลง ตาแดง หรือปวดตา ให้ไปพบจักษุแพทย์ทันที หลังการวินิจฉัย การฉีด triamcinolone acetonide (STTA) ใต้เยื่อบุตา หรือใต้ Tenon capsule ได้ผล และการอักเสบดีขึ้นในกรณีส่วนใหญ่ 20, 21) การให้ยาซ้ำจะตัดสินใจอย่างระมัดระวังหลังจากยืนยันว่าการอักเสบหายแล้วโดยใช้ LFP (เครื่องวัด flare cell ด้วยเลเซอร์) เป็นต้น หากมีการอุดตันของหลอดเลือดรุนแรง การให้ยาซ้ำอาจมีข้อห้าม ดังนั้นควรพิจารณาเปลี่ยนไปใช้ยาทางเลือกอื่น
VEGF จับกับ VEGFR-1 และ VEGFR-2 บนเซลล์บุผนังหลอดเลือด ส่งเสริมการเพิ่มจำนวนเซลล์บุผนังหลอดเลือด การเพิ่มการซึมผ่านของหลอดเลือด และการสร้างหลอดเลือดใหม่
AMD เส้นเลือดใหม่ในคอรอยด์ (CNV ) และการเพิ่มการซึมผ่านของหลอดเลือดDME : การทำลาย Blood-Retinal Barrier (BRB) → การเกิดจอประสาทตา บวมน้ำRVO จอประสาทตา บวมน้ำและเส้นเลือดใหม่
เมื่อระดับ VEGF ลดลงจากการฉีดเข้าแก้วตา การซึมผ่านของหลอดเลือดจะลดลงและจอประสาทตา บวมน้ำดีขึ้น ผลของยาต้าน VEGF เป็นเพียงชั่วคราว จึงจำเป็นต้องฉีดซ้ำอย่างสม่ำเสมอ
การเกิด ROP ดำเนินไปในสองระยะ 27)
ระยะที่ 1 (ระยะหยุดการสร้างหลอดเลือด) : หลังคลอดก่อนกำหนด ในสภาพแวดล้อมที่มีออกซิเจนสูง VEGF และ IGF-1 ถูกยับยั้ง ซึ่งขัดขวางการสร้างหลอดเลือดจอประสาทตา ปกติ ทำให้เกิดจอประสาทตา ที่ไม่มีหลอดเลือด
ระยะที่ 2 (ระยะสร้างเส้นเลือดใหม่ทางพยาธิวิทยา) : หลังจากหยุดออกซิเจน จอประสาทตา ที่ขาดเลือดซึ่งขยายใหญ่ขึ้นตามการเจริญเติบโตจะปล่อย VEGF มากเกินไป การสร้างเส้นเลือดใหม่ทางพยาธิวิทยาเกิดขึ้นที่รอยต่อระหว่างหลอดเลือดและไม่มีหลอดเลือด ดำเนินจากเส้นแบ่งและการยกตัวในระยะที่ 1-2 ไปสู่การสร้างเส้นเลือดใหม่นอกจอประสาทตา ในระยะที่ 3 ในกรณีรุนแรง จะนำไปสู่จอประสาทตาลอก แบบดึงรั้งในระยะที่ 4-5
ยาต้าน VEGF ยับยั้งการสร้างเส้นเลือดใหม่ทางพยาธิวิทยาโดยการกดการผลิต VEGF ที่มากเกินไปในระยะที่ 2 อย่างไรก็ตาม ยาเหล่านี้ยังยับยั้งการสร้างหลอดเลือดทางสรีรวิทยาที่ขึ้นกับ VEGF ดังนั้นจึงต้องติดตามผลกระทบต่อการพัฒนาหลอดเลือดปกติอย่างระมัดระวัง
ยา น้ำหนักโมเลกุล ความสัมพันธ์กับ VEGF-A (Kd) เป้าหมาย โบรลูซิซูแมบ 26 กิโลดาลตัน 28.4 พิโคโมลาร์ VEGF-A (ไอโซฟอร์มทั้งหมด) รานิบิซูแมบ 48 กิโลดาลตัน 20.6 พิโคโมลาร์ VEGF-A (ไอโซฟอร์มทั้งหมด) อะฟลิเบอร์เซปต์ 115 กิโลดาลตัน 0.49 พิโคโมลาร์ (สูงสุด) VEGF-A/B และ PlGF เบวาซิซูแมบ 148 กิโลดาลตัน 35.1 พิโคโมลาร์ VEGF-A ฟาริซิแมบ 149 กิโลดาลตัน — VEGF-A + Ang-2
Ang-2 มีส่วนร่วมในการทำให้หลอดเลือดไม่เสถียรในฐานะตัวต้านรีเซพเตอร์ Tie-2 การยับยั้ง Ang-2 โดยฟาริซิแมบ ทำให้วิถี Tie-2 กลับสู่ปกติ เพิ่มความเสถียรของหลอดเลือดและลดความไวต่อ VEGF ผลการยับยั้งสองทางนี้เป็นพื้นฐานทางเภสัชวิทยาที่ทำให้สามารถยืดระยะห่างระหว่างการให้ยาได้
เหตุผลที่ให้ยา 3-5 ครั้งคงที่ทุกเดือนในระยะนำคือเพื่อระงับกิจกรรมของโรคอย่างรุนแรงตั้งแต่เนิ่นๆ วิธี T&E ให้กรอบที่ไม่ยอมให้เกิดการกลับเป็นซ้ำตราบใดที่ความเข้มข้นของยาในวุ้นตา ยังคงอยู่ในช่วงการรักษา
ใน PDS (ระบบนำส่งผ่านพอร์ต) ของรานิบิซูแมบ ผู้ป่วย 98% ไม่จำเป็นต้องฉีดทุกเดือนหลังการให้ยาเสริมทุก 6 เดือน 12) กำลังพิจารณาเพิ่มข้อบ่งชี้สำหรับ DME ในปี 2025 13) คาดว่าจะลดภาระการฉีดได้อย่างมาก
ในการทดลอง PULSAR (AMD ) ที่ 48 สัปดาห์ 79% รักษาระยะห่าง 12 สัปดาห์ และ 77% รักษาระยะห่าง 16 สัปดาห์ 12) ในการทดลอง PHOTON (DME) 93% บรรลุระยะห่างอย่างน้อย 12 สัปดาห์ 13)
การทดลอง PROUD (เกาหลี) กำลังดำเนินการสำหรับ PCV และภาวะหลอดเลือดฝอยจอประสาทตา ขยายชนิดที่ 1 (AT1) คาดว่าจะสะสมหลักฐานสำหรับโรคเฉพาะในเอเชีย 14, 23)
การทดลอง SALWE EN กำลังดำเนินการเพื่อศึกษาผลของฟาริซิแมบ ในผู้ป่วย PCV 22) พบระดับ Ang-2 สูงในอารมณ์ขัน aqueous ของผู้ป่วย PCV ซึ่งบ่งชี้ถึงผลเสริมที่เป็นไปได้ของการยับยั้ง Ang-2
การให้ไตรแอมซิโนโลน อะซีโทไนด์ ใต้เยื่อบุตา และใต้ถุงเทนนอน (STTA) ร่วมกับโบรลูซิซูแมบ อาจมีประสิทธิภาพในการป้องกัน IOI และควบคุมการรั่วซึม 20, 21) กำลังมีการวิจัยเพื่อกำหนดขนาดยาและระยะเวลาที่เหมาะสม
เพื่อการแยกชนิดตั้งแต่แรกเริ่มระหว่างเยื่อบุตาอักเสบ ชนิดปราศจากเชื้อและติดเชื้อ การวัดโปรไฟล์ไซโตไคน์ในวุ้นตา (IL-6, IL-8, IL-10) คาดว่าจะเป็นเครื่องมือช่วยที่มีศักยภาพ 7)
ไบโอซิมิลาร์ ของรานิบิซูแมบ และเบวาซิซูแมบ กำลังเริ่มปรากฏขึ้น การลดต้นทุนอย่างมีนัยสำคัญคาดว่าจะช่วยเพิ่มอัตราการรักษาต่อเนื่องและการเข้าถึงบริการสุขภาพ 12)
ยาปิดกั้นเบตา (โพรพราโนลอล) : การรับประทานป้องกันการลุกลามของ ROP ระยะที่ 2 ยาหยอดตา 0.2% ถือว่าปลอดภัยและมีประสิทธิภาพ (หากเริ่มในระยะที่ 1 ในช่วง proliferative) แต่ข้อมูลระยะยาวไม่เพียงพออาหารเสริมกรดอะราคิโดนิก (AA) และ DHA : ในการทดลอง Mega Donna Mega Trial ลดการเกิด ROP รุนแรงลง 50% (15.8% เทียบกับ 33.3%)คาเฟอีน : ยารักษาภาวะหยุดหายใจในทารกคลอดก่อนกำหนด แต่มีศักยภาพในการยับยั้งการลุกลามของ ROP โดยการลด VEGF และ MMPsวิตามินเอ : การวิเคราะห์อภิมานพบว่าลดการเกิดและการดำเนินของ ROP
SAFER-ROP ถูกเสนอให้เป็นโปรโตคอลมาตรฐานเพื่อจัดการกับความท้าทายเฉพาะของทารกแรกเกิด (การป้องกันการติดเชื้อในสภาพแวดล้อม NICU การติดตามหลังการฉีด) โดยอิงจากตัวย่อ Short Needle, Antiseptic/Antibiotic, Follow-Up, Extra Attention to Detail, Recheck และใช้เพื่อสร้างมาตรฐานของขั้นตอนในแต่ละสถานพยาบาล
日本眼科学会. 新生血管型加齢黄斑変性の診療ガイドライン. 日眼会誌. 2024.
Lim JI, Kim SJ, Bailey ST, Kovach JL, Vemulakonda GA, Ying GS, Flaxel CJ; American Academy of Ophthalmology Preferred Practice Pattern Retina/Vitreous Committee. Diabetic Retinopathy Preferred Practice Pattern®. Ophthalmology. 2025. doi:10.1016/j.ophtha.2024.12.020. PMID:39918521.
日本未熟児網膜症研究会. 未熟児網膜症に対する抗VEGF療法の手引き(第2版). 2024.
Ikuno Y, Ohno-Matsui K, Wong TY, et al. Intravitreal aflibercept injection for myopic choroidal neovascularization: the MYRROR study. Ophthalmology. 2015;122(6):1220-1227. doi:10.1016/j.ophtha.2015.07.013. PMID:26300374.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024. [Protocol S data]
American Academy of Ophthalmology. Retinal Vein Occlusion Preferred Practice Pattern. Ophthalmology. 2024. [BRAVO data]
Baudin F, et al. Sterile endophthalmitis after anti-vascular endothelial growth factor agents: a literature review. J Fr Ophtalmol. 2015;38(9):865-871. PMID:26501239.
Tadayoni R, Paris LP, Danzig CJ, et al. Efficacy and safety of faricimab for macular edema due to retinal vein occlusion: 24-week results from the BALATON and COMINO trials. Ophthalmology. 2024;131(8):950-960.
Takayama T, et al. Scleritis following intravitreal brolucizumab injection: a case series. J Med Case Rep. 2024;18:80.
Sharma A, et al. Understanding retinal vasculitis associated with brolucizumab. Ocul Immunol Inflamm. 2022;30(6):1508-1510. PMID:34014141.
Nawar AE. Subthreshold micropulse laser combined with ranibizumab versus ranibizumab monotherapy in branch retinal vein occlusion with macular edema. Clin Ophthalmol. 2022;16:1139-1151.
Flaxel CJ, Adelman RA, Bailey ST, et al. Age-related macular degeneration preferred practice pattern. Ophthalmology. 2024;131(1):P1-P68.
Flaxel CJ, Adelman RA, Bailey ST, et al. Diabetic retinopathy preferred practice pattern. Ophthalmology. 2024;131(1):P99-P168.
Sen P, et al. Polypoidal choroidal vasculopathy: update on diagnosis and treatment. Clin Ophthalmol. 2023;17:53-70.
Bloom J, Madani R, Haidar AJ, Alasil T. Faricimab treatment of polypoidal choroidal vasculopathy resistant to intravitreal ranibizumab injections and ranibizumab port delivery (Susvimo ). J VitreoRetin Dis. 2024;8(6):731-734. PMID:39554622.
Siddiqui MZ, Durrani A, Smith BT. Faricimab-associated retinal vasculitis. J VitreoRetin Dis. 2024;8(5):627-630.
Dhillon N, Macleod S. Intraocular inflammation following intravitreal faricimab: insights from five bilateral cases. J VitreoRetin Dis. 2025.
Yavari N, Gupta AS, Mitsios A, et al. Bilateral hemorrhagic occlusive retinal vasculitis and panuveitis following intravitreal faricimab injection. Am J Ophthalmol Case Rep. 2026;41:102532.
Clemens CR, Alten F, Zimmermann JA, Eter N. Old problem in a new guise: retinal pigment epithelium tear after intravitreal faricimab injection. Case Rep Ophthalmol. 2023;14:241-244.
Shigemoto Y, et al. Combination therapy of STTA and IVbr for brolucizumab-related IOI. Medicine. 2021;100(42):e27580.
Saito M, et al. IOI after IVbr monitored by laser flare-cell photometer. Am J Ophthalmol Case Rep. 2022;28:101727.
Cheung CMG, Lai TYY, Teo K, et al. Polypoidal choroidal vasculopathy: consensus nomenclature and non-indocyanine green angiograph diagnostic criteria. Eye. 2024;39:819-834.
Carta V, et al. Effect of intravitreal brolucizumab in PCV with foveal lipid exudation. Cureus. 2023;15(10):e47942.
Breazzano MP, Bond JB 3rd, Beardsley RM, et al. Endophthalmitis after intravitreal injection: early pars plana vitrectomy outcomes from the IRIS Registry (Intelligent Research in Sight). Ophthalmology. 2024. PMID:38432901.
Teo KYC, et al. Brolucizumab-associated intraocular inflammation: type IV hypersensitivity and cytokine activation. Am J Ophthalmol. 2024.
Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very preterm infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559. doi:10.1016/S0140-6736(19)30690-5. PMID:31126750.
Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Ophthalmic Res. 2025.
Stahl A, Lepore D, Fielder AR, et al. Aflibercept vs laser for retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359. doi:10.1001/jama.2022.10727. PMID:35862896.
Marlow N, Reynolds JD, Lepore D, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): five-year outcomes. eClinicalMedicine. 2024;71:102567.
Mintz-Hittner HA, Kennedy KA, Chuang AZ. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.