레이저 광응고

미숙아 망막병증
1. 미숙아 망막병증이란?
섹션 제목: “1. 미숙아 망막병증이란?”미숙아 망막병증(ROP)은 발달 중인 망막 혈관에 발생하는 증식성 질환입니다.
망막 혈관은 태생 제14주경부터 시신경 유두에서 발생하기 시작하여 안저의 전방으로 성장합니다. 표층 혈관은 태생 제30주, 심층 혈관은 태생 제38~40주에 최주변부에 도달하여 성장이 완료됩니다. 개인차가 있으며, 이측은 비측보다 시신경 유두로부터의 거리가 길기 때문에 최주변부 도달이 늦고 ROP가 발생하기 쉽습니다.
미숙아에서는 주변 망막에 무혈관 영역이 남은 상태로 태어납니다. 발달 중인 혈관은 안정적인 모체에서 급격히 환경이 변화하면 가장 미성숙한 세포가 존재하는 성장의 선단부에서 성장을 멈추고 비정상적인 방향으로 증식합니다. 무혈관 영역에서 VEGF(혈관 내피 성장 인자)가 방출되는 것이 그 기전입니다.
증식이 진행되는 기간을 활동기라고 하며, 진정되어 혈관 성분이 퇴축하고 섬유 결합 조직이나 망막의 견인, 변성 등의 후유증을 남긴 상태를 반흔기라고 합니다.
ROP의 발현 빈도와 중증도는 망막 혈관의 성장이 미성숙할수록 높습니다. 재태 주수와 출생 체중이 낮을수록 발병률이 높고 중증이 되기 쉽습니다. 고농도 산소는 ROP를 악화시키는 가장 큰 유발 요인이며, 그 외에 호흡 곤란 증후군, 교환 수혈, 패혈증, 뇌실 내 출혈, 수술 병력, 영양 및 수분 투여 불균형 등이 복잡하게 관여합니다.
1942년 Terry가 처음 보고했고, 1967년 Nagata가 세계 최초로 광응고 치료를 시행하여 표준 치료로 발전해 왔습니다. 미숙아 망막병증의 유행은 역사적으로 3번 발생했으며1), 첫 번째 유행(194050년대)은 인큐베이터 내 고농도 산소 투여가 원인이었고, 두 번째 유행(197080년대)은 초저체중출생아의 생존율 향상에 따른 것이며, 세 번째 유행은 현재 진행 중으로 의료 자원이 제한된 중저소득 국가에서 발생하고 있습니다1). 소아 실명 원인에서 ROP가 차지하는 비율은 1990년 약 10%였으나 현재는 30%까지 증가했습니다. 전 세계적으로 연간 약 184,700명의 조산아가 ROP를 발병하고, 약 20,000명의 소아가 실명 또는 중증 시각 장애를 겪는 것으로 추정됩니다1). 출생 체중 1,000g 미만의 초저체중출생아에서는 86.1%가 발병하고, 치료가 필요한 증례는 41%에 달합니다. 미국에서 ROP 발병률은 2004년 4.4%에서 2019년 8.1%로 증가했습니다1).
발병률의 대략적인 기준은 다음과 같습니다.
| 대상군 | 발병률 |
|---|---|
| 초저체중출생아(<1,000g), 일본 | 86.1% |
| 재태 주수 27주 이하, 미국 | 89.0% |
| 재태 주수 27~31주, 미국 | 51.7% |
| 재태 주수 32주 이상, 미국 | 14.2% |
| 전체 출생(전체), 미국 | 0.12% |
주요 위험 인자는 다음과 같습니다1).
| 위험 인자 | 내용 |
|---|---|
| 재태 기간 32주 미만 | 가장 중요한 위험 인자 중 하나 |
| 출생 체중 1.5kg 미만 | 가장 중요한 위험 인자 중 하나 |
| 고농도·장기 산소 투여 | 발병의 주요 유발 요인 |
| 다태 임신 | 저출생 체중 초래 |
| 신생아 호흡 곤란 증후군(NRDS) | 호흡 관리가 필요한 중증 예 |
| 패혈증·뇌실 내 출혈 | 전신 염증·순환 장애 |
| 출생 후 체중 증가 지연 | IGF-1 저하와 관련 |
| 수혈/에리스로포이에틴 투여 | 산소 운반 능력 변동 |
재태 기간이 짧을수록, 출생 체중이 적을수록 발병 위험이 높습니다. 특히 재태 기간 32주 미만, 출생 체중 1,500g 미만의 조산아가 주요 위험군입니다. 고농도 산소 투여 등 출생 후 환경 요인도 발병에 관여합니다. 여러 위험 요인이 겹치면 중증화되기 쉽습니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”자각 증상
섹션 제목: “자각 증상”미숙아 망막병증의 급성기는 신생아기 및 영아기에 발생하므로 환아 스스로 증상을 호소하지 않습니다. 보호자나 의료진이 다음과 같은 소견을 발견할 수 있습니다.
- 백색 동공(백동증) : 진행된 경우(4~5기) 망막 박리가 발생하면 동공이 하얗게 보입니다.
- 사시 : 시력 불량이나 양안 시 기능 균형의 혼란을 반영합니다.
- 안진 : 고도의 시력 장애를 동반할 때 발생합니다.
임상 소견 및 병기 분류
섹션 제목: “임상 소견 및 병기 분류”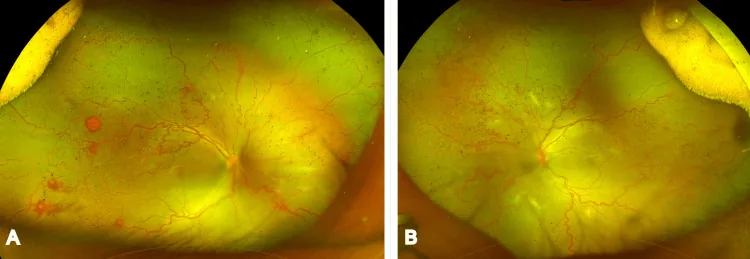
활동기 분류
섹션 제목: “활동기 분류”일본에서는 1975년에 후생성 분류가 만들어졌고 1983년에 개정되었습니다. ROP를 단계적으로 진행하는 I형(고전적 ROP)과 급속히 망막 박리에 이르는 전격성 II형으로 나누었습니다. 국제 분류(ICROP)는 2005년 개정 시 후생성 분류의 개념을 전면적으로 도입하였으며 내용은 거의 동일합니다. 최신 ICROP 제3판(ICROP3)은 2021년에 발표되었습니다2).
후생성 분류와 ICROP3의 대응
| 후생성 분류 | 국제 분류 (ICROP3) |
|---|---|
| I형 1기: 망막 내 신생혈관 | 1기: 경계선 (demarcation line) |
| I형 2기: 경계선 형성 | 2기: 융기 (ridge) |
| I형 3기: 유리체 내 삼출 및 증식 (초기/중기/후기) | 3기: 망막 외 섬유혈관 증식 (경증/중등도/중증) |
| 4기: 부분 망막박리 4A/4B | 4기: 부분 망막박리 (4A 황반 외, 4B 황반 포함) |
| 5기: 전체 망막박리 | 5기: 전체 망막박리 |
| II형: 전격형 | A-ROP (구 AP-ROP) |
| Plus disease (중증 징후) | Plus disease |
구역 분류
섹션 제목: “구역 분류”병변 발생 부위는 zone I~III로 나타냅니다. zone I은 시신경 유두를 중심으로 유두와 황반 중심와 사이 거리의 2배를 반지름으로 하는 원의 안쪽 범위로, +25 D 또는 +28 D 관찰 렌즈의 가장자리를 유두 반대쪽 가장자리에 놓고 보이는 범위에 해당합니다. zone II는 zone I 바깥쪽으로, 유두에서 코쪽 톱니 가장자리까지를 반지름으로 하는 원의 안쪽 범위입니다. zone III는 zone II 바깥쪽 귀쪽 초승달 모양 범위입니다. zone I일수록 병변이 뒤쪽에 위치하며 중증도가 높습니다. ICROP3에서는 후방 zone II (zone I 경계에서 2유두 직경의 띠 영역) 개념이 추가되었습니다 2).
각 단계의 소견
섹션 제목: “각 단계의 소견”1단계 (경계선): 혈관 성장 선단부의 망막 내에 흰색 경계선이 형성됩니다.
2단계 (융기): 전위 영역의 융단형 간엽 세포 증식이 두꺼워지고 경계선이 유리체강으로 돌출하여 융기가 형성됩니다.
3단계 (망막외 섬유혈관 증식): 혈관 다발이 융합하여 아치형이 되고 유리체 내 신생혈관이 혈관 내강을 형성하며 주변에 콜라겐 등의 결합 조직이 생성됩니다. 소견 정도에 따라 경증, 중등증, 중증으로 나눕니다. ICROP3에서는 융기를 동반하지 않은 평평한 망막외 신생혈관 개념이 3단계에 추가되었습니다 2).
4단계 (부분 망막박리): 섬유혈관 증식 내 결합 조직이 수축하여 망막을 견인, 부분 망막박리가 발생합니다. 4A (황반 미포함)와 4B (황반 포함)로 분류합니다.
5단계 (전체 망막박리): 섬유혈관 증식이 광범위하고 강하게 견인하여 망막이 전체 박리됩니다. ICROP3에서는 5단계를 다음 세 가지 아형으로 분류했습니다 2).
| 아형 | 특징 |
|---|---|
| 5A | 검안경으로 시신경 유두가 보임 (열린 깔때기 박리) |
| 5B | 수정체 후방 섬유혈관 조직 또는 닫힌 깔때기로 유두 관찰 불가 |
| 5C | 5B + 전안부 이상 (전방 얕아짐, 홍채-각막-수정체 유착, 각막 혼탁) |
Plus disease 및 pre-plus disease
섹션 제목: “Plus disease 및 pre-plus disease”1~3기에서, 후방 2사분면 이상에서 망막 정맥 확장과 동맥 구불거림이 있는 경우를 plus disease로 정의합니다. ICROP3에서는 plus disease를 정상에서 pre-plus를 거쳐 plus에 이르는 연속 스펙트럼으로 이해하도록 개정되었습니다2). plus disease 평가는 zone I 내의 혈관에서 수행합니다.
A-ROP (공격적 ROP)
섹션 제목: “A-ROP (공격적 ROP)”ICROP3에서는 기존의 AP-ROP (공격적 후방 ROP)가 A-ROP로 개명되었습니다. 이는 후방 이외의 부위에서의 발병, 더 큰 미숙아, 자원이 제한된 지역에서의 발병도 포함하도록 정의가 확장되었기 때문입니다2).
A-ROP의 특징은 다음과 같습니다. 후방 (주로 zone I, zone II 후방도 포함)에 발생하며, plus disease가 현저하고 전주위성 션트를 형성합니다. 혈관 영역과 무혈관 영역의 경계가 불명확하고, 유리체내 신생혈관이 편평하고 반투명하여 식별하기 어렵습니다. 일반적인 1기에서 3기로의 단계적 진행을 보이지 않으며, 치료하지 않으면 빠르게 5기로 진행합니다. 후극을 포함한 광범위한 모세혈관망 결손이 있으며, 광범위한 VEGF 방출이 급속 진행의 기반이 됩니다.
초기 병변의 망막 혈관 끝부분에 션트나 망막내 출혈이 보이면 즉시 광응고술을 시행해야 합니다.
반흔기 분류 (후생성)
섹션 제목: “반흔기 분류 (후생성)”활동기가 진정된 후 반흔기는 다음과 같이 분류됩니다.
- 1도: 주변부 변화만 있음. 안저 후극부에 현저한 변화 없으며, 시력은 일반적으로 정상.
- 2도 (약도): 경미한 시신경 유두 견인. 황반부에 변화 없음.
- 2도 (중등도): 명백한 시신경 유두 견인. 황반부 외측 편위.
- 2도 (강도): 시신경 유두 견인. 황반부에 기질적 변화.
- 3도: 후극부에 다발성 망막박리 (망막 주름).
- 4도: 동공 영역 일부에서 보이는 후방 수정체 섬유 증식.
- 5도: 완전 후방 수정체 섬유 증식.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”미숙아 망막병증의 발생에는 미성숙한 망막 혈관계와 출생 후 산소 환경 및 전신 상태의 상호 작용이 관여합니다. 고농도 산소는 ROP를 악화시키는 가장 큰 유발 요인이며, 그 외에 호흡 곤란 증후군, 교환 수혈, 패혈증, 뇌실 내 출혈, 수술 병력, 영양 및 수분 공급 불균형 등이 복합적으로 관여합니다.
| 위험 요인 | 내용 |
|---|---|
| 재태 주수 | <32주가 고위험 |
| 출생 체중 | <1,500 g이 고위험 |
| 산소 투여 | 고농도·장기 투여 |
| IGF-1 저하 | 출생 후 영양 불량 및 질환1) |
| 패혈증, 빈혈, 수혈 | 전신 상태 악화 |
| 호흡곤란 증후군 | 호흡 관리가 필요한 중증 아기 |
| 다태 출생 | 작은 쪽 쌍둥이에서 진행성 ROP가 더 흔함1) |
| 출생 후 체중 증가 불량 | WINROP/G-ROP 알고리즘의 근거1) |
IGF-1(인슐린 유사 성장 인자-1)은 망막 혈관 발달에 필수적인 신호 인자이며, 조산 후 낮은 IGF-1 상태가 혈관 성장 정지를 촉진합니다1).
4. 병태생리
섹션 제목: “4. 병태생리”망막 혈관 발달과 2단계 병태 모델
섹션 제목: “망막 혈관 발달과 2단계 병태 모델”망막 혈관 발달은 태생 14주경부터 시작되어 출생 전에 최주변부에 도달하여 완료됩니다. 표층 혈관은 태생 30주, 심층 혈관은 태생 38~40주에 도달합니다. 조산아에서는 주변 망막에 무혈관 영역이 남은 상태로 출생합니다.
ROP의 병태는 2단계로 설명됩니다1).
제1상(혈관 발달 정지기): 조산아의 미숙 망막이 고산소 환경(자궁 외)에 노출되면 산소 센서를 통해 VEGF와 IGF-1이 억제됩니다. 이로 인해 정상적인 망막 혈관 발육이 정지되고 무혈관대가 형성됩니다.
제2상(혈관 증식기): 무혈관 망막이 대사적으로 성숙함에 따라 허혈 상태를 보충하기 위해 VEGF가 과잉 생산됩니다. 이 VEGF 과잉이 혈관 내피의 이상 증식을 유발하여 유리체강으로의 섬유혈관 증식 조직 형성(3기 이후)으로 이어집니다.
신생혈관은 유리체강 내 유형 유리체의 섬유를 따라 성장하며 주변에 콜라겐 등의 결합조직을 생성합니다. 이 결합조직이 수축하여 부착된 망막을 견인하면 망막박리가 발생하여 심각한 시력 장애 또는 실명에 이릅니다.
A-ROP에서는 후극을 포함한 광범위한 모세혈관망 결손이 존재하며, 후극을 포함한 광범위한 영역에서 VEGF가 방출되어 급속히 진행됩니다.
IGF-1(인슐린 유사 성장 인자-1)은 망막의 혈관 및 신경 발달 조정에 중요하며, 낮은 IGF-1 상태는 정상 혈관 발달을 지연시켜 ROP 감수성을 증가시킵니다1). 출생 후 체중 증가 지연도 낮은 IGF-1과 관련되어 위험 요인이 됩니다1).
크런치 증후군(crunch syndrome): 항VEGF 치료 후 VEGF가 억제되면 TGF-β(섬유화 촉진 인자)의 상대적 상승으로 VEGF-TGF-β 균형이 깨져 섬유혈관막의 급속한 수축이 발생합니다. 이로 인해 견인성 망막박리가 악화될 위험이 있습니다1).
5. 선별검사와 진단
섹션 제목: “5. 선별검사와 진단”선별검사 기준과 첫 검사 시기
섹션 제목: “선별검사 기준과 첫 검사 시기”NICU에서 선별검사 대상은 재태 기간 34주 미만 또는 출생 체중 1,800g 이하의 영아입니다. 또한 산소 투여, 인공 환기, 수혈, 패혈증, 뇌실 내 출혈, 중증 호흡·순환 장애를 동반한 영아, 전신 마취 수술, 태아 수종은 고위험군으로, 이 기준을 벗어나더라도 안저 검사를 시행해야 합니다.
첫 검사 시기는 다음과 같습니다.
| 출생 시 재태 주수 | 첫 검사 시기 |
|---|---|
| 26주 미만 | 교정 재태 주수 29주부터 |
| 26주 이상 | 생후 3주부터 |
치료 적응증(1형 ROP)
섹션 제목: “치료 적응증(1형 ROP)”치료 적응증은 ETROP 연구에 기반한 type 1 ROP 기준에 따릅니다1). 다음 중 하나에 해당하는 경우 진단 후 72시간 이내에 치료가 권장됩니다.
- ① plus disease를 동반한 zone I 모든 ROP
- ② plus disease를 동반하지 않은 zone I stage 3 ROP
- ③ plus disease를 동반한 zone II stage 3 ROP
- ④ A-ROP (가능한 한 신속히 시행)
위 이외는 type 2 ROP로 경과 관찰합니다. plus disease를 동반한 zone II stage 2 ROP는 사용 약제에 따라 대응이 다릅니다(RAINBOW 시험에서는 대상 외였으나 FIREFLEYE 시험에서는 대상에 포함됨)3).
추적 관찰 간격
섹션 제목: “추적 관찰 간격”소견에 따른 검사 간격의 기준은 다음과 같습니다1).
| 소견 | 다음 검사까지 |
|---|---|
| zone I 미성숙 혈관 또는 stage 1-2, posterior zone II의 미성숙 혈관, A-ROP 의심 | 주 1회 |
| posterior zone II의 미성숙 망막, zone II stage 2, zone I 퇴행기 | 1-2주 |
| zone I stage 1, zone II 미성숙 혈관(ROP 없음), zone II 퇴행기 | 2주 |
| Zone III 1-2기, Zone III 퇴행기 | 2-3주 |
선별검사 종료 기준은 Zone III까지 완전한 혈관화, 또는 교정 주령 45주에 type 1 ROP가 없는 경우입니다. 항VEGF 치료 후에는 최소 교정 주령 65주까지 관찰을 지속해야 합니다1).
산동법
섹션 제목: “산동법”Mydrin®P 또는 Neosynesin®·Mydrin®P·Cyplegin®을 2:1:1 비율로 혼합한 점안액(변형 Capto 점안법)을 진찰 시작 1시간 전부터 10분 간격으로 3회 점안하여 산동합니다.
진단 및 평가 보조 기술
섹션 제목: “진단 및 평가 보조 기술”- 광각 안저 카메라(RetCam 등) : 산동 상태에서 광범위한 안저 촬영이 가능합니다. 원격 판독에도 사용됩니다.
- AI 기반 영상 진단 : Plus disease의 자동 검출에서 안과 전문의와 동등하거나 더 높은 정확도가 보고되었습니다1). 딥러닝 모델 기반 혈관 중증도 점수(VSS)가 plus disease 진단의 객관적 지표로 개발되었습니다1).
- 예측 모델(G-ROP, WINROP) : 재태 주수, 출생 체중, 출생 후 체중 증가를 기반으로 type 1 ROP 예측 민감도 100%를 달성했습니다1).
- FIRST-ROP 알고리즘 : 중등도 위험 아동(재태 주수 27주 이상, 출생 체중 800g 이상)에서는 선별검사 시작을 교정 주수 34주까지 지연할 수 있다는 제안이 있습니다1).
- 형광 안저 조영술 : 재증식의 유무와 범위 평가에 유용합니다. PAR 평가에 활용이 기대됩니다3).
재태 주수 26주 미만이면 교정 주수 29주부터, 재태 주수 26주 이상이면 생후 3주부터 첫 검사를 시작합니다. 이후 소견에 따라 1-3주 간격으로 반복합니다. 항VEGF 치료를 받은 경우 교정 주수 65주 이후까지 관찰 지속이 권장됩니다3). 치료가 필요한 소견 없이 망막 혈관화가 완료되면 종료됩니다.
가족 설명
섹션 제목: “가족 설명”출생 시 재태 주수에 따라 다릅니다. 재태 주수 26주 미만인 경우 교정 재태 주수 29주부터, 재태 주수 26주 이상인 경우 생후 3주부터 첫 안저 검사를 시작합니다. 선별검사 대상은 재태 주수 34주 미만 또는 출생 체중 1,800g 이하이지만, 산소 투여, 수혈, 패혈증 등의 위험 인자가 있으면 기준 외에도 검사가 필요합니다.
6. 표준 치료법
섹션 제목: “6. 표준 치료법”항VEGF 유리체내 주사
적응증: zone I 및 A-ROP에 우선 선택
국내 승인 약물: 라니비주맙 0.2mg, 애플리버셉트 0.4mg
장점: 후극부 중증 예에도 시행 용이, 치료 시간이 짧고 환아 부담 적음
주의: 재발 위험이 높아 장기 추적 관찰 필수
유리체 절제술
적응증: 4기 이후의 망막박리
수술법: 고전적 ROP에서는 수정체보존유리체절제술(LSV)이 일차 선택
성적: 4A기 복위율 7491%, 4B기 6292%, 5기 22~48%1)
공막돌륭술
레이저 광응고술
섹션 제목: “레이저 광응고술”1967년 나가타가 세계 최초의 광응고 치료를 시행한 이후, ROP의 표준 치료로 확립되었습니다. 기본적으로 무혈관 영역 전체에 대한 광응고를 간접검안경 하에서 시행합니다. 현저한 수정체혈관막이나 동공강직이 있는 경우 시행이 어려울 수 있습니다. 응고에 시간이 소요되고 술자의 숙련이 필요하며, 광범위한 응고는 시야 협착이나 근시를 초래할 수 있습니다.
CRYO-ROP 시험에서는 1년 후 불량 구조적 결과가 냉동응고군 25.7% 대 관찰군 47.4%였으며, 15년 후에도 유의한 차이가 지속되었습니다(30% 대 52%)8). ETROP 시험에서는 조기 치료로 불량 구조적 결과가 9.1% 대 15.6%로 감소했습니다9).
항VEGF 요법
섹션 제목: “항VEGF 요법”VEGF가 망막 신생혈관에 관여한다는 점에서, 항VEGF 약물의 유리체내 주사가 ROP에 대해 시도되고 있습니다. 2022년 12월 기준으로 국내에서 승인된 ROP 치료용 항VEGF 약물은 다음 두 가지입니다3).
- 라니비주맙(루센티스®): 0.2 mg/회(0.02 mL). 2019년 11월 국내 승인.
- 아플리버셉트(아일리아®): 0.4 mg/회(0.01 mL). 2022년 9월 국내 승인.
두 약제 모두 바이알 제형만 ROP에 대해 승인되었으며, 재투여 간격은 첨부문서상 1개월 이상입니다3). 베바시주맙은 국내외에서 ROP에 대해 미승인 상태입니다3).
주요 임상시험 결과
| 시험명 | 대상/약물 | 주요 결과 |
|---|---|---|
| BEAT-ROP | zone I 3기+, 베바시주맙 0.625 mg | zone I 재발률 6% 대 레이저 42%5, 1) |
| RAINBOW | 출생 체중 1,500 g 미만, 라니비주맙 0.2 mg | 치료 성공률 80.0% 대 레이저 66.2%. 2세 시 고도 근시 5% 대 20%6, 1) |
| FIREFLEYE | 재태 기간 32주 이하 또는 체중 1,500 g 미만, 애플리버셉트 0.4 mg | 성공률 82.7% 대 레이저 84.2%. 전신 마취율 44.0% 대 65.8%7, 1) |
재발률 비교3):
- 애플리버셉트: 재발률 13.9
28%, 평균 재발 시기 1114.2주 - 라니비주맙: 재발률 20.8
83.0%, 재발 시기 5.99.3주 (재발이 더 빠름)
라니비주맙은 주사 후 14일째 혈중 VEGF 감소가 검출되지 않아 전신 영향이 적은 것으로 생각됩니다. 아플리버셉트에서는 혈장 중 유리형 아플리버셉트가 주사 후 약 8주에 정량 하한치까지 감소합니다3).
소아 특유의 주사 기술3):
- 윤부에서 1.0
1.5 mm 후방에서 삽입 (성인의 34 mm와 다르므로 주의) - 수정체가 상대적으로 크므로 아래쪽(후방)으로 삽입합니다. 안구 중심 방향은 수정체 손상 위험이 있습니다
- 30게이지 이하의 주사침 사용
- NICU 인큐베이터 또는 수술실에서 시행
- 마취는 점안마취, 정맥마취, 전신마취 중 시설에 따라 선택
항VEGF 치료의 목적은 크게 세 가지로 나뉩니다. 첫째, 보조 요법(유리체 절제술 전 시간 벌기), 둘째, 구제 요법(광응고가 효과가 없을 때 망막박리 진행 예방), 셋째, 단독 요법(광응고 대체로서 단독 투여)입니다. 단독 요법 후 ROP가 진정되고 무혈관 영역으로 혈관이 성장하는 것으로 보고되었지만, 장기적으로 증식이 재발할 가능성이 있습니다(지연성 망막증).
항VEGF 치료 후 경과 관찰
섹션 제목: “항VEGF 치료 후 경과 관찰”항VEGF 치료 후 관찰 일정은 다음을 기준으로 합니다 3).
- 주사 후 1년: 가능한 2주에 한 번 안저 검사
- 레이저 추가 후 또는 zone III까지 혈관 발달 후: 2~3개월에 한 번
- A-ROP의 경우: 주사 후 2
3주까지 주 2회, 4개월경까지 주 1회, 이후 12주에 한 번 - 재발 판단은 plus disease의 재출현에 주목하고, ETROP 기준에 따라 추가 치료를 시행합니다
- 형광 안저 조영술은 재증식의 유무 및 범위 파악에 유용합니다
유리체 절제술
섹션 제목: “유리체 절제술”4기 이후의 망막 박리에는 외과적 치료가 필요합니다. I형/고전적 ROP에서는 수정체 보존 유리체 절제술(LSV)이 시행되며, 좋은 망막 재유착률과 시력 예후를 얻을 수 있습니다. 4A기의 조기 수술이 시력 예후를 좌우합니다. II형/A-ROP에서는 혈관 섬유 증식의 활동성이 높아 LSV가 효과적이지 않으며, 수정체 제거가 필요한 경우가 많습니다.
LSV의 해부학적 성공률은 4A기 7491%, 4B기 6292%, 5기 22~48%로 보고됩니다 1). 기대 시력은 4A기 재유착 후 20/80 이상, 4B기 복원 후 보행 시력, 5기 복원 후 수동 변별력으로 알려져 있습니다 1). LSV 후 백내장 형성은 10년 이내에는 드물지만, 발생 시 수술 후 1년 이내가 많습니다 1).
약제에 따라 다릅니다. 아플리베르셉트에서는 13.928%, 라니비주맙에서는 20.883.0%에서 재발이 보고되었으며, RAINBOW 시험에서는 31%가 추가 치료를 필요로 했습니다 3, 1). A-ROP에서는 75.0~87.5%에서 추가 치료가 필요하며, 특히 투여 후 초기부터 엄격한 관찰이 필수적입니다.
7. 장기 예후와 합병증
섹션 제목: “7. 장기 예후와 합병증”퇴축과 재활성화
섹션 제목: “퇴축과 재활성화”ICROP3에서는 퇴축(regression)과 재활성화(reactivation)의 개념이 공식적으로 정의되었습니다2). 퇴축은 완전 퇴축과 불완전 퇴축으로 분류됩니다. 항VEGF 후 13일 내에 혈관 변화의 퇴축이 시작되지만, 레이저 후에는 714일이 걸립니다. 퇴축의 초기 징후는 plus disease의 개선과 주변 무혈관 영역으로의 혈관 신장입니다.
불완전 퇴축 후 지속성 무혈관 망막(PAR)이 남을 수 있습니다. PAR은 레이저 후나 자연 퇴축 후보다 항VEGF 후에 더 빈번하고 범위가 넓습니다2). 재활성화(reactivation)는 항VEGF 요법 후에 더 흔하며, 교정 주수 37~60주에 가장 많습니다. 약제와 용량에 따라 지연될 수 있습니다2).
치료되지 않은 ROP의 후기 소견
섹션 제목: “치료되지 않은 ROP의 후기 소견”다기관 후향적 연구(363안, 186명, 평균 연령 34.5세, 평균 재태 주수 26.6주, 평균 출생 체중 875g)에 따르면, 치료되지 않은 ROP의 장기 안저 소견으로 다음이 보고되었습니다4).
- 격자 변성: 196안(54.0%)
- 위축성 구멍: 126안(34.7%)
- 망막 열공: 111안(30.6%)
- 망막 박리: 140안(38.6%)
- 견인성 망막 분리증: 44안(12.1%)
- 황반 견인: 44안(12.1%)
망막 박리의 위험 인자로 재태 주수 29주 이하(P < 0.05)와 후방 zone 2까지의 혈관화(P = 0.009)가 유의했습니다4). 망막 박리의 86.4%가 열공성 또는 혼합형이었고, 57.9%가 30세 이전에 발생했습니다4). 박리안의 20%(28/140안)가 초진 시 복구 불가능하다고 판단되었습니다4). 불완전 혈관화(zone 3 미도달)가 71.6%에서 관찰되었습니다4).
이 결과는 치료되지 않은 ROP에 대한 정기 검사와 초광각 형광 안저 조영술을 통한 평가를 권장합니다4).
고도 근시
섹션 제목: “고도 근시”레이저 광응고 후 고도 근시는 2세 때 20%, 5년 후 24%에서 발생합니다. 라니비주맙 0.2mg군에서는 2세 때 5%, 5년 후 8%로 유의하게 적었습니다1). 미숙아는 ROP와 독립적으로 고도 근시 및 황반 이상(중심와 무혈관대 축소, 중심와 함몰 둔화 또는 소실)의 위험이 있습니다.
안압 상승 및 녹내장
섹션 제목: “안압 상승 및 녹내장”치료하지 않고 자연 퇴행한 경우 안압 상승이 23.2%, 광응고 단독 치료 시 23.3%, 급성기 수술 후 58.5%에서 관찰됩니다 1). 5기에서는 66.7%, 무수정체안에서는 69.8%에서 안압 상승이 나타납니다 1). 진행된 ROP(4-5기)의 10.0%가 3년 이내에 녹내장을 발병하며, 5기는 4A기보다 6.76배, 수정체 적출술 후에는 2.76배의 위험이 있습니다 1).
일으킬 수 있습니다. 치료하지 않은 ROP의 다기관 연구에서는 성인이 되어서도 격자 변성(54%), 망막 열공(30.6%), 망막 박리(38.6%) 등의 후기 합병증이 높은 비율로 관찰되었습니다 4). 망막 박리의 57.9%가 30세 이전에 발생하여, 평생 정기적인 안저 검사가 필수적입니다.
8. 최신 연구와 향후 전망
섹션 제목: “8. 최신 연구와 향후 전망”PAR 관리의 미래
섹션 제목: “PAR 관리의 미래”항VEGF 요법 후 PAR에 대한 레이저 광응고의 최적 시기는 아직 확립되지 않았습니다 1). 베바시주맙 후 수정 주수 60주에 예방적 레이저를 시행하는 것이 불량한 구조적 결과 감소와 관련이 있다는 후향적 연구가 있습니다 1). 형광 안저 혈관 조영술을 통한 재활성화 위험 평가(수정 주수 60주 시점)가 유용하다고 보고되었습니다 1).
대체 약물 요법
섹션 제목: “대체 약물 요법”- 경구 프로프라놀롤: 2 mg/kg/일로 2기 ROP의 중증화 예방 효과가 보고되었으나, 심호흡기 합병증 위험이 있습니다 1). 국소 프로프라놀롤 0.2% 점안액은 1기부터 시작할 경우 안전하고 효과적이라는 보고가 있습니다 1).
- AA/DHA 보충: Mega Donna Mega 시험(206명, 재태 주령 28주 미만)에서 AA+DHA군의 중증 ROP 발생률 15.8% 대 대조군 33.3%(50% 감소)가 보고되었습니다 1).
- 카페인: 미숙아 무호흡에 투여되는 카페인이 VEGF와 MMP의 하향 조절을 통해 ROP 진행을 억제할 가능성이 시사되고 있습니다 1).
- 콘베르셉트(KH902): 중국에서 승인됨. 라니비주맙과 동등한 유효성으로 재발률 16.7% 대 23.3%(라니비주맙)로 보고되었습니다 1).
AI 및 원격의료
섹션 제목: “AI 및 원격의료”딥러닝 모델을 이용한 plus disease 자동 검출이 전문의와 동등한 정확도를 달성하고 있습니다1). 혈관 중증도 점수(VSS)가 plus disease 중증도의 객관적 정량 지표로 개발되었습니다1). SUNDROP과 같은 원격의료 프로그램은 저소득 및 중간 소득 국가를 포함한 원격지에서의 선별 검사 확대를 실현하고 있으며, 휴대용 OCT를 이용한 침상 평가도 기대됩니다1).
9. 참고문헌
섹션 제목: “9. 참고문헌”- Marra KV, Chen JS, Nudleman E, Robbins SL. Review of retinopathy of prematurity management in the anti-VEGF era: evolving global paradigms, persistent challenges and our AI-assisted future. Clin Exp Ophthalmol. 2025;(in press/online).
- Chiang MF, Quinn GE, Fielder AR, et al. International classification of retinopathy of prematurity, third edition. Ophthalmology. 2021;128(10):e51-e68.
- 日本眼科学会・日本小児眼科学会. 未熟児網膜症診療ガイドライン(第2版). 2024.
- Hamad AE, Moinuddin O, Blair MP, et al. Late-onset retinal findings and complications in untreated retinopathy of prematurity. Ophthalmology. 2020;127(2):240-248.
- Mintz-Hittner HA, Kennedy KA, Chuang AZ; BEAT-ROP Cooperative Group. Efficacy of intravitreal bevacizumab for stage 3+ retinopathy of prematurity. N Engl J Med. 2011;364(7):603-615.
- Stahl A, Lepore D, Fielder A, et al. Ranibizumab versus laser therapy for the treatment of very low birthweight infants with retinopathy of prematurity (RAINBOW): an open-label randomised controlled trial. Lancet. 2019;394(10208):1551-1559.
- Stahl A, Sukgen EA, Wu WC, et al. Effect of intravitreal aflibercept vs laser photocoagulation on treatment success of retinopathy of prematurity: the FIREFLEYE randomized clinical trial. JAMA. 2022;328(4):348-359.
- Cryotherapy for Retinopathy of Prematurity Cooperative Group. Multicenter trial of cryotherapy for retinopathy of prematurity: preliminary results. Arch Ophthalmol. 1988;106(4):471-479.
- Good WV, Hardy RJ, Dobson V, et al; Early Treatment for Retinopathy of Prematurity Cooperative Group. The incidence and course of retinopathy of prematurity: findings from the Early Treatment for Retinopathy of Prematurity Study. Pediatrics. 2005;116(1):15-23.
