結節型
形態:邊界清晰、半球狀隆起的腫塊
轉移風險:轉移罕見。預後最好的類型1)
特徵:腫塊侷限於虹膜實質內,對周圍虹膜浸潤少
治療適應症:小型可行虹膜切除術

虹膜惡性黑色素瘤是起源於葡萄膜組織(虹膜、睫狀體、脈絡膜)黑色素細胞的惡性腫瘤,原發於虹膜。僅佔所有葡萄膜黑色素瘤的約2%,與脈絡膜(超過90%)和睫狀體(約7%)相比是最罕見的部位。
發生率為每10萬人0.025例(約為歐美的1/20),虹膜病例僅佔其中一部分。多見於白人和淺色虹膜人群,東方人罕見。與脈絡膜和睫狀體黑色素瘤相比,惡性程度較低,進展較慢。
虹膜惡性黑色素瘤也可由睫狀體浸潤引起。體積大、有增大趨勢、形狀不規則、隅角浸潤是惡性的判斷指標。小型腫瘤可選擇局部切除(虹膜切除術)。
轉移方式均為血行性(葡萄膜無淋巴管),轉移時肝臟是最常見的部位2)。脈絡膜黑色素瘤的12年死亡率約為40%,而虹膜黑色素瘤的轉移率低得多,預後良好。
虹膜惡性黑色素瘤有年輕化發病趨勢,可在比脈絡膜黑色素瘤發病高峰(約60歲)更早的年齡被發現1)。
即使在整個葡萄膜黑色素瘤中,白人的發生率也僅為每百萬人2至8例,屬於罕見癌症,而虹膜病例僅佔約2%。日本人所有葡萄膜黑色素瘤的發生率為每10萬人0.025例(約為歐美的1/20),虹膜病例更為罕見。如果在虹膜發現色素性病變,應在專業機構進行詳細檢查。
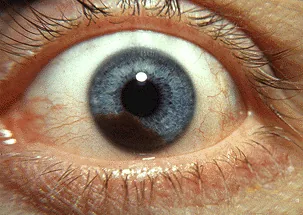
早期小型病變常無症狀,可能在健康檢查或其他疾病檢查中偶然發現。隨著病變增大,出現以下症狀。
表現為虹膜表面的實質性色素性至無色素性腫瘤。提示惡性的臨床指標如下:
結節型
形態:邊界清晰、半球狀隆起的腫塊
轉移風險:轉移罕見。預後最好的類型1)
特徵:腫塊侷限於虹膜實質內,對周圍虹膜浸潤少
治療適應症:小型可行虹膜切除術
瀰漫型
形態:整個虹膜平坦瀰漫的浸潤性病變。邊界不清
轉移風險:比結節型更容易轉移1)
特徵:易引起眼壓升高和隅角浸潤。可能因虹膜異色症(雙眼虹膜顏色不同)而被發現
治療適應症:局部切除困難,常需放射治療或眼球摘除術
發病主要為散發性,確切原因不明。主要風險因素如下。
葡萄膜黑色素瘤(包括虹膜黑色素瘤)的基因突變概況如下。
| 突變基因 | 突變頻率 | 轉移風險/特徵 |
|---|---|---|
| GNAQ/GNA11 | 83–89% | 互斥的起始突變。與轉移風險無直接關聯。 |
| BAP1 | 約45% | 最高轉移風險(高峰在3.5年),第2類腫瘤 |
| SF3B1 | 約23% | 中等風險。特點是晚期轉移(高峰在7年)。 |
| EIF1AX | 約17% | 最低轉移風險 |
GNAQ/GNA11突變是起始突變,損害GTP酶活性並導致持續活化,但與腫瘤大小或轉移風險無直接關聯。二次驅動突變(BAP1、SF3B1、EIF1AX)幾乎完全互斥發生,用於轉移風險分層。
BAP1突變與最高轉移風險相關,而EIF1AX突變表示最低轉移風險。這些突變資訊可透過細針穿刺活檢獲得,並用於個人化轉移監測計劃 1)。
約85%的病例存在GNAQ/GNA11突變,但與轉移風險無直接關聯。轉移風險由二次突變決定:BAP1突變(最高風險,轉移高峰3.5年)、SF3B1突變(中等風險,遲發轉移高峰7年)、EIF1AX突變(最低風險)。透過活檢獲取這些基因圖譜可實現個人化監測頻率。
診斷主要基於影像學檢查和臨床發現的綜合評估。對於虹膜黑色素瘤,以前段為主的檢查很重要。
原發腫瘤確定後,進行以下轉移篩檢。
依情況施行細針吸引切片。越來越多情況下,目的是取得基因譜(GNAQ/GNA11、BAP1、SF3B1、EIF1AX)。考量腫瘤播種風險,需謹慎判斷適應症。
首先用裂隙燈顯微鏡詳細檢查前段,評估腫塊的性質、範圍及隅角浸潤。然後用UBM檢查睫狀體浸潤,用前段OCT記錄腫塊表面形態。懷疑惡性時,用MRI評估眼外浸潤,並進行肝臟超音波及全身CT尋找轉移。建議轉診至專科機構(眼腫瘤專科醫師)。
治療方針根據腫瘤大小、形態、有無睫狀體浸潤以及患者的全身狀況綜合決定。
對於小型且難以與虹膜痣區別的病變,首先透過UBM或前眼部OCT定期監測腫瘤大小。當出現增大或惡化的指標(變大、不規則、隅角浸潤、眼壓升高)時,轉為治療。
小型虹膜黑色素瘤的首選方法。切除包含腫瘤的虹膜(虹膜切除術)。如果睫狀體也受浸潤,則進行虹膜睫狀體切除術(iridocyclectomy)。可保留眼球,並能從切除檢體獲得病理診斷和基因圖譜。
適用於中型腫瘤(局部切除困難時)。
適用於大型腫瘤或難以保留眼球的情況(如瀰漫型、睫狀體大規模浸潤等)。至今仍是重要的選擇之一。
對於轉移性葡萄膜黑色素瘤,替本塔司普(tebentafusp)推薦用於HLA-A*02:01陽性患者1,5)。
在Nathan等人(2021)的第三期隨機對照試驗中,tebentafusp在未經治療的轉移性葡萄膜黑色素瘤患者(HLA-A*02:01陽性)中,與研究者選擇(主要是pembrolizumab)相比,顯示出整體存活期的顯著改善(mOS:21.7個月 vs 16.0個月)4)。
Tebentafusp是一種T細胞受體雙特異性融合蛋白(ImmTAC),通過辨識HLA-A02:01複合物上的腫瘤相關抗原gp100來活化T細胞。給藥前需確認HLA-A02:01陽性,每週一次靜脈注射(劑量遞增:20 mg→30 mg→68 mg)。
給藥期間已報告有脈絡膜變薄、眼底脫色素和皮膚脫色素斑等眼部副作用,需要定期進行眼科監測7)。由於gp100也在正常脈絡膜黑色素細胞上表現,這些副作用可透過機轉解釋7)。
治療後透過定期裂隙燈顯微鏡、UBM和前段OCT監測患眼。同時進行局部復發檢查和轉移監測。建議治療後每6個月一次持續5年,之後每年一次持續10年進行肝臟轉移監測1)。
虹膜黑色素瘤由虹膜黑色素細胞的腫瘤性增生引起。葡萄膜黑色素瘤的發病機轉與皮膚黑色素瘤不同,涉及獨特的分子路徑。
GNAQ/GNA11的Q209位突變是最常見的起始突變,損害GTP酶活性,導致持續的GTP結合活化狀態。這導致包括MAPK路徑(Ras/RAF/MEK/ERK)在內的多條訊息路徑持續活化5)。
二次驅動突變(BAP1、SF3B1、EIF1AX)幾乎完全互斥發生。BAP1突變被歸類為第2類(高轉移風險),與第3號染色體單體密切相關。帶有SF3B1突變的患者轉移後中位總存活期相對較好,以延遲轉移為特徵。
虹膜黑色素瘤比脈絡膜和睫狀體黑色素瘤較不易轉移。與此特性相關的因素包括以下:
由於葡萄膜沒有淋巴管,所有轉移均經由血行途徑發生2)。循環腫瘤細胞隨血流運行,因強烈的肝臟趨向性(種子和土壤理論)導致肝轉移。轉移可能在原發腫瘤治療後25年以上出現2),這就是需要長期監測的原因。
存在腫瘤內異質性,不同形態區域的基因圖譜可能不同6),因此切片取樣位置可能影響預後預測的準確性。
替貝他司普是首個在第三期試驗中顯示總存活期顯著改善的轉移性葡萄膜黑色素瘤治療藥物4)。2023年報告的三年追蹤數據(Hassel et al.)證實了持續的存活改善,三年總存活率為27%(對照組9%)9)。
由於gp100也在虹膜黑色素瘤中表現,因此對於虹膜黑色素瘤轉移的病例也可考慮使用該藥1)。給藥期間的眼部副作用(脈絡膜變薄、眼底脫色素)可能是不可逆的,需要與眼科專家協作7)。
Gαq抑制劑(YM-254890)與MEK抑制劑(trametinib/binimetinib)聯合使用在體外和體內顯示出協同抗腫瘤效果5)。單獨抑制Gαq時,MAPK訊號在24小時內恢復,但與MEK抑制劑聯合使用可抑制MAPK訊號的恢復5)。臨床試驗評估正在進行中。
在葡萄膜黑色素瘤中,免疫檢查點抑制劑的療效與皮膚黑色素瘤相比顯著有限7),單藥治療的有效率約為5%,聯合治療約為12-18%1)。這被認為是由於葡萄膜黑色素瘤的低腫瘤突變負荷(TMB)和免疫微環境的特性所致2)。
然而,據報導,攜帶MBD4(methyl-CpG binding domain-4)基因生殖系或體細胞功能喪失突變的病例可能對檢查點抑制劑更敏感2)。
Johansson等人(2020年)通過全基因組分析在虹膜腫瘤中鑑定出UVR誘導的突變特徵3)。這是首次報告虹膜黑色素瘤在葡萄膜黑色素瘤中具有紫外線相關基因改變,表明其在發病機制上與脈絡膜黑色素瘤存在差異。這一發現可能對紫外線防護的作用以及未來的預防和治療策略有所啟示。
9個自噬相關基因特徵(9-ARG)已被證明可用於預測葡萄膜黑色素瘤的預後8)。在高風險組中,IL6-JAK-STAT3路徑和血管生成相關路徑富集,儘管免疫細胞浸潤(CD8 T細胞、活化記憶CD4 T細胞)增加,但呈現免疫抑制表型,與不良預後相關,這一矛盾發現已被報導8)。這被認為與眼睛是免疫豁免器官有關。
Carter TJ, Broadfoot J, Coupland SE, et al. Uveal Melanoma UK national guidelines: 2023 update. Eur J Cancer. 2023;185:61-73.
Rantala ES, Hernberg MM, Piperno-Neumann S, et al. Metastatic uveal melanoma: The final frontier. Prog Retin Eye Res. 2022;90:101041.
Johansson PA, Brooks K, Newell F, et al. Whole genome landscapes of uveal melanoma show an ultraviolet radiation signature in iris tumours. Nat Commun. 2020;11:2408.
Nathan P, Hassel JC, Rutkowski P, et al. Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021;385(13):1196-1206.
Sriramareddy SN, Smalley KSM. MEK-ing the most of it: strategies to co-target Gαq and MAPK in uveal melanoma. Clin Cancer Res. 2021;27(5):1217-1219.
Fonseca C, Pinto-Proença R, Bergeron S, et al. Intratumoral heterogeneity in uveal melanoma. Ocul Oncol Pathol. 2021;7:17-25.
Krohn J, Vinnem LIH, Jansson RW, et al. Fundus hypopigmentation and choroidal thinning associated with tebentafusp therapy: report of a case and literature review. BMC Ophthalmol. 2025;25:464.
Chuah S, Chew V. Immune implication of an autophagy-related prognostic signature in uveal melanoma. Biosci Rep. 2021;41:BSR20211098.
Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. NEJM Evid. 2023;2(8):EVIDoa2300071.