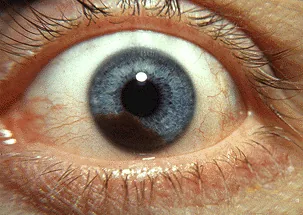
มะเร็งผิวหนังม่านตา ชนิดร้ายเป็นเนื้องอกที่พบได้ยาก คิดเป็นประมาณ 2% ของมะเร็งผิวหนังยูเวีย และมีแนวโน้มที่จะมีความร้ายแรงน้อยกว่าเมื่อเทียบกับที่เกิดจากคอรอยด์ และซิลิอารีบอดี
แสดงเป็นก้อนเนื้อตันของม่านตา ที่มีสีหรือไม่มีสี เมื่อโตขึ้นอาจบุกรุกมุมลูกตาและทำให้ความดันลูกตา สูงขึ้น
การกลายพันธุ์ของ GNAQ/GNA11 พบในประมาณ 85% ของกรณี และการกลายพันธุ์ทุติยภูมิใน BAP1, SF3B1 และ EIF1AX มีความสำคัญต่อการแบ่งชั้นความเสี่ยงของการแพร่กระจาย
ชนิด nodular แพร่กระจายได้น้อย ในขณะที่ชนิด diffuse แพร่กระจายได้มากกว่า 1)
ในก้อนขนาดเล็ก สามารถตัดม่านตา (การตัดออกเฉพาะที่) ได้ ในขนาดกลาง พิจารณาการฉายรังสี ในขนาดใหญ่ พิจารณาการควักลูกตา
หลังการแพร่กระจาย แนะนำให้ใช้ tebentafusp (ในกรณีที่ HLA-A*02:01 เป็นบวก) 1)
มะเร็งผิวหนังม่านตา บางชนิดมีรายงานลายเซ็นที่ถูกกระตุ้นด้วยรังสีอัลตราไวโอเลต ซึ่งบ่งชี้กลไกการเกิดที่แตกต่างจากมะเร็งผิวหนังคอรอยด์ 3)
มะเร็งผิวหนังชนิดร้ายของม่านตา เป็นเนื้องอกร้ายที่เกิดจากเมลาโนไซต์ในม่านตา ซึ่งเป็นส่วนหนึ่งของเนื้อเยื่อยูเวีย (ม่านตา , ซิลิอารีบอดี , คอรอยด์ ) คิดเป็นเพียงประมาณ 2% ของมะเร็งผิวหนังยูเวียทั้งหมด ทำให้เป็นตำแหน่งที่พบได้น้อยที่สุดเมื่อเทียบกับคอรอยด์ (>90%) และซิลิอารีบอดี (ประมาณ 7%)
อุบัติการณ์คือ 0.025 ต่อ 100,000 คน (ประมาณ 1/20 ของอัตราในตะวันตก) และกรณีม่านตา เป็นเพียงส่วนน้อย พบได้บ่อยในคนผิวขาวที่มีม่านตา สีอ่อน และพบได้ยากในคนเอเชีย มีแนวโน้มที่จะมีความร้ายแรงต่ำกว่าและดำเนินโรคช้ากว่ามะเร็งผิวหนังคอรอยด์ และซิลิอารีบอดี
มะเร็งผิวหนังชนิดร้ายของม่านตา อาจเกิดจากการบุกรุกจากซิลิอารีบอดี ขนาดใหญ่ แนวโน้มการโต รูปร่างผิดปกติ และการมีอยู่ของการบุกรุกมุมตาเป็นตัวบ่งชี้ความร้ายแรง ในกรณีขนาดเล็ก การตัดออกเฉพาะที่ (การตัดม่านตา ) อาจเป็นทางเลือก
การแพร่กระจายเป็นทางเลือดเท่านั้น (เนื่องจากไม่มีท่อน้ำเหลืองในยูเวีย) และเมื่อแพร่กระจาย ตับเป็นตำแหน่งที่พบบ่อยที่สุด 2) ในขณะที่อัตราการเสียชีวิต 12 ปีของมะเร็งผิวหนังคอรอยด์ ประมาณ 40% มะเร็งผิวหนังม่านตา มีความถี่ในการแพร่กระจายต่ำกว่ามากและการพยากรณ์โรคดีกว่า
มะเร็งผิวหนังชนิดร้ายของม่านตา มีแนวโน้มที่จะเกิดในอายุน้อย และถูกตรวจพบในกลุ่มอายุที่เร็วกว่าจุดสูงสุดของมะเร็งผิวหนังคอรอยด์ (ประมาณ 60 ปี) 1)
Q
มะเร็งผิวหนังม่านตาพบได้ยากแค่ไหน?
A
แม้แต่มะเร็งผิวหนังยูเวียโดยรวมก็เป็นมะเร็งที่หายาก โดยมีอุบัติการณ์ 2-8 ต่อล้านคนในคนผิวขาว และกรณีม่านตา คิดเป็นเพียงประมาณ 2% ในคนญี่ปุ่น อุบัติการณ์ของมะเร็งผิวหนังยูเวียคือ 0.025 ต่อ 100,000 คน (ประมาณ 1/20 ของตะวันตก) และกรณีม่านตา ยิ่งพบได้ยาก หากพบรอยโรคที่มีสีบนม่านตา การตรวจที่สถานพยาบาลเฉพาะทางเป็นสิ่งสำคัญ
ภาพถ่ายทางคลินิกของมะเร็งเมลาโนมาชนิดร้ายของม่านตา: ก้อนเนื้อตันมีสีและรูม่านตาผิดรูป Trobe JD. The Eyes Have It. Kellogg Eye Center, University of Michigan. 2011. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Iris_melanoma.jpg. License: CC BY 3.0.
ภาพถ่ายทางคลินิกของมะเร็งเมลาโนมาชนิดร้ายของม่านตา ; ก้อนเนื้อตันมีสีนูนขึ้นบนผิวของม่านตา ร่วมกับรูม่านตา ผิดรูป สอดคล้องกับก้อนเนื้อม่านตา ตันมีสีและรูม่านตา ผิดรูปที่กล่าวถึงในหัวข้อ “2. อาการและอาการแสดงทางคลินิกที่สำคัญ”
ในระยะแรก รอยโรคขนาดเล็กมักไม่มีอาการ และพบโดยบังเอิญระหว่างการตรวจสุขภาพหรือการตรวจโรคอื่น เมื่อรอยโรคโตขึ้น จะมีอาการดังต่อไปนี้
การมองเห็น ลดลง/พร่ามัวกลัวแสงและปวดตา : อาจเกิดจากต้อหินทุติยภูมิ จากการลุกลามเข้ามุมหรือความดันลูกตา สูงการเปลี่ยนสีของม่านตา : อาจสังเกตได้จากการขยายของจุดสีที่ม่านตา ข้างเดียวหรือการเปลี่ยนสีการเคลื่อนของเลนส์แก้วตา ม่านตา
ปรากฏเป็นก้อนเนื้อตันที่มีสีจนถึงไม่มีสีบนผิวของม่านตา ตัวชี้วัดทางคลินิกที่บ่งชี้ถึงความร้ายกาจมีดังนี้:
ขนาดใหญ่ (เส้นผ่านศูนย์กลางใหญ่) แนวโน้มการขยายตัว (การขยายขนาดเมื่อติดตามผล)รูปร่างไม่สม่ำเสมอ การลุกลามเข้ามุมและความดันลูกตา สูง เส้นเลือดงอกที่ม่านตา (ชนิดลุกลามเนื้อปรับเลนส์)เลนส์เคลื่อน (ชนิดแทรกซึมของซิลิอารีบอดี )
ชนิดจำกัดเฉพาะที่ (nodular)
ลักษณะ : ก้อนเนื้อขอบเขตชัดเจน นูนขึ้นเป็นรูปครึ่งวงกลม
ความเสี่ยงการแพร่กระจาย : การแพร่กระจายพบได้น้อย เป็นชนิดที่มีพยากรณ์โรคดีที่สุด1)
ลักษณะเด่น : ก้อนเนื้อจำกัดอยู่ภายในสโตรมาของม่านตา มีการแทรกซึมไปยังม่านตา ข้างเคียงน้อย
ข้อบ่งชี้การรักษา : ในก้อนขนาดเล็ก สามารถตัดม่านตา (iridectomy) ได้
ชนิดกระจาย (diffuse)
ลักษณะ : รอยโรคแทรกซึมแผ่ราบไปทั่วทั้งม่านตา ขอบเขตไม่ชัดเจน
ความเสี่ยงการแพร่กระจาย : แพร่กระจายได้ง่ายกว่าชนิดจำกัดเฉพาะที่1)
ลักษณะเด่น : มักทำให้เกิดความดันลูกตา สูงและการแทรกซึมของมุมตา อาจพบเป็นภาวะม่านตา สองสี (heterochromia iridis)
ข้อบ่งชี้การรักษา : การตัดออกเฉพาะที่ทำได้ยาก มักต้องใช้การฉายรังสีหรือการเอาลูกตาออก
การเกิดโรคส่วนใหญ่เป็นแบบประปราย (sporadic) ไม่ทราบสาเหตุที่แน่ชัด ปัจจัยเสี่ยงหลักแสดงไว้ด้านล่าง
ปานของยูเวีย (uveal nevus ) : ปัจจัยเสี่ยงที่พบบ่อยที่สุด ประมาณ 10% เกิดจากปานที่ทราบมาก่อน1) ม่านตา สีอ่อน ผิวขาว แพ้แดดง่ายเม็ดสีเมลานินแต่กำเนิดในตา (Congenital ocular melanocytosis) : ปัจจัยเสี่ยงที่พบได้น้อยรังสีอัลตราไวโอเลต (UVR) : มีรายงานลายเซ็นที่ถูกเหนี่ยวนำโดย UVR ในมะเร็งเมลาโนมาของม่านตา บางส่วน 3) มีการเสนอความคล้ายคลึงกับมะเร็งเมลาโนมาของผิวหนัง ทำให้บทบาทของรังสีอัลตราไวโอเลตได้รับความสนใจ อาจมีกลไกการเกิดที่แตกต่างจากมะเร็งเมลาโนมาของคอรอยด์ ประวัติครอบครัว : การกลายพันธุ์ในสายพันธุ์ของยีน BAP1 (BAP1 predisposition syndrome) เพิ่มความเสี่ยงของมะเร็งเมลาโนมาของยูเวีย 1)
โปรไฟล์การกลายพันธุ์ของยีนในมะเร็งเมลาโนมาของยูเวีย (รวมถึงม่านตา ) มีดังนี้:
ยีนที่กลายพันธุ์ ความถี่ของการกลายพันธุ์ ความเสี่ยงของการแพร่กระจาย / ลักษณะเฉพาะ GNAQ/GNA11 83-89% การกลายพันธุ์เริ่มต้นที่แยกกัน ไม่เกี่ยวข้องโดยตรงกับความเสี่ยงของการแพร่กระจาย BAP1 ประมาณ 45% ความเสี่ยงสูงสุดในการแพร่กระจาย (จุดสูงสุดใหญ่ที่ 3.5 ปี), เนื้องอกคลาส 2 SF3B1 ประมาณ 23% ความเสี่ยงปานกลาง มีลักษณะการแพร่กระจายช้า (จุดสูงสุดใหญ่ที่ 7 ปี) EIF1AX ประมาณ 17% ความเสี่ยงต่ำสุดในการแพร่กระจาย
การกลายพันธุ์ของ GNAQ/GNA11 ทำให้การทำงานของ GTPase บกพร่องและทำให้เกิดการกระตุ้นอย่างต่อเนื่อง แต่ไม่เกี่ยวข้องโดยตรงกับขนาดของเนื้องอกหรือความเสี่ยงในการแพร่กระจาย การกลายพันธุ์ไดรเวอร์ทุติยภูมิ (BAP1, SF3B1, EIF1AX) เกิดขึ้นเกือบจะแยกจากกันโดยสิ้นเชิง และใช้ในการแบ่งชั้นความเสี่ยงของการแพร่กระจาย
การกลายพันธุ์ของ BAP1 สัมพันธ์กับความเสี่ยงสูงสุดในการแพร่กระจาย ในขณะที่การกลายพันธุ์ของ EIF1AX แสดงถึงความเสี่ยงต่ำสุด ข้อมูลการกลายพันธุ์เหล่านี้สามารถหาได้จากการเจาะดูดด้วยเข็มขนาดเล็ก และใช้ในการปรับแผนการเฝ้าระวังการแพร่กระจายให้เป็นรายบุคคล 1)
Q
การกลายพันธุ์ทางพันธุกรรมของมะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตามีผลต่อการพยากรณ์โรคอย่างไร?
A
การกลายพันธุ์ของ GNAQ/GNA11 พบได้ประมาณ 85% ของผู้ป่วย แต่ไม่เกี่ยวข้องโดยตรงกับความเสี่ยงในการแพร่กระจาย ความเสี่ยงในการแพร่กระจายถูกกำหนดโดยการกลายพันธุ์ทุติยภูมิ: การกลายพันธุ์ของ BAP1 (ความเสี่ยงสูงสุด จุดสูงสุดของการแพร่กระจายที่ 3.5 ปี), การกลายพันธุ์ของ SF3B1 (ความเสี่ยงปานกลาง จุดสูงสุดของการแพร่กระจายช้าที่ 7 ปี) และการกลายพันธุ์ของ EIF1AX (ความเสี่ยงต่ำสุด) การได้รับข้อมูลโปรไฟล์ยีนเหล่านี้ผ่านการตัดชิ้นเนื้อทำให้สามารถปรับความถี่ในการเฝ้าระวังให้เป็นรายบุคคลได้
การวินิจฉัยขึ้นอยู่กับการประเมินภาพรวมจากการตรวจด้วยภาพและอาการทางคลินิกเป็นหลัก ในมะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา การตรวจที่เน้นส่วนหน้าของดวงตามีความสำคัญ
กล้องจุลทรรศน์ชนิดกรีด (Slit lamp) : พื้นฐานสำหรับการสังเกตรายละเอียดส่วนหน้า ประเมินรูปร่างของก้อนเนื้อ การสร้างเส้นเลือดใหม่ และการลุกลามเข้ามุม ตรวจ Gonioscopy เพื่อยืนยันการลุกลามของเนื้องอกเข้ามุมUBM (Ultrasound Biomicroscopy)ซิลิอารีบอดี ใช้ในการติดตามขนาดของเนื้องอกและติดตามผลในกรณีขนาดเล็ก การมีอยู่ของการลุกลามไปยังซิลิอารีบอดี ส่งผลโดยตรงต่อแผนการรักษาOCT ส่วนหน้าม่านตา ใช้เสริมเพื่อทำความเข้าใจโครงสร้างภายในของก้อนเนื้อMRI : เนื่องจากคุณสมบัติพาราแมกเนติกของเมลานิน ทำให้แสดงสัญญาณสูงในภาพถ่วงน้ำหนัก T1 และสัญญาณต่ำในภาพถ่วงน้ำหนัก T2 มีประโยชน์ในการประเมินการแพร่กระจายนอกลูกตาหรือไปยังซิลิอารีบอดี อย่างไรก็ตาม การค้นพบนี้ไม่จำเพาะเจาะจงFDG-PET/CT : ใช้ในการตรวจหาการแพร่กระจาย มีรายงานว่ามีความไวและความจำเพาะสูงกว่า CT เพียงอย่างเดียว 2)
หลังจากยืนยันเนื้องอกปฐมภูมิแล้ว ให้ทำการตรวจคัดกรองการแพร่กระจายดังนี้:
อัลตราซาวนด์ช่องท้อง / MRI ตับ : ประเมินการแพร่กระจายไปยังตับ ตับเป็นตำแหน่งที่พบการแพร่กระจายบ่อยที่สุด 2) .CT ทรวงอก-ช่องท้อง : ประเมินปอดและอวัยวะอื่นๆMRI ศีรษะและคอ : ประเมินการลุกลามนอกตาและต่อมน้ำเหลือง
การตัดชิ้นเนื้อด้วยเข็มดูดขนาดเล็กจะดำเนินการตามสถานการณ์ ปัจจุบันมักมีเป้าหมายเพื่อเก็บข้อมูลโปรไฟล์ทางพันธุกรรม (GNAQ/GNA11, BAP1, SF3B1, EIF1AX) ข้อบ่งชี้จะพิจารณาอย่างรอบคอบโดยคำนึงถึงความเสี่ยงของการกระจายของเนื้องอก
ปานม่านตา (iris nevus )UBM หรือ OCT ส่วนหน้าเพื่อให้แน่ใจว่าไม่มีการเจริญเติบโตเนื้องอกม่านตา ที่แพร่กระจาย : การแพร่กระจายจากมะเร็งเต้านมหรือปอด มักมีสีขาวถึงขาวขุ่น หลายตำแหน่ง ประวัติมะเร็งระบบหรือการมีส่วนร่วมของตาทั้งสองข้างช่วยในการวินิจฉัยแยกโรคแซนโทแกรนูโลมาในเด็ก (JXG ) : พบบ่อยในทารก ก้อนสีเหลืองที่ม่านตา ซึ่งอาจหายได้เองกลุ่มอาการโคแกน-รีส (Cogan-Reese syndrome) : ชนิดหนึ่งของกลุ่มอาการเยื่อบุผิวม่านตา มีลักษณะเป็นก้อนที่ม่านตา ความผิดปกติของเยื่อบุผิวกระจกตา และความดันลูกตา สูงเมลาโนไซโตมาของม่านตา : ก้อนสีดำที่ไม่ร้ายแรง ไม่ร้ายแรงทางเนื้อเยื่อ แต่มีรายงานการเปลี่ยนแปลงเป็นมะเร็ง
Q
หากสีของม่านตาเปลี่ยนไป ควรตรวจอะไรบ้าง?
A
ขั้นแรก ตรวจส่วนหน้าอย่างละเอียดด้วยกล้องจุลทรรศน์ชนิดกรีด (slit lamp) เพื่อประเมินลักษณะของก้อน ขอบเขต และการลุกลามเข้ามุม ต่อมาใช้ UBM เพื่อยืนยันการลุกลามของเลนส์ปรับตา และใช้ OCT ส่วนหน้าเพื่อบันทึกลักษณะพื้นผิวของก้อน หากสงสัยว่าเป็นมะเร็ง ให้ทำ MRI เพื่อประเมินการลุกลามนอกตา อัลตราซาวนด์ตับ และ CT ทั่วร่างกายเพื่อค้นหาการแพร่กระจาย ควรส่งต่อผู้ป่วยไปยังศูนย์เฉพาะทาง (จักษุแพทย์ผู้เชี่ยวชาญด้านเนื้องอกตา)
แผนการรักษาจะพิจารณาจากขนาดของเนื้องอก ลักษณะทางสัณฐานวิทยา การลุกลามเข้าสู่ซิลิอารีบอดี และสภาพร่างกายโดยรวมของผู้ป่วย
ในรอยโรคขนาดเล็กที่แยกจากปานม่านตา ได้ยาก ขั้นแรกจะติดตามขนาดเนื้องอกเป็นระยะด้วย UBM หรือ OCT ส่วนหน้า เมื่อมีข้อบ่งชี้ของการเจริญเติบโตหรือการกลายเป็นมะเร็ง (ขนาดใหญ่ขึ้น รูปร่างผิดปกติ การลุกลามเข้ามุมตา ความดันลูกตา สูง) จะเริ่มการรักษา
ทางเลือกแรกสำหรับมะเร็งเมลาโนมาของม่านตา ขนาดเล็ก ทำการตัดม่านตา ที่มีเนื้องอกออก (iridectomy) หากมีการลุกลามเข้าสู่ซิลิอารีบอดี จะทำการตัดม่านตา และซิลิอารีบอดี (iridocyclectomy) สามารถรักษาลูกตาไว้ได้ และข้อดีคือสามารถรับการวินิจฉัยทางพยาธิวิทยาและข้อมูลทางพันธุกรรมจากชิ้นเนื้อที่ตัดออก
บ่งชี้สำหรับเนื้องอกขนาดกลาง (เมื่อการตัดออกเฉพาะที่ทำได้ยาก)
การฝังแร่ : แผ่นกัมมันตภาพรังสีที่มี I-125 (ไอโอดีน-125) หรือ Ru-106 (รูทีเนียม-106) ถูกเย็บติดกับตาขาว เหนือตำแหน่งเนื้องอก ให้ปริมาณรังสีตามกำหนดประมาณ 90 Gy ถึงยอดเนื้องอกการฉายรังสีด้วยอนุภาคหนัก (โปรตอนหรือคาร์บอนไอออน) : ปริมาณรังสีจะรวมอยู่ที่เนื้องอกโดยใช้ปรากฏการณ์ Bragg peak ลดปริมาณรังสีต่อเนื้อเยื่อปกติโดยรอบไซเบอร์ไนฟ์ (การฉายรังสีแบบ Stereotactic) : ทางเลือกที่ไม่ต้องผ่าตัด
บ่งชี้สำหรับเนื้องอกขนาดใหญ่หรือเมื่อการรักษาลูกตาทำได้ยาก (เช่น ชนิดกระจายหรือการลุกลามของซิลิอารีบอดี อย่างกว้างขวาง) ยังคงเป็นทางเลือกสำคัญจนถึงปัจจุบัน
สำหรับมะเร็งเมลาโนมาของยูเวียที่แพร่กระจาย แนะนำให้ใช้ tebentafusp ในผู้ป่วยที่ตรวจพบ HLA-A*02:01 เป็นบวก 1,5)
ในการทดลองแบบสุ่มระยะที่ 3 โดย Nathan และคณะ (2021) tebentafusp แสดงให้เห็นถึงการปรับปรุงอย่างมีนัยสำคัญในอัตราการรอดชีวิตโดยรวมในผู้ป่วยมะเร็งเมลาโนมาคอรอยด์ ระยะแพร่กระจายที่ไม่ได้รับการรักษา (HLA-A*02:01 บวก) เมื่อเทียบกับการเลือกของแพทย์ผู้รักษา (ส่วนใหญ่เป็น pembrolizumab) (mOS: 21.7 เดือน เทียบกับ 16.0 เดือน) 4)
Tebentafusp เป็นโปรตีนฟิวชันแบบสองความจำเพาะของรีเซพเตอร์ทีเซลล์ (ImmTAC) ที่จดจำแอนติเจนที่เกี่ยวข้องกับเนื้องอก gp100 บนคอมเพล็กซ์ HLA-A02:01 และกระตุ้นทีเซลล์ การให้ยาทำโดยการฉีดเข้าหลอดเลือดดำสัปดาห์ละครั้งหลังจากยืนยันผล HLA-A 02:01 บวก (เพิ่มขนาดยา 20 มก. → 30 มก. → 68 มก.)
ระหว่างการให้ยา มีรายงานผลข้างเคียงทางตา เช่น การบางลงของคอรอยด์ การสูญเสียเม็ดสีที่จอตา และจุดด่างขาวบนผิวหนัง ซึ่งจำเป็นต้องมีการติดตามทางจักษุวิทยาเป็นประจำ 7) เนื่องจาก gp100 แสดงออกบนเมลาโนไซต์คอรอยด์ ปกติด้วย ผลข้างเคียงเหล่านี้จึงอธิบายได้ด้วยกลไกดังกล่าว 7)
ปัจจุบันยังไม่มีวิธีการป้องกันที่ชัดเจนสำหรับมะเร็งเมลาโนมาของม่านตา หากคุณมีรอยโรคที่มีเม็ดสีที่ม่านตา หรือได้รับการวินิจฉัยว่าเป็นปานที่ม่านตา โปรดไปพบจักษุแพทย์อย่างสม่ำเสมอ หากเกิดการเปลี่ยนแปลงของสีม่านตา ในตาข้างเดียว รู้สึกว่ามีก้อน ความดันลูกตา เพิ่มขึ้น หรือการมองเห็น เปลี่ยนไป สิ่งสำคัญคือต้องไปพบจักษุแพทย์ทันที
แม้ว่ามะเร็งเมลาโนมาของม่านตา จะมีความเสี่ยงในการแพร่กระจายต่ำกว่ามะเร็งเมลาโนมาคอรอยด์ แต่เมื่อเกิดการแพร่กระจาย การกระจายตัวทางเลือดไปยังตับเป็นหลักจะส่งผลต่อการพยากรณ์โรคอย่างมาก การเฝ้าระวังการแพร่กระจายเป็นประจำ (ส่วนใหญ่คืออัลตราซาวนด์ช่องท้องหรือ MRI ตับทุก 6 เดือนเป็นเวลา 5 ปี จากนั้นปีละครั้งเป็นเวลา 10 ปี) แนะนำให้ทำแม้หลังการรักษา 1) โดยเฉพาะในกรณีที่กลายพันธุ์ BAP1 บวก จำเป็นต้องติดตามอย่างเข้มงวดมากขึ้น โดยคำนึงถึงจุดสูงสุดของการแพร่กระจาย (3.5 ปี)
การติดตามตาที่ได้รับผลกระทบหลังการรักษาทำอย่างสม่ำเสมอด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp), UBM และ OCT ส่วนหน้าของตา การเฝ้าระวังการกลับเป็นซ้ำเฉพาะที่และการเฝ้าระวังการแพร่กระจายทำควบคู่กันไป แนะนำให้เฝ้าระวังการแพร่กระจายไปยังตับทุก 6 เดือนเป็นเวลา 5 ปีหลังการรักษา จากนั้นปีละครั้งเป็นเวลา 10 ปี 1)
เกิดจากการเจริญเติบโตแบบเนื้องอกของเมลาโนไซต์ในม่านตา กลไกการเกิดมะเร็งเมลาโนมาคอรอยด์ แตกต่างจากมะเร็งเมลาโนมาที่ผิวหนัง โดยเป็นไปตามวิถีทางโมเลกุลที่เป็นเอกลักษณ์
การกลายพันธุ์ Q209 ใน GNAQ/GNA11 เป็นการกลายพันธุ์เริ่มต้นที่พบบ่อยที่สุด ทำให้การทำงานของ GTPase บกพร่องและนำไปสู่สภาวะการกระตุ้น GTP อย่างต่อเนื่อง ส่งผลให้เกิดการกระตุ้นวิถีสัญญาณหลายวิถีอย่างต่อเนื่อง รวมถึงวิถี MAPK (Ras/RAF/MEK/ERK) 5)
การกลายพันธุ์ไดรเวอร์ทุติยภูมิ (BAP1, SF3B1, EIF1AX) เกิดขึ้นเกือบจะแยกกันโดยสิ้นเชิง การกลายพันธุ์ BAP1 จัดอยู่ในกลุ่ม 2 (ความเสี่ยงสูงต่อการแพร่กระจาย) และสัมพันธ์อย่างมากกับโมโนโซมี 3 ค่ามัธยฐานการรอดชีวิตโดยรวมหลังการแพร่กระจายในผู้ที่มีการกลายพันธุ์ SF3B1 ค่อนข้างดี โดยมีลักษณะการแพร่กระจายที่ช้า
มะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา มีแนวโน้มที่จะแพร่กระจายน้อยกว่าเมื่อเทียบกับมะเร็งผิวหนังชนิดเมลาโนมาที่คอรอยด์ และซิลิอารีบอดี ปัจจัยที่เกี่ยวข้องกับลักษณะนี้ได้แก่:
ม่านตา มีเลือดไหลเวียนมาก แต่การดำเนินโรคของเนื้องอกต้องใช้เวลาชนิดเป็นก้อน (nodular) แทบไม่แพร่กระจาย ในขณะที่ชนิดกระจาย (diffuse) มีแนวโน้มแพร่กระจายมากกว่า1)
ในมะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา พบลายเซ็นการกลายพันธุ์ที่เกิดจากรังสีอัลตราไวโอเลตในบางราย (Johansson et al. 2020)3) เชื่อว่าสัมพันธ์กับลักษณะทางกายวิภาคของม่านตา ที่อยู่ในส่วนหน้าของดวงตา ซึ่งได้รับรังสีอัลตราไวโอเลตมากกว่าคอรอยด์ การค้นพบนี้ชี้ว่ามะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา อาจมีกลไกการเกิดโรคคล้ายกับมะเร็งผิวหนังชนิดเมลาโนมาที่ผิวหนัง3)
เนื่องจากไม่มีท่อน้ำเหลืองในยูเวีย การแพร่กระจายจึงเกิดขึ้นทางกระแสเลือดทั้งหมด2) เซลล์เนื้องอกที่ไหลเวียนเดินทางตามกระแสเลือดและทำให้เกิดการแพร่กระจายไปยังตับเนื่องจากความชอบต่อตับอย่างมาก (ทฤษฎี seed and soil) การแพร่กระจายอาจปรากฏขึ้นหลังจากรักษาเนื้องอกปฐมภูมิมากกว่า 25 ปี2) ซึ่งเป็นเหตุผลที่ต้องมีการเฝ้าระวังระยะยาว
มีความแตกต่างภายในเนื้องอก ซึ่งโปรไฟล์ทางพันธุกรรมอาจแตกต่างกันระหว่างบริเวณที่มีลักษณะทางสัณฐานวิทยาต่างกัน6) ดังนั้นตำแหน่งที่เก็บตัวอย่างชิ้นเนื้ออาจส่งผลต่อความแม่นยำในการพยากรณ์โรค
Tebentafusp เป็นยาตัวแรกสำหรับมะเร็งผิวหนังชนิดเมลาโนมาที่ยูเวียระยะแพร่กระจายที่แสดงให้เห็นการปรับปรุงการรอดชีวิตโดยรวมอย่างมีนัยสำคัญในการทดลองระยะที่ III4) ในข้อมูลติดตามผล 3 ปีที่รายงานในปี 2023 (Hassel et al.) ยืนยันการปรับปรุงการรอดชีวิตอย่างต่อเนื่อง โดยอัตราการรอดชีวิต 3 ปีอยู่ที่ 27% (เทียบกับ 9% ในกลุ่มควบคุม)9)
เนื่องจาก gp100 แสดงออกในมะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา ด้วย จึงพิจารณาใช้ยาเดียวกันในกรณีที่มีการแพร่กระจายจากมะเร็งผิวหนังชนิดเมลาโนมาที่ม่านตา 1) ผลข้างเคียงทางตาระหว่างการให้ยา (คอรอยด์ บางลง, จอประสาทตา สีจาง) อาจไม่สามารถกลับคืนได้ในบางกรณี จึงจำเป็นต้องทำงานร่วมกับผู้เชี่ยวชาญด้านจักษุวิทยา7)
การใช้ยายับยั้ง Gαq (YM-254890) ร่วมกับยายับยั้ง MEK (trametinib/binimetinib) แสดงให้เห็นฤทธิ์ต้านเนื้องอกแบบเสริมฤทธิ์กันทั้งในหลอดทดลองและในสิ่งมีชีวิต 5) การยับยั้ง Gαq เพียงอย่างเดียวทำให้สัญญาณ MAPK ฟื้นตัวภายใน 24 ชั่วโมง แต่การใช้ร่วมกับยายับยั้ง MEK จะยับยั้งการฟื้นตัวของสัญญาณ MAPK 5) การประเมินในการทดลองทางคลินิกยังคงดำเนินต่อไป
ในมะเร็งเมลาโนมาของยูเวีย (uveal melanoma) ผลของยายับยั้งจุดตรวจภูมิคุ้มกันมีจำกัดอย่างมากเมื่อเทียบกับมะเร็งเมลาโนมาที่ผิวหนัง 7) โดยอัตราการตอบสนองต่อการรักษาเดี่ยวประมาณ 5% และการรักษาแบบผสมผสานประมาณ 12-18% 1) เชื่อว่าเกิดจากปริมาณการกลายพันธุ์ของเนื้องอก (TMB) ที่ต่ำและลักษณะเฉพาะของสภาพแวดล้อมจุลภาคภูมิคุ้มกันของมะเร็งเมลาโนมาของยูเวีย 2)
อย่างไรก็ตาม มีรายงานว่าผู้ป่วยที่มีการกลายพันธุ์แบบสูญเสียหน้าที่ในระดับเซลล์สืบพันธุ์หรือร่างกายในยีน MBD4 (methyl-CpG binding domain-4) อาจมีความไวต่อยายับยั้งจุดตรวจเพิ่มขึ้น 2)
Johansson และคณะ (2020) ระบุลายเซ็นการกลายพันธุ์ที่เกิดจากรังสี UVR ในเนื้องอกของม่านตา โดยใช้การวิเคราะห์จีโนมทั้งหมด 3) นี่เป็นรายงานแรกที่แสดงให้เห็นว่ามะเร็งเมลาโนมาของม่านตา ในบรรดามะเร็งเมลาโนมาของยูเวีย มีการเปลี่ยนแปลงทางพันธุกรรมที่เกี่ยวข้องกับรังสี UVR ซึ่งเป็นการค้นพบที่สำคัญที่แสดงให้เห็นถึงความแตกต่างในกลไกการเกิดเมื่อเทียบกับมะเร็งเมลาโนมาของคอรอยด์ การค้นพบนี้อาจมีนัยต่อบทบาทของการป้องกันรังสี UVR และกลยุทธ์การป้องกันและรักษาในอนาคต
ลายเซ็นยีนที่เกี่ยวข้องกับ autophagy 9 ยีน (9-ARG) ได้รับการแสดงว่ามีประโยชน์ในการทำนายพยากรณ์โรคของมะเร็งเมลาโนมาของยูเวีย 8) ในกลุ่มที่มีความเสี่ยงสูง เส้นทาง IL6-JAK-STAT3 และเส้นทางที่เกี่ยวข้องกับการสร้างเส้นเลือดใหม่จะเพิ่มขึ้น และการแทรกซึมของเซลล์ภูมิคุ้มกัน (เซลล์ T CD8 และเซลล์ T CD4 ความจำที่ถูกกระตุ้น) เพิ่มขึ้น แต่แสดงฟีโนไทป์ที่กดภูมิคุ้มกัน และมีรายงานการค้นพบที่ขัดแย้งซึ่งสัมพันธ์กับการพยากรณ์โรคที่ไม่ดี 8) เชื่อว่าสิ่งนี้เกี่ยวข้องกับความจริงที่ว่าดวงตาเป็นอวัยวะที่มีเอกสิทธิ์ทางภูมิคุ้มกัน
Carter TJ, Broadfoot J, Coupland SE, et al. Uveal Melanoma UK national guidelines: 2023 update. Eur J Cancer. 2023;185:61-73.
Rantala ES, Hernberg MM, Piperno-Neumann S, et al. Metastatic uveal melanoma: The final frontier. Prog Retin Eye Res. 2022;90:101041.
Johansson PA, Brooks K, Newell F, et al. Whole genome landscapes of uveal melanoma show an ultraviolet radiation signature in iris tumours. Nat Commun. 2020;11:2408.
Nathan P, Hassel JC, Rutkowski P, et al. Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021;385(13):1196-1206.
Sriramareddy SN, Smalley KSM. MEK-ing the most of it: strategies to co-target Gαq and MAPK in uveal melanoma. Clin Cancer Res. 2021;27(5):1217-1219.
Fonseca C, Pinto-Proença R, Bergeron S, et al. Intratumoral heterogeneity in uveal melanoma. Ocul Oncol Pathol. 2021;7:17-25.
Krohn J, Vinnem LIH, Jansson RW, et al. Fundus hypopigmentation and choroidal thinning associated with tebentafusp therapy: report of a case and literature review. BMC Ophthalmol. 2025;25:464.
Chuah S, Chew V. Immune implication of an autophagy-related prognostic signature in uveal melanoma. Biosci Rep. 2021;41:BSR20211098.
Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. NEJM Evid. 2023;2(8):EVIDoa2300071.