결절형 (nodular)
형태: 경계가 명확하고 반구형으로 융기된 종괴
전이 위험: 전이는 드물다. 가장 예후가 좋은 병형이다1)
특징: 종괴가 홍채 실질 내에 국한되고 주변 홍채로의 침윤이 적음
치료 적응증: 소형에서는 홍채 절제술(iridectomy)이 가능

홍채 악성 흑색종은 포도막 조직(홍채, 섬모체, 맥락막)의 멜라닌 세포에서 유래한 악성 종양으로, 홍채를 원발 부위로 합니다. 전체 포도막 흑색종의 약 2%를 차지할 뿐이며, 맥락막 발생(90% 초과), 섬모체 발생(약 7%)과 비교하여 가장 드문 발생 부위입니다.
발생 빈도는 인구 10만 명당 0.025명(서양의 약 1/20)이며, 홍채 발생 예는 그 일부에 불과합니다. 백인, 밝은 색 홍채를 가진 인종에 많고, 동양인에서는 발생이 드뭅니다. 맥락막이나 섬모체 흑색종에 비해 비교적 악성도가 낮고 진행이 느린 경향이 있습니다.
홍채 악성 흑색종에는 섬모체로부터의 침윤에 의한 것도 있습니다. 대형, 증대 경향, 불규칙한 형태, 각침윤 유무가 악성 판단 지표가 됩니다. 소형에서는 국소 절제(홍채 절제술)가 선택 가능한 경우가 있습니다.
전이 방식은 모두 혈행성이며(포도막에 림프관이 없기 때문에), 전이 시 간으로의 친화성이 가장 강합니다2). 맥락막 흑색종의 12년 사망률이 약 40%인 반면, 홍채 흑색종에서는 전이 빈도가 훨씬 낮고 예후가 양호한 것으로 알려져 있습니다.
홍채 악성 흑색종은 젊은 연령에서 발병하는 경향이 있으며, 맥락막 흑색종의 발병 피크(약 60세)보다 이른 연령층에서도 발견됩니다1).
포도막 흑색종 전체에서도 백인에서 100만 명당 2~8명으로 희귀암이며, 홍채 발생은 그 약 2%를 차지할 뿐입니다. 일본인에서 전체 포도막 흑색종 발생은 인구 10만 명당 0.025명(서양의 약 1/20)이며, 홍채 발생 예는 더욱 드뭅니다. 홍채에 색소성 병변을 발견한 경우 전문 기관에서 정밀 검사가 중요합니다.
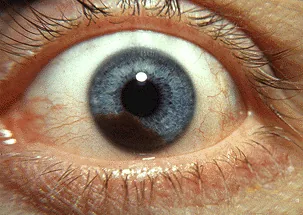
초기 소형 병변은 무증상인 경우가 많으며, 건강 검진이나 다른 질환 검사 중 우연히 발견될 수 있습니다. 병변이 커짐에 따라 다음과 같은 증상이 나타납니다.
홍채 표면에 고형의 색소성~무색소성 종양으로 관찰됩니다. 악성을 시사하는 임상 지표는 다음과 같습니다.
결절형 (nodular)
형태: 경계가 명확하고 반구형으로 융기된 종괴
전이 위험: 전이는 드물다. 가장 예후가 좋은 병형이다1)
특징: 종괴가 홍채 실질 내에 국한되고 주변 홍채로의 침윤이 적음
치료 적응증: 소형에서는 홍채 절제술(iridectomy)이 가능
미만형 (diffuse)
형태: 홍채 전체에 편평하게 퍼지는 침윤성 병변. 경계가 불명확
전이 위험: 결절형에 비해 전이가 잘 됨1)
특징: 안압 상승 및 전방각 침윤을 일으키기 쉬움. 홍채 이색증(양안 홍채색의 차이)으로 발견되기도 함
치료 적응증: 국소 절제가 어렵고 방사선 치료나 안구 적출술이 필요한 경우가 많음
발병은 주로 산발성(sporadic)이며 명확한 원인은 알려져 있지 않습니다. 주요 위험 인자는 다음과 같습니다.
포도막 흑색종(홍채 흑색종 포함)의 유전자 돌연변이 프로필은 다음과 같습니다.
| 돌연변이 유전자 | 돌연변이 빈도 | 전이 위험/특징 |
|---|---|---|
| GNAQ/GNA11 | 83~89% | 상호 배타적인 시작 돌연변이. 전이 위험과 직접적인 연관성 없음. |
| BAP1 | 약 45% | 가장 높은 전이 위험(최고점 3.5년), 클래스 2 종양 |
| SF3B1 | 약 23% | 중간 위험. 늦은 전이(최고점 7년)가 특징입니다. |
| EIF1AX | 약 17% | 가장 낮은 전이 위험 |
GNAQ/GNA11 돌연변이는 GTPase 활성을 손상시켜 지속적인 활성화를 초래하는 시작 돌연변이이지만, 종양 크기나 전이 위험과 직접적인 관련은 없습니다. 2차 드라이버 돌연변이(BAP1, SF3B1, EIF1AX)는 거의 완전히 상호 배타적으로 발생하며 전이 위험 계층화에 사용됩니다.
BAP1 돌연변이는 가장 높은 전이 위험과 관련이 있고, EIF1AX 돌연변이는 가장 낮은 전이 위험을 나타냅니다. 이러한 돌연변이 정보는 세침 흡인 생검을 통해 얻을 수 있으며 전이 감시 계획의 개인화에 활용됩니다 1).
진단은 주로 영상 검사와 임상 소견의 종합 평가에 기반합니다. 홍채 흑색종에서는 전안부를 중심으로 한 검사가 중요합니다.
원발 종양이 확정된 후, 다음과 같은 전이 선별검사를 시행합니다.
상황에 따라 세침 흡인 생검을 시행합니다. 점차 유전자 프로파일(GNAQ/GNA11, BAP1, SF3B1, EIF1AX)을 얻는 것이 목적인 경우가 늘고 있습니다. 종종 파종 위험을 고려하여 적응증을 신중히 판단합니다.
먼저 세극등 현미경으로 전안부를 자세히 관찰하여 종괴의 성상, 범위, 각 침윤 여부를 평가합니다. 다음으로 UBM으로 섬모체 침윤을 확인하고, 전안부 OCT로 종괴의 표면 형태를 기록합니다. 악성이 의심되는 경우 MRI로 안외 침범을 평가하고, 간 초음파 및 전신 CT로 전이 검색을 시행합니다. 전문 기관(안종양 전문의)으로의 의뢰가 바람직합니다.
치료 방침은 종양의 크기, 형태, 모양체 침윤 유무, 환자의 전신 상태를 종합하여 결정합니다.
작고 홍채 모반과의 감별이 어려운 병변에서는 먼저 UBM이나 전안부 OCT로 종양 크기를 정기적으로 모니터링합니다. 증가, 악성화를 나타내는 지표(대형화, 불규칙 모양, 전방각 침윤, 안압 상승)가 나타나면 치료로 전환합니다.
소형 홍채 흑색종의 일차 선택입니다. 종양을 포함한 홍채를 절제합니다(iridectomy). 모양체에도 침윤된 경우 홍채모양체절제술(iridocyclectomy)을 시행합니다. 안구 보존이 가능하고, 절제 검체에서 병리 진단 및 유전자 프로파일을 얻을 수 있는 장점이 있습니다.
중형(국소 절제가 어려운 경우)에 적응됩니다.
대형이거나 안구 보존이 어려운 경우(미만형, 모양체 대규모 침윤 등)에 적응됩니다. 오늘날에도 중요한 선택지 중 하나입니다.
전이성 포도막 흑색종에 대해 테벤타푸스프(tebentafusp)가 HLA-A*02:01 양성 환자에게 권장됩니다1,5).
Nathan 등(2021)의 3상 무작위 대조 시험에서, tebentafusp은 치료받지 않은 전이성 포도막 흑색종 환자(HLA-A*02:01 양성)에서 담당의사 선택(주로 pembrolizumab)과 비교하여 전체 생존 기간의 유의한 개선을 보였습니다(mOS: 21.7개월 대 16.0개월) 4).
Tebentafusp은 T세포 수용체 이중특이성 융합 단백질(ImmTAC)로, HLA-A02:01 복합체 상의 종양 관련 항원 gp100을 인식하여 T세포를 활성화합니다. 투여는 HLA-A02:01 양성 확인 후 주 1회 정맥 주사로 진행됩니다(20 mg→30 mg→68 mg 증량).
투여 중 맥락막 얇아짐, 안저 탈색소, 피부 탈색소 반점 등의 안구 부작용이 보고되었으며, 정기적인 안과적 모니터링이 필요합니다 7). gp100은 정상 맥락막 멜라닌 세포에도 발현되므로, 이러한 부작용은 기전으로 설명됩니다 7).
치료 후 환안 감시는 정기적인 세극등 현미경, UBM, 전안부 OCT로 시행합니다. 국소 재발 확인과 전이 감시를 병행하여 실시합니다. 치료 후 6개월마다 5년간, 이후 1년마다 10년간의 간 전이 감시가 권장됩니다 1).
홍채 흑색종은 홍채 멜라닌 세포의 종양성 증식으로 인해 발생합니다. 포도막 흑색종의 발병 기전은 피부 흑색종과 다르며, 독자적인 분자 경로에 의합니다.
GNAQ/GNA11의 Q209 위치 돌연변이가 시작 돌연변이로 가장 흔하며, GTPase 활성을 손상시켜 지속적인 GTP 결합 활성화 상태를 초래합니다. 이로 인해 MAPK 경로(Ras/RAF/MEK/ERK)를 포함한 여러 신호 경로가 지속적으로 활성화됩니다 5).
2차 드라이버 돌연변이(BAP1, SF3B1, EIF1AX)는 서로 거의 완전히 배타적으로 발생합니다. BAP1 돌연변이는 클래스 2(고전이 위험)로 분류되며 3번 염색체 단일체와 강한 연관성이 있습니다. SF3B1 돌연변이 보유자의 전이 후 전체 생존기간 중앙값은 비교적 양호하며 지연성 전이가 특징입니다.
홍채 흑색종은 맥락막 및 섬모체 흑색종에 비해 전이 경향이 낮습니다. 이 특성과 관련된 요인은 다음과 같습니다.
포도막에는 림프관이 없기 때문에 모든 전이는 혈행성으로 발생합니다2). 순환 종양 세포가 혈류를 타고 간으로 강한 친화성(씨앗과 토양 이론)을 보여 간 전이를 일으킵니다. 전이는 원발 종양 치료 후 25년 이상 지나서 나타날 수도 있어2) 장기 감시가 필요한 이유입니다.
종양 내 이질성이 존재하며 형태학적으로 다른 부위에서 유전자 프로파일이 다를 수 있으므로6) 생검 샘플링 위치가 예후 예측 정확도에 영향을 미칠 수 있습니다.
테벤타푸스프는 3상 시험에서 전체 생존기간의 유의한 개선을 보인 최초의 전이성 포도막 흑색종 치료제입니다4). 2023년에 보고된 3년 추적 데이터(Hassel et al.)에서는 3년 전체 생존율이 27%(대조군 9%)로 지속적인 생존 개선이 확인되었습니다9).
gp100은 홍채 흑색종에서도 발현되므로 홍채 흑색종에서 전이된 경우에도 이 약의 적응이 고려됩니다1). 투여 중 안구 부작용(맥락막 얇아짐, 안저 탈색소)은 비가역적일 수 있으므로 안과 전문의와의 협력이 필요합니다7).
Gαq 억제제(YM-254890)와 MEK 억제제(trametinib/binimetinib)의 병용은 시험관 내 및 생체 내에서 상승적 항종양 효과를 보여주었습니다5). Gαq 단독 억제 시 MAPK 신호는 24시간 내에 회복되지만, MEK 억제제와의 병용은 MAPK 신호의 회복을 억제합니다5). 임상 시험에서의 평가가 계속되고 있습니다.
포도막 흑색종에서는 피부 흑색종에 비해 면역관문억제제의 효과가 현저히 제한적이며7), 단독 요법의 반응률은 약 5%, 병용 요법에서도 12~18% 정도로 알려져 있습니다1). 이는 포도막 흑색종의 낮은 종양 돌연변이 부담(TMB)과 면역 미세환경의 특성 때문인 것으로 생각됩니다2).
그러나 MBD4(methyl-CpG binding domain-4) 유전자의 생식세포 또는 체세포 기능 상실 돌연변이를 가진 증례에서는 면역관문억제제에 대한 감수성이 높아질 가능성이 보고되었습니다2).
Johansson 등(2020)은 전장유전체 분석을 통해 홍채 종양에서 UVR 유발 돌연변이 시그니처를 확인했습니다3). 이는 포도막 흑색종 중에서도 홍채 흑색종이 자외선 관련 유전자 변화를 가짐을 보여주는 첫 번째 보고이며, 발생 기전 측면에서 맥락막 흑색종과의 차이를 나타내는 중요한 발견입니다. 이 발견은 자외선 차단의 역할과 향후 예방 및 치료 전략에 시사점을 줄 수 있습니다.
자가포식 관련 9개 유전자 시그니처(9-ARG)가 포도막 흑색종의 예후 예측에 유용한 것으로 나타났습니다8). 고위험군에서는 IL6-JAK-STAT3 경로와 혈관신생 관련 경로가 농축되고, 면역세포 침윤(CD8 T세포, 활성화 기억 CD4 T세포)이 증가하지만 면역억제 표현형을 나타내어 예후 불량과 관련된다는 역설적 소견이 보고되었습니다8). 이는 눈이 면역 특권 기관이라는 점과 관련이 있는 것으로 생각됩니다.
Carter TJ, Broadfoot J, Coupland SE, et al. Uveal Melanoma UK national guidelines: 2023 update. Eur J Cancer. 2023;185:61-73.
Rantala ES, Hernberg MM, Piperno-Neumann S, et al. Metastatic uveal melanoma: The final frontier. Prog Retin Eye Res. 2022;90:101041.
Johansson PA, Brooks K, Newell F, et al. Whole genome landscapes of uveal melanoma show an ultraviolet radiation signature in iris tumours. Nat Commun. 2020;11:2408.
Nathan P, Hassel JC, Rutkowski P, et al. Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021;385(13):1196-1206.
Sriramareddy SN, Smalley KSM. MEK-ing the most of it: strategies to co-target Gαq and MAPK in uveal melanoma. Clin Cancer Res. 2021;27(5):1217-1219.
Fonseca C, Pinto-Proença R, Bergeron S, et al. Intratumoral heterogeneity in uveal melanoma. Ocul Oncol Pathol. 2021;7:17-25.
Krohn J, Vinnem LIH, Jansson RW, et al. Fundus hypopigmentation and choroidal thinning associated with tebentafusp therapy: report of a case and literature review. BMC Ophthalmol. 2025;25:464.
Chuah S, Chew V. Immune implication of an autophagy-related prognostic signature in uveal melanoma. Biosci Rep. 2021;41:BSR20211098.
Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. NEJM Evid. 2023;2(8):EVIDoa2300071.