มะเร็งเมลาโนมาชนิดร้ายปฐมภูมิของซิลิอารีบอดี คิดเป็นประมาณ 7% ของมะเร็งเมลาโนมาของยูเวีย พบได้บ่อยในวัยกลางคนและผู้สูงอายุ
เนื่องจากตำแหน่งทางกายวิภาคที่ซ่อนอยู่ มักมีขนาดค่อนข้างใหญ่เมื่อตรวจพบ และเส้นเลือดเซนทิเนล (sentinel vessel) เป็นเครื่องชี้นำในการวินิจฉัย
การตรวจ透光 (transillumination) (ส่องแหล่งแสงส่องกล้องจากภายนอกตาขาว ในห้องมืด) มีความสำคัญในการแยกแยะเนื้องอกที่มีเม็ดสีและไม่มีเม็ดสี
UBM (Ultrasound Biomicroscopy) เป็นการตรวจภาพที่มีประโยชน์มากที่สุดในการประเมินขนาดและเสียงสะท้อนภายในของเนื้องอกซิลิอารีบอดี การตัดออกทั้งหมดผ่านตาขาว สำหรับเนื้องอกขนาดเล็ก การฉายรังสีลำอนุภาคหนักหรือการฝังแร่สำหรับเนื้องอกขนาดกลาง และการควักลูกตาสำหรับเนื้องอกขนาดใหญ่เป็นหลักการพื้นฐาน
การพยากรณ์โรคคล้ายกับมะเร็งเมลาโนมาคอรอยด์ และไม่ดี การแพร่กระจายไปตับเป็นตัวกำหนดการพยากรณ์โรค
มะเร็งเมลาโนมาชนิดร้ายของซิลิอารีบอดี เป็นเนื้องอกร้ายที่เกิดจากเมลาโนไซต์ของซิลิอารีบอดี ในบรรดามะเร็งเมลาโนมาของยูเวีย (ม่านตา , ซิลิอารีบอดี , คอรอยด์ ) ที่เกิดจากเมลาโนไซต์ของยูเวีย ประมาณ 7% มาจากซิลิอารีบอดี 2) .
เมื่อตรวจพบเนื้องอกซิลิอารีบอดี ต้องพิจารณาถึงความเป็นไปได้ของมะเร็งเมลาโนมาชนิดร้ายก่อน มะเร็งเมลาโนมาชนิดร้ายของซิลิอารีบอดี จะสังเกตเห็นเป็นส่วนนูนสีน้ำตาลดำของซิลิอารีบอดี ผ่านรูม่านตา แต่เนื่องจากเนื้องอกเกิดจากเนื้อเยื่อของซิลิอารีบอดี สิ่งที่เห็นโดยตรงคือสีของเยื่อบุผิวที่มีเม็ดสี ดังนั้น การที่เนื้องอกมีเม็ดสีหรือไม่นั้นพิจารณาจากการตรวจ透光
อุบัติการณ์โดยรวมของมะเร็งเมลาโนมาของยูเวียในญี่ปุ่นประมาณ 1/20 ของประเทศตะวันตก คาดว่าอยู่ที่ 0.025 ต่อประชากร 100,000 คนต่อปี พบมากที่สุดในคอรอยด์ พบน้อยกว่าในซิลิอารีบอดี เกิดในวัยกลางคนและผู้สูงอายุ พบในเพศชายมากกว่าเล็กน้อย
รูปแบบการแพร่กระจายทั้งหมดเป็นทางเลือด (เนื่องจากยูเวียไม่มีท่อน้ำเหลือง) และแสดงความชอบต่อตับอย่างมาก อายุร median survival โดยรวมหลังการแพร่กระจายเดิมน้อยกว่า 6 เดือน แต่กำลังดีขึ้นด้วยการถือกำเนิดของ tebentafusp
Q
มะเร็งเมลาโนมาซิลิอารีบอดีตรวจพบได้อย่างไร?
A
ซิลิอารีบอดี เป็นบริเวณที่มองเห็นได้ยากในการตรวจอวัยวะภายในลูกตา มักตรวจพบผ่านการตรวจส่วนหน้าหลังจากขยายม่านตา (gonioscopy, slit-lamp) หรือผ่านอาการเช่น การมองเห็น ลดลง, เส้นเลือดเซนทิเนล (sentinel vessel), หรือต้อหินทุติยภูมิ เนื่องจากตรวจพบได้ยากในการตรวจสุขภาพ การไปพบจักษุแพทย์ทันทีเมื่อมีอาการจึงเป็นสิ่งสำคัญ
อาการแสดงเฉพาะของมะเร็งเมลาโนมาของซิลิอารีบอดี้ เนื่องจากลักษณะเฉพาะของตำแหน่งทางกายวิภาค มีลักษณะดังต่อไปนี้ 3) .
การมองเห็น ลดลงแบบไม่เจ็บปวด (พร่ามัว)สายตาเอียง จากการเคลื่อนของเลนส์ตาม่านตา จากเนื้องอกข้อบกพร่องของลานสายตาแบบไม่เจ็บปวดเมื่อเนื้องอกรุกล้ำแนวแกนตา : เกิดขึ้นเมื่อเนื้องอกขยายเข้าไปในโพรงวุ้นตา การมองเห็น ลดลงแบบเจ็บปวดจากความดันลูกตา สูงเฉียบพลันต้อหินมุมปิด ทุติยภูมิ พบความดันลูกตา สูงทุติยภูมิได้ถึง 17% เมื่อวินิจฉัย 3) .
การตรวจส่วนหน้าของตาหลังขยายม่านตา พบก้อนนูนสีน้ำตาลดำบริเวณซิลิอารีบอดี ้ อาการแสดงต่อไปนี้เป็นแนวทางในการวินิจฉัย
มะเร็งเมลาโนมาของซิลิอารีบอดี้
ขนาดเมื่อพบ : เนื่องจากตำแหน่งที่ซ่อนอยู่ทางกายวิภาค มักมีขนาดค่อนข้างใหญ่เมื่อตรวจพบ
เส้นเลือด Sentinel (sentinel vessel) : มักพบร่วมกับเส้นเลือดเอพิสเกลราที่ขยายและคดเคี้ยวเหนือเนื้องอกโดยตรง เป็นสัญญาณวินิจฉัยที่สำคัญ
การเปลี่ยนแปลงของส่วนหน้าตา : การเคลื่อนไปข้างหน้าของผนังกั้นเลนส์-ม่านตา มีแนวโน้มทำให้เกิดต้อหินมุมปิด ทุติยภูมิ
การลุกลามนอกลูกตา : มีความเสี่ยงต่อการลุกลามนอกลูกตาผ่านทางช่องระบาย (emissary canals)
การเปรียบเทียบกับมะเร็งเมลาโนมาของคอรอยด์
ตำแหน่ง : ซิลิอารีบอดี ้อยู่ด้านหน้าจึงสังเกตได้ยากในการตรวจอวัยวะภายในตา คอรอยด์ สามารถมองเห็นได้จากอวัยวะภายในตา
ลักษณะอาการ : ที่ซิลิอารีบอดี ้ การเคลื่อนของเลนส์ตา สายตาเอียง และต้อหินทุติยภูมิ จะเด่นชัดกว่า ที่คอรอยด์ อาการเห็นแสงวาบ ภาพลอย และข้อบกพร่องของลานสายตาพบบ่อยกว่า
ระดับความยากในการวินิจฉัย : การตรวจส่วนหน้าของตา, UBM และการทดสอบการส่องผ่านแสงเป็นสิ่งจำเป็นสำหรับซิลิอารีบอดี ส่วนคอรอยด์ ประเมินด้วยการถ่ายภาพจอตา และอัลตราซาวนด์
ผลการตรวจทางคลินิกที่สำคัญอื่นๆ ได้แก่: ความผิดปกติของรากม่านตา (การกดหรือการเสียรูปจากเนื้องอก), การเสียรูปของเลนส์แก้วตา เนื่องจากการกด (รูปร่างผิดปกติของส่วนหน้า) เมื่อเนื้องอกโตขึ้น อาจเกิดเลือดออกในวุ้นตา หรือต้อกระจก
มะเร็งผิวหนังชนิดร้ายของซิลิอารีบอดี เกิดจากการเพิ่มจำนวนของเซลล์เมลาโนไซต์ในซิลิอารีบอดี อย่างผิดปกติ นอกจากนี้ยังอาจเกิดการเปลี่ยนแปลงเป็นมะเร็งจากปานยูเวียได้
ปัจจัยเสี่ยงหลักมีดังนี้
สีม่านตา อ่อน, ผิวขาว, ไหม้ง่าย : พบมากในคนผิวขาวและชาวนอร์ดิกปานยูเวีย : ปัจจัยเสี่ยงที่พบบ่อยที่สุดเมลาโนไซโตซิสแต่กำเนิดของตาและเมลาโนไซโตมา : ปัจจัยเสี่ยงที่พบได้ยากประวัติครอบครัวเป็นมะเร็งผิวหนังยูเวีย : พบได้ยากแต่มีรายงาน
ความสัมพันธ์ระหว่างการกลายพันธุ์ของยีนและความเสี่ยงของการแพร่กระจายแสดงดังนี้1)
ยีนที่กลายพันธุ์ ความถี่ของการกลายพันธุ์ ความเสี่ยงของการแพร่กระจาย / ลักษณะ GNAQ/GNA11 83–89% การกลายพันธุ์เริ่มต้นที่แยกกัน ไม่เกี่ยวข้องโดยตรงกับความเสี่ยงของการแพร่กระจาย BAP1 45% ความเสี่ยงสูงสุดในการแพร่กระจาย (จุดสูงสุดใหญ่ที่ 3.5 ปี), ชั้น 2 SF3B1 23% ความเสี่ยงปานกลาง มีลักษณะเฉพาะคือการแพร่กระจายช้า (จุดสูงสุดใหญ่ที่ 7 ปี) EIF1AX 17% ความเสี่ยงต่ำสุดในการแพร่กระจาย
การกลายพันธุ์ของ GNAQ/GNA11 ถือเป็นเหตุการณ์เริ่มต้นในการก่อตัวของเนื้องอก และการกลายพันธุ์เพียงอย่างเดียวไม่มีความสัมพันธ์อย่างมีนัยสำคัญกับขนาดของเนื้องอกหรือความเสี่ยงในการแพร่กระจาย การกลายพันธุ์ไดรเวอร์ทุติยภูมิของ BAP1, SF3B1 และ EIF1AX เกิดขึ้นเกือบจะแยกกันโดยสิ้นเชิง และมีความสำคัญอย่างยิ่งในการแบ่งชั้นความเสี่ยงของการแพร่กระจาย 7)
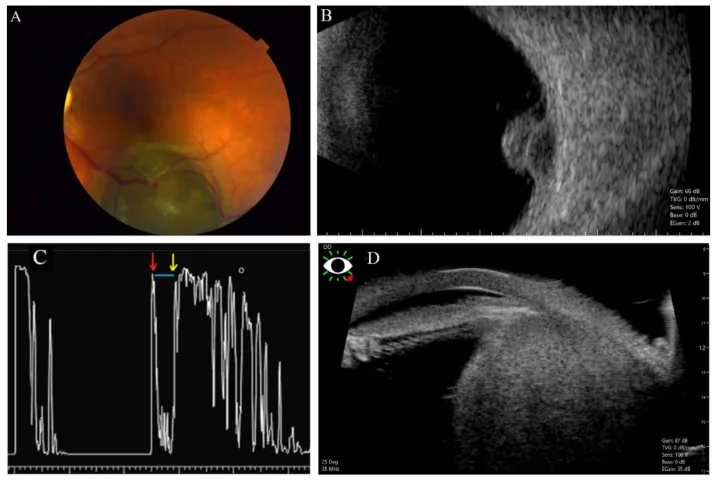
ภาพ UBM ของมะเร็งผิวหนังชนิดเมลาโนมาของซิลิอารีบอดี, อัลตราซาวนด์โหมด A, อัลตราซาวนด์โหมด B, ภาพถ่ายจอตา (4 แผง) Urbańska K, Majewski S. A Review of Current Evidence on Three Key Questions in Uveal Melanoma: What Is the Influence of Heterogeneity, Genetic Testing, and Ocular Oncologists on Patient Survival? Cancers (Basel). 2022;14(13):3147. Figure 3. PM
CI D: PMC9265106. License: CC BY.
(A) ภาพถ่ายจอตาแสดงมะเร็งผิวหนังชนิดเมลาโนมาของคอรอยด์ รูปเห็ด, (B) ภาพอัลตราซาวนด์โหมด B ที่มีโพรงเสียง, (C) รูปคลื่นอัลตราซาวนด์โหมด A แสดงการสะท้อนต่ำของเนื้องอก (ลูกศรสีแดง: ผิวเรตินา, ลูกศรสีเหลือง: ผิวตาขาว , เส้นสีน้ำเงิน: บริเวณสะท้อนต่ำภายในเนื้องอก), (D) ภาพมะเร็งผิวหนังชนิดเมลาโนมาของซิลิอารีบอดี โดยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM ) สอดคล้องกับภาพมะเร็งผิวหนังชนิดเมลาโนมาของซิลิอารีบอดี โดย UBM (กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ) ที่กล่าวถึงในหัวข้อ “4. การวินิจฉัยและวิธีการตรวจ”
ในห้องมืด ใช้แหล่งกำเนิดแสงจากกล้องส่องตรวจส่องจากภายนอกตาขาว และสังเกตผ่านรูม่านตา ว่าแสงส่องผ่านหรือไม่ การตรวจการส่องผ่านแสงนี้เป็นการตรวจพื้นฐานที่สำคัญที่สุดในการกำหนดลักษณะของเนื้องอกซิลิอารีบอดี
มะเร็งเมลาโนมา (ชนิดมีเม็ดสี) : ไม่โปร่งแสง (แสงไม่ผ่าน)เนื้องอกกล้ามเนื้อเรียบ (ชนิดไม่มีเม็ดสี) : โปร่งแสง (แสงผ่าน)
เป็นการตรวจภาพที่สำคัญที่สุดในการประเมินขนาด รูปร่าง และการสะท้อนเสียงภายในของเนื้องอกในซิลิอารีบอดี ใช้อัลตราซาวนด์ความถี่สูงเพื่อแสดงรายละเอียดทางสัณฐานวิทยาของซิลิอารีบอดี มีความโดดเด่นในการประเมินขอบเขตของเนื้องอก การสะท้อนภายใน และการลุกลามไปยังโครงสร้างข้างเคียง (ม่านตา มุมตา เลนส์ตา)
ในเมลาโนมาของซิลิอารีบอดี ลักษณะเด่นคือยอดสูงและการสะท้อนภายในต่ำถึงปานกลาง 3)
แสดงสัญญาณสูงในภาพ T1 และสัญญาณต่ำในภาพ T2 แต่เนื้องอกอื่นๆ ของซิลิอารีบอดี มักให้ผลเหมือนกัน และการเพิ่มความเข้มของสารทึบแสงมักจะน้อย การวินิจฉัยที่แน่นอนด้วย MRI เพียงอย่างเดียวทำได้ยาก ต้องประเมินร่วมกับผลการตรวจอื่นๆ
อัลตราซาวนด์ช่องท้องหรือ CT : ใช้ค้นหาการแพร่กระจายไปยังตับ (อวัยวะที่แพร่กระจายบ่อยที่สุด)CT ทรวงอก : ค้นหาการแพร่กระจายไปยังปอดผู้ป่วยที่มีความเสี่ยงปานกลางถึงสูง : แนะนำให้เฝ้าระวังการแพร่กระจายทุก 6–12 เดือนเป็นเวลา 10 ปี 1)
เนื้องอกในซิลิอารีบอดี มีหลายชนิดตั้งแต่ชนิดไม่ร้ายแรงถึงร้ายแรง การวินิจฉัยแยกโรคที่แม่นยำมีผลต่อแนวทางการรักษา
เนื้องอกกล้ามเนื้อเรียบของซิลิอารีบอดี
การโปร่งแสง : มี (ไม่มีเม็ดสี) การตรวจการโปร่งแสงเป็นเบาะแสสำคัญที่สุดในการวินิจฉัยแยกโรค
รูปร่าง : ครึ่งวงกลมเรียบร้อย ขอบเขตชัดเจน
อายุที่พบบ่อย : วัยกลางคนถึงวัยหนุ่มสาว เกิดได้ทั้งในเพศชายและหญิง
การรักษา : รอยโรคขนาดเล็กสามารถตัดออกทั้งหมดผ่านทางตาขาว รอยโรคขนาดใหญ่หรือมีภาวะแทรกซ้อนรุนแรงต้องตัดลูกตาออก
เมลาโนไซโตมาของซิลิอารีบอดี
การโปร่งแสง : ไม่มี (มีเม็ดสี) แยกจากมะเร็งเมลาโนมาได้ยาก
รูปแบบการเจริญเติบโต : มีลักษณะการเจริญเติบโตช้า การเจริญเติบโตเร็วบ่งชี้ถึงมะเร็งเมลาโนมา
การจัดการ : ติดตามเป็นระยะด้วย UBM หากมีแนวโน้มโตขึ้น ให้พิจารณาตัดออกและตรวจทางพยาธิวิทยา
ถุงน้ำเยื่อบุผิวซิลิอารีบอดี
การโปร่งแสง : มี (เนื่องจากของเหลวในถุงน้ำ)
ลักษณะ : อาจหลุดลอยเข้าไปในวุ้นตา ได้
การวินิจฉัยแยกโรค : ยืนยันลักษณะผนังถุงน้ำและของเหลวภายในด้วย UBM
อะดีโนมาและอะดีโนคาร์ซิโนมาของซิลิอารีบอดี
ต้นกำเนิด : เกิดจากเยื่อบุผิวของซิลิอารีบอดี (เยื่อบุผิวไม่มีเม็ดสีและมีเม็ดสี)
ความถี่ : เป็นเนื้องอกที่พบได้ยาก จำเป็นต้องตรวจทางจุลพยาธิวิทยาเพื่อแยกจากเนื้องอกซิลิอารีบอดี ชนิดอื่น
Q
ฉันถูกบอกว่ามีก้อนที่ซิลิอารีบอดี มันจำเป็นต้องเป็นมะเร็งหรือไม่?
A
เนื้องอกของซิลิอารีบอดี รวมถึงชนิดที่ไม่ร้ายแรงด้วย เนื่องจากเนื้องอกที่ไม่ร้ายแรง เช่น เลโอไมโอมา เมลาโนไซโตมา และซีสต์เยื่อบุผิวสามารถเกิดขึ้นได้ จึงไม่จำเป็นต้องเป็นมะเร็งเมลาโนมาชนิดร้ายเสมอไป การประเมินอย่างละเอียดทำได้โดยการตรวจด้วยแสงส่องผ่าน (transillumination), UBM , MRI และเลือกการสังเกต การผ่าตัด หรือการฉายรังสีตามแนวโน้มการเติบโตและอาการ
การรักษาจะถูกเลือกโดยพิจารณาจากการประเมินขนาดเนื้องอก ตำแหน่ง อาการ และความเป็นไปได้ในการรักษาลูกตาไว้อย่างครอบคลุม
เนื้องอกขนาดเล็ก: การตัดออกทั้งหมดผ่านตาขาว (transscleral total excision)
เมื่อเนื้องอกมีขนาดค่อนข้างเล็กและอยู่ด้านหน้า จะเลือกการตัดออกเฉพาะที่ (การตัดออกทั้งหมดผ่านตาขาว ) ซึ่งเอาตา ขาวบางส่วนและเนื้องอกออกเท่านั้น วิธีนี้สามารถใช้ทั้งการวินิจฉัยที่แน่นอนและการรักษา
เนื้องอกขนาดกลาง (รวมถึงกรณีที่สงสัย): การฉายรังสี
การฉายรังสีเป็นทางเลือกหลักในการรักษาลูกตาไว้
การรักษาด้วยลำอนุภาคคาร์บอนหนัก (HIMAC ฯลฯ) : การรักษาด้วยอนุภาคที่รวมปริมาณรังสีไปที่เนื้องอกโดยใช้ปรากฏการณ์ Bragg peak ข้อบ่งชี้กำลังขยายตัวเมื่อเร็วๆ นี้CyberKnife : หนึ่งในทางเลือกของการฉายรังสีแบบ Stereotacticการฝังแร่ (Ru-106) : การเย็บแผ่นรูทีเนียม-106 บนตาขาว การรักษาด้วยโปรตอน : การรักษาที่รักษาลูกตาไว้โดยให้ปริมาณรังสีต่ำต่อเนื้อเยื่อปกติรอบข้าง
แม้ในกรณีที่สงสัย อาจพิจารณาการฉายรังสีเช่นลำอนุภาคคาร์บอนหนัก
เนื้องอกขนาดใหญ่: การตัดลูกตาออก (enucleation)
สำหรับเนื้องอกขนาดใหญ่ที่ยากต่อการรักษาลูกตาไว้ การตัดลูกตาออกเป็นทางเลือกที่เลือกใช้ การวินิจฉัยที่แน่นอนได้จากการตรวจชิ้นเนื้อที่ตัดออก
การตัดชิ้นเนื้อตามสถานการณ์
อาจพิจารณาการตัดชิ้นเนื้อผ่านตาขาว ผ่านกระจกตา หรือผ่านรูม่านตา เนื่องจากความไม่เป็นเนื้อเดียวกันภายในเนื้องอก แนะนำให้เก็บตัวอย่างจากบริเวณที่มีลักษณะทางสัณฐานวิทยาต่างกัน 7)
Tebentafusp สำหรับมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุลูกตาที่แพร่กระจาย มีข้อบ่งชี้ในผู้ป่วยที่ตรวจพบ HLA-A*02:01 เป็นบวก 5) เป็นยาตัวแรกที่ช่วยเพิ่มอัตราการรอดชีวิตโดยรวมอย่างมีนัยสำคัญในการทดลองระยะที่ 3 สำหรับมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุลูกตาที่แพร่กระจาย
ตามแนวทางของสหราชอาณาจักรสำหรับมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุลูกตาฉบับปรับปรุงปี 2023 แนะนำให้เฝ้าระวังดังนี้ 1) :
โปรแกรมพื้นฐาน : ทุก 6 เดือนเป็นเวลา 5 ปี จากนั้นปีละครั้งเป็นเวลา 10 ปีผู้ที่มีการกลายพันธุ์ SF3B1 : พิจารณาขยายการเฝ้าระวังถึง 15 ปีหลังการตัดลูกตาก็เช่นกัน : ให้เฝ้าระวังการแพร่กระจายต่อไปแม้หลังการรักษาเฉพาะที่สิ้นสุดลง
การพยากรณ์โรคมีแนวโน้มแย่ คล้ายกับมะเร็งผิวหนังชนิดเมลาโนมาที่คอรอยด์ การแพร่กระจายไปยังตับเป็นตัวกำหนดการพยากรณ์โรค และการแพร่กระจายอาจปรากฏชัดหลังจากหลายปีถึงมากกว่า 10 ปีหลังการตัดลูกตา
หลังการผ่าตัดตัดลูกตาหรือการฉายรังสี การตรวจหาการแพร่กระจายทั่วร่างกายเป็นประจำยังคงมีความสำคัญในระยะยาว แม้ไม่มีอาการใดๆ โปรดไปตรวจตามระยะเวลาที่แพทย์กำหนดอย่างต่อเนื่อง ในผู้ป่วยที่มีการกลายพันธุ์ SF3B1 แนะนำให้เฝ้าระวังระยะยาวเป็นพิเศษ
แม้จะตัดลูกตาออกไปแล้ว การแพร่กระจายขนาดเล็กที่กระจายผ่านกระแสเลือดอาจปรากฏชัดในภายหลัง การแพร่กระจายมากกว่า 62% ปรากฏชัดภายใน 5 ปีหลังการรักษาเนื้องอกปฐมภูมิ แต่ส่วนที่เหลืออาจตรวจพบหลังจากมากกว่า 25 ปี สิ่งสำคัญคือต้องตรวจร่างกายทั่วร่างกายเป็นประจำ (เช่น อัลตราซาวนด์ช่องท้อง, CT) ต่อไปแม้หลังการรักษาสิ้นสุดลง
Q
มีการรักษาที่สามารถรักษาลูกตาไว้ได้หรือไม่?
A
สำหรับเนื้องอกขนาดเล็กถึงปานกลาง สามารถเลือกการรักษาที่สงวนลูกตาได้ เช่น การตัดเนื้องอกทั้งหมดผ่านตาขาว การรักษาด้วยลำอนุภาคคาร์บอนหนัก การฝังแร่ (Ru-106) และการรักษาด้วยโปรตอน สำหรับเนื้องอกขนาดใหญ่ อาจจำเป็นต้องตัดลูกตาออก แต่มีการแสดงให้เห็นว่าการเลือกการรักษาเฉพาะที่ไม่มีผลต่ออัตราการแพร่กระจายหรือการรอดชีวิตโดยรวม ดังนั้นจึงพิจารณาความเป็นไปได้ในการสงวนลูกตาในศูนย์ผู้เชี่ยวชาญ โดยให้ความสำคัญกับพยากรณ์ชีวิตเป็นอันดับแรก
กลไกการเกิดมะเร็งผิวหนังชนิดเมลาโนมาที่คอรอยด์ แตกต่างจากมะเร็งผิวหนังชนิดเมลาโนมาที่ผิวหนังผ่านวิถีทางโมเลกุลที่เป็นเอกลักษณ์
การกลายพันธุ์ที่พบบ่อยที่สุดคือการกลายพันธุ์ที่ตำแหน่ง Q209 ของ GNAQ/GNA11 การกลายพันธุ์เหล่านี้ทำให้การทำงานของ GTPase บกพร่อง ส่งผลให้เกิดสถานะการกระตุ้นการจับกับ GTP อย่างต่อเนื่อง การกลายพันธุ์ของ GNAQ/GNA11 ทำให้เกิดการกระตุ้นวิถีสัญญาณหลายอย่างอย่างต่อเนื่อง รวมถึงวิถี MAPK (Ras/RAF/MEK/ERK)6)
การกลายพันธุ์ไดรเวอร์ทุติยภูมิ (BAP1, SF3B1, EIF1AX) เกิดขึ้นเกือบจะแยกกันโดยสิ้นเชิง และมีความสำคัญอย่างยิ่งในการแบ่งชั้นความเสี่ยงของการแพร่กระจาย7)
เนื่องจากซิลิอารีบอดี อยู่ด้านหน้าของคอรอยด์ จึงมีแนวโน้มที่จะบุกรุกเข้าไปในม่านตา และมุมตา ซึ่งเป็นสาเหตุหนึ่งของโรคต้อหินมุมปิด ทุติยภูมิ นอกจากนี้ การขยายตัวของเนื้องอกไปทางด้านหน้าอาจทำให้เลนส์เคลื่อนและเกิดต้อกระจก
การขยายออกนอกลูกตาเกิดขึ้นผ่านทางช่องระบาย (emissary canal) นำไปสู่การขยายเข้าสู่เบ้าตา และทั่วร่างกาย
เนื่องจากไม่มีท่อน้ำเหลืองในยูเวีย การแพร่กระจายทั้งหมดจึงเกิดขึ้นทางเลือด2) ความชอบต่อตับอย่างรุนแรงอธิบายได้ด้วยทฤษฎี seed and soil ในตำแหน่งที่แพร่กระจาย พบ GNAQ (57%) และ GNA11 (36%) แบบแยกกัน
ความเข้มข้นของ VEGF ภายในเนื้องอกสูงกว่าตาปกติอย่างมีนัยสำคัญ มีรายงานกรณีของมะเร็งเมลาโนมาของซิลิอารีบอดี ที่เติบโตอย่างรวดเร็วหลังการฉีดเบวาซิซูแมบ เข้าในวุ้นตา (เส้นผ่านศูนย์กลางฐานจาก 2.51 เป็น 18.0 มม. ความสูงจาก 6.23 เป็น 11.0 มม. ใน 7 สัปดาห์)4) ดังนั้นการฉีดยาต้าน VEGF เข้าในวุ้นตา อาจเป็นข้อห้าม
ความหลากหลายภายในเนื้องอกมีทั้งในด้านสัณฐานวิทยาและพันธุกรรม ส่งผลต่อความแม่นยำของการพยากรณ์โรคจากการตัดชิ้นเนื้อ 7) การขาดโครโมโซมคู่ที่ 3 พบได้ทั่วไปในทุกตำแหน่ง ในขณะที่การขาดหายของ 6q บางครั้งจำกัดเฉพาะบริเวณที่มีเม็ดสีเท่านั้น
Tebentafusp เป็นโปรตีนฟิวชันแบบสองความจำเพาะของรีเซพเตอร์ทีเซลล์ที่ออกแบบมาสำหรับผู้ป่วยที่ตรวจพบ HLA-A02:01 5) มันจดจำแอนติเจนที่เกี่ยวข้องกับเนื้องอก gp100 บนคอมเพล็กซ์ HLA-A 02:01 และกระตุ้นทีเซลล์ให้เกิดฤทธิ์ต้านเนื้องอก เป็นยาตัวแรกที่ช่วยเพิ่มอัตราการรอดชีวิตโดยรวมในมะเร็งเมลาโนมาคอรอยด์ ระยะแพร่กระจายอย่างมีนัยสำคัญในการทดลองระยะที่ 3 และกำลังรวบรวมข้อมูลการรอดชีวิต 3 ปี 11)
ในรายงานผู้ป่วยของ Krohn และคณะ (2025) บันทึกผลลัพธ์ที่ดีหลังการให้ tebentafusp (ฉีดเข้าหลอดเลือดดำทุกสัปดาห์ เพิ่มขนาด: 20→30→68 มก.) เป็นเวลา 26 เดือน โดยมีการแพร่กระจายที่ตับคงที่และไม่มีรอยโรคใหม่ 8) พบว่าความหนาคอรอยด์ ส่วนกลางของตาขวาลดลงจาก 241 ไมครอนเหลือ 123 ไมครอน (49%) จอประสาทตา สีจางลง ขนคิ้วและขนตากลายเป็นสีขาว และมีจุดด่างดำบนผิวหนัง
gp100 ยังแสดงออกบนเมลาโนไซต์คอรอยด์ ปกติ ซึ่งอาจเกี่ยวข้องกับกลไกการทำให้คอรอยด์ บางลง 8) ในระหว่างการให้ยา จำเป็นต้องมีการตรวจติดตามทางจักษุวิทยาเป็นประจำ
การรวมกันของยายับยั้ง Gαq (YM-254890) และยายับยั้ง MEK (trametinib/binimetinib) แสดงฤทธิ์ต้านเนื้องอกแบบเสริมฤทธิ์กันทั้งในหลอดทดลองและในสิ่งมีชีวิต 6) แม้ว่าสัญญาณ MAPK จะฟื้นตัวภายใน 24 ชั่วโมงเมื่อยับยั้ง Gαq เพียงอย่างเดียว แต่การรวมกับยายับยั้ง MEK จะยับยั้งการฟื้นตัวของสัญญาณ MAPK 6)
การทดลองระยะที่ 2 ของ selumetinib แสดงให้เห็นการปรับปรุง PFS แต่การทดลองระยะที่ 3 ของ selumetinib ร่วมกับ dacarbazine (การทดลอง SUMIT) ไม่พบการปรับปรุง PFS 6)
ในมะเร็งเมลาโนมาคอรอยด์ ฤทธิ์ของยายับยั้งจุดตรวจภูมิคุ้มกันมีจำกัดเมื่อเทียบกับมะเร็งเมลาโนมาที่ผิวหนัง เชื่อว่าสาเหตุเกี่ยวข้องกับดวงตาเป็นอวัยวะที่มีภูมิคุ้มกันพิเศษและสภาพแวดล้อมจุลภาคที่กดภูมิคุ้มกัน
วิธีการเฉพาะที่สำหรับรอยโรคระยะแพร่กระจายที่กำลังศึกษาอยู่ ได้แก่ การตัดตับ การจี้ด้วยคลื่นวิทยุ การอุดหลอดเลือดแดงตับ การให้ยา melphalan ผ่านการไหลเวียนตับทางผิวหนัง (PHP) และการฝังแร่ไมโครสเฟียร์อิตเทรียม-90 (SIRT)
มีการแสดงให้เห็นว่าลายเซ็นของยีนที่เกี่ยวข้องกับ autophagy 9 ยีน (9-ARG) มีประโยชน์ในการทำนายพยากรณ์โรคของมะเร็งเมลาโนมาที่คอรอยด์ และเลนส์ปรับตา (ตรวจสอบในผู้ป่วย TCGA 80 ราย + GEO 150 ราย)9) ในกลุ่มที่มีความเสี่ยงสูง เส้นทาง IL6-JAK-STAT3 การสร้างเส้นเลือดใหม่ และชนิดของออกซิเจนที่ว่องไวจะถูกเพิ่มปริมาณ ซึ่งสัมพันธ์กับฟีโนไทป์ที่กดภูมิคุ้มกันและการพยากรณ์โรคที่ไม่ดี9)
Kujala และคณะ (2013) รายงานการแบ่งระยะตามการลุกลามทางกายวิภาคของมะเร็งเมลาโนมาที่ซิลิอารีบอดี และคอรอยด์ โดยใช้การจำแนก T ของ CI OM ซึ่งเป็นพื้นฐานในการแบ่งชั้นความสัมพันธ์ระหว่างตำแหน่งของเนื้องอกและการพยากรณ์โรค10)
Carter TJ, Rivero Rodriguez S, Fernandez-Trigo N, et al. Uveal melanoma UK national guidelines: 2023 update. Eye (Lond). 2023.
Rantala ES, Hernberg M, Kivelä TT. Metastatic uveal melanoma: The final frontier. Prog Retin Eye Res. 2022;90:101041.
Tigari B, Saini M, Manchanda S, et al. Large ciliary body melanoma. BMJ Case Rep. 2021;14:e246386.
Ma J, Roelofs KA, Russell L, et al. Rapid growth of primary uveal melanoma following intravitreal bevacizumab injection: a case report and review of the literature. Digit J Ophthalmol. 2020;26:28-31.
Nathan P, Hassel JC, Rutkowski P, et al. Overall Survival Benefit with Tebentafusp in Metastatic Uveal Melanoma. N Engl J Med. 2021;385(13):1196-1206.
Sriramareddy SN, Smalley KSM. MEK-ing the most of it: strategies to co-target Gαq and MAPK in uveal melanoma. Clin Cancer Res. 2021;27(5):1217-1219.
Fonseca C, Pinto-Proença R, Bergeron S, et al. Intratumoral heterogeneity in uveal melanoma. Ocul Oncol Pathol. 2021;7:17-25.
Krohn J, Vinnem LIH, Jansson RW, et al. Fundus hypopigmentation and choroidal thinning associated with tebentafusp therapy: report of a case and literature review. BMC Ophthalmol. 2025;25:464.
Chuah S, Chew V. Immune implication of an autophagy-related prognostic signature in uveal melanoma. Biosci Rep. 2021;41:BSR20211098.
Kujala E, Damato B, Coupland SE, et al. Staging of ciliary body and choroidal melanomas based on anatomic extent. J Clin Oncol. 2013;31(22):2825-2831.
Hassel JC, Piperno-Neumann S, Rutkowski P, et al. Three-Year Overall Survival with Tebentafusp in Metastatic Uveal Melanoma. NEJM Evid. 2023;2(8).