睫状体黑色素瘤
发现时大小:由于解剖位置隐蔽,发现时通常较大。
哨兵血管:肿瘤正上方常伴有扩张、迂曲的巩膜表面血管。这是重要的诊断线索。
眼前段变化:易出现晶状体-虹膜隔前移、继发性闭角型青光眼。
眼外扩展:存在经导血管向眼外扩展的风险。

睫状体恶性黑色素瘤是起源于睫状体黑色素细胞的恶性肿瘤。在来源于葡萄膜(虹膜、睫状体、脉络膜)黑色素细胞的葡萄膜黑色素瘤中,睫状体起源约占7% 2)。
发现睫状体肿瘤时,应首先考虑恶性黑色素瘤的可能性。睫状体恶性黑色素瘤经瞳孔观察为黑褐色的睫状体隆起,但由于肿瘤起源于睫状体实质,直视下观察到的是色素上皮的颜色。因此,肿瘤是否为色素性需通过透照检查判断。
日本葡萄膜黑色素瘤的总发病率约为欧美的1/20,为每10万人0.025例。脉络膜起源最多,睫状体较少。好发于中老年人,男性略多。
转移方式均为血行性(葡萄膜无淋巴管),对肝脏有强趋向性。转移后中位总生存期以往不足6个月,但随着tebentafusp的出现正在改善。
睫状体在眼底检查中难以看到,常在散瞳后前眼部观察(房角镜、裂隙灯)或因视力下降、哨兵血管、继发性青光眼等症状和体征而被发现。健康体检中难以发现,因此出现症状时及时眼科就诊很重要。
睫状体黑色素瘤的主观症状因其解剖位置的特殊性而表现出以下特征3)。
散瞳后眼前段检查可见睫状体区域有黑褐色隆起性病变。以下所见为诊断线索。
睫状体黑色素瘤
发现时大小:由于解剖位置隐蔽,发现时通常较大。
哨兵血管:肿瘤正上方常伴有扩张、迂曲的巩膜表面血管。这是重要的诊断线索。
眼前段变化:易出现晶状体-虹膜隔前移、继发性闭角型青光眼。
眼外扩展:存在经导血管向眼外扩展的风险。
与脉络膜黑色素瘤的比较
其他重要的临床发现包括虹膜根部异常(肿瘤压迫或变形)、晶状体受压变形(前节异常形态)。肿瘤增大时可能并发玻璃体出血或白内障。
睫状体恶性黑色素瘤由睫状体黑色素细胞肿瘤性增殖引起。也可能由葡萄膜痣恶变而来。
主要风险因素如下所示。
基因突变与转移风险的对应关系如下所示1)。
| 突变基因 | 突变频率 | 转移风险/特征 |
|---|---|---|
| GNAQ/GNA11 | 83~89% | 互斥的起始突变。与转移风险无直接关联。 |
| BAP1 | 45% | 转移风险最高(高峰3.5年),2级 |
| SF3B1 | 23% | 中度风险。特点为晚期转移(高峰7年) |
| EIF1AX | 17% | 转移风险最低 |
GNAQ/GNA11突变被认为是肿瘤形成的早期事件,单独突变与肿瘤大小或转移风险无显著关联。BAP1、SF3B1和EIF1AX的二次驱动突变几乎完全互斥发生,对转移风险分层具有重要意义7)。
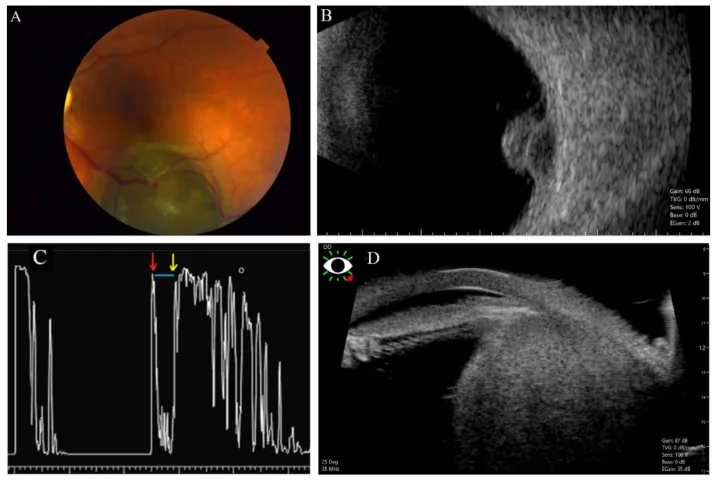
在暗室中,将内窥镜光源从巩膜外照射,通过瞳孔观察光线是否透射。该透照检查是判断睫状体肿瘤性质最重要的基本检查。
这是评估睫状体肿瘤大小、形状和内部回声最重要的影像学检查。高频超声可以显示睫状体的详细形态。它在评估肿瘤边界、内部反射以及向邻近结构(虹膜、房角、晶状体)的浸润方面表现出色。
睫状体黑色素瘤的特征是高波峰和低-中内部反射 3)。
T1加权像呈高信号,T2加权像呈低信号,但其他睫状体肿瘤也常出现相同表现,且增强扫描往往微弱。单独依靠MRI难以确诊,需结合其他发现进行评估。
睫状体肿瘤包括从良性到恶性的多种病变,准确鉴别决定治疗方案。
睫状体平滑肌瘤
透光性:有(非色素性)。透光性检查是鉴别诊断的最大线索。
形态:规则的半球形,边界清晰。
好发年龄:中青年。男女均可发生。
治疗:小型肿瘤可经巩膜全切除。大型或并发症严重者需摘除眼球。
睫状体黑色素细胞瘤
透光性:无(色素性)。与恶性黑色素瘤鉴别困难。
生长方式:特征为缓慢增大。快速增大提示恶性黑色素瘤。
处理:定期进行UBM监测,如有增大趋势,考虑切除和病理检查。
睫状体上皮囊肿
透光性:有(因囊液)。
特征:有时可游离于玻璃体中。
鉴别:通过UBM确认囊壁和囊液的性质。
睫状体腺瘤/腺癌
来源:起源于睫状体上皮(无色素上皮或色素上皮)。
频率:罕见肿瘤,需病理组织检查以与其他睫状体肿瘤鉴别。
睫状体肿瘤也包括良性肿瘤。平滑肌瘤、黑色素细胞瘤、上皮囊肿等良性肿瘤也会发生,因此不一定是恶性黑色素瘤。通过透照检查、UBM、MRI等进行详细评估,根据生长趋势和症状选择观察、手术或放射治疗。
治疗根据肿瘤的大小、位置、症状以及保留眼球的可能性的综合判断来选择。
小型肿瘤:经巩膜肿瘤全切除术
当肿瘤相对较小且位于前方时,可选择局部切除(经巩膜肿瘤全切除术),仅切除部分巩膜和肿瘤。该方法可同时进行确诊和治疗。
中型肿瘤(包括疑似病例):放射治疗
放射治疗是保留眼球的主要选择。
即使是疑似病例,也可能考虑重粒子线等放射治疗。
大型肿瘤:眼球摘除术
对于难以保留眼球的大型肿瘤,选择眼球摘除术。通过摘除标本可得到确诊。
根据情况进行活检
也可考虑经巩膜、经角膜或经瞳孔的活检。考虑到肿瘤内异质性,建议从形态不同的区域取样7)。
替本塔司普(tebentafusp)用于转移性葡萄膜黑色素瘤,适用于HLA-A*02:01阳性患者5)。在III期试验中,它是首个显著改善转移性葡萄膜黑色素瘤总生存期的药物。
根据2023年更新的英国葡萄膜黑色素瘤指南,建议进行以下监测1)。
预后与脉络膜黑色素瘤相似,有不良倾向。肝转移决定预后,眼球摘除术后数年至10年以上才可能发现转移。
对于小到中型肿瘤,可以选择经巩膜肿瘤切除术、重粒子线治疗、近距离放射治疗(Ru-106)、质子线治疗等保留眼球的疗法。对于大型肿瘤,有时需要摘除眼球,但已有研究表明局部治疗的选择不影响转移率和总生存率。在优先考虑生命预后的同时,应在专业机构讨论保留的可能性。
葡萄膜黑色素瘤的发病机制与皮肤黑色素瘤不同,具有独特的分子通路。
GNAQ/GNA11的Q209位突变最为常见。这些突变损害GTP酶活性,导致持续的GTP结合激活状态。GNAQ/GNA11突变导致包括MAPK通路(Ras/RAF/MEK/ERK)在内的多个信号通路持续激活6)。
二次驱动突变(BAP1、SF3B1、EIF1AX)几乎完全互斥发生,对转移风险分层具有重要意义7)。
由于睫状体位于脉络膜前方,容易向虹膜和前房角浸润。这导致继发性闭角型青光眼。此外,肿瘤向前扩展可引起晶状体移位和白内障。
眼外扩展通过导血管发生,导致眼眶和全身扩散。
由于葡萄膜没有淋巴管,所有转移均为血行性2)。对肝脏的强烈趋向性可用种子和土壤理论解释。在转移灶中,GNAQ(57%)和GNA11(36%)互斥检测到。
肿瘤内VEGF浓度显著高于健康眼。有报道称玻璃体内注射贝伐珠单抗后睫状体黑色素瘤快速增大(基底直径2.51→18.0 mm,高度6.23→11.0 mm,7周内)4),因此玻璃体内注射抗VEGF药物可能是禁忌。
肿瘤内异质性在形态学和遗传学两方面都存在,影响活检的预后预测准确性7)。3号染色体单体在肿瘤部位间普遍存在,而6q缺失在某些病例中可能仅限于色素区域。
替贝他司普是一种为HLA-A02:01阳性患者设计的T细胞受体双特异性融合蛋白5)。它识别HLA-A02:01复合物上的肿瘤相关抗原gp100,激活T细胞发挥抗肿瘤作用。它是首个在III期试验中显著改善转移性葡萄膜黑色素瘤总生存期的药物,3年总生存率数据正在积累中11)。
在Krohn等人(2025)的病例报告中,替贝他司普(每周静脉注射:20→30→68 mg递增)治疗26个月后,记录到肝转移稳定且无新病灶的良好病程8)。右眼中心脉络膜厚度从241 μm减少49%至123 μm,并观察到眼底脱色素、眉毛和睫毛的灰发症以及皮肤脱色素斑。
gp100也在正常脉络膜黑色素细胞上表达,被认为与脉络膜变薄的机制有关8)。治疗期间需要定期进行眼科监测。
Gαq抑制剂(YM-254890)与MEK抑制剂(曲美替尼/比美替尼)的联合在体外和体内显示出协同抗肿瘤作用6)。单独抑制Gαq时,MAPK信号在24小时内恢复,但与MEK抑制剂联合可抑制MAPK信号的恢复6)。
司美替尼的II期试验显示PFS改善,但司美替尼联合达卡巴嗪的III期试验(SUMIT试验)未观察到PFS改善6)。
在葡萄膜黑色素瘤中,免疫检查点抑制剂的疗效与皮肤黑色素瘤相比有限。这被认为与眼睛是免疫豁免器官以及免疫抑制微环境有关。
针对转移性病变的局部方法正在研究中,包括肝切除术、射频消融术、肝动脉栓塞术、美法仑经皮肝灌注化疗(PHP)以及钇-90微球近距离放疗(SIRT)。
自噬相关9基因特征(9-ARG)已被证明对预测葡萄膜黑色素瘤的预后有用(在80例TCGA和150例GEO中验证)9)。在高风险组中,IL6-JAK-STAT3通路、血管生成和活性氧通路富集,免疫抑制表型与不良预后相关9)。
Kujala等人(2013)报告了使用CIOM T分类基于睫状体和脉络膜黑色素瘤解剖进展的分期,为分层肿瘤位置与预后的关系提供了依据10)。