脉络膜黑色素瘤
典型外观:单眼出现、边界不规则、隆起的圆顶状灰褐色脉络膜肿块。
色素:55%为重度色素性,30%为混合性,15%为无色素性,色调多样。
蘑菇状形态:约20%突破Bruch膜,呈蘑菇(纽扣)状。Bruch膜穿破后迅速增大。
视网膜下液:常伴有浆液性视网膜脱离。

葡萄膜黑色素瘤(uveal melanoma, UM)是起源于葡萄膜(虹膜、睫状体、脉络膜)黑色素细胞的恶性肿瘤。它是成人最常见的原发性眼内肿瘤,其中脉络膜来源占90%以上,睫状体来源约占7%,虹膜来源占2%。本文主要讨论脉络膜和睫状体黑色素瘤。
发病率约为欧美的1/20,每10万人中0.025人。在白人中,发病率为每百万人2-8例,男性略多,发病高峰约在60岁。所有葡萄膜黑色素瘤中不到1%发生在18岁以下。全球范围内,每年约有600万人被诊断为眼黑色素瘤6)。
所有转移均为血行性(因为葡萄膜没有淋巴管),对肝脏有强烈趋向性。肝转移占70-90%,其他部位包括肺、骨和皮肤6)。超过62%的转移在原发肿瘤治疗后5年内临床显现,但其余可能在25年后才被检测到。由于转移可能在治疗后数年甚至10年以上才变得明显,因此需要长期监测转移。
转移后的中位总生存期(OS)根据荟萃分析(2494名患者,78篇论文)为10-13个月,约2%存活超过5年,13%估计存活超过3年13)。1年生存率报告为43-52%。12年死亡率约为40%,无论选择何种局部治疗,该比例基本相同2)。中型肿瘤的5年生存率为70-80%(眼球保留治疗与眼球摘除无差异),表明治疗选择对生命预后没有显著影响。
对于中高风险患者,建议每6至12个月进行一次肝脏影像学检查,持续10年14)。
在欧美,白种人的发病率为每百万人2至8人,是成人中最常见的原发性眼内肿瘤,但绝对数量较少。日本的发病率约为欧美的1/20,估计为每10万人0.025人。白种人更常见,亚洲人发病率更低。
初诊时约30%的患者无症状,在健康体检或其他疾病检查中偶然发现。出现症状时,其构成为:视力下降38%、闪光感9%、飞蚊症7%、周边视野缺损6%、眼痛2%。
当肿瘤较小且位于眼底周边部时,通常无症状。随着肿瘤增大,出现以下症状。
睫状体黑色素瘤的症状因其解剖位置的特殊性而具有以下特征5)。
继发性眼压升高在睫状体黑色素瘤诊断时最多见于17%的患者3)。
脉络膜黑色素瘤
典型外观:单眼出现、边界不规则、隆起的圆顶状灰褐色脉络膜肿块。
色素:55%为重度色素性,30%为混合性,15%为无色素性,色调多样。
蘑菇状形态:约20%突破Bruch膜,呈蘑菇(纽扣)状。Bruch膜穿破后迅速增大。
视网膜下液:常伴有浆液性视网膜脱离。
睫状体黑色素瘤
发现时大小:由于解剖位置隐蔽,发现时通常较大。
哨兵血管:常伴有肿瘤正上方扩张、迂曲的巩膜表面血管。
眼前段改变:易出现晶状体-虹膜隔前移和继发性闭角型青光眼。
眼外扩展:存在经导血管(emissary canal)的眼外扩展风险。
脉络膜痣与黑色素瘤的鉴别需评估以下8个项目。
如果风险因子为0个,5年内生长概率仅为3%,但1个时升至38%,2个以上时超过50%。
根据COMS方案的大小分类如下所示。用于选择治疗策略。
| 分类 | 顶点高度 | 最大基底直径 |
|---|---|---|
| 小 | 1.0~2.5 mm | 5.0~16.0 mm |
| 中 | 2.5~10 mm | <16 mm |
| 大 | >10 mm | >16 mm |
以下列出发生于脉络膜的主要肿瘤的鉴别要点。
| 恶性黑色素瘤 | 血管瘤 | 转移性肿瘤 | |
|---|---|---|---|
| 色调 | 黑、灰、褐色 | 橙红色 | 黄白色 |
| 形状 | 穹顶形 | 梭形 | 板状 |
| 视网膜脱离 | 无至中度 | 无至轻度 | 显著 |
| 生长 | 相对缓慢 | 无 | 快速 |
通过TFSOM-UHHD的8个风险因素进行评估。0个因素时,5年内生长概率仅为3%,但2个或以上时则升至50%以上。需要定期进行超声和眼底照相随访。
发病主要是散发性的。原因不明,但推测与抑癌基因和癌基因的异常以及日光照射等有关。主要风险因素如下所示。
基因突变与转移风险的对应关系如下所示。
| 突变基因 | 突变频率 | 转移风险/特征 |
|---|---|---|
| GNAQ/GNA11 | 83–89% | 互斥的起始突变。与转移风险无直接关联。 |
| BAP1 | 45% | 最高转移风险(高峰3.5年),2类 |
| SF3B1 | 23% | 中等风险。特点是晚期转移(高峰在7年)。 |
| EIF1AX | 17% | 最低转移风险。 |
GNAQ/GNA11突变被认为是肿瘤形成的早期事件,这些突变本身与肿瘤大小或转移风险无显著关联。存在瘤内异质性,不同形态区域可能具有不同的基因谱(例如,3号染色体单体在各区域常见,而6q缺失可能仅限于色素区域)2)。
BAP1突变与最高转移风险相关1),而EIF1AX突变与最低风险相关1)。
组织学上分为梭形细胞型和上皮样细胞型。上皮样细胞比例越高的病例预后越差。也存在混合型。
BAP1突变转移风险最高(高峰在3.5年),SF3B1突变以晚期转移为特点(高峰在7年),EIF1AX突变风险最低。此外,检测到3号染色体缺失(3号单体)时转移率高,预后不良。这些突变信息通过细针穿刺活检获得,用于个体化转移监测计划。
连续眼底照相对于记录肿瘤生长极为重要,广角眼底成像(如Optos)的应用也很有用。在眼底自发荧光中,利用脂褐质的自发荧光特性,可识别比玻璃膜疣更亮的橙色荧光(橙色色素)。
超声检查是葡萄膜黑色素瘤诊断的核心。恶性黑色素瘤显示特征性衰减。
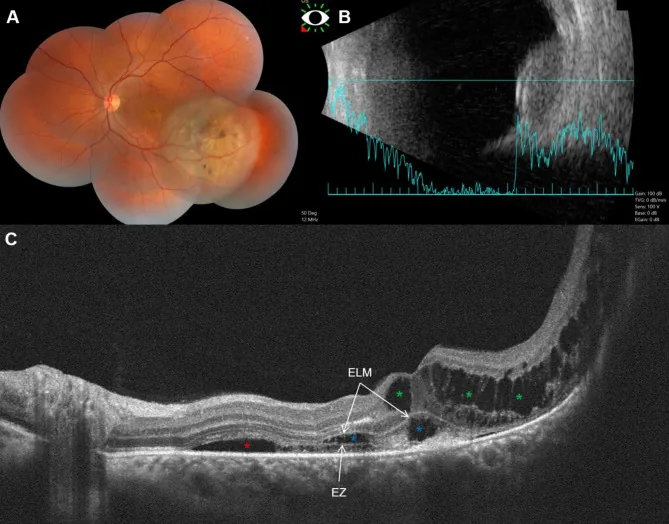
SD-OCT可显示神经感觉视网膜和RPE变化。EDI-OCT的特征性表现(基于37只眼的研究)如下。
T1加权像呈高信号,T2加权像呈低信号。也用于I-125敷贴照射后的肿瘤大小监测7)。
使用123I-IMP(碘苯丙胺)作为示踪剂的SPECT检查,在静脉注射24小时后,患眼出现一致的异常聚集影像,是一种灵敏度和特异度均优的检查方法。FDG-PET也可用于诊断。
中高风险患者建议每6~12个月进行一次转移监测,持续10年14)。
对肿瘤组织或针吸活检获得的细胞进行分子检测,对于转移风险分层至关重要。
在临床诊断不确定的病例中进行。通常与敷贴器近距离放射治疗植入同时进行。由于存在肿瘤播散风险,存在争议,但为了通过获取基因图谱进行预后分层,实施越来越多。考虑到肿瘤异质性,建议从形态学不同的多个区域取样2)。
S-100、HMB-45、MART-1(MelanA)和波形蛋白呈阳性。为确认,建议至少使用两种黑色素细胞抗体与细胞角蛋白(上皮标志物)联合使用。还进行Ki-67增殖指数的半定量评估。在睫状体黑色素瘤中,已确认HMB-45强阳性5)。BAP1核染色在预后分类中起重要的辅助作用2)。
治疗的目标是:①维持患眼的有用视力,②破坏肿瘤,③防止转移和复发。
当与脉络膜痣难以鉴别时,应通过眼底照相和B超进行严密随访。对于脉络膜痣(厚度<2mm,无症状),初次检查后3个月复查,之后每6个月观察一次。对于厚度<3mm的病变,初期进行眼底照相、荧光血管造影和A/B超检查,3-4个月后复查,之后每6-12个月进行一次眼底照相,终身持续。具有3个或以上危险因素的小肿瘤应立即治疗,无需等待生长记录。
近距离放射治疗
钌-106敷贴器巩膜缝置术:将含有钌-106(β射线源)的敷贴器缝合在肿瘤部位的巩膜上。由于β射线组织穿透距离短,适用于小至中型肿瘤。可实施的机构有限。
碘-125敷贴器:将含有碘-125的COMS敷贴器缝合在肿瘤部位的巩膜上。肿瘤顶点的处方剂量为90 Gy。主要用于北美。
适应证:小至中等大小肿瘤的一线治疗。
副作用:放射性黄斑病变/视网膜病变、白内障、新生血管性青光眼、视神经病变、巩膜坏死。大多数发生在治疗后5年内。
复发:80%的局部复发发生在3年内。98%可通过彩色眼底照相检测。
视力预后:COMS 3年数据显示,43-49%的患者视力降至20/200(相当于0.1)或更差。放射性视网膜病变是主要原因10)。
质子束治疗
特点:利用布拉格峰效应将辐射剂量集中到肿瘤的粒子治疗。保留眼球的治疗。
适应证:小至中等大小肿瘤的保留眼球选择。
治疗效果:有报道称质子束治疗后6个月肿瘤完全消退的病例。
优点:对周围正常组织的辐射剂量低。
重粒子线和射波刀等外照射放疗的适应证正在扩大。虽然可以保留眼球,但常因视神经病变、新生血管性青光眼等并发症导致视功能丧失。虽然可实施的机构有限,但已被定位为治疗选择之一。
经瞳孔温热疗法(TTT)适用于小型脉络膜黑色素瘤(厚度≤3mm)。主要参数如下所示9)。
| 参数 | 设定值 |
|---|---|
| 波长 | 810 nm(近红外) |
| 输出功率 | 400~1,000 mW |
| 光斑直径 | 3,000 μm |
| 照射时间 | 每个光斑1~3分钟 |
| 深度 | 3~4 mm |
经瞳孔温热疗法与近距离放射疗法(巩膜板)联合的“三明治疗法”中,5年复发率据报道使用碘-125为3%,使用钌-106为10% 9)。
当肿瘤体积较小且尤其位于前方时,可进行局部切除术(仅切除部分巩膜和肿瘤)。
对于大肿瘤(COMS大分类:顶点高>10 mm,最大基底直径>16 mm)且难以保留眼球时,适用眼球摘除术。至今仍被视为一种选择。眼球摘除后出现眼眶复发时,应在多学科会议上讨论手术和放射治疗。推荐放射治疗剂量为每次2 Gy,总剂量45~50 Gy,分20次。
转移性葡萄膜黑色素瘤的全身治疗选择与皮肤黑色素瘤相比极为有限。
治疗后患眼监测每6个月一次,持续2-5年,之后每年一次。肿瘤完全消退者可转至当地验光师,眼球摘除+R0切除者可在伤口愈合后转至义眼师。
对于转移监测,高风险患者建议每6个月进行肝脏MRI或超声检查,低风险患者每12个月进行肝脏影像检查14)。非电离辐射影像(MRI、超声)因避免辐射暴露而被推荐。对于检出单染色体3的转移高风险患者,应加强转移监测。
对于小至中等大小肿瘤,可选择近距离放疗(如106Ru巩膜敷贴器)、质子束治疗、重离子治疗和射波刀,通常可保留眼球。大肿瘤可能需要眼球摘除,但已显示治疗选择不影响转移率和总生存率。因此,在优先考虑生命预后的同时,探讨保留视功能的可行性。
如果HLA-A*02:01阳性,替本塔司普(tebentafusp)是一线候选药物。它是首个在III期试验中显示显著改善总生存期的药物。对于肝局限转移,如可行R0切除,考虑肝切除术。肝局部治疗(PHP、SIRT、TACE等)也是选择。免疫检查点抑制剂的疗效相对于皮肤黑色素瘤有限(单药有效率约5%),在开始治疗前应在专业机构进行多学科讨论。
葡萄膜黑色素瘤的发病机制涉及与皮肤黑色素瘤不同的独特分子通路。
GNAQ/GNA11的Q209位突变最常见,R183突变和G48L突变也已被鉴定1)。这些突变损害GTP酶活性,导致持续的GTP结合激活状态1)。GNAQ/GNA11突变导致包括MAPK通路(Ras/RAF/MEK/ERK)在内的多条信号通路持续激活1)。GNAQ/GNA11突变是肿瘤形成的早期事件,与肿瘤大小或转移风险无显著关联。
二次驱动突变(BAP1、SF3B1、EIF1AX)几乎完全互斥发生,对转移风险分层具有重要意义。BAP1突变被归类为2类(高转移风险),而携带SF3B1突变的患者转移后中位总生存期为3.9年(95% CI 2.3~6.2),12个月总生存率为94%,预后相对良好。在转移灶中,GNAQ(57%)和GNA11(36%)也以互斥方式被检测到。
罕见的起始突变如CYSLTR2和PLCB4在几乎所有剩余的葡萄膜黑色素瘤中被检测到。
由于葡萄膜没有淋巴管,所有转移均通过血行发生6)。发病初期病变小而扁平,但当高度增加时会穿破Bruch膜并迅速增大。周围可能出现浆液性视网膜脱离。
循环肿瘤细胞在1088%的患者中被检测到。对肝脏的显著趋向性可用种子和土壤理论解释。微转移可能在原发肿瘤无症状期早期发生。转移灶中单体3占70100%,BAP1突变占60~80%。也有转移到甲状腺等罕见部位的报道11)。
肝转移的生长模式有两种:窦状隙浸润型和门静脉周围结节型。浸润型中胶原蛋白产生导致假窦形成,结节型中VEGF诱导的血管生成是主要机制13)。
肿瘤内VEGF浓度显著高于健康眼,并与肿瘤基底直径和高度正相关3)。抗VEGF药物(贝伐珠单抗)的全身给药在小鼠模型中显示出抑制转移的效果,但玻璃体内给药加速肿瘤生长的矛盾结果也有报道3)。
有报道称玻璃体内注射贝伐珠单抗后睫状体黑色素瘤快速生长(基底直径从2.51 mm增至18.0 mm,高度从6.23 mm增至11.0 mm,7周内)3)。典型脉络膜黑色素瘤的中位倍增时间为154~511天,这种快速生长是异常的。
肿瘤内异质性在形态学和遗传学上均存在,影响活检的预后预测准确性2)。这也是推荐从多个部位取样的原因2)。
自噬相关9基因特征(9-ARG:IKBKE、BNIP1、ITGA6、FKBP1A、DLC1、PRKCD、GABARAPL1、LMCD1、TUSC1)已被证明对葡萄膜黑色素瘤的预后预测有用(在TCGA 80例+GEO 150例中验证)8)。在高风险组中,IL6-JAK-STAT3通路、血管新生和活性氧通路富集,尽管免疫细胞浸润(CD8 T细胞、活化记忆CD4 T细胞)增加,但据报道是一种免疫抑制表型,与不良预后相关,这是一个矛盾的发现8)。这被认为与眼睛是免疫豁免器官有关。
替本塔司普是一种针对HLA-A02:01阳性患者设计的T细胞受体双特异性融合蛋白7)。它在HLA-A02:01复合体上识别肿瘤相关抗原gp100,并激活T细胞以发挥抗肿瘤效应。
在III期试验中,对于HLA-A*02:01阳性的转移性葡萄膜黑色素瘤患者,与研究者选择对照相比,总生存期显著改善(中位延长6个月)14)。
Krohn等人(2025)的病例报告显示,一名转移性葡萄膜黑色素瘤患者根据III期试验接受替本塔司普(每周静脉注射:20→30→68 mg递增)治疗,26个月后肝转移稳定,无新病灶,病程良好7)。该患者右眼中心脉络膜厚度从241 μm减少49%至123 μm,并观察到眼底脱色素、眉毛和睫毛变白以及皮肤脱色素斑。
gp100也在正常脉络膜黑色素细胞中表达,被认为与脉络膜变薄的机制有关7)。眼部副作用可能是不可逆的,给药期间需要定期进行眼科监测。
目前,辅助全身治疗的证据不足,不建议在临床试验框架外给药14)。携带BAP1胚系突变的家族(BAP1肿瘤易感综合征)与多种癌症(肾细胞癌、间皮瘤、皮肤黑色素瘤等)风险增加相关,是遗传咨询的对象14)。
Wagle等人(2022)报告了一例COVID-19疫苗接种后出现葡萄膜黑色素瘤肿瘤坏死的病例12)。坏死型葡萄膜黑色素瘤占所有病例的3%–6%,且可能带来病理诊断上的困难。
Gαq抑制剂(YM-254890)与MEK抑制剂(曲美替尼/比美替尼)联合使用在体外和体内显示出协同抗肿瘤效果1)。单独抑制Gαq时,MAPK信号在24小时内恢复,但与MEK抑制剂联合使用可抑制MAPK信号的恢复1)。
在葡萄膜黑色素瘤中,免疫检查点抑制剂的疗效有限,不如皮肤黑色素瘤。单药治疗有效率约5%,纳武利尤单抗联合伊匹木单抗为12%–18%14)。
Madani等人(2022)报告的一例心脏转移病例中,使用纳武利尤单抗1 mg/kg联合伊匹木单抗3 mg/kg(每3周一次,共4个周期)后序贯纳武利尤单抗维持治疗,但出现疾病进展6)。随后改为白蛋白结合型紫杉醇/替莫唑胺方案,但最终预后不良。
针对转移性病变的局部方法包括肝切除术、射频消融术、肝动脉栓塞术、美法仑经皮肝灌注化疗(PHP)、钇-90微球近距离放疗(SIRT)和MR引导下激光诱导热疗。PHP和SIRT的总生存期最长14)。
9-ARG预后特征可能为免疫治疗的个体化提供参考8)。检测MBD4的体细胞致病性突变可能预测对检查点抑制剂的反应。
它是一种针对HLA-A*02:01阳性转移性葡萄膜黑色素瘤患者的T细胞受体双特异性融合蛋白。靶向肿瘤相关抗原gp100,是首个在III期试验中显著改善转移性葡萄膜黑色素瘤总生存期的药物。给药期间需注意脉络膜变薄、眼底脱色素等眼部副作用。