脈絡膜メラノーマ
典型的外観:境界不整、隆起したドーム状の灰褐色脈絡膜腫瘤として片眼性に出現。
色素:55%が重色素、30%混合、15%無色素と色調は多彩。
キノコ状形態:約20%がブルッフ膜を突破しキノコ(カラーボタン)状を呈する。Bruch膜穿破後に急速増大する。
網膜下液:漿液性網膜剥離を高頻度に伴う。
ブドウ膜メラノーマ(uveal melanoma, UM)は、ブドウ膜(虹彩・毛様体・脈絡膜)のメラノサイトから発生する悪性腫瘍である。成人における最も一般的な原発性眼内腫瘍であり、脈絡膜由来が90%超、毛様体由来が約7%、虹彩由来が2%を占める。本記事では脈絡膜および毛様体メラノーマを対象とする。
発生頻度は欧米の約1/20であり、人口10万人あたり0.025人とされる。白人では100万人あたり2〜8人の罹患率であり、やや男性優位で発症ピークは約60歳である。全ブドウ膜メラノーマの1%未満が18歳未満に発症する。世界規模では年間約600万人が眼メラノーマと診断されている6)。
転移の様式はすべて血行性であり(ブドウ膜にリンパ管が存在しないため)、肝臓への強い向性を示す。肝転移は70〜90%に認められ、その他は肺・骨・皮膚に転移する6)。転移の62%以上は原発腫瘍治療後5年以内に臨床的に顕在化するが、残りは25年以上後に検出されることもある。治療後数年から10年以上経過した後に転移が明らかとなる場合もあるため、長期的な転移モニタリングが必要である。
転移後の全生存期間(OS)中央値はメタ解析(2494患者・78論文)で10〜13ヶ月であり、5年超の生存は約2%、13%が3年超生存と推定される13)。1年生存率は43〜52%と報告されている。12年死亡率は約40%であり、局所治療の選択に関わらずほぼ同率である2)。5年生存率は中型腫瘍で70〜80%とされ(眼球温存療法と眼球摘出で差なし)、治療法の違いによる生命予後に大きな差はないことが明らかになっている。
中〜高リスク患者には6〜12ヶ月ごとの肝画像検査を10年間継続することが推奨される14)。
欧米では白人で100万人あたり2〜8人の罹患率であり、成人における最多の原発性眼内腫瘍ではあるが、絶対数は少ない。発生頻度は欧米の約1/20であり、人口10万人あたり0.025人とされる。白人に多く、アジア人での発生はさらに少ない。
初診時に約30%は無症状であり、健診や他疾患の検査中に偶然発見される。症状が出現した場合の内訳は視力低下38%、光視症9%、飛蚊症7%、周辺視野欠損6%、眼痛2%である。
腫瘍が小さく眼底周辺部にある間は一般に無症状である。増大に伴い以下の症状が出現する。
毛様体メラノーマの症状は、その解剖学的位置の特殊性から以下のような特徴を示す5)。
続発眼圧上昇は毛様体メラノーマ診断時に最大17%に認められる3)。
脈絡膜メラノーマ
典型的外観:境界不整、隆起したドーム状の灰褐色脈絡膜腫瘤として片眼性に出現。
色素:55%が重色素、30%混合、15%無色素と色調は多彩。
キノコ状形態:約20%がブルッフ膜を突破しキノコ(カラーボタン)状を呈する。Bruch膜穿破後に急速増大する。
網膜下液:漿液性網膜剥離を高頻度に伴う。
毛様体メラノーマ
発見時サイズ:解剖学的な隠れた位置のため、発見時に比較的大きいことが多い。
見張り血管(sentinel vessel):腫瘍直上の拡張・蛇行した強膜上血管を高頻度に伴う。
前眼部変化:水晶体・虹彩隔壁の前方移動、続発閉塞隅角緑内障を呈しやすい。
眼外進展:乳頭管(emissary canal)経由の眼外進展リスクがある。
脈絡膜母斑とメラノーマの鑑別には以下の8項目を評価する。
リスク因子が0個の場合、5年以内の成長確率は3%にとどまるが、1個で38%、2個以上で50%超に上昇する。
CONSプロトコールによるサイズ分類を以下に示す。治療方針の選択に用いられる。
| 分類 | 頂点高 | 最大基底径 |
|---|---|---|
| 小 | 1.0〜2.5 mm | 5.0〜16.0 mm |
| 中 | 2.5〜10 mm | <16 mm |
| 大 | >10 mm | >16 mm |
脈絡膜に発生する主要な腫瘍の鑑別ポイントを以下に示す。
| 悪性黒色腫 | 血管腫 | 転移性腫瘍 | |
|---|---|---|---|
| 色調 | 黒・灰・褐色 | 橙赤色 | 黄白色 |
| 形 | 丈が高い | 紡錘形 | 板状 |
| 網膜剥離 | なし〜中等度 | なし〜軽度 | 著明 |
| 成長 | 比較的緩徐 | なし | 速い |
TFSOM-UHHDの8つのリスク因子で評価する。因子0個では5年以内の成長確率は3%にとどまるが、2個以上では50%超に上昇する。定期的な超音波や眼底写真での経過観察が必要である。
発症は主に孤発性(sporadic)である。原因は不明であるが、癌抑制遺伝子や癌遺伝子の異常のほか、日光曝露などの関与が推察されている。主なリスク因子を以下に示す。
遺伝子変異と転移リスクの対応を以下に示す。
| 変異遺伝子 | 変異頻度 | 転移リスク・特徴 |
|---|---|---|
| GNAQ/GNA11 | 83〜89% | 相互排他的な開始変異。転移リスクとの直接関連なし |
| BAP1 | 45% | 最も高い転移リスク(大ピーク3.5年)、クラス2 |
| SF3B1 | 23% | 中程度リスク。遅発転移(大ピーク7年)が特徴 |
| EIF1AX | 17% | 最も低い転移リスク |
GNAQ/GNA11変異は腫瘍形成初期の事象と考えられており、これらの変異単独では腫瘍の大きさや転移リスクとの有意な関連はない。腫瘍内不均一性が存在し、形態学的に異なる部位で遺伝子プロファイルが異なりうる(モノソミー3は部位横断的に共通する一方、6q欠失は色素部位のみに限局する例もある)2)。
BAP1変異は最も高い転移リスクに関連し1)、EIF1AX変異は最も低い1)。
組織学的には紡錘形細胞型と類上皮細胞型に分類される。類上皮細胞の割合が高い症例ほど生命予後が不良とされる。混合型も存在する。
BAP1変異は転移リスクが最も高く(大ピーク3.5年)、SF3B1変異では遅発転移(大ピーク7年)が特徴で、EIF1AX変異は最も低いリスクを示す。また染色体3番の欠失(モノソミー3)が検出された場合は高率に転移をきたし、予後不良となる。これらの変異情報は細針吸引生検で得られ、転移サーベイランス計画の個別化に用いられる。
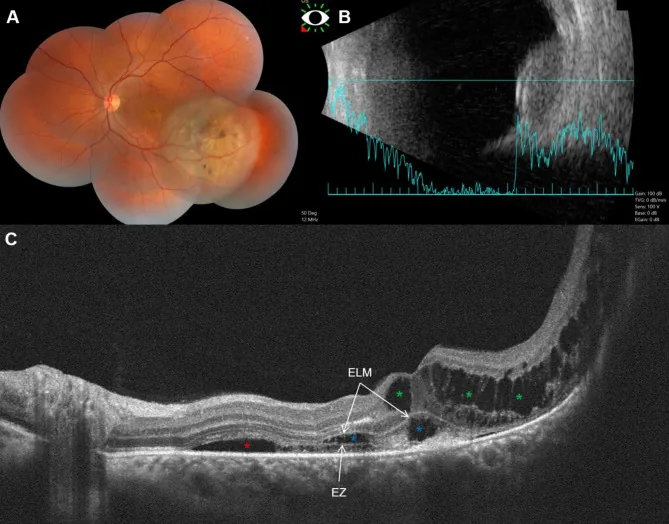
連続的な眼底写真は腫瘍成長の記録に極めて重要であり、広角眼底撮影(Optos等)の活用も有用である。眼底自発蛍光では、リポフスチンの自発蛍光特性を利用し、ドルーゼンより明るい橙色蛍光(オレンジピグメント)を確認する。
超音波検査はブドウ膜メラノーマ診断の中心をなす。悪性黒色腫では特徴的な減衰を示す。
SD-OCTでは神経感覚網膜・RPE変化を可視化する。EDI-OCTによる特徴的所見(37眼の研究より)は以下の通りである。
T1強調画像で高信号、T2強調画像で低信号を示す。I-125プラーク照射後の腫瘍サイズ追跡にも使用される7)。
123I-IMP(ヨウ化アンフェタミン)をトレーサーとしたSPECT検査では、静注24時間後に患眼に一致した異常集積像が得られ、感度・特異度ともに優れた検査法である。FDG-PETも診断に用いられることがある。
中〜高リスク患者には6〜12ヶ月ごと・10年間の転移サーベイランスが推奨される14)。
腫瘍組織や針生検で得られた細胞からの分子検査は、転移リスク層別化に重要である。
臨床的に診断不確実な症例で施行する。通常プラーク小線源療法挿入時に併施する。腫瘍播種リスクがあるため議論があるが、遺伝子プロファイル取得による予後層別化のために実施されることが増えている。腫瘍内不均一性を考慮し、形態学的に異なる領域の複数箇所からのサンプリングが望ましい2)。
S-100・HMB-45・MART-1(MelanA)・ビメンチンが陽性を示す。確認には少なくとも2種のメラノサイト系抗体とサイトケラチン(上皮マーカー)の併用が推奨されている。Ki-67による増殖指数の半定量的評価も行われる。毛様体メラノーマではHMB-45強陽性が確認されている5)。BAP1核染色は予後分類に重要な補助的役割を果たす2)。
治療の目標は、①患眼の有用な視力維持、②腫瘍の破壊、③転移と再発の防止の3点である。
脈絡膜母斑との鑑別が判然としない間は、眼底写真や超音波Bモード検査を行いながら厳重に経過観察を続けていく。脈絡膜母斑(厚さ2mm未満・無症状)は、初回検査後3ヶ月で再検査し、以後6ヶ月ごとの経過観察とする。厚さ3mm未満の病変には眼底写真・FA・A/Bモード超音波検査を初期に施行し、3〜4ヶ月後に再検、以降6〜12ヶ月ごとの眼底写真を生涯にわたり継続する。3つ以上のリスク因子を持つ小腫瘍は成長記録を待たず速やかに治療を開始する。
小線源療法
106Ru小線源強膜縫着療法:ルテニウム-106(β線源)を含むプラークを腫瘍部位の強膜上に縫合する。β線のため組織内照射距離が短く、小〜中型腫瘍に適する。実施可能な施設は限られている。
I-125プラーク:ヨウ素125を含むCOMSプラークを腫瘍部位の強膜上に縫合する。照射線量は腫瘍頂点への処方線量90 Gy。主に北米で使用される。
適応:小〜中等大腫瘍の第一選択。
副作用:放射線黄斑症・網膜症、白内障、新生血管緑内障、視神経症、強膜壊死。ほとんどは治療後5年以内に発生。
再発:局所再発の80%は3年以内。98%は眼底カラー写真で検出可能。
視力予後:COMS 3年データで43〜49%の患者が20/200(0.1相当)以下となる。放射線網膜症が主な原因である10)。
陽子線治療
特徴:ブラッグピーク効果で腫瘍に線量を集中させる粒子線治療。眼球温存療法。
適応:小〜中等大腫瘍の眼球温存選択肢。
治療効果:陽子線治療後6ヶ月で腫瘍の完全退縮が得られた症例も報告されている。
利点:周囲正常組織への線量が少ない。
重粒子線やサイバーナイフなどの放射線外照射の適応が拡大しつつある。眼球温存は可能だが、視神経障害や血管新生緑内障などの合併症により視機能が失われることも多い。実施可能施設は限られているが、選択肢の一つとして位置づけられている。
小型脈絡膜メラノーマ(厚さ3mm以下)に対して経瞳孔温熱療法(transpupillary thermotherapy, TTT)が適応となる。主なパラメータを以下に示す9)。
| パラメータ | 設定値 |
|---|---|
| 波長 | 810 nm(近赤外) |
| 出力 | 400〜1,000 mW |
| スポット径 | 3,000 μm |
| 照射時間 | 1スポット1〜3分 |
| 深達度 | 3〜4 mm |
経瞳孔温熱療法と小線源療法(プラーク)を組み合わせた「サンドイッチ療法」では、5年再発率は125I使用で3%、106Ru使用で10%と報告されている9)。
腫瘍のサイズが比較的小さく、特に前方に局在している場合には、強膜の一部と腫瘍のみを切除する局所切除術が行われることがある。
大きな腫瘍(COMS大分類:頂点高>10 mm、最大基底径>16 mm)で眼球温存が困難な場合に適応となる。今日でも選択肢の一つとして位置づけられる。眼球摘出後の眼窩再発に対しては、多職種カンファレンスで外科的・放射線治療を検討する。放射線治療は2 Gy超/frで計45〜50 Gy/20回が推奨されている。
転移性ブドウ膜メラノーマに対する全身治療は、皮膚メラノーマに比べ著しく選択肢が限られる。
治療後の患眼監視は6ヶ月ごと2〜5年、以後は年1回を継続する。腫瘍完全退縮例は地域の検眼医に移行可能であり、眼球摘出+R0切除例は創傷治癒後に義眼士に移行可能である。
転移サーベイランスとして、高リスク患者には6ヶ月ごとの肝MRIまたは超音波、低リスク患者には12ヶ月ごとの肝画像検査を推奨する14)。非電離放射線画像(MRI・超音波)が放射線被曝回避の観点から推奨される。モノソミー3が検出された転移高リスク患者では転移モニタリングを強化する。
小〜中等大腫瘍には小線源療法(106Ru強膜縫着療法など)や陽子線治療、重粒子線・サイバーナイフが選択肢であり、眼球温存が可能な場合が多い。大腫瘍では眼球摘出術が必要な場合があるが、治療法の選択が転移率・全生存率に影響しないことが示されており、生命予後を優先しつつ視機能温存の可否を検討する。
HLA-A*02:01陽性であればテベンタフスプが第一選択候補となる。第III相試験でOS有意改善が示された初の薬剤である。肝限局転移にはR0切除可能なら肝切除を検討する。肝局所療法(PHP、SIRT、TACE等)も選択肢となる。免疫チェックポイント阻害薬の効果は皮膚メラノーマに比べ限定的(単剤奏効率約5%)であり、治療開始前に専門施設での多職種カンファレンスを行うことが重要である。
ブドウ膜メラノーマの発症機序は皮膚メラノーマとは異なる独自の分子経路による。
GNAQ/GNA11のQ209位変異が最も多く、R183変異やG48L変異も同定されている1)。これらの変異はGTPase活性を障害し、恒常的なGTP結合活性化状態をもたらす1)。GNAQ/GNA11変異により、MAPK経路(Ras/RAF/MEK/ERK)を含む複数のシグナル経路が持続的に活性化される1)。GNAQ/GNA11変異は腫瘍形成初期の事象であり、腫瘍の大きさや転移リスクとの有意な関連はない。
二次ドライバー変異(BAP1・SF3B1・EIF1AX)は互いにほぼ完全に排他的に生じ、転移リスクの層別化に重要な意味を持つ。BAP1変異はクラス2(高転移リスク)に分類され、SF3B1変異保持者の転移後全生存期間中央値は3.9年(95%CI 2.3〜6.2)、12ヶ月全生存率は94%と比較的良好な経過をたどる。転移巣においてもGNAQ(57%)とGNA11(36%)が相互排他的に検出される。
稀な開始変異としてCYSLTR2・PLCB4変異が残りのほぼ全てのブドウ膜メラノーマで検出される。
ブドウ膜にリンパ管が存在しないため、転移はすべて血行性に生じる6)。発症初期は小さく扁平な病変であるが、丈が高くなるとBruch膜を穿破し急速に増大する。周囲に漿液性網膜剥離を生じることがある。
循環腫瘍細胞は10〜88%の患者で検出される。肝臓への注目すべき向性はseed and soil理論で説明される。微小転移は原発腫瘍の無症候期から早期に生じうる。転移巣のモノソミー3は70〜100%、BAP1変異は60〜80%に認められる。甲状腺など稀な転移部位への転移例も報告されている11)。
肝転移の成長パターンとして、類洞浸潤型(sinusoidal infiltrative)と門脈周囲結節型(periportal nodular)の2パターンが知られる。浸潤型ではコラーゲン産生による偽類洞腔形成、結節型ではVEGF誘導性血管新生が主要な機序である13)。
腫瘍内VEGF濃度は健常眼より有意に高く、腫瘍の基底径・高さと正相関する3)。抗VEGF薬(ベバシズマブ)の全身投与はマウスモデルで転移抑制効果が示されたが、硝子体内投与では腫瘍増大を加速したとの矛盾した結果が報告されている3)。
硝子体内ベバシズマブ注射後に毛様体メラノーマが急速増大した症例(基底径2.51→18.0 mm、高さ6.23→11.0 mm/7週間)が報告されている3)。通常の脈絡膜メラノーマの倍加時間の中央値は154〜511日であり、この急速増大は異例である。
腫瘍内不均一性が形態学的・遺伝的両面で存在し、生検の予後予測精度に影響する2)。複数箇所からのサンプリングが推奨される理由もここにある2)。
オートファジー関連9遺伝子シグネチャー(9-ARG:IKBKE, BNIP1, ITGA6, FKBP1A, DLC1, PRKCD, GABARAPL1, LMCD1, TUSC1)がブドウ膜メラノーマの予後予測に有用であることが示されている(TCGA 80例+GEO 150例で検証)8)。高リスク群ではIL6-JAK-STAT3経路・血管新生・活性酸素種経路が濃縮し、免疫細胞浸潤(CD8 T細胞・活性化記憶CD4 T細胞)が増加するものの、免疫抑制的表現型であり予後不良に関連するという逆説的知見が報告されている8)。これは眼が免疫特権臓器であることと関連すると考えられる。
テベンタフスプはHLA-A02:01陽性患者向けに設計されたT細胞受容体二重特異性融合蛋白である7)。腫瘍関連抗原gp100をHLA-A02:01複合体上で認識し、T細胞を活性化することで抗腫瘍効果を発揮する。
第III相試験では、HLA-A*02:01陽性の転移性ブドウ膜メラノーマ患者において全生存期間の有意な改善(investigator’s choice比較対照に対し中央値6ヶ月の延長)が示された14)。
Krohnら(2025)の症例報告では、第III相試験に基づくテベンタフスプ(週1回IV:20→30→68 mgの漸増)の投与を受けた転移性ブドウ膜メラノーマ患者において、26ヶ月の投与後に肝転移安定・新病変なしという良好な経過が記録された7)。同患者では右眼中心脈絡膜厚が241μmから123μmへ49%菲薄化し、眼底脱色素・眉毛睫毛のポリオーシス・皮膚脱色素斑が観察された。
gp100は正常脈絡膜メラノサイトにも発現しており、脈絡膜菲薄化の機序に関連すると考えられる7)。眼副作用は不可逆的な場合もあり、投与中は定期的な眼科的モニタリングが必要である。
現時点で補助全身療法のエビデンスは不十分であり、臨床試験の枠組み外での投与は推奨されない14)。BAP1生殖細胞系列変異を有する家系(BAP1素因症候群)では、複数の癌(腎細胞癌・中皮腫・皮膚メラノーマ等)のリスク上昇と関連しており、遺伝カウンセリングの対象となる14)。
Wagleら(2022)はCOVID-19ワクチン接種後にぶどう膜メラノーマの腫瘍壊死を呈した症例を報告した12)。壊死型ブドウ膜メラノーマは全体の3〜6%を占め、病理診断上の困難を伴う場合がある。
Gαq阻害薬(YM-254890)とMEK阻害薬(trametinib/binimetinib)の併用が、in vitro・in vivoで相乗的抗腫瘍効果を示している1)。Gαq単独阻害ではMAPKシグナルが24時間で回復するが、MEK阻害薬との併用によりMAPKシグナルの回復が抑制される1)。
ブドウ膜メラノーマでは皮膚メラノーマに比べ免疫チェックポイント阻害薬の効果は限定的である。単剤の奏効率は約5%、ニボルマブ+イピリムマブ併用で12〜18%と報告されている14)。
Madaniら(2022)の心転移症例では、nivolumab 1 mg/kg+ipilimumab 3 mg/kg(3週毎×4サイクル)→nivolumab維持療法を施行したが、病勢進行に至った6)。その後nab-paclitaxel・temozolomide療法に変更されたが、最終的に転帰不良であった。
転移性病変に対する局所アプローチとして、肝切除・ラジオ波焼灼術・肝動脈塞栓術・メルファランによる経皮的肝灌流化学療法(PHP)・イットリウム-90マイクロスフィア近接照射療法(SIRT)・MRガイド下レーザー誘発熱療法が研究されている。PHPとSIRTが最長のOSを示す14)。
9-ARG予後シグネチャーは免疫療法の個別化に示唆を与える可能性がある8)。MBD4の体細胞病原性変異の検出はチェックポイント阻害薬への反応を予測しうるとされている。
HLA-A*02:01陽性の転移性ブドウ膜メラノーマ患者向けのT細胞受容体二重特異性融合蛋白である。腫瘍関連抗原gp100を標的とし、第III相試験で転移性ブドウ膜メラノーマの全生存期間を有意に改善した初の薬剤である。投与中は脈絡膜菲薄化・眼底脱色素などの眼副作用への注意が必要である。