脈絡膜黑色素瘤
典型外觀:單眼出現、邊界不規則、隆起的圓頂狀灰褐色脈絡膜腫塊。
色素:55%為重度色素性,30%為混合性,15%為無色素性,色調多樣。
蘑菇狀形態:約20%突破Bruch膜,呈蘑菇(紐扣)狀。Bruch膜穿破後迅速增大。
視網膜下液:常伴有漿液性視網膜剝離。

葡萄膜黑色素瘤(uveal melanoma, UM)是起源於葡萄膜(虹膜、睫狀體、脈絡膜)黑色素細胞的惡性腫瘤。它是成人最常見的原發性眼內腫瘤,其中脈絡膜來源佔90%以上,睫狀體來源約佔7%,虹膜來源佔2%。本文主要討論脈絡膜和睫狀體黑色素瘤。
發生率約為歐美的1/20,每10萬人中0.025人。在白人中,發生率為每百萬人2-8例,男性略多,發病高峰約在60歲。所有葡萄膜黑色素瘤中不到1%發生在18歲以下。全球範圍內,每年約有600萬人被診斷為眼黑色素瘤6)。
所有轉移均為血行性(因為葡萄膜沒有淋巴管),對肝臟有強烈趨向性。肝轉移佔70-90%,其他部位包括肺、骨和皮膚6)。超過62%的轉移在原發腫瘤治療後5年內臨床顯現,但其餘可能在25年後才被檢測到。由於轉移可能在治療後數年甚至10年以上才變得明顯,因此需要長期監測轉移。
轉移後的中位總生存期(OS)根據統合分析(2494名患者,78篇論文)為10-13個月,約2%存活超過5年,13%估計存活超過3年13)。1年存活率報告為43-52%。12年死亡率約為40%,無論選擇何種局部治療,該比例基本相同2)。中型腫瘤的5年存活率為70-80%(眼球保留治療與眼球摘除無差異),表明治療選擇對生命預後沒有顯著影響。
對於中高風險患者,建議每6至12個月進行一次肝臟影像檢查,持續10年14)。
在歐美,白種人的發生率為每百萬人2至8人,是成人中最常見的原發性眼內腫瘤,但絕對數量較少。日本的發生率約為歐美的1/20,估計為每10萬人0.025人。白種人較常見,亞洲人發生率更低。
初診時約30%的患者無症狀,在健康檢查或其他疾病檢查中偶然發現。出現症狀時,其構成如下:視力下降38%、閃光感9%、飛蚊症7%、周邊視野缺損6%、眼痛2%。
當腫瘤較小且位於眼底周邊部時,通常無症狀。隨著腫瘤增大,出現以下症狀。
睫狀體黑色素瘤的症狀因其解剖位置的特殊性而具有以下特徵5)。
續發性眼壓升高在睫狀體黑色素瘤診斷時最多見於17%的患者3)。
脈絡膜黑色素瘤
典型外觀:單眼出現、邊界不規則、隆起的圓頂狀灰褐色脈絡膜腫塊。
色素:55%為重度色素性,30%為混合性,15%為無色素性,色調多樣。
蘑菇狀形態:約20%突破Bruch膜,呈蘑菇(紐扣)狀。Bruch膜穿破後迅速增大。
視網膜下液:常伴有漿液性視網膜剝離。
睫狀體黑色素瘤
發現時大小:由於解剖位置隱蔽,發現時通常較大。
哨兵血管:常伴有腫瘤正上方擴張、迂曲的鞏膜表面血管。
眼前段改變:易出現水晶體-虹膜隔前移和續發性閉角型青光眼。
眼外擴展:存在經由導血管(emissary canal)的眼外擴展風險。
脈絡膜痣與黑色素瘤的鑑別需評估以下8個項目。
如果風險因子為0個,5年內生長機率僅為3%,但1個時升至38%,2個以上時超過50%。
根據COMS方案的大小分類如下所示。用於選擇治療策略。
| 分類 | 頂點高度 | 最大基底直徑 |
|---|---|---|
| 小 | 1.0~2.5 mm | 5.0~16.0 mm |
| 中 | 2.5~10 mm | <16 mm |
| 大 | >10 mm | >16 mm |
以下列出發生於脈絡膜的主要腫瘤的鑑別要點。
| 惡性黑色素瘤 | 血管瘤 | 轉移性腫瘤 | |
|---|---|---|---|
| 色調 | 黑、灰、褐色 | 橙紅色 | 黃白色 |
| 形狀 | 穹頂形 | 紡錘形 | 板狀 |
| 視網膜剝離 | 無至中度 | 無至輕度 | 顯著 |
| 生長 | 相對緩慢 | 無 | 快速 |
透過TFSOM-UHHD的8個風險因子進行評估。0個因子時,5年內生長機率僅為3%,但2個或以上時則升至50%以上。需要定期進行超音波和眼底照相追蹤。
發病主要是散發性的。原因不明,但推測與抑癌基因和癌基因的異常以及日光曝曬等有關。主要風險因素如下所示。
基因突變與轉移風險的對應關係如下所示。
| 突變基因 | 突變頻率 | 轉移風險/特徵 |
|---|---|---|
| GNAQ/GNA11 | 83–89% | 互斥的起始突變。與轉移風險無直接關聯。 |
| BAP1 | 45% | 最高轉移風險(高峰3.5年),2類 |
| SF3B1 | 23% | 中度風險。特點是晚期轉移(高峰在7年)。 |
| EIF1AX | 17% | 最低轉移風險。 |
GNAQ/GNA11突變被認為是腫瘤形成的早期事件,這些突變本身與腫瘤大小或轉移風險無顯著關聯。存在腫瘤內異質性,不同形態區域可能具有不同的基因譜(例如,3號染色體單體在各區域常見,而6q缺失可能僅限於色素區域)2)。
BAP1突變與最高轉移風險相關1),而EIF1AX突變與最低風險相關1)。
組織學上分為梭形細胞型和上皮樣細胞型。上皮樣細胞比例越高的病例預後越差。也存在混合型。
BAP1突變轉移風險最高(高峰在3.5年),SF3B1突變以晚期轉移為特點(高峰在7年),EIF1AX突變風險最低。此外,檢測到3號染色體缺失(3號單體)時轉移率高,預後不良。這些突變資訊通過細針穿刺活檢獲得,用於個體化轉移監測計劃。
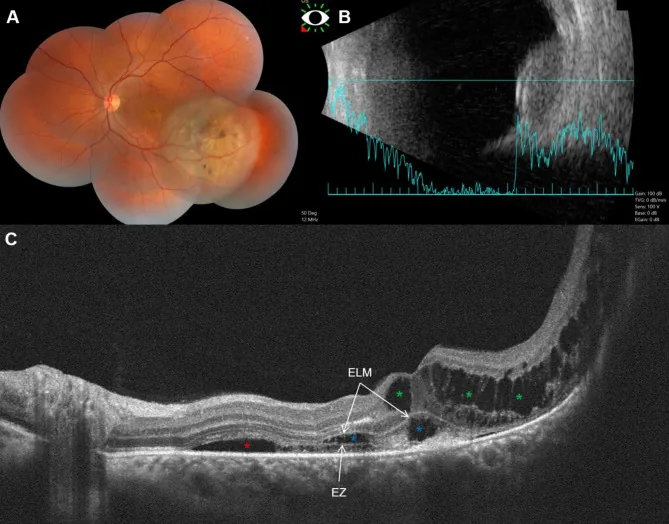
連續眼底照相對於記錄腫瘤生長極為重要,廣角眼底攝影(如Optos)的應用也很有用。在眼底自發螢光中,利用脂褐質的自發螢光特性,可辨識比玻璃膜疣更亮的橙色螢光(橙色色素)。
超音波檢查是葡萄膜黑色素瘤診斷的核心。惡性黑色素瘤顯示特徵性衰減。
SD-OCT可顯示神經感覺視網膜和RPE變化。EDI-OCT的特徵性表現(基於37隻眼的研究)如下。
T1加權影像呈高信號,T2加權影像呈低信號。也用於I-125敷貼照射後的腫瘤大小追蹤7)。
使用123I-IMP(碘苯丙胺)作為示蹤劑的SPECT檢查,在靜脈注射24小時後,患眼出現一致的異常聚集影像,是一種靈敏度和特異度均優的檢查方法。FDG-PET也可用於診斷。
中高風險患者建議每6~12個月進行一次轉移監測,持續10年14)。
對腫瘤組織或針刺切片獲得的細胞進行分子檢測,對於轉移風險分層至關重要。
在臨床診斷不確定的病例中進行。通常與敷貼器近距離放射治療植入同時進行。由於存在腫瘤播散風險,存在爭議,但為了透過獲取基因圖譜進行預後分層,實施越來越多。考慮到腫瘤異質性,建議從形態學不同的多個區域取樣2)。
S-100、HMB-45、MART-1(MelanA)和波形蛋白呈陽性。為確認,建議至少使用兩種黑色素細胞抗體與細胞角蛋白(上皮標記物)聯合使用。也進行Ki-67增殖指數的半定量評估。在睫狀體黑色素瘤中,已確認HMB-45強陽性5)。BAP1核染色在預後分類中扮演重要的輔助角色2)。
治療目標為:①維持患眼的有用視力,②破壞腫瘤,③防止轉移和復發。
當與脈絡膜痣難以鑑別時,應透過眼底照相和B超進行嚴密追蹤。對於脈絡膜痣(厚度<2mm,無症狀),初次檢查後3個月複查,之後每6個月觀察一次。對於厚度<3mm的病變,初期進行眼底照相、螢光血管攝影和A/B超檢查,3-4個月後複查,之後每6-12個月進行一次眼底照相,終身持續。具有3個或以上危險因子的小腫瘤應立即治療,無需等待生長記錄。
近接放射治療
釕-106敷貼器鞏膜縫置術:將含有釕-106(β射線源)的敷貼器縫合在腫瘤部位的鞏膜上。由於β射線組織穿透距離短,適用於小至中型腫瘤。可實施的機構有限。
碘-125敷貼器:將含有碘-125的COMS敷貼器縫合在腫瘤部位的鞏膜上。腫瘤頂點的處方劑量為90 Gy。主要用於北美。
適應症:小至中等大小腫瘤的第一線治療。
副作用:放射性黃斑病變/視網膜病變、白內障、新生血管性青光眼、視神經病變、鞏膜壞死。大多數發生在治療後5年內。
復發:80%的局部復發發生在3年內。98%可透過彩色眼底照相檢測。
視力預後:COMS 3年數據顯示,43-49%的患者視力降至20/200(相當於0.1)或更差。放射性視網膜病變是主要原因10)。
質子束治療
特點:利用布拉格峰效應將輻射劑量集中到腫瘤的粒子治療。保留眼球的治療。
適應症:小至中等大小腫瘤的保留眼球選擇。
治療效果:有報導稱質子束治療後6個月腫瘤完全消退的病例。
優點:對周圍正常組織的輻射劑量低。
重粒子線和電腦刀等體外放射治療的適應症正在擴大。雖然可以保留眼球,但常因視神經病變、新生血管性青光眼等併發症導致視功能喪失。雖然可實施的機構有限,但已被定位為治療選擇之一。
經瞳孔溫熱療法(TTT)適用於小型脈絡膜黑色素瘤(厚度≤3mm)。主要參數如下所示9)。
| 參數 | 設定值 |
|---|---|
| 波長 | 810 nm(近紅外) |
| 輸出功率 | 400~1,000 mW |
| 光斑直徑 | 3,000 μm |
| 照射時間 | 每個光斑1~3分鐘 |
| 深度 | 3~4 mm |
經瞳孔溫熱療法與近距離放射療法(鞏膜板)聯合的「三明治療法」中,5年復發率據報導使用碘-125為3%,使用釕-106為10% 9)。
當腫瘤體積較小且尤其位於前方時,可進行局部切除術(僅切除部分鞏膜和腫瘤)。
對於大腫瘤(COMS大分類:頂點高>10 mm,最大基底直徑>16 mm)且難以保留眼球時,適用眼球摘除術。至今仍被視為一種選擇。眼球摘除後出現眼眶復發時,應在多學科會議上討論手術和放射治療。推薦放射治療劑量為每次2 Gy,總劑量45~50 Gy,分20次。
轉移性葡萄膜黑色素瘤的全身治療選擇與皮膚黑色素瘤相比極為有限。
治療後患眼監測每6個月一次,持續2-5年,之後每年一次。腫瘤完全消退者可轉至當地驗光師,眼球摘除+R0切除者可在傷口癒合後轉至義眼師。
對於轉移監測,高風險患者建議每6個月進行肝臟MRI或超音波檢查,低風險患者每12個月進行肝臟影像檢查14)。非電離輻射影像(MRI、超音波)因避免輻射暴露而被推薦。對於檢出單染色體3的轉移高風險患者,應加強轉移監測。
對於小至中等大小腫瘤,可選擇近距離放射治療(如106Ru鞏膜敷貼器)、質子束治療、重離子治療和電腦刀,通常可保留眼球。大腫瘤可能需要眼球摘除,但已顯示治療選擇不影響轉移率和總存活率。因此,在優先考慮生命預後的同時,探討保留視功能的可行性。
如果HLA-A*02:01陽性,替本塔司普(tebentafusp)是一線候選藥物。它是首個在III期試驗中顯示顯著改善總存活期的藥物。對於肝侷限轉移,如可行R0切除,考慮肝切除術。肝局部治療(PHP、SIRT、TACE等)也是選擇。免疫檢查點抑制劑的療效相對於皮膚黑色素瘤有限(單藥有效率約5%),在開始治療前應在專業機構進行多學科討論。
葡萄膜黑色素瘤的發病機制涉及與皮膚黑色素瘤不同的獨特分子路徑。
GNAQ/GNA11的Q209位突變最常見,R183突變和G48L突變也已被鑑定1)。這些突變損害GTP酶活性,導致持續的GTP結合激活狀態1)。GNAQ/GNA11突變導致包括MAPK路徑(Ras/RAF/MEK/ERK)在內的多條信號路徑持續激活1)。GNAQ/GNA11突變是腫瘤形成的早期事件,與腫瘤大小或轉移風險無顯著關聯。
二次驅動突變(BAP1、SF3B1、EIF1AX)幾乎完全互斥發生,對轉移風險分層具有重要意義。BAP1突變被歸類為第2類(高轉移風險),而攜帶SF3B1突變的患者轉移後中位總生存期為3.9年(95% CI 2.3~6.2),12個月總生存率為94%,預後相對良好。在轉移灶中,GNAQ(57%)和GNA11(36%)也以互斥方式被檢測到。
罕見的起始突變如CYSLTR2和PLCB4在幾乎所有其餘的葡萄膜黑色素瘤中被檢測到。
由於葡萄膜沒有淋巴管,所有轉移均經由血行發生6)。發病初期病變小而扁平,但當高度增加時會穿破Bruch膜並迅速增大。周圍可能出現漿液性視網膜剝離。
循環腫瘤細胞在1088%的患者中被檢測到。對肝臟的顯著趨向性可用種子和土壤理論解釋。微轉移可能在原發腫瘤無症狀期早期發生。轉移灶中單體3佔70100%,BAP1突變佔60~80%。也有轉移到甲狀腺等罕見部位的報導11)。
肝轉移的生長模式有兩種:竇狀隙浸潤型和門靜脈周圍結節型。浸潤型中膠原蛋白產生導致假竇形成,結節型中VEGF誘導的血管生成是主要機制13)。
腫瘤內VEGF濃度顯著高於健康眼,並與腫瘤基底直徑和高度正相關3)。抗VEGF藥物(貝伐珠單抗)的全身給藥在小鼠模型中顯示出抑制轉移的效果,但玻璃體內給藥加速腫瘤生長的矛盾結果也有報導3)。
有報導稱玻璃體內注射貝伐珠單抗後睫狀體黑色素瘤快速生長(基底直徑從2.51 mm增至18.0 mm,高度從6.23 mm增至11.0 mm,7週內)3)。典型脈絡膜黑色素瘤的中位倍增時間為154~511天,這種快速生長是異常的。
腫瘤內異質性在形態學和遺傳學上均存在,影響活檢的預後預測準確性2)。這也是推薦從多個部位取樣的原因2)。
自噬相關9基因特徵(9-ARG:IKBKE、BNIP1、ITGA6、FKBP1A、DLC1、PRKCD、GABARAPL1、LMCD1、TUSC1)已被證明對葡萄膜黑色素瘤的預後預測有用(在TCGA 80例+GEO 150例中驗證)8)。在高風險組中,IL6-JAK-STAT3路徑、血管新生和活性氧路徑富集,儘管免疫細胞浸潤(CD8 T細胞、活化記憶CD4 T細胞)增加,但據報導是一種免疫抑制表現型,與不良預後相關,這是一個矛盾的發現8)。這被認為與眼睛是免疫特權器官有關。
替本塔司普是一種針對HLA-A02:01陽性患者設計的T細胞受體雙特異性融合蛋白7)。它在HLA-A02:01複合體上識別腫瘤相關抗原gp100,並激活T細胞以發揮抗腫瘤效應。
在III期試驗中,對於HLA-A*02:01陽性的轉移性葡萄膜黑色素瘤患者,與研究者選擇對照相比,總存活期顯著改善(中位延長6個月)14)。
Krohn等人(2025)的病例報告顯示,一名轉移性葡萄膜黑色素瘤患者根據III期試驗接受替本塔司普(每週靜脈注射:20→30→68 mg遞增)治療,26個月後肝轉移穩定,無新病灶,病程良好7)。該患者右眼中心脈絡膜厚度從241 μm減少49%至123 μm,並觀察到眼底脫色素、眉毛和睫毛變白以及皮膚脫色素斑。
gp100也在正常脈絡膜黑色素細胞中表現,被認為與脈絡膜變薄的機制有關7)。眼部副作用可能是不可逆的,給藥期間需要定期進行眼科監測。
目前,輔助全身治療的證據不足,不建議在臨床試驗框架外給藥14)。攜帶BAP1胚系突變的家族(BAP1腫瘤易感症候群)與多種癌症(腎細胞癌、間皮瘤、皮膚黑色素瘤等)風險增加相關,是遺傳諮詢的對象14)。
Wagle等人(2022)報告了一例COVID-19疫苗接種後出現葡萄膜黑色素瘤腫瘤壞死的病例12)。壞死型葡萄膜黑色素瘤佔所有病例的3%–6%,且可能帶來病理診斷上的困難。
Gαq抑制劑(YM-254890)與MEK抑制劑(trametinib/binimetinib)聯合使用在體外和體內顯示出協同抗腫瘤效果1)。單獨抑制Gαq時,MAPK訊號在24小時內恢復,但與MEK抑制劑聯合使用可抑制MAPK訊號的恢復1)。
在葡萄膜黑色素瘤中,免疫檢查點抑制劑的療效有限,不如皮膚黑色素瘤。單藥治療有效率約5%,nivolumab聯合ipilimumab為12%–18%14)。
Madani等人(2022)報告的一例心臟轉移病例中,使用nivolumab 1 mg/kg聯合ipilimumab 3 mg/kg(每3週一次,共4個療程)後續以nivolumab維持治療,但出現疾病進展6)。隨後改為nab-paclitaxel/temozolomide方案,但最終預後不良。
針對轉移性病變的局部方法包括肝切除術、射頻消融術、肝動脈栓塞術、melphalan經皮肝灌流化療(PHP)、釔-90微球近接放射治療(SIRT)和MR引導下雷射誘導熱療法。PHP和SIRT的總存活期最長14)。
9-ARG預後特徵可能為免疫治療的個體化提供參考8)。檢測MBD4的體細胞致病性突變可能預測對檢查點抑制劑的反應。
它是一種針對HLA-A*02:01陽性轉移性葡萄膜黑色素瘤患者的T細胞受體雙特異性融合蛋白。靶向腫瘤相關抗原gp100,是首個在III期試驗中顯著改善轉移性葡萄膜黑色素瘤總生存期的藥物。給藥期間需注意脈絡膜變薄、眼底脫色素等眼部副作用。