
脉络膜痣
1. 什么是脉络膜痣?
Section titled “1. 什么是脉络膜痣?”脉络膜痣是脉络膜黑色素细胞良性增生形成的色素性病变。眼底检查表现为灰黑色类圆形视网膜下病变,通常呈静止性(非增大性)经过。
患病率在西方人中约为5%,日本人约为0.3%,多分布于后极部。也可能出现在赤道部或锯齿缘附近的最周边部。多数情况下是在成人定期眼科检查或评估其他疾病时偶然发现。
恶性转化的频率在欧美报道中为0.5-3%/10年。日本人中更为罕见,但如果发生恶性转化,则按脉络膜恶性黑色素瘤(脉络膜黑色素瘤)处理。有报道称约10%的脉络膜黑色素瘤来源于已知的痣。
脉络膜痣是良性色素性病变,多数情况下没有问题。但是,如果厚度或积液等多种风险因素叠加,则需要定期随访。请遵医嘱定期检查,如果出现视力变化、飞蚊症或闪光感等新症状,请及时就诊。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”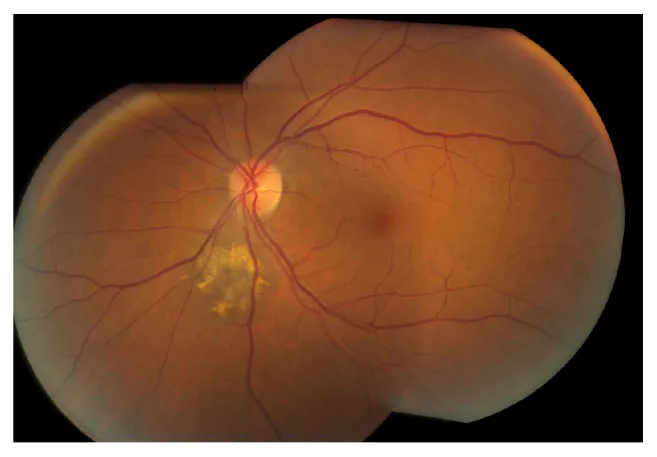
大多数脉络膜痣无症状,在无自觉症状时被发现。如果病变累及黄斑部或视乳头附近,或伴有视网膜下液,可能出现以下症状。
典型的脉络膜痣表现如下:
- 灰黑色类圆形视网膜下隆起
- 直径通常在3个视盘直径(DD)以内
- 高度(厚度)小于2mm,低平,不超过直径的1/5
- 边界相对清晰
- 通常为静止性(非进展性)病程
橙色色素(脂褐素沉积) 是恶性转化的重要预测因子。 由RPE(视网膜色素上皮)产生的老化色素沉积,在眼底自发荧光中表现为高荧光。
视网膜下液的存在 是需要警惕的征象,提示RPE屏障破坏。 如果存在视网膜下液,需进行恶性转化的进一步检查。
使用TFSOM-UHHD进行恶性转化风险评估
Section titled “使用TFSOM-UHHD进行恶性转化风险评估”为鉴别脉络膜痣与脉络膜黑色素瘤,使用TFSOM-UHHD标准评估以下8项风险因素。
| 项目 | 标准 | 意义 |
|---|---|---|
| T 厚度 | 超过2毫米 | 肿瘤体积增大 |
| F 液体 | 存在视网膜下液 | RPE屏障破坏 |
| S 症状 | 闪光感和飞蚊症 | 肿瘤活性指标 |
| O 橙色色素 | 脂褐素沉积 | 肿瘤代谢活性 |
| M 边缘 | 距视盘3毫米以内 | 视盘浸润风险 |
| Ultrasound Hollow(超声低反射) | 内部低回声 | 肿瘤血管密度 |
| Halo absent(晕环缺失) | 无晕环(光轮) | 良性指标缺失 |
| Drusen absent(玻璃膜疣缺失) | 无玻璃膜疣 | 慢性改变缺失 |
风险因素数量与5年内生长概率的关系如下所示。
| 风险因素数量 | 5年生长概率 |
|---|---|
| 0个 | 约3% |
| 1个 | 约38% |
| 2个或以上 | 超过50% |
3. 病因与风险因素
Section titled “3. 病因与风险因素”脉络膜痣是脉络膜黑色素细胞的良性增生病变,确切病因尚不明确。多为散发性发生。
恶性转化风险因素
Section titled “恶性转化风险因素”以下全身性和临床因素被认为会增加恶性转化的风险。
- 浅色虹膜、白皙皮肤(白种人/北欧血统)
- 先天性眼黑变病(与太田痣相关的眼部疾病)
- 葡萄膜黑色素瘤家族史
- BAP1肿瘤易感综合征(BRCA1相关蛋白1的胚系突变)
TFSOM-UHHD的每个因素反映了局部恶性转化的风险。
- 橙色色素(脂褐素):RPE来源的衰老色素积聚是肿瘤活性的指标
- 视网膜下液:提示肿瘤导致RPE屏障破坏
- 厚度≥2mm:反映肿瘤体积增大
- 视盘接触:视神经浸润风险增加
- 超声内部低反射:提示肿瘤内血管存在
基因异常与恶性转化
Section titled “基因异常与恶性转化”脉络膜黑色素瘤的恶性转化涉及基因异常的积累。主要相关异常包括单染色体3(第3染色体单体)和BAP1突变。这些突变在脉络膜黑色素瘤中频繁检测到,但在良性痣中通常不出现。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”眼底检查与眼底照相
Section titled “眼底检查与眼底照相”眼底检查(检眼镜、广角眼底照相) 是筛查和随访的基础。连续眼底照相记录对于判断肿瘤生长至关重要,广角眼底照相(如Optos)也很有用。
光学相干断层扫描(OCT)
Section titled “光学相干断层扫描(OCT)”OCT 在显示视网膜下液和RPE变化方面具有优势。EDI-OCT(增强深度成像OCT)可评估脉络膜结构,观察到以下表现:
- 光学脉络膜阴影
- 视网膜下液的存在
- RPE变化(萎缩、隆起)
- 视网膜下高反射物质(SRHM)
眼底自发荧光
Section titled “眼底自发荧光”橙色色素(脂褐素)表现为比玻璃膜疣更亮的高荧光。有助于评估脂褐素沉积,并有助于判断恶性转化风险。
荧光素眼底血管造影(FA)
Section titled “荧光素眼底血管造影(FA)”FA(荧光素眼底血管造影)可见高荧光模式。色素引起的遮蔽荧光和脂褐质沉积引起的高荧光混合存在。
超声检查(B型、彩色多普勒)
Section titled “超声检查(B型、彩色多普勒)”B型超声用于测量肿瘤高度和评估内部回声模式。彩色多普勒超声可确认肿瘤基底部有无搏动性血流。脉络膜痣常为彩色多普勒阴性(无肿瘤血流),而黑色素瘤常为彩色多普勒阳性。这一发现是痣与黑色素瘤的重要鉴别点。
脉络膜肿瘤的鉴别诊断(三大疾病)
Section titled “脉络膜肿瘤的鉴别诊断(三大疾病)”以下列出脉络膜肿瘤主要鉴别诊断的特征。
| 恶性黑色素瘤 | 血管瘤 | 转移性肿瘤 | |
|---|---|---|---|
| 颜色 | 黑、灰、褐色 | 橙红色 | 黄白色 |
| 形状 | 较高 | 纺锤形 | 板状 |
| 视网膜脱离 | 无至中度 | 无至轻度 | 显著 |
| 生长 | 相对缓慢 | 无 | 快速 |
其他鉴别诊断包括视网膜色素上皮先天性肥大(CHRPE)、脉络膜出血和黑色素细胞瘤。
根据危险因素的数量差异很大。在TFSOM-UHHD的8项中,如果危险因素为0个,5年内生长的概率约为3%。但如果有1个,则升至约38%,2个以上则超过50%。定期进行超声和眼底照相随访很重要,如果发现增大,应立即转为脉络膜恶性黑色素瘤的治疗方案。
5. 标准治疗方法
Section titled “5. 标准治疗方法”脉络膜痣的基本治疗是观察。目前对痣本身没有药物治疗或手术适应症,通过定期眼底检查监测病变是否增大。
低风险病变(无危险因素、小型痣)
Section titled “低风险病变(无危险因素、小型痣)”根据TFSOM-UHHD无危险因素的小型痣作为低风险进行管理。
- 观察间隔:每12~24个月定期眼底检查
- 通过眼底照相和B超记录有无增大
- 若无异常发现,继续按相同频率随访
中高风险病变(有危险因素)
Section titled “中高风险病变(有危险因素)”如果存在一个或多个TFSOM-UHHD危险因素,需进行谨慎的定期观察。
- 初次检查后3个月 复查(确认有无生长)
- 之后 每6个月 进行眼底照相和超声检查,终身持续
- 对于具有3个或以上危险因素的小肿瘤,应考虑不等生长记录而尽快开始治疗
如果在随访中确认肿瘤增大,则转为按脉络膜恶性黑色素瘤的治疗方案。具体治疗选择根据肿瘤大小和视功能决定,包括放射治疗(敷贴器近距离治疗、质子束治疗)或眼球摘除术(详见脉络膜和睫状体黑色素瘤的文章)。
观察间隔因风险而异。对于无风险因素的低风险病变,建议每12至24个月检查一次。而对于有风险因素的中高风险病变,在最初3个月后复查,之后每6个月进行一次眼底检查和超声检查,并终身持续。定期观察的持续最为重要。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”良性增殖的机制
Section titled “良性增殖的机制”脉络膜痣是脉络膜黑色素细胞局部良性增殖形成的病变。正常脉络膜黑色素细胞来源于神经嵴细胞,具有产生色素的能力。在良性增殖阶段,细胞形态得以保持,不会发生浸润性生长或转移。
恶性转化的分子机制
Section titled “恶性转化的分子机制”从脉络膜痣到黑色素瘤的恶性转化需要多种基因异常的积累。
- GNAQ/GNA11突变:约90%的脉络膜黑色素瘤中检测到的起始突变。导致GTP结合持续激活,持续激活MAPK通路等多个信号通路。
- 第3号染色体单体:与转移风险密切相关的继发突变。
- BAP1突变:与最高转移风险相关。也是BAP1肿瘤易感综合征的致病基因。
- SF3B1突变:中等转移风险,以迟发转移为特征。
- EIF1AX突变:最低转移风险。
这些恶性突变通常在痣阶段不出现。基因异常的积累被认为导致从良性到恶性的连续变化。
风险因素的生物学意义
Section titled “风险因素的生物学意义”TFSOM-UHHD的每个项目反映了以下病理状态。
橙色色素(脂褐素):由RPE产生的衰老色素。反映肿瘤的代谢活性以及肿瘤与RPE的相互作用,肿瘤活性越高,积累越多。
视网膜下液:提示肿瘤导致RPE屏障破坏的征象。 当肿瘤生长并活跃时,RPE泵功能下降,液体在视网膜下积聚。
超声内部低回声:提示肿瘤内血管密度高。 脉络膜黑色素瘤通常富含肿瘤内血管,常表现为内部低回声。 良性痣通常具有均匀的高回声内部回声模式。
彩色多普勒阳性(搏动性血流):表明肿瘤有自身的血液供应。 痣通常为彩色多普勒阴性,这是与黑色素瘤的重要鉴别点。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”TFSOM-UHHD标准的准确性验证
Section titled “TFSOM-UHHD标准的准确性验证”TFSOM-UHHD标准的敏感性和特异性验证研究正在进行中,预计临床使用准确性将得到提高。 未来可能实现结合5年风险计算模型的更精确的风险分层。
OCT血管成像的应用
Section titled “OCT血管成像的应用”利用OCT血管成像(OCTA)无创显示肿瘤内血管的研究正在进行中。 与彩色多普勒超声结合,有望进一步提高区分痣和黑色素瘤的准确性。
橙色色素的定量评估
Section titled “橙色色素的定量评估”利用眼底自发荧光定量评估脂褐素(橙色色素)的方法正在开发中。 目标是通过量化色素量来提高风险预测的准确性。
基于分子生物标志物的风险分层
Section titled “基于分子生物标志物的风险分层”利用液体活检(如血液中的循环肿瘤DNA)进行无创基因组评估的研究正在推进。 未来可能与眼底检查结果结合,用于早期检测恶性转化。
8. 参考文献
Section titled “8. 参考文献”- Finger PT. Laser treatment for choroidal melanoma. Surv Ophthalmol. 2023;68(2):211-224.
- Qureshi MB, Lentz PC, Xu TT, White LJ, Olsen TW, Pulido JS, et al. Choroidal Nevus Features Associated with Subspecialty Referral. Ophthalmol Retina. 2023;7(12):1097-1108. PMID: 37517800.
- Chien JL, Sioufi K, Surakiatchanukul T, Shields JA, Shields CL. Choroidal nevus: a review of prevalence, features, genetics, risks, and outcomes. Curr Opin Ophthalmol. 2017;28(3):228-237. PMID: 28141766.
