
Naevus choroïdien
1. Qu’est-ce qu’un naevus choroïdien ?
Section intitulée « 1. Qu’est-ce qu’un naevus choroïdien ? »Le naevus choroïdien est une lésion pigmentée bénigne résultant d’une prolifération de mélanocytes dans la choroïde. Il apparaît comme une lésion sous-rétinienne gris-noir arrondie à l’examen du fond d’œil et suit généralement une évolution stationnaire (non proliférative).
La prévalence est d’environ 5 % chez les Caucasiens et d’environ 0,3 % chez les Japonais, avec une distribution plus fréquente au pôle postérieur. On peut également en trouver à l’équateur ou près de l’ora serrata en périphérie extrême. Dans la plupart des cas, ils sont découverts fortuitement lors d’examens ophtalmologiques de routine chez l’adulte ou lors de l’évaluation d’autres pathologies.
La fréquence de transformation maligne est estimée à 0,5-3 % sur 10 ans dans les rapports occidentaux. Elle est considérée comme encore plus rare chez les Japonais, mais en cas de transformation maligne, elle est traitée comme un mélanome malin de la choroïde (mélanome choroïdien). Environ 10 % des mélanomes choroïdiens proviendraient de naevus connus.
Le naevus choroïdien est une lésion pigmentée bénigne et ne pose généralement pas de problème. Cependant, si plusieurs facteurs de risque tels que l’épaisseur ou l’épanchement liquidien sont présents, une surveillance régulière est nécessaire. Suivez les instructions de votre médecin pour des examens réguliers et consultez rapidement en cas de changement de vision, de myodésopsies ou de photopsies.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »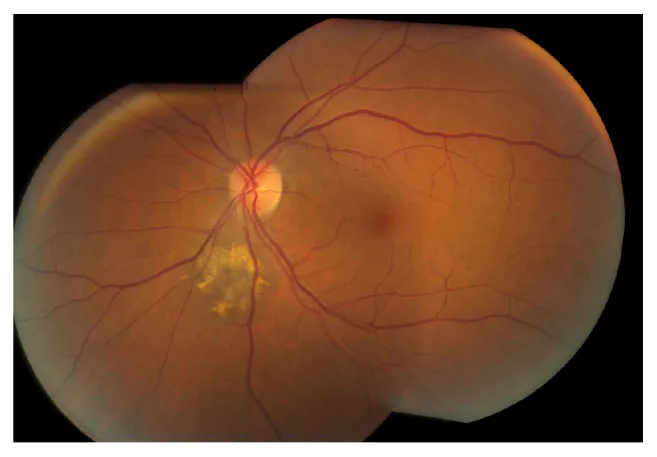
Symptômes subjectifs
Section intitulée « Symptômes subjectifs »La grande majorité des naevus choroïdiens sont asymptomatiques et découverts sans symptômes subjectifs. Cependant, si la lésion s’étend à la macula ou près de la papille optique, ou si elle s’accompagne d’un décollement sous-rétinien, les symptômes suivants peuvent apparaître.
- Baisse de l’acuité visuelle et métamorphopsie : en cas d’atteinte maculaire
- Photopsies : dues à une stimulation mécanique de la rétine
- Myodésopsies : rarement causées par une atteinte du vitré
Signes cliniques
Section intitulée « Signes cliniques »Les signes typiques d’un naevus choroïdien sont les suivants :
- Élévation sous-rétinienne arrondie, de couleur gris-noir
- Diamètre généralement inférieur à 3 diamètres papillaires (DD)
- Hauteur (épaisseur) inférieure à 2 mm, faible, ≤ 1/5 du diamètre
- Limites relativement nettes
- Évolution généralement stationnaire (non progressive)
Pigment orange (dépôts de lipofuscine) est un facteur prédictif important de transformation maligne. Il s’agit de dépôts de pigment de sénescence produits par l’EPR (épithélium pigmentaire rétinien), visibles en hyperfluorescence sur l’autofluorescence du fond d’œil.
Présence de liquide sous-rétinien est un signe d’alerte, suggérant une rupture de la barrière de l’EPR. En cas de liquide sous-rétinien, un bilan approfondi est nécessaire en envisageant une transformation maligne.
Évaluation du risque de transformation maligne selon TFSOM-UHHD
Section intitulée « Évaluation du risque de transformation maligne selon TFSOM-UHHD »Pour différencier un naevus choroïdien d’un mélanome choroïdien, on utilise les critères TFSOM-UHHD évaluant les 8 facteurs de risque suivants.
| Facteur | Critère | Signification |
|---|---|---|
| Épaisseur | Supérieure à 2 mm | Augmentation du volume tumoral |
| Liquide | Présence de liquide sous-rétinien | Rupture de la barrière de l’EPR |
| Symptômes | Photopsie, myodésopsies | Indicateur d’activité tumorale |
| Pigment orange | Dépôts de lipofuscine | Activité métabolique tumorale |
| Marge | À moins de 3 mm de la papille optique | Risque d’infiltration papillaire |
| Ultrasound Hollow (hypoéchogène) | Hypoéchogénicité interne | Densité vasculaire tumorale |
| Halo absent (absence de halo) | Absence de halo | Absence d’indicateur bénin |
| Drusen absent (absence de drusen) | Absence de drusen | Absence de changements chroniques |
La relation entre le nombre de facteurs de risque et la probabilité de croissance dans les 5 ans est présentée ci-dessous.
| Nombre de facteurs de risque | Probabilité de croissance à 5 ans |
|---|---|
| 0 | Environ 3 % |
| 1 | Environ 38 % |
| 2 ou plus | >50% |
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »Mécanisme de développement
Section intitulée « Mécanisme de développement »Le naevus choroïdien est une lésion bénigne résultant de la prolifération des mélanocytes de la choroïde, dont la cause exacte est inconnue. Il survient le plus souvent de manière sporadique.
Facteurs de risque de transformation maligne
Section intitulée « Facteurs de risque de transformation maligne »Les facteurs systémiques et cliniques suivants sont considérés comme augmentant le risque de transformation maligne :
- Iris clair, peau blanche (personnes d’origine caucasienne/nordique)
- Mélanocytose oculaire congénitale (maladie oculaire associée au naevus d’Ota)
- Antécédents familiaux de mélanome uvéal
- Syndrome de prédisposition tumorale BAP1 (mutation germinale de la protéine 1 associée à BRCA1)
Chaque facteur du TFSOM-UHHD reflète un risque local de transformation maligne.
- Pigment orange (lipofuscine) : L’accumulation de pigment de sénescence dérivé de l’EPR est un indicateur de l’activité tumorale
- Liquide sous-rétinien : Suggère une rupture de la barrière de l’EPR par la tumeur
- Épaisseur ≥ 2 mm : Reflète l’augmentation du volume tumoral
- Contact papillaire : risque accru d’infiltration du nerf optique
- Hypoéchogénicité interne à l’échographie : suggère la présence de vaisseaux intratumoraux
Anomalies génétiques et transformation maligne
Section intitulée « Anomalies génétiques et transformation maligne »La transformation maligne en mélanome choroïdien implique l’accumulation d’anomalies génétiques. Les principales anomalies associées sont la monosomie 3 et les mutations BAP1. Ces mutations sont fréquemment détectées dans le mélanome choroïdien mais généralement absentes dans les naevus bénins.
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »Examen du fond d’œil et photographie du fond d’œil
Section intitulée « Examen du fond d’œil et photographie du fond d’œil »L’examen du fond d’œil (ophtalmoscopie, photographie grand angle) est la base du dépistage et du suivi. L’enregistrement continu de photographies du fond d’œil est essentiel pour évaluer la croissance tumorale, et la photographie grand angle (Optos, etc.) est également utile.
Tomographie par cohérence optique (OCT)
Section intitulée « Tomographie par cohérence optique (OCT) »L’OCT est excellente pour visualiser le liquide sous-rétinien et les modifications de l’EPR. L’EDI-OCT (OCT à imagerie en profondeur) permet d’évaluer la structure choroïdienne et d’observer les signes suivants.
- Ombre choroïdienne optique
- Présence de liquide sous-rétinien
- Modifications de l’EPR (atrophie, soulèvement)
- Matériel hyperréflectif sous-rétinien (SRHM)
Autofluorescence du fond d’œil
Section intitulée « Autofluorescence du fond d’œil »Le pigment orange (lipofuscine) apparaît comme une hyperfluorescence plus brillante que les drusen. Utile pour évaluer les dépôts de lipofuscine et aider à déterminer le risque de transformation maligne.
Angiographie à la fluorescéine (FA)
Section intitulée « Angiographie à la fluorescéine (FA) »L’angiographie à la fluorescéine (FA) montre un motif d’hyperfluorescence. Une fluorescence de blocage due au pigment et une hyperfluorescence due aux dépôts de lipofuscine sont mélangées.
Échographie (mode B et Doppler couleur)
Section intitulée « Échographie (mode B et Doppler couleur) »L’échographie en mode B est utilisée pour mesurer la hauteur de la tumeur et évaluer le motif échogène interne. L’échographie Doppler couleur permet de vérifier la présence d’un flux sanguin pulsatile à la base de la tumeur. Dans le naevus choroïdien, le Doppler couleur est souvent négatif (pas de flux tumoral), tandis que dans le mélanome, il est souvent positif. Cette constatation est un point de différenciation important entre le naevus et le mélanome.
Diagnostic différentiel des tumeurs choroïdiennes (3 maladies principales)
Section intitulée « Diagnostic différentiel des tumeurs choroïdiennes (3 maladies principales) »Les caractéristiques des principales tumeurs choroïdiennes à différencier sont présentées ci-dessous.
| Mélanome malin | Hémangiome | Tumeur métastatique | |
|---|---|---|---|
| Couleur | Noir, gris, brun | Orange-rouge | Jaune-blanc |
| Forme | Haute | Fusiforme | En plaque |
| Décollement de la rétine | Aucun à modéré | Aucun à léger | Marqué |
| Croissance | Relativement lente | Aucune | Rapide |
Les autres diagnostics différentiels incluent l’hypertrophie congénitale de l’épithélium pigmentaire rétinien (CHRPE), l’hémorragie choroïdienne et le mélanocytome.
Il varie considérablement en fonction du nombre de facteurs de risque. Parmi les 8 éléments du TFSOM-UHHD, si aucun facteur de risque n’est présent, la probabilité de croissance dans les 5 ans est d’environ 3 %. Mais avec un facteur, elle est d’environ 38 %, et avec deux ou plus, elle dépasse 50 %. Un suivi régulier par échographie et photographie du fond d’œil est important ; en cas d’augmentation, on passe rapidement à une stratégie de traitement du mélanome malin choroïdien.
5. Traitement standard
Section intitulée « 5. Traitement standard »Le traitement de base du naevus choroïdien est la surveillance. Il n’existe actuellement aucun traitement médicamenteux ni indication chirurgicale pour le naevus lui-même ; un examen régulier du fond d’œil permet de surveiller l’augmentation de la lésion.
Lésions à faible risque (aucun facteur de risque, petit naevus)
Section intitulée « Lésions à faible risque (aucun facteur de risque, petit naevus) »Les petits naevus sans facteur de risque TFSOM-UHHD sont gérés comme à faible risque.
- Intervalle d’observation : examen du fond d’œil régulier tous les 12 à 24 mois
- Enregistrer toute augmentation de taille par photographie du fond d’œil et échographie en mode B
- Si aucun signe anormal, poursuivre la surveillance au même rythme
Lésions à risque intermédiaire/élevé (avec facteurs de risque)
Section intitulée « Lésions à risque intermédiaire/élevé (avec facteurs de risque) »Si au moins un facteur de risque TFSOM-UHHD est présent, une surveillance régulière attentive est nécessaire.
- Réexamen à 3 mois après l’examen initial (vérifier la croissance)
- Ensuite, poursuivre tous les 6 mois avec photographie du fond d’œil et échographie à vie
- Pour les petites tumeurs avec 3 facteurs de risque ou plus, envisager un traitement rapide sans attendre la preuve de croissance
En cas de croissance confirmée
Section intitulée « En cas de croissance confirmée »Si une croissance tumorale est confirmée pendant la surveillance, la stratégie thérapeutique doit être modifiée pour un mélanome malin de la choroïde. Les options thérapeutiques spécifiques sont déterminées en fonction de la taille de la tumeur et de la fonction visuelle, et comprennent la radiothérapie (curiethérapie par plaque, protonthérapie) ou l’énucléation (voir l’article sur le mélanome de la choroïde et du corps ciliaire pour plus de détails).
L’intervalle de surveillance varie en fonction du risque. Pour les lésions à faible risque sans facteurs de risque, un examen tous les 12 à 24 mois est recommandé. Pour les lésions à risque intermédiaire ou élevé avec facteurs de risque, un réexamen est effectué après les 3 premiers mois, puis un fond d’œil et une échographie tous les 6 mois à vie. La poursuite de la surveillance régulière est primordiale.
6. Physiopathologie et mécanismes détaillés
Section intitulée « 6. Physiopathologie et mécanismes détaillés »Mécanisme de la prolifération bénigne
Section intitulée « Mécanisme de la prolifération bénigne »Le naevus choroïdien est une lésion due à une prolifération bénigne locale des mélanocytes de la choroïde. Les mélanocytes choroïdiens normaux dérivent des cellules de la crête neurale et ont une capacité de production de pigment. Au stade de prolifération bénigne, la morphologie cellulaire est préservée, et il n’y a pas de prolifération invasive ni de métastase.
Mécanismes moléculaires de la transformation maligne
Section intitulée « Mécanismes moléculaires de la transformation maligne »La transformation maligne du naevus choroïdien en mélanome nécessite l’accumulation de plusieurs anomalies génétiques.
- Mutations GNAQ/GNA11 : Mutation initiatrice détectée dans environ 90 % des mélanomes choroïdiens. Elle entraîne une activation constitutive de la liaison au GTP et active de manière persistante plusieurs voies de signalisation, dont la voie MAPK.
- Monosomie 3 : Mutation secondaire fortement associée au risque métastatique.
- Mutations BAP1 : Associées au risque métastatique le plus élevé. Également connu comme gène causal du syndrome de prédisposition tumorale BAP1.
- Mutations SF3B1 : Risque métastatique intermédiaire. Caractérisées par des métastases tardives.
- Mutations EIF1AX : Risque métastatique le plus faible.
Au stade du naevus, ces mutations malignes ne sont généralement pas observées. On pense que l’accumulation d’anomalies génétiques entraîne une transformation progressive de bénin à malin.
Signification biologique des facteurs de risque
Section intitulée « Signification biologique des facteurs de risque »Chaque élément du TFSOM-UHHD reflète les pathologies suivantes.
Pigment orange (lipofuscine) : Pigment de vieillissement produit par l’EPR. Il reflète l’activité métabolique de la tumeur et l’interaction entre la tumeur et l’EPR ; plus l’activité tumorale est élevée, plus l’accumulation est importante.
Liquide sous-rétinien : signe suggérant une rupture de la barrière de l’EPR par la tumeur. Lorsque la tumeur se développe et s’active, la fonction de pompe de l’EPR diminue, entraînant une accumulation de liquide sous la rétine.
Faible échogénicité interne à l’échographie : suggère une densité élevée de vaisseaux intratumoraux. Dans le mélanome choroïdien, les vaisseaux intratumoraux sont abondants et montrent souvent une faible échogénicité interne. Les naevus bénins présentent généralement un motif échogène interne homogène et une échogénicité élevée.
Doppler couleur positif (flux pulsatile) : indique un apport vasculaire propre à la tumeur. Les naevus sont souvent négatifs au Doppler couleur, ce qui constitue un point de différenciation important avec le mélanome.
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Validation de la précision des critères TFSOM-UHHD
Section intitulée « Validation de la précision des critères TFSOM-UHHD »Les études de validation de la sensibilité et de la spécificité des critères TFSOM-UHHD se poursuivent, et on espère améliorer la précision de leur utilisation clinique. À l’avenir, une stratification plus précise des risques intégrant un modèle de calcul du risque à 5 ans pourrait être réalisée.
Application de l’angiographie OCT
Section intitulée « Application de l’angiographie OCT »La visualisation non invasive des vaisseaux intratumoraux par angiographie OCT (OCTA) est à l’étude. Combinée à l’échographie Doppler couleur, elle devrait améliorer encore la précision de la différenciation entre naevus et mélanome.
Évaluation quantitative du pigment orange
Section intitulée « Évaluation quantitative du pigment orange »Le développement d’une méthode d’évaluation quantitative de la lipofuscine (pigment orange) par autofluorescence du fond d’œil progresse. L’objectif est d’améliorer la précision de la prédiction du risque par quantification de la quantité de pigment.
Stratification du risque par biomarqueurs moléculaires
Section intitulée « Stratification du risque par biomarqueurs moléculaires »La recherche sur l’évaluation génomique non invasive par biopsie liquide (ADN tumoral circulant dans le sang, etc.) progresse. À l’avenir, combinée aux observations du fond d’œil, elle pourrait être utilisée pour la détection précoce de la transformation maligne.
8. Références
Section intitulée « 8. Références »- Finger PT. Laser treatment for choroidal melanoma. Surv Ophthalmol. 2023;68(2):211-224.
- Qureshi MB, Lentz PC, Xu TT, White LJ, Olsen TW, Pulido JS, et al. Choroidal Nevus Features Associated with Subspecialty Referral. Ophthalmol Retina. 2023;7(12):1097-1108. PMID: 37517800.
- Chien JL, Sioufi K, Surakiatchanukul T, Shields JA, Shields CL. Choroidal nevus: a review of prevalence, features, genetics, risks, and outcomes. Curr Opin Ophthalmol. 2017;28(3):228-237. PMID: 28141766.
