
Aderhautnävus
1. Was ist ein Aderhautnävus?
Abschnitt betitelt „1. Was ist ein Aderhautnävus?“Ein Aderhautnävus ist eine gutartige pigmentierte Läsion, die durch eine benigne Proliferation von Melanozyten in der Aderhaut entsteht. Im Fundus erscheint er als grau-schwarze, runde subretinale Läsion und verläuft in der Regel stationär (nicht wachsend).
Die Prävalenz beträgt bei Westlern etwa 5 %, bei Japanern etwa 0,3 %, mit einer häufigeren Verteilung am hinteren Pol. Sie können auch am Äquator oder in der äußersten Peripherie nahe der Ora serrata gefunden werden. In den meisten Fällen werden sie zufällig bei routinemäßigen augenärztlichen Untersuchungen von Erwachsenen oder bei der Beurteilung anderer Erkrankungen entdeckt.
Die Häufigkeit einer malignen Transformation wird in westlichen Berichten mit 0,5–3 % pro 10 Jahre angegeben. Bei Japanern wird sie als noch seltener angesehen, aber im Falle einer malignen Transformation wird sie als malignes Aderhautmelanom (Aderhautmelanom) behandelt. Etwa 10 % der Aderhautmelanome entstehen aus bekannten Nävi.
Ein Aderhautnävus ist eine gutartige pigmentierte Läsion und in den meisten Fällen unbedenklich. Wenn jedoch mehrere Risikofaktoren wie Dicke oder Flüssigkeitsansammlung vorliegen, ist eine regelmäßige Überwachung erforderlich. Befolgen Sie die Anweisungen Ihres Arztes für regelmäßige Untersuchungen und suchen Sie frühzeitig einen Arzt auf, wenn neue Symptome wie Sehveränderungen, Floater oder Photopsien auftreten.
2. Hauptsymptome und klinische Befunde
Abschnitt betitelt „2. Hauptsymptome und klinische Befunde“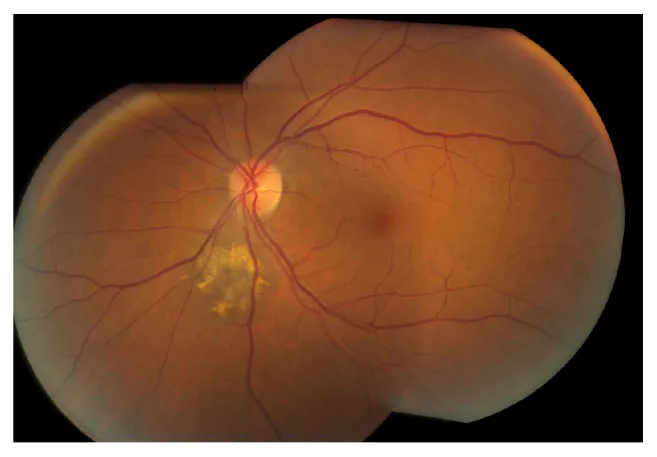
Subjektive Symptome
Abschnitt betitelt „Subjektive Symptome“Die überwiegende Mehrheit der Aderhautnävi ist asymptomatisch und wird ohne subjektive Symptome entdeckt. Wenn die Läsion jedoch die Makula oder die Nähe der Papille betrifft oder mit subretinaler Flüssigkeit einhergeht, können die folgenden Symptome auftreten.
- Sehverschlechterung und Metamorphopsie : bei Beteiligung der Makula
- Photopsien : durch mechanische Stimulation der Netzhaut
- Mouches volantes : selten durch Beteiligung des Glaskörpers verursacht
Klinische Befunde
Abschnitt betitelt „Klinische Befunde“Typische Befunde eines Aderhautnävus sind:
- Grauschwarze, rundliche subretinale Erhebung
- Durchmesser meist ≤ 3 Papillendurchmesser (DD)
- Höhe (Dicke) < 2 mm, flach, ≤ 1/5 des Durchmessers
- Relativ scharfe Begrenzung
- In der Regel stationärer (nicht progredienter) Verlauf
Orangefarbenes Pigment (Lipofuszinablagerungen) ist ein wichtiger Prädiktor für maligne Transformation. Es handelt sich um Ablagerungen von Alterungspigment, das vom RPE (retinales Pigmentepithel) produziert wird, und zeigt sich in der Fundusautofluoreszenz als Hyperfluoreszenz.
Vorhandensein von subretinaler Flüssigkeit ist ein Warnzeichen, das auf eine Störung der RPE-Barriere hindeutet. Bei subretinaler Flüssigkeit ist eine gründliche Abklärung unter Berücksichtigung einer malignen Transformation erforderlich.
Risikobewertung der malignen Transformation mittels TFSOM-UHHD
Abschnitt betitelt „Risikobewertung der malignen Transformation mittels TFSOM-UHHD“Zur Unterscheidung zwischen Aderhautnävus und Aderhautmelanom werden die TFSOM-UHHD-Kriterien verwendet, die die folgenden 8 Risikofaktoren bewerten.
| Faktor | Kriterium | Bedeutung |
|---|---|---|
| Dicke | Über 2 mm | Zunahme des Tumorvolumens |
| Flüssigkeit | Vorhandensein subretinaler Flüssigkeit | RPE-Barriere-Störung |
| Symptome | Photopsie, Mouches volantes | Indikator für Tumoraktivität |
| Oranges Pigment | Lipofuszin-Ablagerungen | Tumorstoffwechselaktivität |
| Rand | Innerhalb von 3 mm zur Papille | Risiko einer Papilleninfiltration |
| Ultrasound Hollow (hypoechogen) | Interne Hypoechogenität | Tumorvaskuläre Dichte |
| Halo absent (fehlender Halo) | Kein Halo | Fehlen eines benignen Indikators |
| Drusen absent (fehlende Drusen) | Keine Drusen | Fehlen chronischer Veränderungen |
Der Zusammenhang zwischen der Anzahl der Risikofaktoren und der Wahrscheinlichkeit eines Wachstums innerhalb von 5 Jahren ist unten dargestellt.
| Anzahl der Risikofaktoren | 5-Jahres-Wachstumswahrscheinlichkeit |
|---|---|
| 0 | Etwa 3 % |
| 1 | Etwa 38 % |
| 2 oder mehr | >50% |
3. Ursachen und Risikofaktoren
Abschnitt betitelt „3. Ursachen und Risikofaktoren“Entstehungsmechanismus
Abschnitt betitelt „Entstehungsmechanismus“Das Aderhautnävus ist eine gutartige Proliferation von Melanozyten der Aderhaut, deren genaue Ursache unbekannt ist. Es tritt meist sporadisch auf.
Risikofaktoren für maligne Transformation
Abschnitt betitelt „Risikofaktoren für maligne Transformation“Die folgenden systemischen und klinischen Faktoren gelten als risikosteigernd für eine maligne Transformation:
- Helle Iris, weiße Haut (kaukasische/nordische Herkunft)
- Angeborene okuläre Melanozytose (Augenerkrankung im Zusammenhang mit Nävus Ota)
- Familienanamnese von uvealem Melanom
- BAP1-Tumorprädispositionssyndrom (Keimbahnmutation des BRCA1-assoziierten Proteins 1)
Jeder Faktor des TFSOM-UHHD spiegelt ein lokales Risiko für maligne Transformation wider.
- Orangefarbenes Pigment (Lipofuszin) : Die Ansammlung von altersbedingtem Pigment aus dem RPE ist ein Indikator für Tumoraktivität
- Subretinale Flüssigkeit : Deutet auf eine Störung der RPE-Barriere durch den Tumor hin
- Dicke ≥ 2 mm : Spiegelt die Zunahme des Tumorvolumens wider
- Papillenkontakt : erhöhtes Risiko einer Infiltration des Sehnervs
- Interne Hypoechogenität im Ultraschall : deutet auf das Vorhandensein von Tumorgefäßen hin
Genetische Anomalien und maligne Transformation
Abschnitt betitelt „Genetische Anomalien und maligne Transformation“Die maligne Transformation zum Aderhautmelanom beinhaltet die Akkumulation genetischer Anomalien. Wichtige assoziierte Anomalien sind Monosomie 3 und BAP1-Mutationen. Diese Mutationen werden häufig im Aderhautmelanom nachgewiesen, aber in gutartigen Nävi normalerweise nicht gefunden.
4. Diagnose und Untersuchungsmethoden
Abschnitt betitelt „4. Diagnose und Untersuchungsmethoden“Fundusuntersuchung und Fundusfotografie
Abschnitt betitelt „Fundusuntersuchung und Fundusfotografie“Die Fundusuntersuchung (Ophthalmoskopie, Weitwinkel-Fundusfotografie) ist die Grundlage für Screening und Nachsorge. Die kontinuierliche Aufzeichnung von Fundusfotografien ist für die Beurteilung des Tumorwachstums unerlässlich, und die Weitwinkel-Fundusfotografie (Optos usw.) ist ebenfalls nützlich.
Optische Kohärenztomographie (OCT)
Abschnitt betitelt „Optische Kohärenztomographie (OCT)“Die OCT eignet sich hervorragend zur Darstellung von subretinaler Flüssigkeit und RPE-Veränderungen. Die EDI-OCT (tiefenbildgebende OCT) ermöglicht die Beurteilung der Aderhautstruktur, wobei folgende Befunde beobachtet werden.
- Optische Aderhautverschattung
- Vorhandensein subretinaler Flüssigkeit
- RPE-Veränderungen (Atrophie, Abhebung)
- Subretinales hyperreflektives Material (SRHM)
Fundus-Autofluoreszenz
Abschnitt betitelt „Fundus-Autofluoreszenz“Das orangefarbene Pigment (Lipofuszin) erscheint als hellere Hyperfluoreszenz als Drusen. Nützlich zur Beurteilung von Lipofuszinablagerungen und hilfreich bei der Bestimmung des Risikos einer malignen Transformation.
Fluoreszenzangiographie (FA)
Abschnitt betitelt „Fluoreszenzangiographie (FA)“In der FA (Fluoreszenzangiographie) wird ein hyperfluoreszierendes Muster beobachtet. Blockierungsfluoreszenz durch Pigment und Hyperfluoreszenz durch Lipofuszinablagerungen sind gemischt.
Ultraschalluntersuchung (B-Mode und Farbdoppler)
Abschnitt betitelt „Ultraschalluntersuchung (B-Mode und Farbdoppler)“B-Mode-Ultraschall wird zur Messung der Tumorhöhe und Beurteilung des internen Echomusters verwendet. Farbdoppler-Ultraschall kann das Vorhandensein eines pulsierenden Blutflusses an der Tumorbasis bestätigen. Bei einem Aderhautnävus ist der Farbdoppler oft negativ (kein Tumorblutfluss), während er bei einem Melanom oft positiv ist. Dieser Befund ist ein wichtiger Unterscheidungspunkt zwischen Nävus und Melanom.
Differenzialdiagnose von Aderhauttumoren (3 Haupterkrankungen)
Abschnitt betitelt „Differenzialdiagnose von Aderhauttumoren (3 Haupterkrankungen)“Die Merkmale der wichtigsten zu unterscheidenden Aderhauttumoren sind unten aufgeführt.
| Malignes Melanom | Hämangiom | Metastatischer Tumor | |
|---|---|---|---|
| Farbe | Schwarz, grau, braun | Orange-rot | Gelb-weiß |
| Form | Hoch | Spindelförmig | Plattenförmig |
| Netzhautablösung | Keine bis mäßig | Keine bis leicht | Ausgeprägt |
| Wachstum | Relativ langsam | Keines | Schnell |
Weitere Differenzialdiagnosen sind die kongenitale Hypertrophie des retinalen Pigmentepithels (CHRPE), Aderhautblutung und Melanozytom.
Es variiert stark je nach Anzahl der Risikofaktoren. Von den 8 Punkten des TFSOM-UHHD beträgt die Wahrscheinlichkeit eines Wachstums innerhalb von 5 Jahren bei 0 Risikofaktoren etwa 3 %. Bei einem Faktor liegt sie bei etwa 38 %, bei zwei oder mehr über 50 %. Regelmäßige Nachkontrollen mittels Ultraschall und Fundusfotografie sind wichtig; bei Zunahme wird schnell auf die Behandlungsstrategie eines malignen Aderhautmelanoms umgestellt.
5. Standardbehandlung
Abschnitt betitelt „5. Standardbehandlung“Die Grundbehandlung des Aderhautnävus ist die Beobachtung. Derzeit gibt es keine medikamentöse Therapie oder Operationsindikation für den Nävus selbst; regelmäßige Fundusuntersuchungen überwachen das Wachstum der Läsion.
Niedrigrisiko-Läsionen (keine Risikofaktoren, kleiner Nävus)
Abschnitt betitelt „Niedrigrisiko-Läsionen (keine Risikofaktoren, kleiner Nävus)“Kleine Nävi ohne TFSOM-UHHD-Risikofaktoren werden als niedriges Risiko eingestuft.
- Beobachtungsintervall: Regelmäßige Fundusuntersuchung alle 12–24 Monate
- Dokumentation einer Größenzunahme mittels Fundusfotografie und B-Bild-Sonographie
- Bei unauffälligen Befunden Fortführung der Nachsorge im gleichen Rhythmus
Mittel- bis Hochrisikoläsionen (mit Risikofaktoren)
Abschnitt betitelt „Mittel- bis Hochrisikoläsionen (mit Risikofaktoren)“Bei Vorliegen von mindestens einem Risikofaktor nach TFSOM-UHHD ist eine sorgfältige regelmäßige Nachsorge erforderlich.
- Nachuntersuchung 3 Monate nach der Erstuntersuchung (Überprüfung auf Wachstum)
- Danach alle 6 Monate Fundusfotografie und Sonographie lebenslang fortsetzen
- Bei kleinen Tumoren mit 3 oder mehr Risikofaktoren sollte eine rasche Behandlung ohne Abwarten des Wachstumsnachweises erwogen werden
Bei bestätigtem Wachstum
Abschnitt betitelt „Bei bestätigtem Wachstum“Wird während der Nachsorge ein Tumorwachstum bestätigt, ist die Behandlungsstrategie auf ein malignes Aderhautmelanom umzustellen. Die spezifischen Behandlungsoptionen werden je nach Tumorgröße und Sehfunktion festgelegt und umfassen Strahlentherapie (Brachytherapie mit Plaque, Protonentherapie) oder Enukleation (siehe Artikel zum Aderhaut- und Ziliarkörpermelanom für Details).
Das Überwachungsintervall variiert je nach Risiko. Bei risikoarmen Läsionen ohne Risikofaktoren wird eine Untersuchung alle 12–24 Monate empfohlen. Bei mittel- bis hochriskanten Läsionen mit Risikofaktoren erfolgt eine erneute Untersuchung nach den ersten 3 Monaten, danach lebenslang alle 6 Monate eine Funduskopie und Ultraschalluntersuchung. Die Fortsetzung der regelmäßigen Überwachung ist am wichtigsten.
6. Pathophysiologie und detaillierte Entstehungsmechanismen
Abschnitt betitelt „6. Pathophysiologie und detaillierte Entstehungsmechanismen“Mechanismus der benignen Proliferation
Abschnitt betitelt „Mechanismus der benignen Proliferation“Das Aderhautnävus ist eine Läsion, die durch lokale benigne Proliferation von Melanozyten der Aderhaut entsteht. Normale Aderhautmelanozyten stammen von Neuralleistenzellen ab und besitzen die Fähigkeit zur Pigmentproduktion. Im Stadium der benignen Proliferation bleibt die Zellmorphologie erhalten, und es kommt zu keiner invasiven Proliferation oder Metastasierung.
Molekulare Mechanismen der malignen Transformation
Abschnitt betitelt „Molekulare Mechanismen der malignen Transformation“Für die maligne Transformation vom Aderhautnävus zum Melanom ist die Akkumulation mehrerer genetischer Anomalien erforderlich.
- GNAQ/GNA11-Mutationen: Initiierende Mutation, die bei etwa 90 % der Aderhautmelanome nachgewiesen wird. Sie führt zu einem konstitutiven GTP-Bindungsaktivierungszustand und aktiviert dauerhaft mehrere Signalwege, darunter den MAPK-Weg.
- Monosomie 3: Sekundäre Mutation, die stark mit dem Metastasierungsrisiko assoziiert ist.
- BAP1-Mutationen: Mit dem höchsten Metastasierungsrisiko assoziiert. Auch als ursächliches Gen des BAP1-Tumorprädispositionssyndroms bekannt.
- SF3B1-Mutationen: Mittleres Metastasierungsrisiko. Gekennzeichnet durch späte Metastasierung.
- EIF1AX-Mutationen: Geringstes Metastasierungsrisiko.
Im Nävusstadium werden diese malignen Mutationen normalerweise nicht beobachtet. Es wird angenommen, dass die Akkumulation genetischer Anomalien zu einer kontinuierlichen Veränderung von benigne zu maligne führt.
Biologische Bedeutung der Risikofaktoren
Abschnitt betitelt „Biologische Bedeutung der Risikofaktoren“Jeder Punkt des TFSOM-UHHD spiegelt die folgenden Pathologien wider.
Orangefarbenes Pigment (Lipofuszin): Alterspigment, das vom RPE produziert wird. Es spiegelt die metabolische Aktivität des Tumors und die Interaktion zwischen Tumor und RPE wider; je höher die Tumoraktivität, desto stärker die Akkumulation.
Subretinale Flüssigkeit: Hinweis auf eine Störung der RPE-Barriere durch den Tumor. Wenn der Tumor wächst und aktiv wird, nimmt die RPE-Pumpfunktion ab, und es sammelt sich Flüssigkeit unter der Netzhaut.
Niedrige interne Echogenität im Ultraschall: deutet auf eine hohe Dichte intratumoraler Gefäße hin. Beim Aderhautmelanom sind die intratumoralen Gefäße reichlich vorhanden und zeigen oft eine niedrige interne Echogenität. Gutartige Nävi weisen in der Regel ein homogenes internes Echomuster mit hoher Echogenität auf.
Farbdoppler-positiv (pulsatiler Blutfluss): zeigt eine eigene Blutversorgung des Tumors an. Nävi sind häufig farbdoppler-negativ, was ein wichtiges Unterscheidungsmerkmal zum Melanom darstellt.
7. Aktuelle Forschung und zukünftige Perspektiven
Abschnitt betitelt „7. Aktuelle Forschung und zukünftige Perspektiven“Validierung der Genauigkeit der TFSOM-UHHD-Kriterien
Abschnitt betitelt „Validierung der Genauigkeit der TFSOM-UHHD-Kriterien“Validierungsstudien zur Sensitivität und Spezifität der TFSOM-UHHD-Kriterien werden fortgesetzt, und es wird eine Verbesserung der klinischen Anwendungsgenauigkeit erwartet. In Zukunft könnte eine präzisere Risikostratifizierung unter Einbeziehung eines 5-Jahres-Risikoberechnungsmodells möglich sein.
Anwendung der OCT-Angiographie
Abschnitt betitelt „Anwendung der OCT-Angiographie“Die nicht-invasive Darstellung intratumoraler Gefäße mittels OCT-Angiographie (OCTA) wird erforscht. In Kombination mit dem Farbdoppler-Ultraschall wird eine weitere Verbesserung der Unterscheidungsgenauigkeit zwischen Nävus und Melanom erwartet.
Quantitative Bewertung des orangefarbenen Pigments
Abschnitt betitelt „Quantitative Bewertung des orangefarbenen Pigments“Die Entwicklung einer quantitativen Bewertungsmethode für Lipofuszin (orangefarbenes Pigment) mittels Fundus-Autofluoreszenz schreitet voran. Ziel ist die Verbesserung der Risikovorhersagegenauigkeit durch Quantifizierung der Pigmentmenge.
Risikostratifizierung durch molekulare Biomarker
Abschnitt betitelt „Risikostratifizierung durch molekulare Biomarker“Die Forschung zur nicht-invasiven genomischen Bewertung mittels Flüssigbiopsie (zirkulierende Tumor-DNA im Blut usw.) schreitet voran. In Zukunft könnte sie in Kombination mit Fundusbefunden zur Früherkennung einer malignen Transformation eingesetzt werden.
8. Referenzen
Abschnitt betitelt „8. Referenzen“- Finger PT. Laser treatment for choroidal melanoma. Surv Ophthalmol. 2023;68(2):211-224.
- Qureshi MB, Lentz PC, Xu TT, White LJ, Olsen TW, Pulido JS, et al. Choroidal Nevus Features Associated with Subspecialty Referral. Ophthalmol Retina. 2023;7(12):1097-1108. PMID: 37517800.
- Chien JL, Sioufi K, Surakiatchanukul T, Shields JA, Shields CL. Choroidal nevus: a review of prevalence, features, genetics, risks, and outcomes. Curr Opin Ophthalmol. 2017;28(3):228-237. PMID: 28141766.
