
Nevo coroidale
1. Cos’è il nevo coroidale?
Sezione intitolata “1. Cos’è il nevo coroidale?”Il nevo coroidale è una lesione pigmentata benigna derivante dalla proliferazione benigna dei melanociti nella coroide. All’esame del fondo oculare appare come una lesione sottoretinica grigio-nera di forma rotondeggiante e di solito ha un decorso stazionario (non in crescita).
La prevalenza è di circa il 5% nei caucasici e circa lo 0,3% nei giapponesi, con una distribuzione più frequente al polo posteriore. Può essere riscontrato anche all’equatore o nella periferia estrema vicino all’ora serrata. Nella maggior parte dei casi viene scoperto incidentalmente durante visite oculistiche di routine in adulti o durante la valutazione di altre patologie.
La frequenza di trasformazione maligna è riportata come 0,5-3% in 10 anni nei rapporti occidentali. Nei giapponesi è considerata ancora più rara, ma in caso di trasformazione maligna viene trattata come melanoma maligno coroidale (melanoma coroidale). Circa il 10% dei melanomi coroidali origina da nevi noti.
Il nevo coroidale è una lesione pigmentata benigna e nella maggior parte dei casi non causa problemi. Tuttavia, se sono presenti più fattori di rischio come spessore o accumulo di liquido, è necessario un monitoraggio regolare. Seguire le istruzioni del medico per controlli regolari e consultare tempestivamente in caso di nuovi sintomi come cambiamenti della vista, miodesopsie o fotopsie.
2. Principali sintomi e segni clinici
Sezione intitolata “2. Principali sintomi e segni clinici”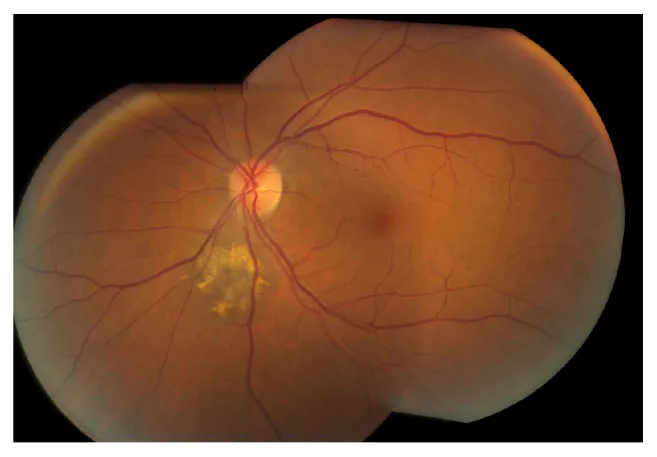
Sintomi soggettivi
Sezione intitolata “Sintomi soggettivi”La stragrande maggioranza dei nevi coroidali è asintomatica e viene scoperta senza sintomi soggettivi. Tuttavia, se la lesione si estende alla macula o in prossimità della papilla ottica, o se è associata a liquido sottoretinico, possono comparire i seguenti sintomi.
- Riduzione dell’acuità visiva e metamorfopsia : in caso di coinvolgimento maculare
- Fotopsie : dovute a stimolazione meccanica della retina
- Miodesopsie : raramente causate da interessamento del vitreo
Reperti clinici
Sezione intitolata “Reperti clinici”I reperti tipici di un nevo coroidale sono i seguenti:
- Rialzo sottoretinico rotondeggiante di colore grigio-nero
- Diametro solitamente entro 3 diametri papillari (DD)
- Altezza (spessore) inferiore a 2 mm, basso, ≤ 1/5 del diametro
- Margini relativamente netti
- Decorso solitamente stazionario (non progressivo)
Pigmento arancione (depositi di lipofuscina) è un importante predittore di trasformazione maligna. Si tratta di depositi di pigmento di invecchiamento prodotti dall’RPE (epitelio pigmentato retinico), visibili come iperfluorescenza all’autofluorescenza del fundus.
Presenza di liquido sottoretinico è un segno di allarme, che suggerisce una rottura della barriera dell’RPE. In caso di liquido sottoretinico, è necessaria una valutazione approfondita considerando una trasformazione maligna.
Valutazione del rischio di trasformazione maligna secondo TFSOM-UHHD
Sezione intitolata “Valutazione del rischio di trasformazione maligna secondo TFSOM-UHHD”Per differenziare un nevo coroidale da un melanoma coroidale, si utilizzano i criteri TFSOM-UHHD che valutano i seguenti 8 fattori di rischio.
| Fattore | Criterio | Significato |
|---|---|---|
| Spessore | Superiore a 2 mm | Aumento del volume tumorale |
| Liquido | Presenza di liquido sottoretinico | Rottura della barriera dell’EPR |
| Sintomi | Fotopsia, miodesopsie | Indicatore di attività tumorale |
| Pigmento arancione | Depositi di lipofuscina | Attività metabolica tumorale |
| Margine | Entro 3 mm dal disco ottico | Rischio di infiltrazione del disco |
| Ultrasound Hollow (ipoecogeno) | Ipoecogenicità interna | Densità vascolare tumorale |
| Halo absent (assenza di alone) | Assenza di alone | Assenza di indicatore benigno |
| Drusen absent (assenza di drusen) | Assenza di drusen | Assenza di cambiamenti cronici |
La relazione tra il numero di fattori di rischio e la probabilità di crescita entro 5 anni è mostrata di seguito.
| Numero di fattori di rischio | Probabilità di crescita a 5 anni |
|---|---|
| 0 | Circa 3% |
| 1 | Circa 38% |
| 2 o più | >50% |
3. Cause e fattori di rischio
Sezione intitolata “3. Cause e fattori di rischio”Meccanismo di insorgenza
Sezione intitolata “Meccanismo di insorgenza”Il nevo coroideale è una proliferazione benigna dei melanociti della coroide, la cui causa esatta è sconosciuta. Si verifica più spesso sporadicamente.
Fattori di rischio di trasformazione maligna
Sezione intitolata “Fattori di rischio di trasformazione maligna”I seguenti fattori sistemici e clinici sono considerati aumentare il rischio di trasformazione maligna:
- Iride chiara, pelle bianca (persone di origine caucasica/nordica)
- Melanocitosi oculare congenita (malattia oculare associata al nevo di Ota)
- Anamnesi familiare di melanoma uveale
- Sindrome di predisposizione tumorale BAP1 (mutazione germinale della proteina 1 associata a BRCA1)
Ciascun fattore del TFSOM-UHHD riflette un rischio locale di trasformazione maligna.
- Pigmento arancione (lipofuscina) : L’accumulo di pigmento senescente derivato dall’EPR è un indicatore di attività tumorale
- Liquido sottoretinico : Suggerisce una rottura della barriera dell’EPR da parte del tumore
- Spessore ≥ 2 mm : Riflette l’aumento del volume tumorale
- Contatto papillare : aumento del rischio di infiltrazione del nervo ottico
- Ipoecogenicità interna all’ecografia : suggerisce la presenza di vasi intratumorali
Anomalie genetiche e trasformazione maligna
Sezione intitolata “Anomalie genetiche e trasformazione maligna”La trasformazione maligna in melanoma coroidale comporta l’accumulo di anomalie genetiche. Le principali anomalie associate sono la monosomia 3 e le mutazioni BAP1. Queste mutazioni sono frequentemente rilevate nel melanoma coroidale ma di solito non sono presenti nei nevi benigni.
4. Diagnosi e metodi di esame
Sezione intitolata “4. Diagnosi e metodi di esame”Esame del fondo oculare e fotografia del fondo
Sezione intitolata “Esame del fondo oculare e fotografia del fondo”L’esame del fondo oculare (oftalmoscopia, fotografia grandangolare del fondo) è la base per lo screening e il follow-up. La registrazione continua di fotografie del fondo è essenziale per valutare la crescita tumorale, e la fotografia grandangolare del fondo (Optos, ecc.) è anch’essa utile.
Tomografia a coerenza ottica (OCT)
Sezione intitolata “Tomografia a coerenza ottica (OCT)”L’OCT è eccellente per visualizzare il liquido sottoretinico e le alterazioni dell’EPR. L’EDI-OCT (OCT a imaging profondo) consente di valutare la struttura coroidale e si osservano i seguenti reperti.
- Ombreggiatura coroidale ottica
- Presenza di liquido sottoretinico
- Alterazioni dell’EPR (atrofia, sollevamento)
- Materiale iperriflettente sottoretinico (SRHM)
Autofluorescenza del fondo oculare
Sezione intitolata “Autofluorescenza del fondo oculare”Il pigmento arancione (lipofuscina) appare come un’iperfluorescenza più brillante rispetto ai drusen. Utile per valutare i depositi di lipofuscina e aiuta a determinare il rischio di trasformazione maligna.
Angiografia con fluoresceina (FA)
Sezione intitolata “Angiografia con fluoresceina (FA)”Nella FA (angiografia con fluoresceina) si osserva un pattern di iperfluorescenza. La fluorescenza di blocco dovuta al pigmento e l’iperfluorescenza dovuta ai depositi di lipofuscina sono mescolate.
Ecografia (B-mode e color Doppler)
Sezione intitolata “Ecografia (B-mode e color Doppler)”L’ecografia in B-mode viene utilizzata per misurare l’altezza del tumore e valutare il pattern ecogeno interno. L’ecografia color Doppler consente di verificare la presenza di flusso sanguigno pulsatile alla base del tumore. Nel nevo coroidale, il color Doppler è spesso negativo (nessun flusso tumorale), mentre nel melanoma è spesso positivo. Questo reperto è un importante punto di differenziazione tra nevo e melanoma.
Diagnosi differenziale dei tumori coroidali (3 malattie principali)
Sezione intitolata “Diagnosi differenziale dei tumori coroidali (3 malattie principali)”Le caratteristiche dei principali tumori coroidali da differenziare sono mostrate di seguito.
| Melanoma maligno | Emangioma | Tumore metastatico | |
|---|---|---|---|
| Colore | Nero, grigio, marrone | Arancio-rosso | Giallo-bianco |
| Forma | Alta | Fusiforme | A placca |
| Distacco di retina | Assente o moderato | Assente o lieve | Marcato |
| Crescita | Relativamente lenta | Nessuna | Rapida |
Altre diagnosi differenziali includono l’ipertrofia congenita dell’epitelio pigmentato retinico (CHRPE), l’emorragia coroidale e il melanocitoma.
Varia notevolmente in base al numero di fattori di rischio. Degli 8 elementi del TFSOM-UHHD, se non ci sono fattori di rischio, la probabilità di crescita entro 5 anni è circa il 3%. Ma con un fattore è circa il 38%, e con due o più supera il 50%. È importante un follow-up regolare con ecografia e fotografia del fondo oculare; in caso di aumento, si passa rapidamente a una strategia di trattamento per il melanoma maligno coroidale.
5. Trattamento standard
Sezione intitolata “5. Trattamento standard”Il trattamento di base del nevo coroidale è l’osservazione. Attualmente non esiste una terapia farmacologica o un’indicazione chirurgica per il nevo stesso; un esame regolare del fondo oculare monitora la crescita della lesione.
Lesioni a basso rischio (nessun fattore di rischio, nevo piccolo)
Sezione intitolata “Lesioni a basso rischio (nessun fattore di rischio, nevo piccolo)”I piccoli nevi senza fattori di rischio TFSOM-UHHD sono gestiti come a basso rischio.
- Intervallo di osservazione: esame del fondo oculare regolare ogni 12-24 mesi
- Registrare l’eventuale aumento di dimensioni con fotografia del fondo oculare ed ecografia in modalità B
- Se non si riscontrano anomalie, proseguire il follow-up con la stessa cadenza
Lesioni a rischio medio-alto (con fattori di rischio)
Sezione intitolata “Lesioni a rischio medio-alto (con fattori di rischio)”Se è presente almeno un fattore di rischio TFSOM-UHHD, è necessario un attento follow-up regolare.
- Riesame a 3 mesi dal primo esame (verificare la crescita)
- Successivamente, proseguire ogni 6 mesi con fotografia del fondo oculare ed ecografia per tutta la vita
- Per piccoli tumori con 3 o più fattori di rischio, considerare un trattamento rapido senza attendere la prova di crescita
In caso di crescita confermata
Sezione intitolata “In caso di crescita confermata”Se durante il follow-up viene confermata la crescita del tumore, la strategia terapeutica deve essere modificata in melanoma maligno coroidale. Le opzioni terapeutiche specifiche sono determinate in base alle dimensioni del tumore e alla funzione visiva e includono la radioterapia (brachiterapia con placca, protonterapia) o l’enucleazione (per i dettagli, vedere l’articolo sul melanoma coroidale e del corpo ciliare).
L’intervallo di sorveglianza varia in base al rischio. Per le lesioni a basso rischio senza fattori di rischio, si consiglia un esame ogni 12-24 mesi. Per le lesioni a rischio medio-alto con fattori di rischio, si effettua un riesame dopo i primi 3 mesi, quindi si prosegue per tutta la vita con esame del fondo oculare ed ecografia ogni 6 mesi. La cosa più importante è continuare il monitoraggio regolare.
6. Fisiopatologia e meccanismi dettagliati di insorgenza
Sezione intitolata “6. Fisiopatologia e meccanismi dettagliati di insorgenza”Meccanismo della proliferazione benigna
Sezione intitolata “Meccanismo della proliferazione benigna”Il nevo coroideo è una lesione dovuta alla proliferazione benigna locale dei melanociti della coroide. I melanociti coroidei normali derivano dalle cellule della cresta neurale e hanno capacità di produzione di pigmento. Nella fase di proliferazione benigna, la morfologia cellulare è preservata e non si verificano proliferazione invasiva o metastasi.
Meccanismi molecolari della trasformazione maligna
Sezione intitolata “Meccanismi molecolari della trasformazione maligna”La trasformazione maligna del nevo coroideo in melanoma richiede l’accumulo di diverse anomalie genetiche.
- Mutazioni GNAQ/GNA11: Mutazione iniziale rilevata in circa il 90% dei melanomi coroidei. Porta a uno stato di attivazione costitutiva del legame GTP e attiva persistentemente molteplici vie di segnalazione, inclusa la via MAPK.
- Monosomia 3: Mutazione secondaria fortemente associata al rischio metastatico.
- Mutazioni BAP1: Associate al più alto rischio metastatico. Noto anche come gene causale della sindrome di predisposizione tumorale BAP1.
- Mutazioni SF3B1: Rischio metastatico intermedio. Caratterizzate da metastasi tardive.
- Mutazioni EIF1AX: Rischio metastatico più basso.
Nello stadio del nevo, queste mutazioni maligne non sono generalmente osservate. Si ritiene che l’accumulo di anomalie genetiche porti a un cambiamento continuo da benigno a maligno.
Significato biologico dei fattori di rischio
Sezione intitolata “Significato biologico dei fattori di rischio”Ogni elemento del TFSOM-UHHD riflette le seguenti condizioni patologiche.
Pigmento arancione (lipofuscina): Pigmento dell’invecchiamento prodotto dall’RPE. Riflette l’attività metabolica del tumore e l’interazione tra tumore e RPE; maggiore è l’attività tumorale, maggiore è l’accumulo.
Liquido sottoretinico: segno che suggerisce una rottura della barriera dell’EPR da parte del tumore. Quando il tumore cresce e si attiva, la funzione di pompa dell’EPR diminuisce e il liquido si accumula sotto la retina.
Bassa ecogenicità interna all’ecografia: suggerisce un’alta densità di vasi intratumorali. Nel melanoma coroidale, i vasi intratumorali sono abbondanti e spesso mostrano una bassa ecogenicità interna. I nevi benigni di solito presentano un pattern ecogeno interno omogeneo e un’alta ecogenicità.
Color Doppler positivo (flusso pulsatile): indica un apporto vascolare proprio del tumore. I nevi sono spesso negativi al Color Doppler, il che rappresenta un importante punto di differenziazione dal melanoma.
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Validazione dell’accuratezza dei criteri TFSOM-UHHD
Sezione intitolata “Validazione dell’accuratezza dei criteri TFSOM-UHHD”Gli studi di validazione della sensibilità e specificità dei criteri TFSOM-UHHD sono in corso e si prevede un miglioramento dell’accuratezza del loro uso clinico. In futuro, potrebbe essere realizzata una stratificazione del rischio più precisa che incorpori un modello di calcolo del rischio a 5 anni.
Applicazione dell’angiografia OCT
Sezione intitolata “Applicazione dell’angiografia OCT”È in fase di studio la visualizzazione non invasiva dei vasi intratumorali mediante angiografia OCT (OCTA). In combinazione con l’ecografia Color Doppler, si prevede un ulteriore miglioramento dell’accuratezza nella differenziazione tra nevo e melanoma.
Valutazione quantitativa del pigmento arancione
Sezione intitolata “Valutazione quantitativa del pigmento arancione”È in corso lo sviluppo di un metodo di valutazione quantitativa della lipofuscina (pigmento arancione) mediante autofluorescenza del fondo oculare. L’obiettivo è migliorare l’accuratezza della previsione del rischio attraverso la quantificazione della quantità di pigmento.
Stratificazione del rischio mediante biomarcatori molecolari
Sezione intitolata “Stratificazione del rischio mediante biomarcatori molecolari”La ricerca sulla valutazione genomica non invasiva mediante biopsia liquida (DNA tumorale circolante nel sangue, ecc.) è in corso. In futuro, in combinazione con i reperti del fondo oculare, potrebbe essere utilizzata per la rilevazione precoce della trasformazione maligna.
8. Riferimenti
Sezione intitolata “8. Riferimenti”- Finger PT. Laser treatment for choroidal melanoma. Surv Ophthalmol. 2023;68(2):211-224.
- Qureshi MB, Lentz PC, Xu TT, White LJ, Olsen TW, Pulido JS, et al. Choroidal Nevus Features Associated with Subspecialty Referral. Ophthalmol Retina. 2023;7(12):1097-1108. PMID: 37517800.
- Chien JL, Sioufi K, Surakiatchanukul T, Shields JA, Shields CL. Choroidal nevus: a review of prevalence, features, genetics, risks, and outcomes. Curr Opin Ophthalmol. 2017;28(3):228-237. PMID: 28141766.
