良性型の組織学的特徴
nonteratoid型:神経上皮様の管腔構造を形成する。
teratoid型:神経上皮様構造に加え、軟骨・横紋筋など異所性組織を含む。
共通:核異型が軽度で、浸潤所見・核分裂像が少ない。

髄上皮腫(medulloepithelioma)は、毛様体無色素上皮から発生するまれな眼内腫瘍である。毛様体無色素上皮は胎生期の神経管上皮に由来しており、髄上皮腫はその多分化能を反映した独特の組織像を示す。かつては網膜芽細胞腫の類縁腫瘍として記載されることもあった。
発生部位としては毛様体が最も多く、視神経や網膜から発生するケースはまれである。小児、特に1〜10歳に好発し、成人での発症は例外的である。Kaliki らの41症例の解析では診断時の年齢中央値は5歳と報告されている1。非常にまれな腫瘍であり、正確な発生頻度の把握は困難であるが、眼科臨床において経験する機会は極めて少ない2。
同年代の小児に発症し白色瞳孔を呈する網膜芽細胞腫との鑑別が臨床上の最重要課題となる。確定診断は多くの場合、眼球摘出後の病理組織検査によってなされる。
髄上皮腫は初期には無症状であることが多く、保護者による気づきや乳幼児健診での眼反射異常を契機に発見されることがある。主な発見契機を以下に示す。
Kaliki らの41症例の解析では、続発緑内障44%、虹彩血管新生51%、白内障46%、水晶体亜脱臼27%が認められ、白色瞳孔・続発緑内障・水晶体異常が特徴的な臨床三徴をなすことが報告されている13。
散瞳後の前眼部観察および隅角鏡検査では、毛様体領域の白色〜黄白色の腫瘤が確認される。腫瘤の表面は不整で、嚢胞状構造を含むことがある。
良性型の組織学的特徴
nonteratoid型:神経上皮様の管腔構造を形成する。
teratoid型:神経上皮様構造に加え、軟骨・横紋筋など異所性組織を含む。
共通:核異型が軽度で、浸潤所見・核分裂像が少ない。
悪性型の組織学的特徴
浸潤所見:周囲組織への明らかな浸潤を認める。
核分裂像:多数の核分裂像を呈する。
眼外浸潤リスク:強膜外・眼窩への浸潤・転移が起こりうる。
腫瘍が増大・眼球外に浸潤すると、眼球突出・眼球運動障害が出現する。続発性緑内障による眼圧上昇・角膜浮腫を呈することもある。
髄上皮腫の発生は毛様体無色素上皮の胎生期発生異常に起因すると考えられている。正常発生における神経管上皮の形成過程が腫瘍形成に関与していると推察されるが、具体的な発症機序の詳細は未解明な部分が多い。
特定の環境的リスク因子は確立されていない。性差・地域差・人種差についても明確なデータは乏しい。
遺伝的背景として、DICER1遺伝子変異との関連が一部の症例で報告されている。DICER1変異は胸膜肺芽腫・腎腫瘍・甲状腺腫など多臓器腫瘍の原因となる癌素因症候群(DICER1症候群)の原因遺伝子であり、毛様体髄上皮腫が胸膜肺芽腫を伴う家族性腫瘍素因症候群の一徴候として現れうることが報告されている45。さらに、孤発例においても腫瘍組織内に体細胞性DICER1変異が同定された例があり、DICER1経路の異常が腫瘍発生に関与する可能性が示唆されている6。ただし、髄上皮腫の多くは孤発性であり、家族性発症は少数例にとどまる。
テラトイド型では、軟骨・横紋筋など多様な異所性組織が含まれることから、腫瘍形成に多能性細胞が関与していると考えられる。これは、毛様体無色素上皮が胎生期において多分化能を保持していることと整合している。
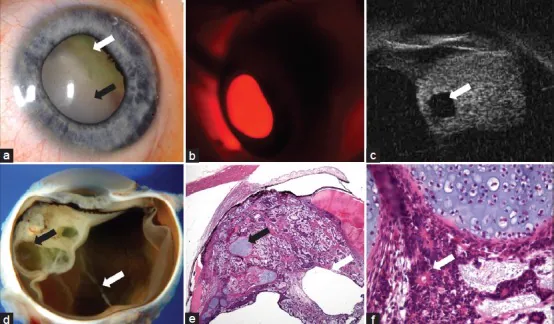
**超音波生体顕微鏡(UBM)**は毛様体腫瘤の確認・形態評価に最も有用な検査である。毛様体に接する充実性または嚢胞混在性腫瘤を描出でき、腫瘤の範囲・毛様体との関係・前眼部への浸潤の有無を評価できる。Kaliki らの解析では腫瘍内嚢胞が61%の症例で確認されており、UBM での嚢胞性構造の描出は本症を強く示唆する所見となる1。
MRIは腫瘍範囲と眼球外浸潤の評価に用いられる。眼窩・視神経への浸潤が疑われる場合、治療方針決定に不可欠な情報を提供する。
CTスキャンは石灰化の有無の評価に有用であり、網膜芽細胞腫との鑑別に役立つ(網膜芽細胞腫では石灰化を高頻度に認める)。
眼底検査・前眼部検査は散瞳下での細隙灯顕微鏡・倒像鏡を用いて行う。毛様体腫瘤の直接観察および網膜の合併病変(漿液性網膜剥離など)の確認を行う。
確定診断は眼球摘出後の病理組織検査によってなされることが多い。毛様体は生検が技術的に困難であり、生検による腫瘍播種のリスクもあるため、臨床・画像所見から髄上皮腫が強く疑われる場合は眼球摘出を先行させることが一般的である。
病理組織学的には、胎生期神経管上皮に類似した管腔・乳頭・シート状構造を形成する上皮性腫瘤として診断される。テラトイド型では軟骨・横紋筋・脳組織様成分など異所性組織の存在が特徴的である。
| 疾患 | 鑑別ポイント |
|---|---|
| 網膜芽細胞腫 | 白色瞳孔・CT上の石灰化・多発性が特徴。網膜から発生。髄上皮腫は毛様体腫瘤が主体 |
| 毛様体黒色細胞腫(メラノサイトーマ) | 良性で色素性が強い。中高年に多く、UBMで高輝度腫瘤 |
| 毛様体悪性黒色腫(メラノーマ) | 中高年に発症。色素性腫瘤で、見張り血管(sentinel vessel)を伴うことがある |
| 永続性胎児血管症(PHPV) | 先天性。硝子体内の線維血管膜を形成し、白色瞳孔を呈する |
大多数の髄上皮腫では眼球摘出術が選択される12。その理由として以下が挙げられる。
眼球摘出後は義眼を用いる。整容的・社会的適応を考慮し、早期から眼窩インプラントが挿入されることが多い。
小型の腫瘍で良性が強く示唆される場合、毛様体切除術(cyclectomy)による局所切除が選択肢となる。ただし、毛様体への手術アクセスは技術的に難易度が高く、施行できる施設・術者は限られる。また、切除後も腫瘍再発のリスクがあるため、慎重な症例選択と厳密な術後経過観察が必要である。
眼球外浸潤が進行し眼窩内に腫瘍が及んでいる場合は、眼窩内容除去術(orbital exenteration)が必要となる。侵襲が大きく術後の整容的問題も生じるため、実施適応は慎重に判断される。
| 病型 | 予後の特徴 |
|---|---|
| 良性型 | 眼球摘出後、転移がなければ良好。局所再発率は低い |
| 悪性型 | 眼球外浸潤・遠隔転移のリスクがある。転移した場合の予後は不良 |
| 眼外浸潤例 | 眼窩内容除去術後も局所再発・転移に注意が必要 |
遠隔転移は比較的まれとされているが、悪性型・眼外浸潤例では十分な経過観察が求められる。転移があった場合の治療は化学療法・放射線療法などが検討されるが、標準レジメンは確立していない。
髄上皮腫は毛様体無色素上皮を起源とする。毛様体無色素上皮は胎生期において神経管由来の神経上皮から形成される。このため、髄上皮腫の組織像は胎生期の神経管上皮に類似した管腔・乳頭・シート状構造を示す。
**nonteratoid型(非テラトイド型)**は、神経上皮様の管腔・乳頭構造のみを形成する。正常な神経管上皮の形態に最も近い型である。細胞は円柱状〜立方状で、偽重層配列を示すことがある。
**teratoid型(テラトイド型)**は、神経上皮様構造に加え、軟骨・横紋筋・脳組織様成分など多様な組織を含む。これは腫瘍発生細胞の高い多分化能を反映しており、奇形腫(teratoma)に類似した組織像となる。良性のteratoid型では核異型・核分裂像が少なく、境界明瞭な増殖にとどまる。
悪性型では、神経上皮様構造に加えて以下の所見が認められる。
これらの所見が悪性度の判定と予後予測の根拠となる。良性・悪性の境界が曖昧な中間型も報告されており、病理診断には経験が求められる。
悪性型では腫瘍細胞が強膜乳頭管(emissary canal)を通じて眼窩に浸潤する経路が主要とされる。血行性転移の経路としては、毛様体の豊富な血管網を介した全身播種が考えられているが、詳細な機序の解明は進行中である。
DICER1遺伝子は低分子RNAの生合成に関与するRNaseIII酵素をコードする。DICER1の生殖細胞系列変異はDICER1症候群を引き起こし、胸膜肺芽腫・腎腫瘍・甲状腺腫などの多発腫瘍と関連する。近年、髄上皮腫の一部にDICER1変異が認められることが報告されており、眼腫瘍とDICER1症候群の関連性が注目されている。
DICER1変異の同定は遺伝子カウンセリングの対象選択、および家族の遺伝スクリーニング適応を検討するうえで重要となりうる。最近の毛様体髄上皮腫の臨床病理学的解析では、分子遺伝学的検索を組み込んだ系統的な評価の重要性が改めて指摘されている7。
髄上皮腫は症例数が少なく、大規模な臨床研究が困難な疾患である。Shields らをはじめとする眼腫瘍専門施設による大規模症例シリーズの集積が、良性・悪性の病理学的鑑別基準の精緻化に寄与している。核分裂像数・浸潤所見の定量的評価基準の標準化が今後の課題とされる。
小型・良性型の髄上皮腫に対する局所切除(毛様体切除術)の適応拡大が検討されている。眼球摘出を回避して視機能を温存できる可能性があるが、術後再発のリスク管理・長期経過観察プロトコールの確立が求められる。
テラトイド型と非テラトイド型で、悪性化頻度・眼外浸潤リスク・予後に差異があるかどうかは十分に解明されていない。大規模多施設研究による比較検討が期待されている。
Kaliki S, Shields CL, Eagle RC Jr, Vemuganti GK, Almeida A, Manjandavida FP, Mulay K, Honavar SG, Shields JA. Ciliary body medulloepithelioma: analysis of 41 cases. Ophthalmology. 2013;120(12):2552-2559. doi:10.1016/j.ophtha.2013.05.015. PMID: 23796765. ↩ ↩2 ↩3 ↩4
Tadepalli SH, Shields CL, Shields JA, Honavar SG. Intraocular medulloepithelioma - A review of clinical features, DICER 1 mutation, and management. Indian J Ophthalmol. 2019;67(6):755-762. doi:10.4103/ijo.IJO_845_19. PMID: 31124483; PMCID: PMC6552580. ↩ ↩2
Peshtani A, Kaliki S, Eagle RC, Shields CL. Medulloepithelioma: A triad of clinical features. Oman J Ophthalmol. 2014;7(2):93-95. doi:10.4103/0974-620X.137171. PMID: 25136238; PMCID: PMC4134557. ↩
Kramer GD, Arepalli S, Shields CL, Shields JA. Ciliary body medulloepithelioma association with pleuropulmonary blastoma in a familial tumor predisposition syndrome. J Pediatr Ophthalmol Strabismus. 2014;51:e48-e50. doi:10.3928/01913913-20140709-03. PMID: 25032694. ↩
Priest JR, Williams GM, Manera R, Jenkinson H, Bründler MA, Davis S, Murray TG, Galliani CA, Dehner LP. Ciliary body medulloepithelioma: four cases associated with pleuropulmonary blastoma—a report from the International Pleuropulmonary Blastoma Registry. Br J Ophthalmol. 2011;95(7):1001-1005. doi:10.1136/bjo.2010.189779. PMID: 21156700. ↩
Durieux E, Descotes F, Nguyen AM, Grange JD, Devouassoux-Shisheboran M. Somatic DICER1 gene mutation in sporadic intraocular medulloepithelioma without pleuropulmonary blastoma syndrome. Hum Pathol. 2015;46(5):783-787. doi:10.1016/j.humpath.2015.01.020. PMID: 25791583. ↩
August AH, Cernichiaro-Espinosa LA, Moctezuma-Davila M, Wibbelsman TD, Wilson MW, Chévez-Barrios P, Shields CL, Lally SE, Eberhart CG, Orr BA, Simpson E, Eagle RC, Milman T. Ciliary Body Medulloepithelioma: Clinical and Pathologic Challenges with a Focus on Molecular Genetics. Semin Ophthalmol. 2025;40(6):518-528. doi:10.1080/08820538.2025.2457066. PMID: 39869033. ↩