양성형의 조직학적 특징
비기형종형: 신경상피양 관강 구조를 형성합니다.
기형종형: 신경상피양 구조 외에 연골, 횡문근 등 이소성 조직을 포함합니다.
공통: 핵 이형성이 경미하고, 침윤 소견 및 핵분열상이 적습니다.

수질상피종(medulloepithelioma)은 섬모체 무색소 상피에서 발생하는 드문 안내 종양입니다. 섬모체 무색소 상피는 배아기의 신경관 상피에서 유래하며, 수질상피종은 그 다분화능을 반영한 독특한 조직상을 보입니다. 과거에는 망막모세포종의 유사 종양으로 기술되기도 했습니다.
발생 부위로는 섬모체가 가장 흔하며, 시신경이나 망막에서 발생하는 경우는 드뭅니다. 소아, 특히 1~10세에 호발하고, 성인에서의 발병은 예외적입니다. Kaliki 등의 41증례 분석에서는 진단 시 연령 중앙값이 5세로 보고되었습니다1. 매우 드문 종양으로 정확한 발생 빈도 파악은 어렵지만, 안과 임상에서 경험할 기회는 극히 드뭅니다2.
같은 연령의 소아에서 발생하여 백색 동공을 나타내는 망막모세포종과의 감별이 임상상 가장 중요한 과제입니다. 확진은 대부분 안구 적출 후 병리조직검사를 통해 이루어집니다.
수질상피종은 초기에는 무증상인 경우가 많고, 보호자에 의한 발견이나 영유아 건강검진에서의 안반사 이상을 계기로 발견되기도 합니다. 주요 발견 계기는 다음과 같습니다.
Kaliki 등의 41증례 분석에서는 속발 녹내장 44%, 홍막 혈관 신생 51%, 백내장 46%, 수정체 아탈구 27%가 확인되었고, 백색 동공·속발 녹내장·수정체 이상이 특징적인 임상 삼징을 이룬다고 보고되었습니다13.
산동 후 전안부 검사 및 각경 검사에서 섬모체 부위의 흰색에서 황백색 종괴가 확인됩니다. 종괴의 표면은 불규칙하고 낭성 구조를 포함할 수 있습니다.
양성형의 조직학적 특징
비기형종형: 신경상피양 관강 구조를 형성합니다.
기형종형: 신경상피양 구조 외에 연골, 횡문근 등 이소성 조직을 포함합니다.
공통: 핵 이형성이 경미하고, 침윤 소견 및 핵분열상이 적습니다.
악성형의 조직학적 특징
침윤 소견: 주변 조직으로의 명확한 침윤이 관찰됩니다.
핵분열상: 다수의 핵분열상을 보입니다.
안외 침윤 위험: 공막외, 안와로의 침윤 및 전이가 발생할 수 있습니다.
종양이 커지고 안구 밖으로 침윤되면 안구돌출과 안구운동장애가 나타납니다. 속발성 녹내장으로 인한 안압 상승과 각막 부종이 나타날 수도 있습니다.
수질상피종은 섬모체 무색소 상피의 배아기 발생 이상으로 인해 발생하는 것으로 생각됩니다. 정상 발생에서 신경관 상피의 형성 과정이 종양 형성에 관여하는 것으로 추정되지만, 구체적인 발병 기전은 아직 밝혀지지 않은 부분이 많습니다.
특정 환경적 위험 요인은 확립되지 않았습니다. 성별, 지역별, 인종별 차이에 대한 명확한 데이터도 부족합니다.
유전적 배경으로서, 일부 증례에서 DICER1 유전자 변이와의 연관성이 보고되었습니다. DICER1 변이는 흉막폐모세포종, 신장 종양, 갑상선 종양 등 다기관 종양을 유발하는 암 소인 증후군(DICER1 증후군)의 원인 유전자이며, 섬모체 수질상피종이 흉막폐모세포종을 동반한 가족성 종양 소인 증후군의 한 징후로 나타날 수 있다고 보고되었습니다45. 또한, 산발성 증례에서도 종양 조직 내 체세포성 DICER1 변이가 확인된 예가 있어, DICER1 경로의 이상이 종양 발생에 관여할 가능성이 시사됩니다6. 그러나 수질상피종의 대부분은 산발성이며, 가족성 발병은 소수에 불과합니다.
기형종형에서는 연골, 횡문근 등 다양한 이소성 조직이 포함되므로, 종양 형성에 다능성 세포가 관여하는 것으로 생각됩니다. 이는 섬모체 무색소 상피가 배아기 동안 다분화 능력을 유지하고 있다는 사실과 일치합니다.
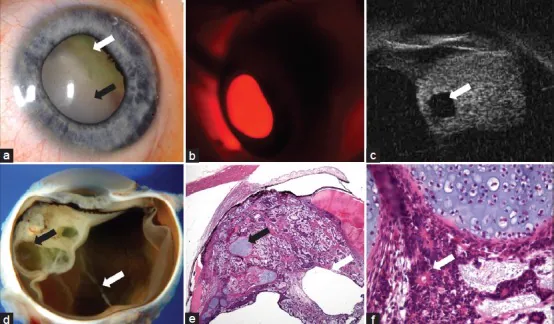
**초음파생체현미경(UBM)**은 섬모체 종괴의 확인 및 형태 평가에 가장 유용한 검사입니다. 섬모체에 접하는 고형 또는 낭종 혼합 종괴를 묘사할 수 있으며, 종괴의 범위, 섬모체와의 관계, 전안부 침윤 유무를 평가할 수 있습니다. Kaliki 등의 분석에서는 종양 내 낭종이 61%의 증례에서 확인되었으며, UBM에서 낭성 구조의 묘사는 본 질환을 강력히 시사하는 소견입니다1.
MRI는 종양 범위와 안구 외 침윤 평가에 사용됩니다. 안와나 시신경 침윤이 의심되는 경우 치료 방침 결정에 필수적인 정보를 제공합니다.
CT 스캔은 석회화 유무 평가에 유용하며, 망막모세포종과의 감별에 도움이 됩니다(망막모세포종에서는 석회화가 빈번하게 관찰됨).
안저 검사 및 전안부 검사는 산동 하에 세극등 현미경 및 도상경을 사용하여 시행합니다. 섬모체 종괴의 직접 관찰 및 망막 합병 병변(장액성 망막박리 등)의 확인을 시행합니다.
확진은 안구 적출 후 병리조직 검사에 의해 이루어지는 경우가 많습니다. 섬모체는 생검이 기술적으로 어렵고 종양 파종의 위험이 있으므로, 임상 및 영상 소견에서 수질상피종이 강력히 의심되는 경우 안구 적출을 우선 시행하는 것이 일반적입니다.
조직병리학적으로 배아기 신경관 상피와 유사한 관상, 유두상, 또는 시트상 구조를 형성하는 상피성 종양으로 진단됩니다. 기형종형에서는 연골, 횡문근, 뇌 조직 유사 성분 등 이소성 조직의 존재가 특징적입니다.
| 질환 | 감별 포인트 |
|---|---|
| 망막모세포종 | 백색동공, CT상 석회화, 다발성이 특징입니다. 망막에서 발생합니다. 수질상피종은 주로 섬모체 종괴로 나타납니다. |
| 섬모체 흑색세포종(멜라노사이토마) | 양성이며 색소 침착이 강합니다. 중장년층에 많고, UBM에서 고에코 종괴로 보입니다. |
| 섬모체 악성 흑색종(멜라노마) | 중장년층에 발생합니다. 색소성 종괴로, 감시 혈관(sentinel vessel)을 동반할 수 있습니다. |
| 영구 태아 혈관증(PHPV) | 선천성입니다. 유리체 내 섬유혈관막을 형성하고 백색동공을 나타냅니다. |
대부분의 수질상피종에서 안구적출술이 선택됩니다12. 그 이유는 다음과 같습니다:
안구적출 후 의안을 사용합니다. 미용적·사회적 적응을 고려하여 조기에 안와 임플란트를 삽입하는 경우가 많습니다.
양성이 강력히 시사되는 소형 종양의 경우, 섬모체 절제술(cyclectomy)을 통한 국소 절제가 선택지가 됩니다. 그러나 섬모체에 대한 수술적 접근은 기술적으로 난이도가 높아 시행 가능한 시설과 술자가 제한됩니다. 또한 절제 후에도 종양 재발 위험이 있으므로 신중한 증례 선택과 엄격한 수술 후 경과 관찰이 필요합니다.
안구외 침윤이 진행되어 안와 내에 종양이 미치는 경우, 안와 내용물 제거술(orbital exenteration)이 필요합니다. 침습이 크고 수술 후 미용적 문제도 발생하므로 시행 적응증은 신중히 판단됩니다.
| 병형 | 예후의 특징 |
|---|---|
| 양성형 | 안구적출 후 전이가 없으면 예후가 좋습니다. 국소 재발률이 낮습니다. |
| 악성형 | 안외 침윤 및 원격 전이의 위험이 있습니다. 전이된 경우 예후가 좋지 않습니다. |
| 안외 침윤 예 | 안와 내용물 제거술 후에도 국소 재발 및 전이에 주의가 필요합니다. |
원격 전이는 비교적 드물지만, 악성형 및 안외 침윤 예에서는 충분한 경과 관찰이 필요합니다. 전이가 있는 경우 화학요법, 방사선요법 등이 고려되지만, 표준 요법은 확립되어 있지 않습니다.
수질상피종은 섬모체 무색소 상피에서 기원합니다. 섬모체 무색소 상피는 태생기에 신경관 유래 신경상피에서 형성됩니다. 따라서 수질상피종의 조직상은 태생기 신경관 상피와 유사한 관강, 유두, 시트상 구조를 보입니다.
비기형종형은 신경상피양 관강 및 유두 구조만을 형성합니다. 정상 신경관 상피의 형태에 가장 가까운 형입니다. 세포는 원주형~입방형이며, 위중층 배열을 보일 수 있습니다.
기형종형은 신경상피양 구조에 더하여 연골, 횡문근, 뇌조직양 성분 등 다양한 조직을 포함합니다. 이는 종양 발생 세포의 높은 다분화능을 반영하며, 기형종과 유사한 조직상이 됩니다. 양성 기형종형에서는 핵 이형성 및 핵분열상이 적고, 경계가 명확한 증식에 그칩니다.
악성형에서는 신경상피양 구조에 더하여 다음 소견이 인정됩니다.
이러한 소견은 악성도 판정과 예후 예측의 근거가 됩니다. 양성과 악성의 경계가 모호한 중간형도 보고되어 있으며, 병리 진단에는 경험이 필요합니다.
악성형에서는 종양 세포가 공막 유두관(emissary canal)을 통해 안와로 침윤하는 경로가 주요 경로로 간주됩니다. 혈행성 전이는 섬모체의 풍부한 혈관망을 통한 전신 파종으로 생각되지만, 자세한 기전은 아직 연구 중입니다.
DICER1 유전자는 소형 RNA의 생합성에 관여하는 RNase III 효소를 코딩합니다. DICER1의 생식세포 계열 변이는 DICER1 증후군을 유발하며, 흉막폐모세포종, 신장 종양, 갑상선 종양 등 여러 종양과 관련됩니다. 최근 수질상피종의 일부에서 DICER1 변이가 확인되었다는 보고가 있어, 안종양과 DICER1 증후군의 연관성이 주목받고 있습니다.
DICER1 변이의 확인은 유전 상담 대상 선정 및 가족 유전자 검사 적응증을 고려하는 데 중요할 수 있습니다. 최근 섬모체 수질상피종의 임상병리학적 분석에서는 분자유전학적 검사를 포함한 체계적 평가의 중요성이 다시 강조되었습니다7.
수질상피종은 증례 수가 적어 대규모 임상 연구가 어려운 질환입니다. Shields 등을 비롯한 안종양 전문 기관의 대규모 증례 시리즈 축적이 양성·악성의 병리학적 감별 기준 정밀화에 기여하고 있습니다. 핵분열상 수 및 침윤 소견의 정량적 평가 기준 표준화가 향후 과제로 여겨집니다.
소형, 양성형 수질상피종에 대한 국소 절제(섬모체 절제술)의 적응증 확대가 검토되고 있습니다. 안구 적출을 피하고 시각 기능을 보존할 가능성이 있지만, 수술 후 재발 위험 관리 및 장기 추적 관찰 프로토콜의 확립이 요구됩니다.
기형종형과 비기형종형 간에 악성화 빈도, 안외 침윤 위험, 예후에 차이가 있는지 여부는 충분히 밝혀지지 않았습니다. 대규모 다기관 연구를 통한 비교 검토가 기대됩니다.
Kaliki S, Shields CL, Eagle RC Jr, Vemuganti GK, Almeida A, Manjandavida FP, Mulay K, Honavar SG, Shields JA. Ciliary body medulloepithelioma: analysis of 41 cases. Ophthalmology. 2013;120(12):2552-2559. doi:10.1016/j.ophtha.2013.05.015. PMID: 23796765. ↩ ↩2 ↩3 ↩4
Tadepalli SH, Shields CL, Shields JA, Honavar SG. Intraocular medulloepithelioma - A review of clinical features, DICER 1 mutation, and management. Indian J Ophthalmol. 2019;67(6):755-762. doi:10.4103/ijo.IJO_845_19. PMID: 31124483; PMCID: PMC6552580. ↩ ↩2
Peshtani A, Kaliki S, Eagle RC, Shields CL. Medulloepithelioma: A triad of clinical features. Oman J Ophthalmol. 2014;7(2):93-95. doi:10.4103/0974-620X.137171. PMID: 25136238; PMCID: PMC4134557. ↩
Kramer GD, Arepalli S, Shields CL, Shields JA. Ciliary body medulloepithelioma association with pleuropulmonary blastoma in a familial tumor predisposition syndrome. J Pediatr Ophthalmol Strabismus. 2014;51:e48-e50. doi:10.3928/01913913-20140709-03. PMID: 25032694. ↩
Priest JR, Williams GM, Manera R, Jenkinson H, Bründler MA, Davis S, Murray TG, Galliani CA, Dehner LP. Ciliary body medulloepithelioma: four cases associated with pleuropulmonary blastoma—a report from the International Pleuropulmonary Blastoma Registry. Br J Ophthalmol. 2011;95(7):1001-1005. doi:10.1136/bjo.2010.189779. PMID: 21156700. ↩
Durieux E, Descotes F, Nguyen AM, Grange JD, Devouassoux-Shisheboran M. Somatic DICER1 gene mutation in sporadic intraocular medulloepithelioma without pleuropulmonary blastoma syndrome. Hum Pathol. 2015;46(5):783-787. doi:10.1016/j.humpath.2015.01.020. PMID: 25791583. ↩
August AH, Cernichiaro-Espinosa LA, Moctezuma-Davila M, Wibbelsman TD, Wilson MW, Chévez-Barrios P, Shields CL, Lally SE, Eberhart CG, Orr BA, Simpson E, Eagle RC, Milman T. Ciliary Body Medulloepithelioma: Clinical and Pathologic Challenges with a Focus on Molecular Genetics. Semin Ophthalmol. 2025;40(6):518-528. doi:10.1080/08820538.2025.2457066. PMID: 39869033. ↩