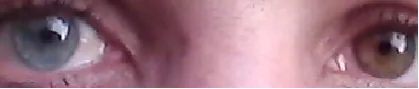
フックス異色性虹彩毛様体炎(FHI)は虹彩 異色・慢性虹彩 毛様体 炎・白内障 を3主徴とする疾患である
20〜40歳代に好発し、ほとんどが片眼性で、性差はない
日本人では褐色虹彩 のため虹彩 異色が目立たず、びまん性虹彩 萎縮が診断の鍵となる
星状の角膜 後沈着物(KP)が角膜 後面全体にびまん性に分布する点が特徴的である
炎症は軽度かつ慢性であり、ステロイド 点眼にほとんど反応しないため原則として経過観察とする
風疹ウイルスとの関連が示唆されており、前房 水PCRにより鑑別診断が可能となった8)
続発緑内障 (10〜59%)が最も視機能を脅かす合併症であり、薬物療法抵抗性が高い2) 1906年にオーストリアの眼科医Ernst Fuchsが、虹彩 異色・毛様体 炎・白内障 を呈する38例を報告した。フックス異色性虹彩毛様体炎(Fuchs heterochromic iridocyclitis: FHI)は、フックスぶどう膜炎 症候群(Fuchs uveitis syndrome: FUS)とも呼ばれる。虹彩 異色・虹彩 毛様体 炎・白内障 を3主徴とする片眼性ぶどう膜炎 であり、20〜40歳代に多く性差はない。
FHIは全ぶどう膜炎 の2〜11%を占めるとされる2) 。ぶどう膜炎 診療ガイドラインの集計(3,055例)では0.5%(15例)であった3) 。有病率は過小評価されている可能性があり、日本人では褐色虹彩 のために虹彩 異色が目立ちにくく診断が遅れやすい7) 。大部分は片眼性であり、両眼性は約10〜13%にとどまる2) 。
FHI自体は続発緑内障 を発症しない限り良性の経過をたどり、治療を必要としないことが多い。一方、続発緑内障 はFHIにおいて最も視機能を脅かす合併症であり、長期追跡ほど合併率が高まる。
Q
日本人ではFHIの診断が難しいのはなぜですか?
A
日本人は褐色虹彩 であるため、虹彩 色調の左右差が明らかに現れにくい。単純な虹彩 異色ではなく、虹彩 輪や虹彩 紋理が健眼と比べて不明瞭となること、また小虹彩 輪を中心としたびまん性の虹彩 萎縮が生じていることに注目する。散瞳 前に僚眼と比較することが診断のポイントである。
フックス虹彩異色性虹彩毛様体炎の虹彩異色 Wikimedia Commons. Heterochromia iridis. License: CC BY-SA.
両眼の虹彩 色の差(heterochromia iridis)。罹患眼側の虹彩 実質萎縮により虹彩 色素が減少し、対側眼と比較して虹彩 の色が薄く変化している。FHIの3主徴のひとつである虹彩 異色の所見。
FHI患者は他の前部ぶどう膜炎 と異なり、痛み・充血 ・羞明 を伴わない。受診まで長年無症状であることも少なくない。
白内障 による視力 低下白内障 としてFHIが発見されることが多い飛蚊症 硝子体 を中心とした炎症性デブリによる硝子体混濁 が原因となる
虹彩異色(虹彩萎縮)
患者の75〜90%にみられる。通常、色の薄い方が罹患眼である。日本人では褐色虹彩 のためびまん性虹彩 萎縮として現れる。無散瞳 の状態で僚眼と比較することが大切である。
星状KP(角膜後面沈着物)
白色・微細な星状で角膜 後面全体にびまん性分布。角膜 上方まで均等に分布する点が他のぶどう膜炎 と異なる。診断上最も特異的な所見である。
虹彩毛様体炎・白内障
前房 炎症は慢性・軽度。白内障 は他のぶどう膜炎 より進行が早い。虹彩後癒着 は生じない(最重要の鑑別点)。Koeppe/Busacca型虹彩 結節を認めることがある。
虹彩 異色(heterochromia)2) 。通常、色の薄い方が罹患眼である。虹彩 の前実質が消失し暗色の色素上皮が露出する「逆異色」も報告されている虹彩 萎縮虹彩 が萎縮し、虹彩 陰窩が消失して滑らかな実質構造(虫食い状外観)を呈する。萎縮はしばしば虹彩 異色に先行する。日本人をはじめアジア人では褐色虹彩 のため虹彩 異色が明らかでないことが多く、虹彩 捲縮輪より瞳孔 側(小虹彩 輪)の色調に着目することが重要である。無散瞳 の状態で僚眼と比較することが大切である虹彩 結節瞳孔 縁)やBusacca結節(虹彩 実質)がみられることがある3) 。しかし虹彩後癒着 は生じない
星状KP :白色・微細な星状で、フィブリンの架橋により相互連結する2) 。通常のぶどう膜炎 のKPが角膜 下方のArlt三角内に集中するのに対し、FHIのKPは角膜 後面全体にびまん性に分布する。嚢胞様黄斑浮腫 (CME )は通常みられない隅角 新生血管 隅角鏡検査 で線維柱帯 上を通過する血管新生がしばしば確認される2) 。前房穿刺 や隅角 圧迫によりこれらの脆弱な血管が破綻し、対側の隅角 から前房出血 を生じることがある(Amsler徴候)
後嚢下白内障 (PSC) :FHI患者の水晶体 混濁の約3/4を占める2) 。白内障 は他のぶどう膜炎 に比べて進行が早いRussell小体 :虹彩 表面にみられる小さく屈折 性の高い結晶で、球状免疫グロブリンの凝集体である2) 脈絡網膜 瘢痕 :症例の7〜65%に認められるが、トキソプラズマ症との決定的な関連は証明されていない
続発緑内障 隅角 型。最も視機能を脅かす合併症2) Amsler徴候 :前房穿刺 時の隅角 からの出血。隅角 新生血管 の脆弱性による硝子体混濁 硝子体手術 を要する
Q
虹彩後癒着がある場合はFHIではないのですか?
A
その通りである。FHIでは虹彩後癒着 は生じないのが原則であり、虹彩後癒着 の存在はFHIに反する重要な所見である。虹彩後癒着 を認めた場合はサルコイドーシス ・ヘルペス性虹彩炎 ・CMV虹彩 毛様体 炎など他疾患の鑑別を要する。
FHIの正確な病因はいまだ不明であり、多因子性と考えられている。歴史的には変性疾患説・トキソプラズマ/HS V感染説・免疫異常説・血管異常説(Amsler徴候から)など多くの仮説が提唱されてきたが、現在は多くが否定されている。
HS V・チクングニアウイルス前房 水からウイルスDNA/RNAが分離された報告があるが、症例報告レベルにとどまる交感神経機能不全説 :虹彩 実質メラノサイトへの神経支配減少を想定した理論であるが、1,746例中ホルネル症候群 との関連はわずか25例(1.4%)であり否定的であるトキソプラズマ症 :脈絡網膜 瘢痕の有病率は高いが、液性・細胞性免疫との有意な関連は証明されていない
近年最も有力な仮説として風疹ウイルスとの関連が注目されている。Mohamed & Zamir(2005)のレビューでは、胎児期・小児期の風疹感染後に持続的眼内低悪性度感染が成立する可能性が示された7) 。de Groot-Mijnes ら(2006)はFHI患者の前房 水PCRで風疹ウイルスRNA(ゲノム)を検出し、Goldmann-Witmer係数による眼内抗体産生を確認した。欧州の64例中48例(75%)でRVに対する眼内抗体産生が認められた8) 。風疹ワクチン普及地域でFHIの発生率が低下傾向にあることも風疹関与説の根拠となっている。
アジアではCMV感染がFHI様炎症として報告されている。Chee & Jap(2008)はCMV陽性FHI様前部ぶどう膜炎 をCMV陰性のFHIおよびPosner-Schlossman症候群 と比較し、高眼圧 ・前房 細胞が共通するが、FHI的所見(星状KP・虹彩 萎縮)はCMV陰性例と類似していることを示した9) 。CMV前部ぶどう膜炎 の国際タスクフォース(TITAN 2024)では、前房 水PCRによるCMV-DNAの同定が鑑別に有用であることが強調されている4) 。
FHIに伴う続発緑内障 の報告頻度は10〜59%と幅が広く、長期追跡ほど高率となる2) 。ぶどう膜炎 診療ガイドラインでは10〜20%とされている3) 。リスクを高める因子として以下が報告されている。
高齢
診断までの期間が長い
男性
ベースライン時の虹彩 結節の存在
白内障 の合併両眼性の症例2)
FHIの診断は臨床所見の組み合わせに基づく。確定的な診断テストは存在しない。La Hey ら(1994)が提示した診断基準10) が参照される。他疾患の除外後に初めて診断される。
前眼部炎症(片眼性または著しく非対称性)
微細・白色・星状KPの角膜 後面全体へのびまん性分布
虹彩 変化(異色・萎縮・結節のいずれか)虹彩後癒着 の不在隅角 の血管異常(新生血管 )の可能性白内障 ・硝子体混濁 を合併しうる
無散瞳 での僚眼比較 :虹彩 萎縮の確認に必須。散瞳 後では萎縮が不明瞭になる前房 水PCR眼圧 を伴う場合のCMV鑑別に活用する9) 蛍光虹彩 造影 :虹彩 血管異常・Amsler徴候の評価隅角鏡検査 隅角 と新生血管 の確認
疾患 KP 虹彩後癒着 眼圧 特徴 FHI 星状・びまん性 なし 慢性上昇(10〜59%) 無症状・単眼性 Posner-Schlossman症候群 少数・白色 なし 発作性(40〜70 mmHg)2) 反復・急性 CMV虹彩 毛様体 炎 少数 なし 上昇 CMV-PCR陽性4) サルコイドーシス 羊脂状・肉芽腫性 あり 正常〜上昇 両眼性・全身所見 ヘルペス性虹彩炎 少数 可能性あり 上昇 角膜知覚 低下・セクター萎縮
その他の鑑別疾患は以下の通りである。
VZV虹彩 毛様体 炎 :経過中に限局性の虹彩 萎縮と麻痺性散瞳 がみられることが多く、FHIのびまん性萎縮とは異なる3) HS V虹彩 毛様体 炎虹彩 萎縮を特徴とする先天性ホルネル症候群 :虹彩 色素脱失を伴うWaardenburg症候群 :虹彩 異色に加え内眼角側方偏位、感音難聴 を伴うICE症候群 虹彩 萎縮を伴うが、角膜浮腫 ・角膜 虹彩癒着 を特徴とするびまん性虹彩 メラノーマ :色素沈着型の虹彩 異色を呈するステロイド緑内障 ステロイド が使用された場合、ステロイド緑内障 との鑑別が問題となる5)
Q
前房水の検査(PCR)は必要ですか?
A
すべての例で必須ではないが、高眼圧 を伴う場合・治療にステロイド や抗ウイルス薬の使い分けが必要な場合・CMVとFHIの鑑別が困難な場合には前房 水PCRが有用である9) 。特にアジア人ではCMV陽性FHI様炎症の報告が多く、鑑別が治療方針を変えうる。
FHIの前房 症状はステロイド 点眼にほとんど反応せず、長期使用はステロイド 白内障 やステロイド緑内障 のリスクを高める。ぶどう膜炎 診療ガイドラインでは「ステロイド 薬を点眼せずに経過観察する」ことを原則としている3) 。虹彩後癒着 が生じないため散瞳薬 も不要である。
FHIに合併する白内障 は他のぶどう膜炎 と比較して手術結果が良好である。ぶどう膜炎 診療ガイドラインでは「活動性の炎症が存在していても白内障 手術によって炎症の増悪を来すことの少ない疾患」と明記されている3) 。
水晶体 乳化吸引術+後房IOL 挿入術術中はAmsler徴候(隅角 からの出血)に注意し、低眼圧 灌流・粘弾性物質 の充分な使用が推奨される
術後に虹彩 異色が進行することがあるため術前説明が必要である
続発緑内障 に対する濾過手術 の可能性がある場合は、上方結膜 を温存して角膜 切開 で白内障 手術を行う
続発緑内障 の有病率は10〜59%に及び、73%が最大量の薬物療法に反応せず手術が必要となる2) 。
薬剤 使用 注意点 β遮断薬 (チモロール0.5% 1日2回等)第一選択2, 6) 房水 産生抑制炭酸脱水酵素阻害薬 (ドルゾラミド 等)第二選択2, 5) 点眼・内服 α2作動薬(ブリモニジン0.1%) 第二選択2) 房水 産生+ぶどう膜強膜 流出促進PGA製剤 慎重投与 炎症悪化・CME リスクあり2) 縮瞳薬(ピロカルピン等) 禁忌 2) 炎症悪化・毛様体 痙攣
薬物療法で眼圧 コントロールが不十分な場合、手術治療が必要となる。日本緑内障 診療ガイドライン第5版では、ぶどう膜炎続発緑内障 に対して線維柱帯切除術 (代謝拮抗薬 併用)またはチューブシャント 手術が推奨されている5) 。
FHIを含むぶどう膜炎 緑内障 の手術成績を以下に示す。
術式 対象 成績 MMC併用線維柱帯切除術 (1年) ぶどう膜炎 緑内障 成功率58〜90.9%2) MMC併用線維柱帯切除術 (4年) ぶどう膜炎 緑内障 成功率62.3%2) Baerveldt(2年) ぶどう膜炎 緑内障 成功率91.7%2) Ahmed弁(2年) ぶどう膜炎 緑内障 成功率68.4%2)
線維柱帯切除術 (MMC併用)ぶどう膜炎 眼は結膜 下瘢痕化の傾向から成功率が低下しやすい。1年成功率58〜90.9%、4年成功率62.3%2) 緑内障ドレナージデバイス (GDD)2) 。結膜 の瘢痕化がある症例では特に有用であるGAT T緑内障 への有効性は限定的(Yuksel Elgin 2025 の4症例で全例不成功)1) 毛様体 光凝固術 (ダイオード・Nd:YAGレーザー)房水 産生を抑制するが、炎症を増悪させるリスクがある。視機能予後が不良な眼での最終手段として位置づけられる2) レーザー線維柱帯形成術 (SLT /ALT)5, 6)
Q
FHIの炎症にステロイドを使った方がよいですか?
A
原則として使用しない。FHIの軽度の前房 反応はステロイド 点眼にほとんど反応せず、長期使用はステロイド 白内障 やステロイド緑内障 のリスクを高める。虹彩後癒着 が生じないため散瞳薬 も不要である。ぶどう膜炎 診療ガイドラインでも「必要以上の治療は行わない」とされている3) 。
胎児期・小児期の風疹感染後に前房 内で持続的低悪性度感染が成立するとする説が最も有力とされている7, 8) 。前房 水中の風疹ウイルスRNA・Goldmann-Witmer係数による眼内抗体産生の証明、および風疹ワクチン普及地域でのFHI減少傾向がエビデンスとして蓄積されている8) 。
CD8+T細胞優位の慢性T細胞介在性炎症 が星状KP・虹彩 萎縮・血管新生を誘発する虹彩 メラノサイトへの持続的な免疫攻撃が脱色素(虹彩 萎縮)を引き起こす前房 関連免疫偏向(ACAID )の破綻が慢性炎症の持続を促す
FHIに伴う続発緑内障 は開放隅角 型であり、以下の機序が眼圧 上昇に関与する2) 。
線維柱帯 炎(trabeculitis)房水 流出路を閉塞する6) 隅角 新生血管 (ルベオーシス)前房出血 )を引き起こす後線維柱帯 の不可逆的瘢痕化 :GAT T等の線維柱帯切開術 が効果を発揮しにくい原因1) Schlemm管の虚脱 :房水 流出抵抗が恒常的に増大する不可逆的な構造変化 :炎症が消退した後も緑内障 が持続する症例が多く、可逆的な炎症性閉塞だけでなく不可逆的な線維柱帯 の構造変化が生じていると考えられている
FHIでは虹彩後癒着 ・周辺虹彩前癒着 (PAS )・瞳孔ブロック は通常みられないため、閉塞隅角 機序は一般的ではなく、開放隅角 における線維柱帯 レベルの障害が主体である5) 。典型的にFHIの緑内障 は炎症が沈静化した後も持続する傾向があり、ステロイド に反応しない2) 。この点がステロイド緑内障 との鑑別の一助となる。
隅角鏡検査 では開放隅角 と線維柱帯 を横切る血管新生が確認される2) 。虹彩 蛍光造影では虹彩 血管の漏出や虚血性変化が認められることがある。
参考として、ぶどう膜炎 に伴う眼圧 上昇には以下の機序も関与しうる2) 。
線維柱帯 への炎症性デブリの蓄積線維柱帯 浮腫隅角 結節周辺虹彩前癒着 (PAS )ステロイド 薬血管新生
虹彩後癒着 に伴う瞳孔ブロック
このうちFHIでは後癒着・PAS ・瞳孔ブロック は通常関与せず、主に線維柱帯 炎と構造変化が眼圧 上昇の原因となる。
慢性・低グレードの炎症が持続することにより、水晶体 上皮細胞が変性し後嚢下白内障 (PSC)が形成される。FHI患者の水晶体 混濁の約3/4を後嚢下型が占め、他のぶどう膜炎 に比べ進行が早い。ステロイド 治療を行わない場合でも白内障 は進行するため、定期的な経過観察が必要である。
Yuksel Elgin & Hepokur(2025)は、FUS関連緑内障 に対するGAT Tを4症例で報告した。全例で手術は不成功に終わり、平均6か月後に3例はMMC併用線維柱帯切除術 を、1例はダイオードレーザー毛様体 光凝固術 を要した1) 。FUS緑内障 では後線維柱帯 領域の瘢痕化が主因であり、GAT Tでは十分な眼圧 下降が得られない可能性が示された。
多重PCR技術の向上により、風疹ウイルス・CMV・HS Vの前房 内共存・鑑別が精度よく行えるようになった。アジアのCMV前部ぶどう膜炎 では抗ウイルス治療(ガンシクロビル点眼・バルガンシクロビル内服)の有用性が検討されている4) 。
iStent ・Hydrus などのインプラントデバイスは炎症性デブリによる閉塞が懸念されるが、カナルプラスティでは予備的に有望な成績が報告されている。FHI緑内障 特有のMIGS アルゴリズムの確立が課題となっている。
風疹ワクチンの普及に伴うFHI疫学変化の継続的追跡が行われており、若年世代でのFHI発生率の低下傾向が報告されている7) 。
FHI関連緑内障 におけるGDDと濾過手術 の優劣を明らかにする大規模研究
風疹ウイルスやCMVの病因的役割の解明と、抗ウイルス治療の有用性の検討
FHI特異的な緑内障 治療アルゴリズムの確立
Q
FHIの緑内障に低侵襲緑内障手術(MIGS)は有効ですか?
A
現時点ではFHI緑内障 に対するMIGS の有効性は限定的と考えられている。GAT Tの4症例報告では全例が不成功に終わった1) 。FHI緑内障 では後線維柱帯 領域の瘢痕化が関与する可能性があり、隅角 手術のみでは十分な効果が得られない場合がある。iStent やXenなどのインプラントデバイスは炎症性デブリによる閉塞が懸念される。
Yuksel Elgin C, Hepokur M. Highlighting the limited efficacy of gonioscopy-assisted transluminal trabeculectomy in Fuchs uveitis syndrome: a case series. BMC Ophthalmol. 2025;25(1):180.
Bodh SA, Kumar V, Raina UK, Ghosh B, Thakar M. Inflammatory glaucoma. Oman J Ophthalmol. 2011;4(1):3-9.
日本眼炎症学会. ぶどう膜炎 診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
Chee SP, Jap A, Engelen S, et al. CMV anterior uveitis: what we have learnt. The International Taskforce for Anterior segment Novel therapies (TITAN) report 2. Graefes Arch Clin Exp Ophthalmol. 2024;262(5):1415-1428.
日本緑内障 学会. 緑内障 診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma. 5th ed. Savona: PubliComm; 2020.
Mohamed Q, Zamir E. Update on Fuchs’ uveitis syndrome. Curr Opin Ophthalmol. 2005;16(6):356-363.
de Groot-Mijnes JDF, de Visser L, Rothova A, et al. Rubella virus is associated with Fuchs heterochromic iridocyclitis. Am J Ophthalmol. 2006;141(1):212-214.
Chee SP, Jap A. Presumed Fuchs heterochromic iridocyclitis and Posner-Schlossman syndrome: comparison of cytomegalovirus-positive and negative eyes. Am J Ophthalmol. 2008;146(6):883-889.
La Hey E, de Jong PTVM, Kijlstra A. Fuchs’ heterochromic cyclitis: review of the literature on the pathogenetic mechanisms. Br J Ophthalmol. 1994;78(4):307-312.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください