هتروکرومی عنبیه (آتروفی عنبیه)
در 75 تا 90٪ بیماران دیده میشود. معمولاً چشم با رنگ روشنتر، چشم مبتلا است. در ژاپنیها به دلیل عنبیه قهوهای، به صورت آتروفی منتشر عنبیه ظاهر میشود. مقایسه با چشم مقابل در حالت بدون گشاد کردن مردمک مهم است.

در سال ۱۹۰۶، ارنست فوکس، چشمپزشک اتریشی، ۳۸ مورد با هتروکرومی عنبیه، سیکلیت و آب مروارید گزارش کرد. یووئیت هتروکرومیک فوکس (FHI) که سندرم یووئیت فوکس (FUS) نیز نامیده میشود، یک یووئیت یک طرفه با سه علامت اصلی هتروکرومی عنبیه، یووئیت و آب مروارید است که بیشتر در دهه ۲۰ تا ۴۰ سالگی رخ میدهد و تفاوت جنسیتی ندارد.
گفته میشود FHI 2 تا 11 درصد از کل یووئیتها را تشکیل میدهد 2). در جمعبندی راهنمای بالینی یووئیت (3055 مورد) 0.5٪ (15 مورد) بود 3). احتمال دارد شیوع کمتر از حد واقعی برآورد شده باشد و در ژاپنیها به دلیل عنبیه قهوهای، هتروکرومی کمتر مشخص بوده و تشخیص دیرتر انجام میشود 7). اکثر موارد یک طرفه هستند و موارد دوطرفه تنها حدود 10 تا 13٪ را تشکیل میدهند 2).
FHI به خودی خود سیر خوشخیمی دارد مگر اینکه گلوکوم ثانویه ایجاد شود و اغلب نیازی به درمان ندارد. از سوی دیگر، گلوکوم ثانویه جدیترین عارضه تهدیدکننده بینایی در FHI است و با پیگیری طولانیتر، میزان عارضه افزایش مییابد.
از آنجا که ژاپنیها عنبیه قهوهای دارند، تفاوت رنگ عنبیه بین دو چشم به وضوح ظاهر نمیشود. به جای هتروکرومی ساده، باید به نامشخص شدن حلقه عنبیه و بافت عنبیه در مقایسه با چشم سالم و همچنین آتروفی منتشر عنبیه به ویژه در اطراف حلقه کوچک عنبیه توجه کرد. مقایسه با چشم مقابل قبل از گشاد کردن مردمک نکته کلیدی در تشخیص است.
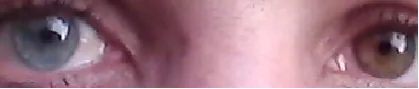
برخلاف سایر یووئیتهای قدامی، بیماران FHI درد، قرمزی یا فتوفوبی ندارند. اغلب تا سالها بدون علامت هستند تا زمانی که به پزشک مراجعه کنند.
هتروکرومی عنبیه (آتروفی عنبیه)
در 75 تا 90٪ بیماران دیده میشود. معمولاً چشم با رنگ روشنتر، چشم مبتلا است. در ژاپنیها به دلیل عنبیه قهوهای، به صورت آتروفی منتشر عنبیه ظاهر میشود. مقایسه با چشم مقابل در حالت بدون گشاد کردن مردمک مهم است.
رسوبات ستارهای شکل در سطح پشتی قرنیه (KP)
رسوبات سفید، ریز و ستارهای شکل که به صورت منتشر در سراسر سطح خلفی قرنیه پخش شدهاند. توزیع یکنواخت تا قسمت فوقانی قرنیه، این وضعیت را از سایر انواع یووئیت متمایز میکند. این مشخصهترین یافته برای تشخیص است.
ایریدوسیکلیت و آب مروارید
التهاب اتاق قدامی مزمن و خفیف است. آب مروارید سریعتر از سایر انواع یووئیت پیشرفت میکند. چسبندگی خلفی عنبیه رخ نمیدهد (مهمترین نکته افتراقی). گرههای عنبیه از نوع Koeppe/Busacca ممکن است دیده شوند.
درست است. در FHI اصولاً چسبندگی عنبیه به عدسی رخ نمیدهد و وجود آن یافته مهمی علیه FHI است. در صورت مشاهده چسبندگی عنبیه به عدسی، باید سایر بیماریها مانند سارکوئیدوز، عنبیه هرپسی و سیکلیت CMV را افتراق داد.
علت دقیق FHI هنوز ناشناخته است و چندعاملی در نظر گرفته میشود. از نظر تاریخی فرضیههای زیادی مانند بیماری دژنراتیو، عفونت توکسوپلاسما/HSV، ناهنجاری ایمنی و ناهنجاری عروقی (بر اساس علامت Amsler) مطرح شدهاند، اما امروزه بسیاری از آنها رد شدهاند.
در سالهای اخیر قویترین فرضیه ارتباط با ویروس سرخجه است. در مرور محمد و ضمیر (2005) احتمال ایجاد عفونت مزمن درون چشمی با درجه پایین پس از عفونت سرخجه در جنینی یا کودکی مطرح شد 7). de Groot-Mijnes و همکاران (2006) RNA ویروس سرخجه (ژنوم) را در PCR زلالیه بیماران FHI تشخیص دادند و تولید آنتیبادی درون چشمی را با ضریب Goldmann-Witmer تأیید کردند. در 48 نفر از 64 بیمار اروپایی (75%) تولید آنتیبادی درون چشمی علیه RV مشاهده شد 8). کاهش بروز FHI در مناطقی که واکسن سرخجه رایج است نیز از فرضیه دخالت سرخجه حمایت میکند.
در آسیا عفونت CMV به عنوان التهاب شبه FHI گزارش شده است. Chee و Jap (2008) یووئیت قدامی شبه FHI مثبت CMV را با FHI منفی CMV و سندرم پوسنر-شلوسمن مقایسه کردند و نشان دادند که فشار بالای چشم و سلولهای اتاق قدامی مشترک هستند، اما یافتههای FHI (KP ستارهای، آتروفی عنبیه) مشابه موارد منفی CMV بود 9). کارگروه بینالمللی یووئیت قدامی CMV (TITAN 2024) تأکید کرد که شناسایی DNA CMV در PCR زلالیه برای افتراق مفید است 4).
فراوانی گزارششده گلوکوم ثانویه همراه با FHI بین ۱۰ تا ۵۹ درصد متغیر است و با پیگیری طولانیمدت افزایش مییابد 2). در دستورالعملهای بالینی یووئیت، ۱۰ تا ۲۰ درصد ذکر شده است 3). عوامل زیر به عنوان افزایشدهنده خطر گزارش شدهاند:
تشخیص FHI بر اساس ترکیبی از یافتههای بالینی است. هیچ آزمایش تشخیصی قطعی وجود ندارد. معیارهای تشخیصی ارائهشده توسط La Hey و همکاران (1994) 10) مرجع هستند. تشخیص تنها پس از رد سایر بیماریها داده میشود.
| بیماری | رسوبات قرنیه (KP) | سینشیای خلفی عنبیه | فشار چشم | ویژگیها |
|---|---|---|---|---|
| FHI | ستارهای/منتشر | ندارد | افزایش مزمن (۱۰-۵۹٪) | بدون علامت/تک چشمی |
| سندرم پوزنر-شلوسمن | تعداد کم/سفید | ندارد | حملهای (۴۰-۷۰ میلیمتر جیوه) 2) | عودکننده/حاد |
| ایریدوسیکلیت CMV | تعداد کم | ندارد | افزایش یافته | CMV-PCR مثبت 4) |
| سارکوئیدوز | چرب مانند / گرانولوماتوز | وجود دارد | طبیعی تا افزایش یافته | دوچشمی / یافتههای سیستمیک |
| عنبیه هرپسی | تعداد کم | احتمال وجود دارد | افزایش یافته | کاهش حس قرنیه / آتروفی سکتوری |
سایر تشخیصهای افتراقی به شرح زیر است:
در همه موارد ضروری نیست، اما در موارد همراه با فشار بالای چشم، زمانی که نیاز به انتخاب بین استروئید و داروی ضد ویروس است، یا زمانی که تمایز بین CMV و FHI دشوار است، PCR زلالیه مفید است9). به ویژه در آسیاییها، گزارشهای زیادی از التهاب شبه FHI با CMV مثبت وجود دارد و تمایز میتواند برنامه درمانی را تغییر دهد.
علائم اتاق قدامی در FHI تقریباً به قطرههای استروئیدی پاسخ نمیدهند و استفاده طولانی مدت خطر آب مروارید استروئیدی و گلوکوم استروئیدی را افزایش میدهد. در راهنمای بالینی یووئیت، اصل بر «پیگیری بدون تجویز قطره استروئیدی» است3). از آنجایی که چسبندگی خلفی عنبیه رخ نمیدهد، قطرههای گشادکننده نیز ضروری نیستند.
نتایج جراحی آب مروارید همراه با FHI در مقایسه با سایر یووئیتها خوب است. در راهنمای بالینی یووئیت ذکر شده است که «حتی در حضور التهاب فعال، جراحی آب مروارید به ندرت باعث تشدید التهاب میشود»3).
شیوع گلوکوم ثانویه بین ۱۰ تا ۵۹ درصد است و ۷۳ درصد موارد به حداکثر درمان دارویی پاسخ نمیدهند و نیاز به جراحی دارند2).
| دارو | مصرف | نکات احتیاط |
|---|---|---|
| مسدودکنندههای بتا (تیمولول ۰٫۵٪ دو بار در روز و غیره) | خط اول2, 6) | کاهش تولید زلالیه |
| مهارکنندههای کربنیک آنهیدراز (دورزولامید و غیره) | خط دوم2, 5) | قطره چشمی / خوراکی |
| آگونیستهای آلفا-۲ (بریمونیدین ۰٫۱٪) | خط دوم2) | کاهش تولید زلالیه + افزایش خروج از راه یووهواسکلرال |
| داروهای PGA | تجویز با احتیاط | خطر تشدید التهاب و CME 2) |
| داروهای میوتیک (مانند پیلوکارپین) | منع مصرف2) | تشدید التهاب و اسپاسم عضله مژگانی |
در صورت کنترل ناکافی فشار داخل چشم با دارو، درمان جراحی ضروری است. در ویرایش پنجم راهنمای بالینی گلوکوم ژاپن، ترابکولکتومی (همراه با داروی ضد متابولیت) یا جراحی شنت لوله برای گلوکوم ثانویه ناشی از یووئیت توصیه شده است 5).
نتایج جراحی گلوکوم یووئیتی از جمله FHI در زیر نشان داده شده است.
| روش جراحی | جمعیت مورد مطالعه | نتایج |
|---|---|---|
| ترابکولکتومی با MMC (1 سال) | گلوکوم یووئیتی | نرخ موفقیت 58 تا 90.9% 2) |
| ترابکولکتومی با MMC (4 سال) | گلوکوم یووئیتی | نرخ موفقیت 62.3%2) |
| Baerveldt (2 سال) | گلوکوم یووئیتی | نرخ موفقیت 91.7%2) |
| شنت Ahmed (2 سال) | گلوکوم یووئیتی | نرخ موفقیت 68.4%2) |
در اصل استفاده نمیشود. واکنش خفیف اتاق قدامی در FHI به ندرت به قطرههای استروئیدی پاسخ میدهد و استفاده طولانی مدت خطر آب مروارید استروئیدی و گلوکوم استروئیدی را افزایش میدهد. از آنجایی که چسبندگی عنبیه به عدسی ایجاد نمیشود، داروهای گشادکننده مردمک نیز ضروری نیستند. در راهنمای بالینی یووئیت نیز ذکر شده است که «درمان بیش از حد لازم انجام نشود» 3).
فرضیهای که بر اساس آن پس از عفونت سرخجه در دوران جنینی یا کودکی، یک عفونت پایدار با درجه پایین در اتاق قدامی ایجاد میشود، قویترین فرضیه محسوب میشود 7, 8). شواهدی مانند RNA ویروس سرخجه در زلالیه، اثبات تولید آنتیبادی داخل چشمی با ضریب Goldmann-Witmer، و کاهش روند FHI در مناطقی که واکسن سرخجه رایج است، جمعآوری شده است 8).
گلوکوم ثانویه همراه با FHI از نوع زاویه باز است و مکانیسمهای زیر در افزایش فشار داخل چشم نقش دارند 2).
در FHI، چسبندگی خلفی عنبیه، چسبندگی قدامی محیطی عنبیه (PAS) و بلوک مردمکی معمولاً دیده نمیشود، بنابراین مکانیسم زاویه بسته شایع نیست و آسیب در سطح شبکه ترابکولار در زاویه باز غالب است5). به طور معمول، گلوکوم FHI تمایل دارد حتی پس از فروکش التهاب ادامه یابد و به استروئیدها پاسخ نمیدهد2). این نکته به تمایز از گلوکوم استروئیدی کمک میکند.
در گونیوسکوپی، زاویه باز و عروق جدید عبوری از شبکه ترابکولار مشاهده میشود2). آنژیوگرافی فلورسین عنبیه ممکن است نشت عروق عنبیه یا تغییرات ایسکمیک را نشان دهد.
به عنوان مرجع، افزایش فشار داخل چشم همراه با یووئیت ممکن است شامل مکانیسمهای زیر نیز باشد2):
در میان این موارد، در FHI معمولاً چسبندگی خلفی، PAS و بلوک مردمکی دخیل نیستند و عمدتاً ترابکولیت و تغییرات ساختاری باعث افزایش فشار داخل چشم میشوند.
ادامه التهاب مزمن و کمدرجه باعث دژنراسیون سلولهای اپیتلیال عدسی و تشکیل آب مروارید زیرکپسولی خلفی (PSC) میشود. حدود سه چهارم کدورتهای عدسی در بیماران FHI از نوع زیرکپسولی خلفی است و نسبت به سایر یووئیتها پیشرفت سریعتری دارد. حتی در صورت عدم درمان با استروئید، آب مروارید پیشرفت میکند، بنابراین پیگیری منظم ضروری است.
Yuksel Elgin & Hepokur (2025) GATT را برای گلوکوم مرتبط با FUS در 4 مورد گزارش کردند. جراحی در همه موارد ناموفق بود و به طور متوسط پس از 6 ماه، 3 مورد نیاز به ترابکولکتومی با MMC و 1 مورد نیاز به سیکلوفوتوکواگولاسیون با لیزر دیود داشتند 1). در گلوکوم FUS، اسکار ناحیه ترابکولار خلفی عامل اصلی است و GATT ممکن است کاهش کافی فشار داخل چشم را ایجاد نکند.
با بهبود تکنیک PCR چندگانه، تشخیص همزمان و تمایز ویروس سرخجه، CMV و HSV در زلالیه با دقت بالا امکانپذیر شده است. در یووئیت قدامی CMV در آسیا، اثربخشی درمان ضدویروسی (قطره گانسیکلوویر، والگانسیکلوویر خوراکی) در حال بررسی است 4).
دستگاههای ایمپلنت مانند iStent و Hydrus ممکن است با انسداد ناشی از بقایای التهابی مواجه شوند، اما کانالوپلاستی نتایج اولیه امیدوارکنندهای را نشان داده است. ایجاد الگوریتم MIGS خاص برای گلوکوم FHI یک چالش است.
پیگیری مداوم تغییرات اپیدمیولوژیک FHI به دنبال گسترش واکسن سرخجه انجام میشود و روند کاهشی بروز FHI در نسلهای جوان گزارش شده است 7).
در حال حاضر، اثربخشی MIGS برای گلوکوم ناشی از یووئیت قدامی (FHI) محدود در نظر گرفته میشود. در یک گزارش از ۴ مورد GATT، همه موارد ناموفق بودند1). در گلوکوم FHI، ممکن است زخم شدن ناحیه ترابکولار خلفی نقش داشته باشد و جراحی زاویه به تنهایی ممکن است اثر کافی نداشته باشد. انسداد ایمپلنتهایی مانند iStent و Xen توسط بقایای التهابی نگرانکننده است.