ม่านตาอักเสบ ร่วมกับซิลิอารีบอดี แบบสีต่างของฟุคส์ (FHI ) เป็นโรคที่มีสามอาการหลัก: ม่านตา สีต่าง, ม่านตาอักเสบ ร่วมกับซิลิอารีบอดี เรื้อรัง, และต้อกระจก พบบ่อยในช่วงอายุ 20-40 ปี ส่วนใหญ่เป็นข้างเดียว ไม่มีความแตกต่างทางเพศ
ในคนญี่ปุ่น เนื่องจากม่านตา สีน้ำตาล การมีสีต่างจึงไม่ชัดเจน การฝ่อของม่านตา แบบกระจายเป็นกุญแจสำคัญในการวินิจฉัย
คราบกระจกตา รูปดาว (KP) ที่กระจายอย่างทั่วถึงบนผิวด้านหลังของกระจกตา เป็นลักษณะเฉพาะ
การอักเสบเล็กน้อยและเรื้อรัง แทบไม่ตอบสนองต่อยาหยอดสเตียรอยด์ ดังนั้นโดยหลักการแล้วให้สังเกตอาการ
สงสัยว่าเกี่ยวข้องกับไวรัสหัดเยอรมัน และการวินิจฉัยแยกโรคทำได้โดย PCR ของน้ำในช่องหน้าตา8)
ต้อหินทุติยภูมิ (10-59%) เป็นภาวะแทรกซ้อนที่คุกคามการมองเห็น มากที่สุด และมักดื้อต่อการรักษาด้วยยา2) ในปี ค.ศ. 1906 จักษุแพทย์ชาวออสเตรีย Ernst Fuchs รายงานผู้ป่วย 38 รายที่มีม่านตา สีต่าง, ซิลิอารีบอดี อักเสบ, และต้อกระจก ม่านตาอักเสบ ร่วมกับซิลิอารีบอดี แบบสีต่างของฟุคส์ (FHI ) เรียกอีกอย่างว่า Fuchs uveitis syndrome (FUS) เป็นยูเวียอักเสบข้างเดียวที่มีสามอาการหลัก: ม่านตา สีต่าง, ม่านตาอักเสบ ร่วมกับซิลิอารีบอดี อักเสบ, และต้อกระจก พบบ่อยในช่วงอายุ 20-40 ปี ไม่มีความแตกต่างทางเพศ
FHI คาดว่าคิดเป็น 2-11% ของยูเวียอักเสบทั้งหมด 2) จากการรวบรวมข้อมูลแนวทางการวินิจฉัยและรักษายูเวียอักเสบ (3,055 ราย) พบ 0.5% (15 ราย) 3) ความชุกอาจถูกประเมินต่ำเกินไป และในคนญี่ปุ่น เนื่องจากม่านตา สีน้ำตาล ทำให้ภาวะม่านตา สีต่างกันสังเกตได้ยาก ส่งผลให้การวินิจฉัยล่าช้า 7) ส่วนใหญ่เป็นข้างเดียว และเป็นสองข้างเพียงประมาณ 10-13% 2)
FHI เองมีแนวทางที่ไม่ร้ายแรง เว้นแต่จะเกิดต้อหินทุติยภูมิ และมักไม่ต้องการการรักษา ในทางกลับกัน ต้อหินทุติยภูมิ เป็นภาวะแทรกซ้อนที่คุกคามการมองเห็น มากที่สุดใน FHI และยิ่งติดตามนานขึ้น อัตราการเกิดภาวะแทรกซ้อนก็ยิ่งสูงขึ้น
Q
ทำไมการวินิจฉัย FHI ในคนญี่ปุ่นจึงยาก?
A
เนื่องจากคนญี่ปุ่นมีม่านตา สีน้ำตาล ความแตกต่างของสีม่านตา ระหว่างสองตาจึงไม่ชัดเจน แทนที่จะเป็นม่านตา สีต่างกันแบบง่าย ควรสังเกตว่าวงแหวนม่านตา หรือลายม่านตา ไม่ชัดเจนเมื่อเทียบกับตาปกติ และเกิดการฝ่อของม่านตา แบบกระจายรอบวงแหวนเล็ก การเปรียบเทียบกับตาอีกข้างก่อนขยายม่านตา เป็นจุดสำคัญของการวินิจฉัย
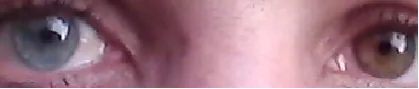
ม่านตาสีต่างกันใน Fuchs heterochromic iridocyclitis Wikimedia Commons. Heterochromia iridis. License: CC BY-SA.
ความแตกต่างของสี
ม่านตา ระหว่างสองตา (
ม่านตา สีต่างกัน) การฝ่อของสโตรมา
ม่านตา ในตาที่เป็นโรคทำให้เม็ดสี
ม่านตา ลดลง ส่งผลให้สี
ม่านตา จางลงเมื่อเทียบกับตาอีกข้าง นี่เป็นหนึ่งในสามอาการหลักของ
FHI แตกต่างจากยูเวียอักเสบส่วนหน้าชนิดอื่น ผู้ป่วย FHI ไม่มีอาการปวด ตาแดง หรือกลัวแสง ไม่ใช่เรื่องแปลกที่จะไม่มีอาการเป็นเวลาหลายปีจนกระทั่งมาพบแพทย์
การมองเห็น ลดลงจากต้อกระจก FHI มักถูกค้นพบว่าเป็นต้อกระจก ข้างเดียวที่ดำเนินไปอย่างรวดเร็วในคนหนุ่มสาวจุดลอยในตา : เกิดจากขุ่นของวุ้นตา เนื่องจากเศษซากการอักเสบในวุ้นตา ส่วนหน้า
ม่านตาสีต่างกัน (ม่านตาฝ่อ)
พบในผู้ป่วย 75-90% โดยปกติ ตาที่มีสีจางกว่าคือตาที่เป็นโรค ในคนญี่ปุ่น เนื่องจากม่านตา สีน้ำตาล จึงปรากฏเป็นม่านตา ฝ่อแบบกระจาย สิ่งสำคัญคือต้องเปรียบเทียบกับตาอีกข้างโดยไม่ขยายม่านตา
เคราติกพรีซิพิเทตแบบรูปดาว (คราบที่กระจกตาชั้นใน)
กระจายแบบแพร่กระจายทั่วผิวด้านหลังของกระจกตา เป็นรูปดาวสีขาวละเอียด แตกต่างจากม่านตาอักเสบ ชนิดอื่นตรงที่กระจายอย่างสม่ำเสมอจนถึงส่วนบนของกระจกตา นี่เป็นลักษณะที่จำเพาะที่สุดในการวินิจฉัย
ม่านตาอักเสบร่วมกับซิลิอารีบอดี · ต้อกระจก
การอักเสบในช่องหน้าม่านตา เป็นแบบเรื้อรังและไม่รุนแรง ต้อกระจก ดำเนินเร็วกว่าม่านตาอักเสบ ชนิดอื่น ไม่เกิดพังผืดยึดม่านตา ด้านหลัง (จุดแยกที่สำคัญที่สุด) อาจพบก้อนม่านตา ชนิด Koeppe/Busacca
สีม่านตา ไม่เท่ากัน (heterochromia) : พบใน 75-90% ของผู้ป่วย 2) โดยปกติตาข้างที่ได้รับผลกระทบจะมีสีอ่อนกว่า มีรายงาน “heterochromia แบบกลับด้าน” ซึ่งสโตรมาชั้นหน้าของม่านตา หายไปและเยื่อบุผิวสีเข้มโผล่ออกมาฝ่อของม่านตา : ม่านตา ฝ่อแบบกระจาย โดยรอยหยักของม่านตา หายไปและเกิดโครงสร้างสโตรมาที่เรียบ (ลักษณะเหมือนถูกแมลงกัด) การฝ่อมักเกิดก่อนสีม่านตา ไม่เท่ากัน ในคนญี่ปุ่นและคนเอเชีย เนื่องจากม่านตา มีสีน้ำตาล สีม่านตา ไม่เท่ากันมักไม่ชัดเจน ดังนั้นจึงสำคัญที่จะต้องเน้นที่สีบริเวณรูม่านตา (วงแหวนม่านตา ส่วนใน) ของวงแหวนหดรัดม่านตา สิ่งสำคัญคือต้องเปรียบเทียบกับตาอีกข้างโดยไม่ขยายม่านตา ก้อนม่านตา : อาจพบก้อน Koeppe (ที่ขอบรูม่านตา ) หรือก้อน Busacca (ในสโตรมาของม่านตา ) 3) อย่างไรก็ตาม ไม่เกิดพังผืดยึดม่านตา ด้านหลัง
เคอราติกพรีซิพิเทตรูปดาว : สีขาว ละเอียด รูปดาว เชื่อมต่อกันด้วยสะพานไฟบริน 2) ในขณะที่ KP ของม่านตาอักเสบ ทั่วไปจะรวมตัวในสามเหลี่ยม Arlt ด้านล่าง KP ของ FHI จะกระจายแบบแพร่กระจายทั่วผิวด้านหลังของกระจกตา โดยปกติไม่พบจอประสาทตา บวมน้ำชนิดซีสตอยด์ (CME )เส้นเลือดใหม่ที่มุม : ในการส่องกล้องตรวจมุมตา มักพบเส้นเลือดใหม่พาดผ่าน trabecular meshwork 2) การเจาะช่องหน้าม่านตา หรือกดมุมอาจทำให้เส้นเลือดที่เปราะบางเหล่านี้แตก ส่งผลให้มีเลือดออกในช่องหน้าม่านตา จากมุมตรงข้าม (Amsler sign)
ต้อกระจก ชนิดใต้แคปซูลด้านหลัง (PSC)FHI 2) ต้อกระจก ดำเนินเร็วกว่าเมื่อเทียบกับม่านตาอักเสบ ชนิดอื่นRussell body : ผลึกขนาดเล็กหักเหแสงสูงบนผิวม่านตา ซึ่งเป็นกลุ่มก้อนทรงกลมของอิมมูโนโกลบูลิน 2) แผลเป็นคอริโอเรตินัล : พบใน 7-65% ของกรณี แต่ยังไม่พิสูจน์ความสัมพันธ์ที่แน่ชัดกับทอกโซพลาสโมซิส
ต้อหินทุติยภูมิ การมองเห็น มากที่สุด2) เครื่องหมาย Amsler : เลือดออกจากมุมระหว่างการเจาะช่องหน้าม่านตา เนื่องจากความเปราะบางของเส้นเลือด新生ที่มุมความขุ่นของวุ้นตา วุ้นตา
Q
หากมีพังผืดยึดม่านตาด้านหลัง แสดงว่าไม่ใช่ FHI ใช่หรือไม่?
A
ถูกต้อง ใน FHI โดยหลักการแล้วจะไม่เกิดพังผืดยึดม่านตา ด้านหลัง และการมีพังผืดยึดม่านตา ด้านหลังเป็นสิ่งสำคัญที่ขัดแย้งกับ FHI หากพบพังผืดยึดม่านตา ด้านหลัง ต้องแยกโรคอื่นๆ เช่น ซาร์คอยโดซิส ม่านตาอักเสบจากเริม ม่านตาอักเสบ จาก CMV
สาเหตุที่แน่ชัดของ FHI ยังไม่ทราบ และเชื่อว่าเกิดจากหลายปัจจัย ในอดีตมีสมมติฐานมากมาย เช่น ทฤษฎีโรคเสื่อม ทฤษฎีการติดเชื้อทอกโซพลาสมา/HS V ทฤษฎีความผิดปกติของภูมิคุ้มกัน ทฤษฎีความผิดปกติของหลอดเลือด (จากเครื่องหมาย Amsler) แต่ปัจจุบันส่วนใหญ่ถูกปฏิเสธ
ไวรัส HS V และ Chikungunya : มีรายงานการแยก DNA/RNA ของไวรัสจากอารมณ์ขันในช่องหน้าม่านตา แต่ยังอยู่ในระดับรายงานผู้ป่วยทฤษฎีความผิดปกติของระบบประสาทซิมพาเทติก : ทฤษฎีที่สันนิษฐานว่าการลดลงของเส้นประสาทที่ไปเลี้ยงเมลาโนไซต์ในสโตรมาของม่านตา แต่จาก 1,746 ราย มีเพียง 25 ราย (1.4%) ที่เกี่ยวข้องกับกลุ่มอาการฮอร์เนอร์ จึงไม่สนับสนุนโรคทอกโซพลาสโมซิส : ความชุกของแผลเป็นคอริโอเรตินาสูง แต่ยังไม่พิสูจน์ความสัมพันธ์ที่มีนัยสำคัญกับภูมิคุ้มกันแบบฮิวเมอรัลหรือเซลลูลาร์
ในช่วงไม่กี่ปีที่ผ่านมา ความสัมพันธ์กับไวรัสหัดเยอรมันเป็นสมมติฐานที่แข็งแกร่งที่สุด ในการทบทวนของ Mohamed & Zamir (2005) ได้เสนอความเป็นไปได้ของการติดเชื้อในลูกตา ระดับต่ำแบบต่อเนื่องหลังการติดเชื้อหัดเยอรมันในทารกในครรภ์หรือวัยเด็ก7) de Groot-Mijnes และคณะ (2006) ตรวจพบ RNA ของไวรัสหัดเยอรมัน (จีโนม) โดย PCR ในอารมณ์ขันในช่องหน้าม่านตา ของผู้ป่วย FHI และยืนยันการผลิตแอนติบอดีภายในลูกตาโดยใช้ค่าสัมประสิทธิ์ Goldmann-Witmer ใน 48 จาก 64 รายในยุโรป (75%) พบการผลิตแอนติบอดีภายในลูกตาต่อ RV8) การลดลงของอุบัติการณ์ FHI ในพื้นที่ที่มีการฉีดวัคซีนหัดเยอรมันอย่างแพร่หลายก็เป็นหลักฐานสำหรับทฤษฎีการเกี่ยวข้องของหัดเยอรมัน
ในเอเชีย มีรายงานการติดเชื้อ CMV ว่าเป็นการอักเสบคล้าย FHI Chee & Jap (2008) เปรียบเทียบม่านตาอักเสบ ส่วนหน้าคล้าย FHI ที่เป็นบวก CMV กับ FHI ที่เป็นลบ CMV และกลุ่มอาการ Posner-Schlossman และแสดงให้เห็นว่าความดันลูกตา สูงและเซลล์ในช่องหน้าม่านตา เหมือนกัน แต่ลักษณะ FHI (เคราติกพรีซิพิเทตรูปดาว, ฝ่อของม่านตา ) คล้ายกับกรณีที่ลบ CMV9) คณะทำงานเฉพาะกิจระหว่างประเทศสำหรับม่านตาอักเสบส่วนหน้าจาก CMV (TITAN 2024) เน้นว่าการระบุ DNA ของ CMV โดย PCR ในอารมณ์ขันในช่องหน้าม่านตา มีประโยชน์ในการวินิจฉัยแยกโรค4)
ความถี่ของการรายงานโรคต้อหินทุติยภูมิ ที่เกี่ยวข้องกับ FHI อยู่ระหว่าง 10–59% และสูงขึ้นเมื่อติดตามระยะยาว 2) แนวทางปฏิบัติสำหรับม่านตาอักเสบ ระบุไว้ที่ 10–20% 3) มีรายงานปัจจัยต่อไปนี้ที่เพิ่มความเสี่ยง:
อายุมาก
ระยะเวลาจนกระทั่งวินิจฉัยนาน
เพศชาย
การมีก้อนที่ม่านตา เมื่อเริ่มต้น
การเกิดต้อกระจก ร่วม
กรณีที่เป็นสองตา 2)
การวินิจฉัย FHI ขึ้นอยู่กับการรวมกันของผลการตรวจทางคลินิก ไม่มีการตรวจวินิจฉัยที่แน่ชัด เกณฑ์การวินิจฉัยที่เสนอโดย La Hey และคณะ (1994) 10) ถูกอ้างอิง การวินิจฉัยจะทำหลังจากแยกโรคอื่นออกแล้วเท่านั้น
การอักเสบของส่วนหน้าของตา (ข้างเดียวหรือไม่สมมาตรอย่างชัดเจน)
การกระจายตัวแบบกระจายของตะกอนกระจกตา ขนาดเล็ก สีขาว รูปดาว ทั่วทั้งพื้นผิวด้านหลังของกระจกตา
การเปลี่ยนแปลงของม่านตา (อย่างใดอย่างหนึ่ง: สีต่างกัน, ฝ่อ, ปุ่ม)
ไม่มีพังผืดยึดม่านตา ด้านหลัง
ความเป็นไปได้ของความผิดปกติของหลอดเลือดที่มุมตา (เส้นเลือดใหม่)
อาจร่วมกับต้อกระจก และขุ่นของวุ้นตา
เปรียบเทียบตาข้างตรงข้ามโดยไม่ขยายม่านตา : จำเป็นเพื่อยืนยันการฝ่อของม่านตา การฝ่อจะไม่ชัดเจนหลังขยายม่านตา PCR ของน้ำในช่องหน้าตา : มีประโยชน์ในการระบุ DNA ของไวรัสหัดเยอรมันและ CMV ใช้โดยเฉพาะเพื่อแยก CMV ในกรณีที่มีความดันลูกตา สูง 9) การตรวจหลอดเลือดม่านตา ด้วยฟลูออเรสซีน : เพื่อประเมินความผิดปกติของหลอดเลือดม่านตา และสัญญาณ Amslerการตรวจ Gonioscopy : เพื่อยืนยันมุมเปิดและเส้นเลือดใหม่
โรค ตะกอนที่กระจกตา พังผืดยึดม่านตา ด้านหลัง ความดันลูกตา ลักษณะเฉพาะ FHI รูปดาว/กระจาย ไม่มี เพิ่มขึ้นเรื้อรัง (10-59%) ไม่มีอาการ / ตาเดียว กลุ่มอาการพอสเนอร์-ชลอสแมน น้อย / สีขาว ไม่มี เพิ่มขึ้นแบบ paroxysmal (40-70 มม.ปรอท) 2) เป็นซ้ำ / เฉียบพลัน ม่านตาอักเสบ และซิลิอารีบอดี อักเสบจาก CMVน้อย ไม่มี เพิ่มขึ้น CMV-PCR บวก 4) ซาร์คอยโดซิส คล้ายไขมัน / แกรนูโลมา มี ปกติถึงสูง สองตา / อาการทั่วร่างกาย ม่านตาอักเสบ จากเฮอร์ปีส์น้อย เป็นไปได้ สูง ความรู้สึกกระจกตา ลดลง / ฝ่อเฉพาะส่วน
โรคที่ต้องแยกอื่นๆ มีดังนี้:
ม่านตา และซิลิอารีบอดี อักเสบจาก VZVม่านตา ฝ่อเฉพาะจุดและม่านตา ขยายเป็นอัมพาตระหว่างดำเนินโรค ซึ่งแตกต่างจากการฝ่อแบบกระจายใน FHI 3) ม่านตา และซิลิอารีบอดี อักเสบจาก HS Vม่านตา ฝ่อเฉพาะจุดรูปวงกลมเล็กกลุ่มอาการฮอร์เนอร์ แต่กำเนิดม่านตา กลุ่มอาการวาร์เดนเบิร์ก : นอกจากม่านตา สองสีแล้ว ยังร่วมกับการเบี่ยงของหัวตาด้านในและการสูญเสียการได้ยินจากประสาทรับเสียงICE syndrome : มีภาวะม่านตา ฝ่อข้างเดียว แต่มีลักษณะเด่นคือกระจกตา บวมและม่านตาติด กระจกตา มะเร็งเมลาโนมาของม่านตา แบบกระจาย : แสดงสีม่านตา ไม่เท่ากันชนิดเม็ดสีต้อหินจากสเตียรอยด์ สเตียรอยด์ เป็นเวลานานสำหรับ FHI การวินิจฉัยแยกโรคกับต้อหินจากสเตียรอยด์ กลายเป็นปัญหา5)
Q
จำเป็นต้องตรวจน้ำในช่องหน้าตา (PCR) หรือไม่?
A
ไม่จำเป็นในทุกกรณี แต่มีประโยชน์ในกรณีที่มีความดันลูกตา สูง เมื่อจำเป็นต้องแยกการใช้สเตียรอยด์ และยาต้านไวรัส หรือเมื่อแยก CMV และ FHI ได้ยาก9) โดยเฉพาะในคนเอเชีย มีรายงานการอักเสบคล้าย FHI ที่พบ CMV บวกจำนวนมาก และการวินิจฉัยสามารถเปลี่ยนแผนการรักษาได้
อาการในช่องหน้าตาของ FHI แทบไม่ตอบสนองต่อยาหยอดสเตียรอยด์ และการใช้ระยะยาวเพิ่มความเสี่ยงต่อต้อกระจก จากสเตียรอยด์ และต้อหินจากสเตียรอยด์ แนวทางการรักษาม่านตาอักเสบ ระบุหลักการ “สังเกตอาการโดยไม่ใช้ยาหยอดสเตียรอยด์ ”3) เนื่องจากไม่เกิดม่านตาติด ด้านหลัง จึงไม่จำเป็นต้องใช้ยาหยอดขยายม่านตา
สเตียรอยด์ โดยไม่จำเป็น
การอักเสบในช่องหน้าเล็กน้อยของ FHI ยากที่จะกำจัดให้หมดไปแม้ใช้สเตียรอยด์ และการใช้ระยะยาวเสี่ยงต่อการเกิดต้อหินจากสเตียรอยด์ โดยเฉพาะการวินิจฉัยแยกโรคกับต้อหินทุติยภูมิ จาก FHI ทำได้ยาก ควรใช้ในปริมาณน้อยที่สุดและระยะสั้นเท่าที่จำเป็น และการวัดความดันลูกตา เป็นประจำเป็นสิ่งจำเป็น3)
ต้อกระจก ที่เกิดร่วมกับ FHI มีผลการผ่าตัดดีกว่าเมื่อเทียบกับม่านตาอักเสบ ชนิดอื่น แนวทางการรักษาม่านตาอักเสบ ระบุว่าเป็น “โรคที่ rarely ทำให้การอักเสบแย่ลงจากการผ่าตัดต้อกระจก แม้ในขณะที่มีการอักเสบ active”3)
การสลายต้อกระจก ด้วยคลื่นเสียงความถี่สูง + การใส่เลนส์แก้วตาเทียม ในช่องหลัง เป็นมาตรฐาน การอักเสบหลังผ่าตัดค่อนข้างน้อยระหว่างผ่าตัด ควรระวังสัญญาณ Amsler (เลือดออกจากมุมตา) และแนะนำให้ใช้การให้น้ำเกลือความดันต่ำและสารหนืดหยุ่นอย่างเพียงพอ
สีม่านตา ไม่เท่ากันอาจดำเนินต่อไปหลังผ่าตัด ดังนั้นจำเป็นต้องอธิบายก่อนผ่าตัด
หากมีความเป็นไปได้ที่จะต้องผ่าตัดกรองสำหรับต้อหินทุติยภูมิ ให้ทำการผ่าตัดต้อกระจก ด้วยการกรีดกระจกตา โดยสงวนเยื่อบุตา ส่วนบนไว้
ความชุกของต้อหินทุติยภูมิ อยู่ระหว่าง 10–59% และ 73% ไม่ตอบสนองต่อการรักษาด้วยยาสูงสุดและจำเป็นต้องผ่าตัด2)
ยา การใช้ ข้อควรระวัง ยาปิดกั้นเบตา (ไทโมลอล 0.5% วันละ 2 ครั้ง เป็นต้น) ทางเลือกแรก2, 6) ยับยั้งการผลิตอารมณ์ขันน้ำ ยายับยั้งคาร์บอนิกแอนไฮเดรส (ดอร์โซลาไมด์ เป็นต้น) ทางเลือกที่สอง2, 5) ยาหยอดตา / รับประทาน ยาออกฤทธิ์ต่ออัลฟา-2 (ไบรโมนิดีน 0.1%) ทางเลือกที่สอง2) ยับยั้งการผลิตอารมณ์ขันน้ำ + เพิ่มการไหลออกทางยูวีโอสเคลอรัล ยากลุ่ม PGA ใช้ด้วยความระมัดระวัง เสี่ยงต่อการอักเสบรุนแรงขึ้นและจอประสาทตา บวมน้ำชนิด CME 2) ยาหดม่านตา (เช่น pilocarpine) ห้ามใช้ 2) การอักเสบรุนแรงขึ้นและกล้ามเนื้อเลนส์ปรับตัวหดเกร็ง
เมื่อการควบคุมความดันลูกตา ด้วยยาไม่เพียงพอ จำเป็นต้องรักษาด้วยการผ่าตัด แนวทางปฏิบัติทางคลินิกโรคต้อหิน ของญี่ปุ่นฉบับที่ 5 แนะนำให้ทำ trabeculectomy (ร่วมกับยาต้านการเจริญเติบโตของเซลล์) หรือการผ่าตัดใส่ท่อระบายน้ำสำหรับต้อหินทุติยภูมิ จากม่านตาอักเสบ 5) .
ผลการผ่าตัดสำหรับต้อหิน จากม่านตาอักเสบ รวมถึง FHI แสดงไว้ด้านล่าง
วิธีการผ่าตัด กลุ่มประชากร ผลลัพธ์ Trabeculectomy ร่วมกับ MMC (1 ปี) ต้อหิน จากม่านตาอักเสบ อัตราความสำเร็จ 58–90.9% 2) การตัดเนื้อเยื่อโพรงม่านตา ออกด้วย MMC (4 ปี) ต้อหิน จากม่านตาอักเสบ อัตราความสำเร็จ 62.3%2) Baerveldt (2 ปี) ต้อหิน จากม่านตาอักเสบ อัตราความสำเร็จ 91.7%2) ลิ้น Ahmed (2 ปี) ต้อหิน จากม่านตาอักเสบ อัตราความสำเร็จ 68.4%2)
การตัดเนื้อเยื่อโพรงม่านตา ออก (ร่วมกับ MMC) : ดวงตาที่มีม่านตาอักเสบ มีแนวโน้มที่จะมีอัตราความสำเร็จต่ำกว่าเนื่องจากเกิดแผลเป็นใต้เยื่อบุตา อัตราความสำเร็จ 1 ปี 58-90.9%, 4 ปี 62.3%2) อุปกรณ์ระบายต้อหิน (GDD) : ลิ้น Ahmed, รากฟันเทียม Baerveldt และรากฟันเทียม Molteno เป็นทางเลือก มีรายงานผลลัพธ์ที่ดีโดยเฉพาะกับ Baerveldt โดยมีอัตราความสำเร็จ 91.7% ใน 2 ปี2) มีประโยชน์อย่างยิ่งในกรณีที่มีแผลเป็นที่เยื่อบุตา GAT Tต้อหิน ที่เกี่ยวข้องกับ FUS (ทั้ง 4 รายไม่สำเร็จใน Yuksel Elgin 2025)1) การจี้เลนส์ปรับแสงด้วยแสง (ไดโอด, Nd:YAG) : ลดการผลิตอารมณ์ขันในน้ำ แต่มีความเสี่ยงที่จะทำให้การอักเสบรุนแรงขึ้น ถือเป็นทางเลือกสุดท้ายในดวงตาที่มีการพยากรณ์โรคทางสายตาไม่ดี2) การทำ trabeculoplasty ด้วยเลเซอร์ (SLT /ALT) : มักไม่ได้ผลและโดยหลักการแล้วไม่ควรทำ5, 6)
ต้อหิน
ใน FHI การทำเลเซอร์ trabeculoplasty มักไม่ได้ผลและไม่แนะนำ 5) ยาหดม่านตา ก็มีข้อห้ามใช้เนื่องจากเพิ่มความเสี่ยงของการยึดติดหลังม่านตา และการอักเสบที่แย่ลง ความสำเร็จของการผ่าตัดต้อหิน ขึ้นอยู่กับการควบคุมการอักเสบก่อนและหลังผ่าตัดอย่างมาก ดังนั้นการประเมินโรคปฐมภูมิจึงสำคัญ หากใช้สเตียรอยด์ เป็นเวลานาน จำเป็นต้องแยกความแตกต่างจากต้อหินจากสเตียรอยด์ 5)
Q
ควรใช้สเตียรอยด์สำหรับการอักเสบของ FHI หรือไม่?
A
โดยหลักการแล้วไม่ใช้ ปฏิกิริยาช่องหน้าม่านตา เล็กน้อยใน FHI แทบไม่ตอบสนองต่อยาหยอดสเตียรอยด์ และการใช้เป็นเวลานานเพิ่มความเสี่ยงของต้อกระจก จากสเตียรอยด์ และต้อหินจากสเตียรอยด์ เนื่องจากไม่เกิดการยึดติดหลังม่านตา จึงไม่จำเป็นต้องใช้ยาขยายม่านตา แนวทางปฏิบัติสำหรับม่านตาอักเสบ ยังระบุว่า “ไม่ควรทำการรักษาที่ไม่จำเป็น” 3)
สมมติฐานที่มีน้ำหนักมากที่สุดคือการติดเชื้อหัดเยอรมันในระยะทารกในครรภ์หรือวัยเด็กทำให้เกิดการติดเชื้อเรื้อรังระดับต่ำในช่องหน้าม่านตา 7, 8) หลักฐานที่สะสมรวมถึง RNA ของไวรัสหัดเยอรมันในอารมณ์ขัน aqueous การพิสูจน์การผลิตแอนติบอดีภายในตาโดยใช้ Goldmann-Witmer coefficient และแนวโน้มการลดลงของ FHI ในพื้นที่ที่มีการฉีดวัคซีนหัดเยอรมันอย่างแพร่หลาย 8)
การอักเสบเรื้อรังที่อาศัย T cell โดยเด่น CD8+ T cell เหนี่ยวนำให้เกิด keratic precipitates (KP) แบบดาว ฝ่อของม่านตา และการสร้างเส้นเลือดใหม่การโจมตีทางภูมิคุ้มกันอย่างต่อเนื่องต่อ melanocyte ของม่านตา ทำให้เกิดการสูญเสียเม็ดสี (ฝ่อของม่านตา )
การหยุดชะงักของ immune deviation ที่เกี่ยวข้องกับช่องหน้าม่านตา (ACAID ) ส่งเสริมให้การอักเสบเรื้อรังคงอยู่
ต้อหินทุติยภูมิ ที่เกี่ยวข้องกับ FHI เป็นชนิดมุมเปิด และกลไกต่อไปนี้มีส่วนทำให้ความดันลูกตา สูงขึ้น 2)
Trabeculitis : การแทรกซึมของเซลล์อักเสบที่เด่นด้วยลิมโฟไซต์และพลาสมาเซลล์ การสะสมของเซลล์อักเสบ เศษซาก และการเกิดแผลเป็นทุติยภูมิอุดกั้นทางระบายอารมณ์ขัน aqueous 6) เส้นเลือดใหม่ที่มุมตา (rubeosis) : หลอดเลือดที่เปราะบางทำให้เกิด Amsler sign (เลือดออกในช่องหน้าม่านตา )การเกิดแผลเป็นที่ไม่สามารถกลับคืนได้ของ trabecular meshwork ด้านหลัง : สาเหตุที่การผ่าตัดเปิด trabecular เช่น GAT T ได้ผลน้อย 1) การยุบตัวของ Schlemm’s canal : ความต้านทานการไหลของอารมณ์ขัน aqueous เพิ่มขึ้นอย่างต่อเนื่องการเปลี่ยนแปลงโครงสร้างที่ไม่สามารถกลับคืนได้ : ในหลายกรณี โรคต้อหิน ยังคงอยู่แม้หลังการอักเสบสงบ และเชื่อว่านอกเหนือจากการอุดตันจากการอักเสบที่สามารถกลับคืนได้ ยังมีการเปลี่ยนแปลงโครงสร้างที่ไม่สามารถกลับคืนได้ใน trabecular meshwork
ใน FHI มักไม่พบการยึดติดของม่านตา ด้านหลัง, การยึดติดของม่านตาส่วนปลายด้านหน้า (PAS ) และการอุดตันของรูม่านตา ดังนั้นกลไกมุมปิดจึงไม่พบได้บ่อย ความเสียหายในระดับ trabecular meshwork ในมุมเปิดเป็นหลัก 5) โดยทั่วไปแล้ว โรคต้อหิน ใน FHI มักจะคงอยู่แม้หลังการอักเสบสงบ และไม่ตอบสนองต่อสเตียรอยด์ 2) จุดนี้ช่วยในการแยกความแตกต่างจากต้อหินจากสเตียรอยด์
การตรวจ gonioscopy พบมุมเปิดและเส้นเลือดใหม่ที่พาดผ่าน trabecular meshwork 2) การตรวจ fluorescein angiography ของม่านตา อาจพบการรั่วซึมหรือการเปลี่ยนแปลงจากการขาดเลือดของหลอดเลือดม่านตา
สำหรับอ้างอิง กลไกต่อไปนี้อาจเกี่ยวข้องกับความดันลูกตา สูงที่เกิดร่วมกับม่านตาอักเสบ 2) :
การสะสมของเศษซากจากการอักเสบใน trabecular meshwork
อาการบวมน้ำของ trabecular meshwork
ก้อนที่มุมตา
การยึดติดของม่านตาส่วนปลายด้านหน้า (PAS )ยาสเตียรอยด์
การสร้างเส้นเลือดใหม่
การอุดตันของรูม่านตา จากการยึดติดของม่านตา ด้านหลัง
ในจำนวนนี้ การยึดติดของม่านตา ด้านหลัง, PAS และการอุดตันของรูม่านตา มักไม่เกี่ยวข้องใน FHI ; สาเหตุหลักของความดันลูกตา สูงคือ trabeculitis และการเปลี่ยนแปลงโครงสร้าง
การอักเสบเรื้อรังระดับต่ำอย่างต่อเนื่องทำให้เซลล์เยื่อบุผิวเลนส์เสื่อมและเกิดต้อกระจก ชนิด subcapsular ด้านหลัง (PSC) ประมาณสามในสี่ของความขุ่นของเลนส์ในผู้ป่วย FHI เป็นชนิด subcapsular ด้านหลัง และมีการดำเนินโรคเร็วกว่าเมื่อเทียบกับม่านตาอักเสบ ชนิดอื่น แม้ไม่ได้รับการรักษาด้วยสเตียรอยด์ ต้อกระจก ก็ยังดำเนินต่อไป ดังนั้นจึงจำเป็นต้องติดตามผลอย่างสม่ำเสมอ
Yuksel Elgin & Hepokur (2025) รายงานผู้ป่วย 4 รายที่ได้รับการผ่าตัด GAT T สำหรับโรคต้อหิน ที่เกี่ยวข้องกับ FUS การผ่าตัดล้มเหลวทั้งหมด และหลังจากเฉลี่ย 6 เดือน ผู้ป่วย 3 รายจำเป็นต้องได้รับการผ่าตัด trabeculectomy ร่วมกับ MMC และ 1 รายจำเป็นต้องได้รับการจี้เลเซอร์ไดโอดที่ซิลิอารีบอดี 1) ในโรคต้อหิน FUS การเกิดแผลเป็นบริเวณ trabecular meshwork ด้านหลังเป็นสาเหตุหลัก ซึ่งบ่งชี้ว่า GAT T อาจไม่สามารถลดความดันลูกตา ได้อย่างเพียงพอ
ด้วยการปรับปรุงเทคโนโลยี PCR หลายเป้าหมาย ทำให้สามารถแยกความแตกต่างระหว่างไวรัสหัดเยอรมัน CMV และ HS V ในอารมณ์ขันในช่องหน้าม่านตา ได้อย่างแม่นยำ ในม่านตาอักเสบส่วนหน้าจาก CMV ในเอเชีย กำลังศึกษาประโยชน์ของการรักษาด้วยยาต้านไวรัส (ยาหยอดตาแกนซิโคลเวียร์, วัลแกนซิโคลเวียร์ชนิดรับประทาน) 4)
สำหรับอุปกรณ์ฝัง เช่น iStent และ Hydrus มีความกังวลเกี่ยวกับการอุดตันจากเศษซากการอักเสบ แต่มีรายงานผลลัพธ์เบื้องต้นที่มีแนวโน้มดีสำหรับ canaloplasty การสร้างอัลกอริทึม MIGS เฉพาะสำหรับโรคต้อหิน ที่เกี่ยวข้องกับ FHI ยังคงเป็นความท้าทาย
มีการติดตามการเปลี่ยนแปลงทางระบาดวิทยาของ FHI อย่างต่อเนื่องควบคู่กับการแพร่กระจายของวัคซีนหัดเยอรมัน และมีรายงานแนวโน้มลดลงของอุบัติการณ์ FHI ในกลุ่มคนรุ่นใหม่ 7)
การศึกษาในวงกว้างเพื่อชี้แจงความเหนือกว่าระหว่าง GDD และการผ่าตัดกรอง ในโรคต้อหิน ที่เกี่ยวข้องกับ FHI
การชี้แจงบทบาทเชิงสาเหตุของไวรัสหัดเยอรมันและ CMV และการศึกษาประโยชน์ของการรักษาด้วยยาต้านไวรัส
การสร้างอัลกอริทึมการรักษาเฉพาะสำหรับโรคต้อหิน ที่เกี่ยวข้องกับ FHI
Q
การผ่าตัดต้อหินแบบรุกรานน้อยที่สุด (MIGS) มีประสิทธิภาพสำหรับต้อหินที่เกี่ยวข้องกับม่านตาอักเสบ (FHI) หรือไม่?
A
ในปัจจุบัน ประสิทธิภาพของ MIGS สำหรับต้อหิน FHI ถือว่ามีจำกัด ในรายงานผู้ป่วย 4 รายของ GAT T ทุกรายล้มเหลว 1) ในต้อหิน FHI อาจมีการเกี่ยวข้องของพังผืดในบริเวณ trabecular ด้านหลัง และการผ่าตัดมุมตาเพียงอย่างเดียวอาจไม่เพียงพอ สำหรับอุปกรณ์ปลูกถ่าย เช่น iStent และ Xen มีความกังวลเรื่องการอุดตันจากเศษซากการอักเสบ
Yuksel Elgin C, Hepokur M. Highlighting the limited efficacy of gonioscopy-assisted transluminal trabeculectomy in Fuchs uveitis syndrome: a case series. BMC Ophthalmol. 2025;25(1):180.
Bodh SA, Kumar V, Raina UK, Ghosh B, Thakar M. Inflammatory glaucoma. Oman J Ophthalmol. 2011;4(1):3-9.
日本眼炎症学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
Chee SP, Jap A, Engelen S, et al. CMV anterior uveitis: what we have learnt. The International Taskforce for Anterior segment Novel therapies (TITAN) report 2. Graefes Arch Clin Exp Ophthalmol. 2024;262(5):1415-1428.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
European Glaucoma Society. Terminology and Guidelines for Glaucoma. 5th ed. Savona: PubliComm; 2020.
Mohamed Q, Zamir E. Update on Fuchs’ uveitis syndrome. Curr Opin Ophthalmol. 2005;16(6):356-363.
de Groot-Mijnes JDF, de Visser L, Rothova A, et al. Rubella virus is associated with Fuchs heterochromic iridocyclitis. Am J Ophthalmol. 2006;141(1):212-214.
Chee SP, Jap A. Presumed Fuchs heterochromic iridocyclitis and Posner-Schlossman syndrome: comparison of cytomegalovirus-positive and negative eyes. Am J Ophthalmol. 2008;146(6):883-889.
La Hey E, de Jong PTVM, Kijlstra A. Fuchs’ heterochromic cyclitis: review of the literature on the pathogenetic mechanisms. Br J Ophthalmol. 1994;78(4):307-312.