手術特點

角膜內皮移植術(DMEK)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是DMEK?
Section titled “1. 什麼是DMEK?”Descemet膜角膜內皮移植術(DMEK)是一種針對角膜內皮功能不全進行的角膜內皮移植術。2006年由Melles等人首次報告1)。從捐贈角膜中僅分離Descemet膜和角膜內皮細胞層,移除受體的病變Descemet膜,透過氣體填塞將移植片附著在角膜後表面。移植片厚度約為15μm,與包含基質的DSAEK(約50-150μm)相比非常薄1)。
角膜內皮移植的兩大術式是DSAEK和DMEK。DMEK不含基質層,因此光學性能優越,引起的散光極小,且幾乎不發生排斥反應。然而,術中移植物操作困難,移植物剝離的風險高於DSAEK1)。
DMEK的優點包括:對技術設備要求較低,與DSAEK相比可降低成本;並且可以進行角膜劈開移植(將一枚供體角膜用於兩名患者,分別行DMEK和DALK)1)。
2. 適應症與禁忌症
Section titled “2. 適應症與禁忌症”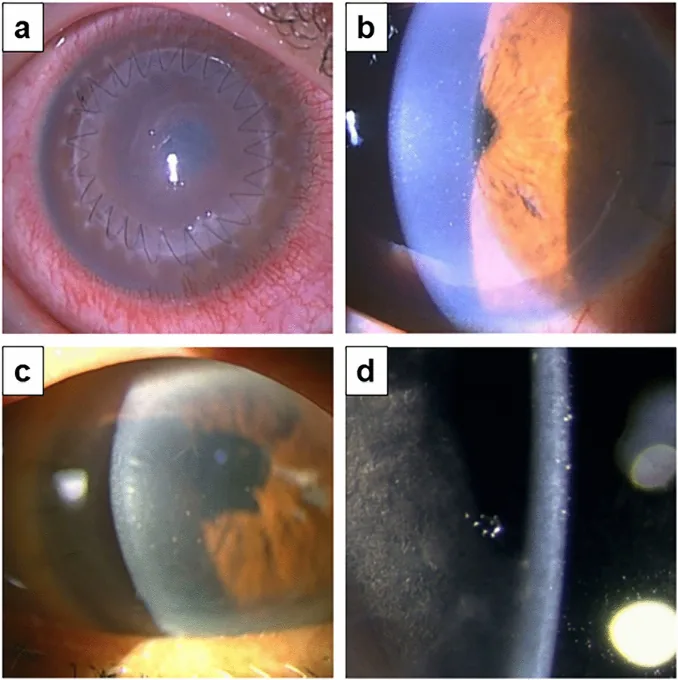
DMEK的主要適應症是角膜內皮功能不全。
- Fuchs角膜內皮營養不良(FECD):最常見的適應症疾病。全球發生率最高的角膜內皮營養不良,通常在50
60歲發病8)。女性多見(男女比1:34)。嚴重程度採用Krachmer分級評估8)- 0~1級:散在或非融合性角膜小滴。角膜透明性保持。
- 2
3級:中央15mm融合性角膜小滴。呈錘擊金屬樣外觀。 - 4級:中央超過5mm的融合性角膜小滴。基質水腫及上皮水疱形成。
- 人工水晶體性大疱性角膜病變(PBK):白內障術後內皮損傷。
- 既往內皮移植術後失敗:再次DMEK。
- 氬雷射虹膜切開術後大疱性角膜病變。
如果角膜基質有疤痕,DMEK可能殘留混濁或不規則散光,因此應考慮全層角膜移植。原則上,最好為人工水晶體眼。
Scheimpflug斷層掃描有助於判斷FECD的手術適應症。以下三個發現強烈預測FECD的進展和角膜移植的必要性8)。
- 中央4mm內等厚線的不規則
- 最薄點的位移(通常向鼻側)
- 角膜後表面的局部凹陷
當三個發現都存在時,5年進展率約為90%;都不存在時約為7%。對於角膜厚度≤640μm的患者,白內障術後1年內不需要角膜移植的機率為95%8)。
DMEK對於與COL8A2基因突變(p.Leu450Trp)相關的早發性Fuchs角膜內皮營養不良也有效,有報告稱所有眼均達到20/20至20/30的良好視力7)。儘管有長期角膜水腫,術後角膜仍可變得透明7)。
以下眼睛不適合DMEK:
- 無虹膜眼
- 廣泛虹膜前粘連
- 麻痺性瞳孔散大或大範圍虹膜缺損
- 無水晶體眼
在前房操作困難的病例(如嚴重水疱性角膜病變、前房極淺等)中,可能會選擇DSAEK。
3. 術式與技巧
Section titled “3. 術式與技巧”捐贈角膜的準備
Section titled “捐贈角膜的準備”SCUBA法(submerged cornea using backgrounds away technique)被廣泛使用。將捐贈角鞏膜片內皮面朝上,用新月刀或高爾夫刀在Schlemm管內側的Descemet膜上做360°淺切口1)。用無齒鑷緩慢提起內側部分,剝離Descemet膜。剝離的Descemet膜形成內皮細胞朝外的卷狀。
用0.06%台盼藍染色,用環鑽切出適合患者的圓形,並裝入Jones管。在Descemet膜的基質側用台盼藍標記”S”或”F”,可降低前房內移植物正反面誤認的風險。
採用球後麻醉或Tenon囊麻醉。對於預計玻璃體壓力高的病例,術前用Honan球囊降低眼壓。
合併白內障病例的手術策略
Section titled “合併白內障病例的手術策略”由於FECD和白內障的好發年齡重疊,根據角膜狀態選擇以下三種策略8)。
- 白內障手術優先:輕度FECD(Krachmer 1
2級),白內障是視力下降的主要原因。但2.54級時,術後約20%需要角膜內皮移植。 - DMEK優先:角膜水腫是主要原因,白內障較輕。術後使用類固醇可能加重白內障。
- 同時手術(Triple-DMEK):角膜厚度≥640μm,內皮細胞密度<1,000 cells/mm²,早晨有霧視時考慮。
Triple-DMEK需注意以下幾點:
- 製作較小的連續環形撕囊(CCC)
- 避免使用親水性丙烯酸酯人工水晶體(IOL)(有IOL表面鈣化風險)
- 推薦單焦點人工水晶體:FECD患者對比敏感度下降且易出現眩光,多焦點人工水晶體相對禁忌
- 人工水晶體度數計算時,需考慮DMEK術後遠視偏移(目標近視−0.75至−1.00 D)3)
- 軟殼技術:用擴散型OVD覆蓋角膜內皮,用凝聚型OVD維持前房。有助於超音波乳化過程中的內皮保護
Descemetorhexis(撕除Descemet膜)
Section titled “Descemetorhexis(撕除Descemet膜)”在BSS(平衡鹽溶液)或空氣灌注下,使用反向Sinskey鉤在受體角膜上製作圓形Descemet膜撕除。撕除直徑通常約為8.0 mm。
移植物植入
植入器械:Jones管(玻璃管)或玻璃注射器
切口寬度:2.2–2.4 mm足夠
預置縫線:預置10-0尼龍縫線,植入後快速閉合
步驟:將移植物基質面朝上,用水流沖入前房
展開與氣體注入
展開操作:交替進行角膜表面輕敲和BSS注入/抽吸1)
正反確認:透過術中OCT或S/F標記確認
氣體填充:注入20% SF6氣體或空氣
術後姿勢:維持仰臥位30-60分鐘
植入移植片後,從側切口放出少量房水以降低眼壓,防止移植片脫出。用10-0尼龍線縫合角膜切口。通常在移植片展開和氣體注入後進行周邊虹膜切除術。
4. 併發症與術後管理
Section titled “4. 併發症與術後管理”移植片剝離與再氣泡注入:這是DMEK最常見的併發症。DMEK的移植片剝離發生率高於DSAEK1)。統合分析顯示,再氣泡注入(再次氣體注入)的勝算比為2.76(95% CI 1.46-5.22),DMEK顯著較高2)。發生移植片剝離時,早期再氣泡注入通常可達成再附著。
術後眼壓升高:角膜內皮移植術後20-30%的患者發生。鑑別類固醇性青光眼和術後發炎引起的續發性青光眼很重要。使用前段OCT評估虹膜前粘連的存在。
排斥反應:DMEK後的排斥率約為1%,低於DSAEK(5-10%)。據報導,5年排斥事件率為2.6%6)。與全層角膜移植不同,角膜內皮移植後的排斥反應通常僅用類固醇眼藥水即可緩解。
COVID-19疫苗相關排斥:有報導稱接種BNT162b2 mRNA疫苗後出現雙側DMEK排斥6)。一名94歲女性在接種2週後出現雙側移植片排斥,最終需要再次DMEK6)。建議在疫苗接種前後增加類固醇眼藥水的使用6)。
囊樣黃斑水腫(CME):DMEK後約10-13.8%的患者發生4)。頻繁使用類固醇眼藥水可有效預防,但也有與疱疹病毒再活化相關的續發性CME的報導4)。
疱疹病毒再活化與復發性移植片衰竭:有報導稱FECD患者DMEK後出現復發性移植片衰竭,前房穿刺PCR檢測單純疱疹病毒-1陽性4)。當出現無技術原因的復發性DMEK衰竭、宿主和移植片均出現角膜水腫、輕微前房反應伴眼壓升高時,應鑑別疱疹性葡萄膜炎4)。
術中前房纖維蛋白反應:約3.7%的DMEK術中可能發生自發性纖維蛋白形成5)。來自虹膜的纖維蛋白絲會妨礙移植片展開,導致80%的移植片失敗5)。其背景被認為是慢性血-房水屏障(BAB)破壞5)。在進展期FECD中,前房內細胞激素升高已有報導,虹膜的微小創傷可觸發纖維蛋白形成5)。預防措施包括術前使用NSAID眼藥水、術中曲安奈德和r-TPA(重組組織型纖溶酶原激活劑)5)。
術後每2~3天使用前節OCT檢查角膜厚度改善情況和移植片貼附情況。即使移植片看起來已貼附,如果水腫沒有改善,日後仍可能發生移植片剝離。
高頻率開始使用類固醇眼藥水(氯替潑諾或地塞米松),並逐步減量。為預防排斥反應,減量必須非常緩慢。移植片感染罕見,但多來自捐贈者。如果角膜保存液培養檢出念珠菌等,則處方抗真菌眼藥水。
5. 臨床結果
Section titled “5. 臨床結果”DMEK vs UT-DSAEK
Section titled “DMEK vs UT-DSAEK”Dunker等人的多中心隨機對照試驗(54眼)顯示,術後12個月平均最佳矯正視力(BCVA)(logMAR)DMEK組為0.08,UT-DSAEK組為0.15,無顯著差異3)。但最佳矯正視力達到20/25或以上的比例,DMEK組為66%,顯著高於UT-DSAEK組的33%(P=0.02)3)。12個月時內皮細胞密度(ECD)兩組間無顯著差異(DMEK 1870 cells/mm² vs UT-DSAEK 1612 cells/mm²)3)。
| 項目 | DMEK | UT-DSAEK |
|---|---|---|
| 20/25達成率 | 66%3) | 33%3) |
| 12個月最佳矯正視力 | 0.08 logMAR3) | 0.15 logMAR3) |
| 內皮細胞密度(12個月) | 1870 cells/mm²3) | 1612 cells/mm²3) |
Sela等人的統合分析(8項研究,376隻眼)顯示,DMEK組12個月最佳矯正視力顯著較佳(平均差 −0.06 logMAR;95%CI −0.10至−0.02)2)。但DMEK組的再次氣泡注入率顯著較高(OR 2.76;95%CI 1.46-5.22),因此適當的患者選擇至關重要2)。對於厚度小於70μm的超薄DSAEK移植片,最佳矯正視力無顯著差異2)。
兩種術式均會引起輕度遠視偏移,但DMEK的偏移量較小(DMEK +0.22D vs UT-DSAEK +0.58D)3)。據報導,兩種術式的5年移植片存活率和內皮細胞損失率相當1)。
針對COL8A2突變的DMEK
Section titled “針對COL8A2突變的DMEK”對4隻眼(2名患者)因COL8A2基因突變(p.Leu450Trp)導致的早發型Fuchs角膜內皮營養不良實施了DMEK7)。術前平均中央角膜厚度(CCT)從713μm降至術後1個月的529μm,所有眼均達到20/20至20/30的最佳矯正視力7)。但術後第一年觀察到3至3.6D的屈光波動,表明COL8A2突變患者可能需要更長時間才能達到屈光穩定7)。
許多患者在術後12個月內達到20/25(0.8)或更好的最佳矯正視力。一項多中心隨機對照試驗中,66%的眼達到20/25或以上。但如果存在角膜基質疤痕或長期水腫導致的不可逆變化,恢復可能有限。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”角膜內皮損傷的機制
Section titled “角膜內皮損傷的機制”正常角膜內皮細胞通過Na⁺/K⁺-ATP酶泵將水從角膜基質泵入前房,維持角膜含水量約78%。在FECD和PBK中,這種泵功能失效,導致基質內水分過多積聚,引起角膜水腫和混濁。
在DMEK中,通過Descemetorhexis移除病變的Descemet膜和功能不全的內皮,移植健康的捐贈者Descemet膜-內皮複合體,從而恢復角膜的幫浦功能。一旦移植片貼附於角膜後表面,內皮細胞重新開始排水,角膜水腫迅速改善。
不進行內皮移植的Descemetorhexis(DWEK)
Section titled “不進行內皮移植的Descemetorhexis(DWEK)”有報告指出,在內皮移植後移植片脫離或單獨進行Descemetorhexis後,角膜自然恢復透明1)。這種現象發生在FECD中,但不會發生在水泡性角膜病變中,提示FECD周邊殘留的內皮細胞可能向中央遷移並恢復功能1)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”DMEK vs UT-DSAEK:移植片厚度的極限
Section titled “DMEK vs UT-DSAEK:移植片厚度的極限”統合分析表明,當超薄角膜內皮移植術移植片厚度小於70 μm時,與DMEK的視力差異可能消失2)。Nanothin DSAEK(小於50 μm)可能取得與DMEK相當的結果,但它仍然是附加性移植,而非真正的替代手術。
COL8A2突變中的DMEK應用
Section titled “COL8A2突變中的DMEK應用”首次對早發型Fuchs角膜內皮營養不良(COL8A2 p.Leu450Trp突變)施行DMEK,所有眼均獲得良好視力7)。由於術後屈光變化較大,人工水晶體度數計算和追蹤策略是未來研究的課題7)。
疫苗相關排斥反應
Section titled “疫苗相關排斥反應”已有多個COVID-19疫苗接種後DMEK移植片排斥反應的報告6)。疫苗誘導的免疫應答變化可能引發移植片排斥,建議在接種前後增加類固醇眼藥水的使用6)。
術中纖維蛋白反應的應對措施
Section titled “術中纖維蛋白反應的應對措施”術中前房纖維蛋白形成發生在約3.7%的DMEK病例中,並導致高比例的移植片失敗5)。術前使用NSAID眼藥水預防、術中曲安奈德檢測纖維蛋白、以及r-TPA溶解纖維蛋白已被提出作為新的管理策略5)。
8. 參考文獻
Section titled “8. 參考文獻”-
Deng SX, Lee WB, Hammersmith KM, et al. Descemet membrane endothelial keratoplasty: safety and outcomes: a report by the American Academy of Ophthalmology. Ophthalmology. 2018;125(2):295-310. doi:10.1016/j.ophtha.2017.08.015. PMID:28923499.
-
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. BMJ Open Ophthalmol. 2023;8:e001397.
-
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet membrane endothelial keratoplasty versus ultrathin Descemet stripping automated endothelial keratoplasty: a multicenter randomized controlled clinical trial. Ophthalmology. 2020;127(9):1152-1159.
-
Matar C, Seitz B, Daas L. Rezidivierendes DMEK-Versagen [Recurrent DMEK failure]. Ophthalmologe. 2021;118(7):719-723.
-
Trinh L, Bouheraoua N, Muraine M, Baudouin C. Anterior chamber fibrin reaction during Descemet membrane endothelial keratoplasty. Am J Ophthalmol Case Rep. 2022;25:101323.
-
Forshaw TRJ, Jørgensen C, Kyhn MC, Cabrerizo J. Acute bilateral Descemet membrane endothelial keratoplasty graft rejection after the BNT162b2 mRNA COVID-19 vaccine. Int Med Case Rep J. 2022;15:201-204.
-
Dzhaber D, Fliotsos MJ, Abousy M, et al. Descemet membrane endothelial keratoplasty in eyes with COL8A2-associated corneal dystrophy. Am J Ophthalmol Case Rep. 2022;26:101544.
-
Matthaei M, Hribek A, Clahsen T, et al. Fuchs endothelial corneal dystrophy: clinical, genetic, pathophysiologic, and therapeutic aspects. Annu Rev Vis Sci. 2019;5:151-175.
