原发性先天性青光眼(PCG)是一种罕见的先天性疾病,由于前房 角发育异常(小梁发育不良)导致房水 流出受阻,眼压 升高,属于发育性青光眼 的早发型。
白种人发病率为每12,000至18,000名新生儿中有1例,近亲结婚时发病率增加5至10倍1) 。日本报告每10万名新生儿中有1.8至2.4例。
畏光 、流泪和眼睑痉挛 的“三联征”是典型的早期症状,眼压 升高可导致牛眼(buphthalmos)和Haab纹1) 。CYP1B1是最常见的致病基因,但基因检测仅能确定约24-40%病例的病因7) 。
首选治疗是手术(房角 切开术或小梁切开术 ),在出生后1个月至2岁期间进行房角 切开术的成功率为94%,效果良好。
药物治疗作为辅助手段,例如口服乙酰唑胺 5-10 mg/kg,每6-8小时一次2) 。
早期诊断和治疗可获得良好的视功能。约60%的手术成功病例维持矫正视力 0.5以上。
需要终身进行眼压 管理、屈光 矫正和弱视 治疗1) 。
发育性青光眼 (developmental glaucoma)是由于房水 流出道发育异常引起的青光眼 的总称,根据发病时间分为早发型和晚发型。早发型发育性青光眼 相当于传统的“原发性先天性青光眼”,眼压 升高的原因仅限于小梁网 的发育异常。晚发型发育性青光眼 由于房角 发育异常程度较轻,发病较晚,房角镜检查 难以发现异常,通常也没有角膜 直径扩大或Haab纹。
原发性先天性青光眼(primary congenital glaucoma; PCG)是一种罕见的疾病,由遗传决定的小梁网 和前房 角异常导致眼压 升高,不伴有其他眼部或全身发育异常。以前曾使用小梁发育不良(trabeculodysgenesis)、房角 发育不良(goniodysgenesis)和原发性婴儿型青光眼 等术语,但2013年儿童青光眼 研究网络(CGRN)的国际分类将其统一为原发性先天性青光眼1) 。
原发性先天性青光眼是原发性儿童青光眼 中最常见的类型,根据发病时间分为以下四型1) 。
新生儿期发病 (0-1个月):最严重的类型。婴儿期发病 (1个月以上至24个月):最常见,好发于出生后3-9个月。迟发型(延迟认知型) (2岁以上):发病越晚,症状和体征越不明显。自然停止型 :极为罕见。眼压 正常,但可见牛眼和Haab纹等原发性先天性青光眼的典型表现。
白种欧洲人的发病率为每12,000至18,000名新生儿中有1例1) 。在东欧部分地区,发病率高达每1,250人中有1例。存在近亲结婚时,发病率增加5至10倍1) 。65%至80%的病例为双眼性,男女比例约为3:2,男性居多1) 。
原发性先天性青光眼占所有眼病患者的不到0.01%,但据估计占全球儿童失明的5%。75%为双眼性,65%为男童,80%在出生后1年内发病。
在ANZRAG的大型队列(290例儿童青光眼 )中,PCG最常见,占57.6%(167/290例),其中婴儿期发病的PCG最多,占53.3%(89/167例)。PCG的男女比例为1.46:1,诊断年龄中位数为0.25岁(IQR 0至0.6岁)7) 。
先天性青光眼 除了原发性先天性青光眼外,还包括继发性类型。世界青光眼 协会(WGA)对儿童继发性青光眼 的4种分类如下所示。
分类 主要疾病 伴有先天性眼部异常的青光眼 Axenfeld-Rieger异常、Peters异常 、先天性无虹膜 等 伴有先天性全身异常的青光眼 唐氏综合征 、Sturge-Weber综合征、神经纤维瘤病 等继发于后天性疾病或药物的青光眼 葡萄膜炎 后、类固醇 诱导性等先天性白内障 术后青光眼 手术时年龄小、小眼球是危险因素
Q
原发性先天性青光眼的发病频率是多少?
A
在白人中,每12,000至18,000名新生儿中有1例,但在近亲结婚多的地区,可上升至每1,250人中有1例。65%至80%为双眼发病1) 。
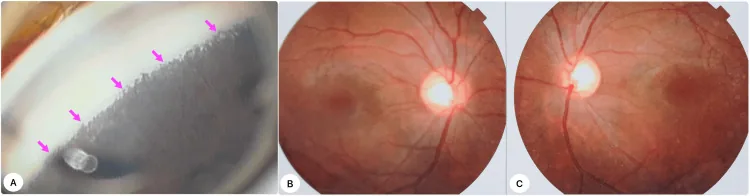
原发性先天性青光眼的前房角镜所见和双眼眼底照片。显示虹膜前附着和视盘凹陷扩大。 Iqbal MI, et al. A Landmark Case of Childhood Glaucoma Care in Bangladesh: Gonioscopy-Assisted Transluminal Trabeculotomy in Primary Congenital Glaucoma. Cureus. 2025. Figure 1. PM
CI D: PMC11934033. License: CC BY.
左图为前房 角镜照片,显示虹膜 前附着导致前房 角发育异常。中图和右图为双眼眼底照片,可见视盘凹陷 扩大。这些对应于本文“主要症状与临床所见”部分讨论的原发性先天性青光眼的临床所见。
原发性先天性青光眼患者因眼压 升高导致角膜水肿 ,出现刺激症状,表现为以下“临床三联征”中的一项或多项1) 。
畏光 怕光 ,在户外眯眼。溢泪 :无眼分泌物的流泪为特征。与鼻泪管阻塞 的鉴别很重要。眼睑痉挛
角膜水肿 /混浊导致的视力 下降、进行性近视 和散光 也会发生。在婴幼儿中,监护人常注意到“眼白”、“眼大”或“眼发蓝”而就诊。
角膜所见
Haab线 :Descemet膜的水平至斜向断裂,是先天性青光眼 的强指标1) 。
角膜 直径增大青光眼 。
角膜水肿 和混浊
眼球及视神经所见
牛眼(buphthalmos) :因眼压 升高导致整个眼球扩大。角膜 扩大可持续至约3岁,巩膜 伸展可持续至约10岁。
视盘凹陷 青光眼 。眼压 正常化后凹陷可能改善(逆转)。
眼轴长度 增加1) 。
关于Haab线:当角膜 直径迅速增大时,Descemet膜无法充分伸展而出现撕裂。这些撕裂称为Haab线,会导致角膜 散光 ,阻碍视力 发育。
角膜 直径正常值参考:新生儿约为9.5–10.5 mm,至1岁左右增至10.0–11.5 mm。出生后不久超过12.0 mm时,应高度怀疑本病。
诊断标准(依据青光眼 诊疗指南)
青光眼 诊疗指南规定,满足以下四项中至少一项即可诊断:
两次或以上测量眼压 ≥22 mmHg
杯盘比增大(≥0.3,或双眼差≥0.2)
存在提示青光眼 的视野缺损
角膜 直径或眼轴长度 增大
根据EGS第6版,满足以下5项中的至少2项即可诊断为原发性先天性青光眼1) 。
眼压 角膜 表现角膜水肿 、角膜 直径增大(新生儿≥11 mm,1岁≥12 mm,任何年龄>13 mm)视盘凹陷 进行性近视 :与年龄不相称的眼轴 增长房角 表现虹膜 高位附着、残留葡萄膜组织、小梁发育不全
Q
孩子只是眼睛大,也可能是青光眼吗?
A
任何年龄角膜 直径超过13 mm时,青光眼 的可能性极高。在自然停止型原发性先天性青光眼中,尽管眼压 正常,仍可能出现牛眼和Haab纹,需要作为疑似青光眼 进行随访。
大多数原发性先天性青光眼为散发性(无家族史),但约10%~40%为家族性,呈常染色体隐性遗传 ,外显率为40%~100%1) 。连锁分析已鉴定出5个基因座。
主要致病基因如下:
基因 基因座 染色体 功能 CYP1B1 GLC3A 2p22-p21 脂肪酸/维生素代谢酶 LTBP2 GLC3D 14q24.2-q24.3 潜在型TGF-β结合蛋白 TEK/TIE2 GLC3E 9p21 Schlemm管发育信号
CYP1B1 (GLC3A):最常见的致病基因。在胎儿和成人的神经上皮和睫状体 中表达,代谢眼部发育必需的化合物。CYP1B1缺陷小鼠出现严重的小梁网 萎缩。CYP1B1突变病例通常发病较早,双眼受累,病程典型。LTBP2 (GLC3D):在小梁网 和睫状突中表达,但在眼中的作用尚未完全阐明。TEK/TIE2 (GLC3E):血管生成素/TEK信号通路对Schlemm管的发育至关重要,TEK基因敲除小鼠缺乏Schlemm管。MYOC :可能参与高达5.5%的原发性先天性青光眼病例。EFEMP1 也被报道为候选基因1) 。
根据ANZRAG队列的基因诊断率报告,总体24.7%(125/506例)获得了分子诊断。在PCG中,30.4%(41/135例)可实现分子诊断,包括CYP1B1双等位基因突变15.6%(21例)、TEK杂合突变5.9%(8例)、CPAM D8 3.7%(5例)、FOXC1杂合突变3.7%(5例)。基于基因诊断的PCG亚型重新分类发生在10.4%的病例中(FOXC1突变重新分类为ARS,CPAM D8突变重新分类为ASD )7) 。CYP1B1双等位基因突变在PCG女性中更常见(66.7% vs 33.3%,P=0.02)7) 。
通过基因检测确定病因的概率约为24-40%。建议进行基因检测以排除其他先天异常并用于计划生育1) 。
近亲结婚被认为是疾病严重程度和预后不良的因素1) 。原发性先天性青光眼患者的第二个孩子患病的概率通常低于3%,但如果已有两个孩子患病,假设常染色体隐性遗传 ,则概率升至25%。
Q
是否应该接受基因检测?
A
EGS指南建议从排除其他先天异常和计划生育的角度进行基因检测1) 。ANZRAG队列显示PCG的基因诊断率为30.4%,基因诊断导致10.4%的病例亚型重新分类7) 。检测阴性不能排除原发性先天性青光眼,但可能有助于诊断准确性和适当管理。
原发性先天性青光眼的诊断通常可以在眼压测量 不准确的情况下临床做出。Haab纹的存在是先天性青光眼 的强指标1) 。
眼压测量 眼压 计(包括回弹式眼压计 )进行测量1) 。注意:哭闹的儿童可能出现假性高值,全身麻醉药物会导致假性低值。回弹式眼压计 也可用于家庭测量1) 。全身麻醉下使用的所有药物都会降低眼压 。唯一的例外是分离性麻醉药盐酸氯胺酮,它可能使眼压 轻度升高。如果在七氟烷麻醉下眼压 为20 mmHg,清醒时眼压 将超过30 mmHg。有观点认为七氟烷麻醉下正常上限为15 mmHg或12 mmHg。角膜 直径和厚度测量角膜 直径;如果超过年龄相应的正常范围,则怀疑眼压 控制不良。中央角膜 厚度即使没有水肿也可能增加,并可能影响眼压测量 值1) 。眼轴长度 测量近视 进展和眼轴长度 增加提示青光眼 进展。房角镜检查 角膜 混浊导致房角镜检查 困难,超声生物显微镜 (UBM )很有用。视盘评估 :应记录基线眼底照片。眼压 降低后常可见杯凹改善。特别是1岁以下通过手术治疗获得良好眼压 控制的病例中,约50%的杯盘比减少0.2以上,表明儿童视盘杯凹具有可逆性,与成人不同。视力 和屈光 检查散光 、角膜 混浊和Haab纹可导致弱视 ,因此在随访期间应定期进行屈光 检查,与眼压测量 并行。
可能与原发性先天性青光眼混淆的疾病如下所示1) 。
鉴别疾病 鉴别要点 结膜炎 有眼部分泌物和充血 ;角膜 直径正常 鼻泪管阻塞 有眼部分泌物;角膜 直径正常 PPM D角膜 后表面的囊泡样改变CHED 双眼角膜水肿 ,眼压 正常 X连锁巨角膜 角膜 直径增大,眼压 正常出生时外伤 外伤史,Haab纹通常垂直
手术是首选治疗方法2) 。原因是原发性先天性青光眼由房角 发育异常引起,可通过手术解决;婴幼儿药物疗效难以确认;且存在依赖照护者依从性的问题2) 。药物治疗作为围手术期或术后辅助手段使用2) 。
应在具有足够小儿眼科和青光眼 治疗经验的机构进行,需要包括再次手术、长期随访和弱视 治疗在内的综合管理2) 。
小梁切开术 (trabeculotomy)角膜 透见困难的情况下也可施行2) 。需要制作结膜 瓣和巩膜 瓣,可能使未来的滤过手术 变得困难。使用微导管的360°小梁切开术 也有尝试2) 。出生后2个月内发病的病例成功率为78%,略低;但此后发病的病例成功率为96%,效果良好。房角 切开术(goniotomy)角膜 透明的病例2) 。一次手术可切开90-120°,最多可从不同部位进行3次操作2) 。出生后1个月至2岁发病的成功率为94%,尤其良好。但出生后1个月内发病的病例成功率为26%,2岁以后发病的病例为38%,较低。对于出生后3-12个月发病的原发性先天性青光眼,房角 切开术和小梁切开术 的成功率相似(70-90%)2) 。术式选择取决于术者经验。失败的危险因素是房角 发育不良的程度和前段过度扩张2) 。
滤过手术 (trabeculectomy)房角 手术无效的病例2) 。原发性先天性青光眼患者的巩膜 薄,制作瓣膜困难,即使联合抗代谢药 物,滤过泡形成也可能困难。1年成功率为50-87%,较成人差2) 。带引流管 的植入物手术(GDD) :用于滤过手术 无效的病例。一项针对Ahmed瓣膜和Baerveldt植入物的32项研究、1221只眼的荟萃分析显示,术前平均眼压 31.8±3.4 mmHg,术后12个月平均眼压 降至16.5 mmHg(95% CI 15.517.6)8) 。成功率随时间下降:12个月87%(95% CI 0.830.91),24个月77%(95% CI 0.71~0.83),120个月37%。Ahmed组和Baerveldt组的成功率无显著差异8) ,主要并发症包括前房 变浅13.6%、低眼压 11.7%、脉络膜 渗出8.3%。睫状体破坏术 眼压 时考虑使用2) 。
药物治疗是辅助治疗,旨在术前短期降低眼压 和术后控制眼压 2) 。参照原发性开角型青光眼 联合使用药物,但需注意以下事项。
婴幼儿相对于体重和体表面积,剂量容易过大,因此应尽可能从低浓度药物开始。
口服乙酰唑胺 (碳酸酐酶抑制剂 ) :按510 mg/kg每68小时给药一次。对术前紧急降低眼压 有效2) 。β受体阻滞剂 α2肾上腺素能受体激动剂 (如溴莫尼定)在2岁以下儿童中绝对禁忌。可引起神经精神症状(嗜睡、心动过缓、低血压等)1) 2) 。前列腺素FP受体激动剂 在儿童中的效果较成人弱2) 。儿童葡萄膜巩膜 流出道发育不全,无应答者较多,但被认为比β受体阻滞剂 有稍好的降眼压 效果。滴眼液从泪囊、鼻黏膜直接进入全身循环,因此儿童即使一滴也容易引起严重的全身性副作用。建议指导滴眼后压迫泪囊部。
必须终身监测眼压 ,并通过屈光 矫正和弱视 治疗支持最佳的视觉发育1) 。
Q
为什么首选手术而非药物治疗?
A
原发性先天性青光眼的原因是房角 发育异常,可通过手术解决。在婴幼儿中,药物效果难以确认,且存在依从性问题。此外,儿童可用的药物有限,例如α₂受体激动剂的禁忌症和前列腺素类药物的效果减弱2) 。
原发性先天性青光眼的眼压 升高是由于前房 角发育异常导致房水 流出受阻所致1) 。
在1950至60年代,曾认为原因是覆盖房角 的非穿孔性膜(Barkan膜),但随后的组织学调查否定了这种膜的存在。目前认为流出障碍源于小梁网 本身。
正常情况下,妊娠第三孕期睫状体 和周边虹膜 会向后移动,远离角膜 和巩膜 。在原发性先天性青光眼中,小梁网 内胶原梁的过度或过早积累阻碍了这种后移,导致虹膜 根部和睫状肌保持前附着,阻塞小梁网 或压迫Schlemm管。
Rao(2025)对4名原发性先天性青光眼患者的小梁网 标本进行了组织学分析,报告了近小管网(JCM)和角膜 巩膜 网的扩大、小梁网 梁的增厚、梭形核的增加(提示上皮间质转化),以及JCM内存在两个形态不同的区域3) 。这些发现提示原发性先天性青光眼中小梁网 各区域的异常分化和分化异质性。
GAT T(gonioscopy-assisted transluminal trabeculotomy)是一种相对较新的技术,通过角膜 切口在房角 镜下将微导管或缝线插入Schlemm管,切开全周小梁网 。其在成人青光眼 中的有效性正在确立,并逐渐应用于儿童。
Song等人(2022)报告了一例对3岁原发性先天性青光眼男童实施GAT T的病例。虹膜 覆盖了整个房角 直至Schwalbe线,正常房角 结构不可见,但通过钩操作剥离虹膜 以识别Schlemm管,成功实施了GAT T。术后6个月眼压 稳定4) 。
Elhusseiny等人(2023)报告了6名既往有青光眼 手术史的原发性先天性青光眼患者7只眼接受GAT T的1年结果。平均眼压 从术前的25.7±5.9 mmHg显著下降至12个月后的12.0±1.5 mmHg。完全成功率为85.7%(6/7眼),包括限定性成功在内为100%,没有眼需要额外青光眼 手术。未观察到严重并发症5) 。
Dada等人(2022)报告了一种针对伴有角膜 混浊的原发性先天性青光眼的新技术,使用23G激光内镜探头在可视化房角 结构的同时进行房角 切开术6) 。传统上,房角 切开术需要透明角膜 ,但借助内镜辅助,即使在角膜 混浊眼中也可能可行。
对于有家族史或近亲结婚较多地区等高危人群,未来产前基因筛查可能作为一种预防措施出现。在ANZRAG队列中,基因诊断使10.4%的PCG亚型得到重新分类,表明基因诊断有助于更精确的诊断和适当的管理7) 。期待未来大型国际队列的证据积累。
一项关于儿童青光眼 患者QOL的系统评价发现,使用了10种患者报告结局指标(PROMs),但目前尚无针对儿童青光眼 的特异性问卷9) 。IVI _C、CVAQC和LVP-FVQ-II作为视觉特异性儿童量表获得了相对较高的评分(5/7分)。儿童青光眼 患者对未来存在担忧(就业、家庭计划、对手术的恐惧),现有PROMs未能充分覆盖9) 。开发儿童青光眼 特异性PROMs是未来的挑战。
手术成功病例的长期视力 预后相对良好。无论是房角 切开术还是小梁切开术 ,约60%的成功病例保持矫正视力 0.5以上。
尽早进行屈光 检查和屈光 矫正,并频繁进行屈光 检查以应对度数变化。
Haab纹引起的角膜 散光 可导致弱视 ,因此应同时进行散光 管理和弱视 治疗。
必须终身监测眼压 。
儿童青光眼 患者的健康相关QoL(HRQoL)与先天性心脏病或急性淋巴细胞白血病患儿相当(PedsQL 4.0评分约76-79/100)。视力 良好组、原发型和单眼性患者的QoL较好;手术次数、滴眼液次数和双眼性与QoL降低相关9) 。
Q
手术后的长期视力预后如何?
A
手术成功病例中,约60%可维持矫正视力 0.5以上。但终身眼压 管理、屈光 矫正和弱视 治疗不可或缺。处理Haab纹引起的角膜 散光 和进行性近视 是维持视功能的关键。需要GDD手术的病例,12个月成功率为87%,24个月为77%,随时间推移而下降,因此长期随访是必需的8) 。
European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):S1-S270.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Rao A. Histopathological changes in the trabecular meshwork in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2025;38:102340.
Song Y, Zhang X, Weinreb RN. Gonioscopy-assisted transluminal trabeculotomy in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2022;25:101366.
Elhusseiny AM, Aboulhassan RM, El Sayed YM, et al. Gonioscopy-assisted transluminal trabeculotomy following failed glaucoma surgery in primary congenital glaucoma: one-year results. Case Rep Ophthalmol Med. 2023;2023:6761408.
Dada T, Satpuke K, Bukke AN, et al. Endoscope-assisted goniotomy in primary congenital glaucoma with corneal opacification. BMJ Case Rep. 2022;15:e252958.
Knight LSW, Ruddle JB, Taranath DA, et al. Childhood and early onset glaucoma classification and genetic profile in a large Australasian disease registry. Ophthalmology. 2024;131(1):62-73.
Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: a systematic review and meta-analysis. J AAPOS. 2023;27(3):139.e1-139.e10.
Stingl JV, Cascant Ortolano L, Azuara-Blanco A, Hoffmann EM. Systematic review of instruments for the assessment of patient-reported outcomes and quality of life in patients with childhood glaucoma. Ophthalmol Glaucoma. 2024;7(4):391-400.